Кислота аскорбиновая проявляет восстановительные свойства. В растворах под действием слабых окислителей различной природы она окисляется до дегидроаскорбиновой кислоты:
Процесс этот — обратимый. Кислотные свойства кислоте аскорбиновой придает наличие в молекуле двух енольных гидроксилов. Разрыва лактонного цикла в этих условиях не происходит, а образуются нейтральные растворимые монозамещенные соли
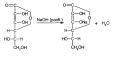 Эта реакция лежит в основе определения кислоты аскорбиновой методом нейтрализации.
Эта реакция лежит в основе определения кислоты аскорбиновой методом нейтрализации.
Кислотные свойства кислоты аскорбиновой используют для испытания подлинности. После добавления карбоната натрия в водном растворе происходит образование ионизированной формы кислоты аскорбиновой. К полученной натриевой соли прибавляют сульфат железа (II). Появляется темно-фиолетовое окрашивание, обусловленное образованием аскорбината железа, Исчезающее после добавления разведенной серной кислоты: -
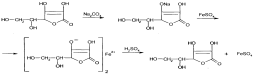
При добавлении к ее раствору реактива Фелинга появляется оранжево-желтый осадок оксида меди (I). При взаимодействии препарата с раствором нитрата серебра его ион восстанавливается до металлического серебра (реакция образования «серебряного зеркала»):
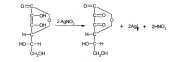
Восстановительными свойствами кислоты аскорбиновой обусловлено превращение окрашенного в синий цвет раствора 2,6 -дихлорфенолиндофенола в бесцветное лейкооснование:
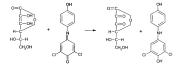
Количественно определяют кислоту аскорбиновую, используя в качестве титранта-окислителя 0,1 M раствор иодата калия в присутствии иодида калия:
Избыток иода окрашивает крахмал в синий цвет. Окисление кислоты аскорбиновой иодом до дегидроаскорбиновой кислоты лежит в основе иодометрического определения.:
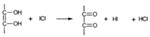
В эквивалентной точке выделяется иод, окрашивающий крахмал в синий цвет:
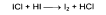
Периметрическое определение основано на том же процессе окисления кислоты аскорбиновой (в среде серной кислоты). Индикатором служит комплексное соединение железа (II) с о-фенантролином. Оно имеет интенсивно-красное окрашивание. В эквивалентной точке избыток сульфата церия
(IV) окисляет ион железа до трехзарядного и происходит образование комплексного соединения голубого цвета:
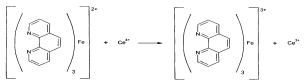
Кислоту аскорбиновую хранят в хорошо укупоренной таре» предохраняя от действия света и кислорода воздуха.
7.Общая характеристика физико-химических и химико-аналитических и свойств лекарственных веществ, относящихся к аминокислотам и их производным. Кислота глутаминовая. Получение, контроль качества, условия хранения.
Дата: 2019-07-30, просмотров: 484.