В медицинской практике применяют раствор формальдегида (формалин) Формальдегид получают окислением метилового спирта кислородом воздуха, Смесь даров метилового спирта и воздуха пропускают через нагретые до 500—600°С трубки, наполненные катализатором (медь, серебро, кокс):
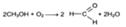 После охлаждения формальдегид (бесцветный газ с острым запахом) растворяют в воде до получения 36,5—37,5 % водного раствора, который называют формалином,.
После охлаждения формальдегид (бесцветный газ с острым запахом) растворяют в воде до получения 36,5—37,5 % водного раствора, который называют формалином,.
Идентифицировать формальдегид можно с помощью реакций образования окрашенных продуктов взаимодействия с хромотроповой или салициловой кислотами в присутствии концентрированной серной кислоты. ГФ рекомендует для этого использовать салициловую кислоту (появляется красное окрашивание). Образующееся окрашенное соединение называется ауриновым красителем:
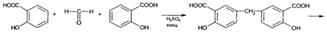
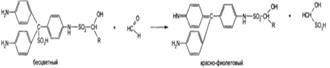
Формальдегид дает положительную реакцию с фуксинсернистой кислотой:::::.
Для установления подлинности раствора формальдегида ГФ рекомендует использовать общую на альдегиды реакцию восстановления серебра (реакцию серебряного зеркала»):

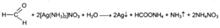
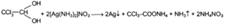
Общими для альдегидов являются и другие реакции окисления. Они дают положительную реакцию с реактивом Несслера, при нагревании происходит образование бурого осадка металлической ртути:
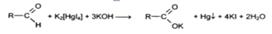
При взаимодействии с реактивом Фелинга (смесь водного раствора сульфата меди и щелочного раствора натрия-калия тартрата) после нагревания до кипения выпадает кирпично-красный осадок оксида меди (I):
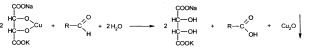
Количественное определение формальдегида в растворе и хлоралгидрата можно провести, используя реакцию окисления альдегидов иодом в щелочной среде. Иод при этом образует гипоиодит (сильный окислитель):
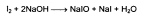
Гипоиодит окисляет альдегиды до кислот:
Затем добавляют избыток серной кислоты, непрореагировавший гипоиодит превращается в иод, который оттитровывают тиосульфатом натрия:
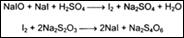 Аналогичный химический процесс происходит при окислении формальдегида пероксидом водорода в щелочной среде: Эту реакцию используют для определения формальдегида.
Аналогичный химический процесс происходит при окислении формальдегида пероксидом водорода в щелочной среде: Эту реакцию используют для определения формальдегида.
Окисл-е происх при цериметрическом опред-ии формальдегида • Дей-ют изб титр-го раствора сульфата церия (IV):
Избыток его оттитровывают раствором соли Мopa: (NH4)2SO4*FeSO4*6H2O
В условиях аптеки формальдегид в растворах определяют рефрактометрическим методом.
Р-р формальдегида следует хранить в хорошо закрытых склянках при температуре не ниже 4*9°С* При более низкой температуре происходит полимеризация с образованием параформа [СН2О]п — твердого белого вещества. Для предохранения от полимеризации к препарату добавляют до 1% метилового спирта .
Дата: 2019-07-30, просмотров: 1051.