Кафедра технологии редких элементов и наноматериалов на их основе
ВЫПУСКНАЯ КВАЛИФИКАЦИОННАЯ РАБОТА
на тему
« Экстракционная переработка щелочных и карбонатных растворов после выщелачивания отработанного алюмокобальтмолибденового катализатора»
Зав. кафедрой,
д.х.н., проф. С.И. Степанов
Научный руководитель
д.х.н., проф. С.И.Степанов
Дипломник И.М. Мельникова
МОСКВА 2019
| Содержание | Стр. | |
| Введение……………………………………………………………….. | 6 | |
| 1. | Литературный обзор…………………………..………...……………... | 9 |
| 1.1. | Катализаторы гидроочистки…………………..……………………… | 9 |
| 1.2. | Методы переработки катализаторов………………...………………. | 13 |
| 1.3. | Экстракция Мо(VI) анионообменными экстрагентами……………. | 15 |
| 1.4. | Состояние Мо(VI) в водных растворах…………..………...……….. | 21 |
| Заключение………………………………………………...…………… | 29 | |
| 2. | Методическая часть………………………………...……………….. | 30 |
| 2.1. | Исходные вещества и реагенты……………………………………….. | 30 |
| 2.2. | Методики получения солей МТОА и МТАА………………………… | 30 |
| 2.3. | Методика определения концентрации металлов в органических экстрактах методом мокрого сжигания……………………...……..… | 31 |
| 2.4. | Методика определения R4N+-групп в экстрагенте ………………. | 31 |
| 2.5. | Методика определения концентрации Мо(VΙ) в водных растворах... | 32 |
| 2.6. | Определение концентрации Al в водных растворах ……………… | 33 |
| 2.7 | Методика гравиметрического определения концентраций Со в водных растворах…………………………………………………… | 34 |
| 2.8 | Методика определения CO32- - ионов в водных и органических растворов ..……………………………………………...………… | 36 |
| 2 . 9 | Методика проведения экстракции Мо(VI) в двухфазной и в трёхфазной системе жидкость-жидкость-углекислый газ………...… | 37 |
| 2.10 | Методика проведения выщелачивания молибдена из отработанного АКМ катализатора…………………………………… | 38 |
| 2.11 | Методика проведения выщелачивания кобальта из алюмо-кобальтового кека…………………………………………………… | 40 |
| 2.12 | Рентгенофазовый анализ твердых образцов…………………………. | 40 |
| 3. | Обсуждение результатов………………………………………………. | 41 |
| 3.1 | Экстракция Mo(VI) из растворов выщелачивания отработанных катализаторов солями ЧАО …………………………………… | 41 |
| 3.1.1 | Экстракция Mo(VI) из щелочного раствора выщелачивания отработанного катализатора карбонатом МТАА………………… | 42 |
| 3.1.2 | Экстракция Mo(VI) из бикарбонатного раствора выщелачивания отработанного катализатора метилсульфатом МТОА…………….. | 49 |
| 3.1.3 | Экстракция Mo(VI) из бикарбонатного раствора выщелачивания отработанного катализатора карбонатом МТОА……………………. | 51 |
| 3.1.4 | Экстракция Mo(VI) из карбонатного раствора выщелачивания отработанного катализатора сульфатом МТОА……………………... | 58 |
| 3.1.5 | Экстракция Mo(VI) из карбонатного раствора выщелачивания отработанного катализатора карбонатом МТОА в присутствии газообразного СО2………………………………………………… | 60 |
| 3.1.6 | Экстракция Mo(VI) из карбонатного раствора выщелачивания отработанного катализатора молибдатом МТОА в присутствии газообразного СО2……………………………………………………. | 63 |
| 3.2 | Реэкстракция Мо(VI) из экстрактов молибдата МТОА и полимолибдата МТОА в толуоле……………………………………. | 65 |
| 3.2.1 | Реэкстракция Мо(VI) из экстрактов молибдата МТОА и полимолибдата МТОА в толуоле водными растворами (NН4)2СО3 | 66 |
| 3.2. 2 | Реэкстракция Мо(VI) из экстрактов молибдата МТОА и полимолибдата МТОА в толуоле NН4НCO3………………………… | 67 |
| 3.2. 3 | Реэкстракция Мо(VI) из экстрактов молибдата МТОА и полимолибдата МТОА в толуоле NН4ОН…………………………… | 70 |
| 3.3 | Переработка алюминий-кобальтового кека……………………….. | 73 |
| 3.3.1 | Аммиачно-карбонатное выщелачивание кобальта из алюмо-кобальтового кека..…………………………………………………… | |
| 3.3.2 | Разработка метода спектрофотометрического определения кобальта в водных растворах………………………………………… | 73 |
| 3.3.3 | Выщелачивание кобальта из алюминий-кобальтового кека водными растворами NH4OH……………………………………….. | 76 |
| 3.3.4 | Выщелачивание кобальта водными растворами из алюминий-кобальтового кека NH4OH - (NH4)2CO3………………..…………… | 78 |
| 3.3.5 | Выщелачивание кобальта из алюминий-кобальтового кека водными растворами (NH4)2CO3 - NH4НCO3………………………… | 83 |
| 3.4 | Серно-кислотное выщелачивание кобальта из алюминий-кобальтового кека……………………………….………………….. | 90 |
| 3.5 | Экстракционное извлечение кобальта из аммиачных и аммиачно-карбонатных растворов ………………………………………………. | 91 |
| 3.6 | Осадительное выделение кобальта из аммиачных и аммиачно-карбонатных растворов……………………………………………….. | 93 |
| 3.7 | Описание технологической схемы переработки отработанного АКМ катализатора……………………………………………………. | 94 |
| Выводы………………………………………………………………. | 104 | |
| Список использованной литературы……………………………… | 106 | |
| Приложение…………………………………………………………. | 110 | |
Введение
В наше время мы все больше сталкиваемся с разного рода экологическими проблемами и одной из таких проблем является образование огромного количества отходов от различных химических производств, в том числе от гидроочистки нефти. Отходами такого производства являются отработанные катализаторы в своем составе содержащие Мо, W, V, Co, Ni, Al и др. ценные металлы или их соединения. Поэтому такие катализаторы могут рассматриваться в качестве сырья для извлечения этих ценных компонентов.
В промышленности широко распространены алюмокобальтмолибденовые (АКМ) и алюмоникельмолибденовые (АНМ) каталитические системы. Это катализаторы гидрогенизационных процессов нефтепереработки, катализаторы гидрообессеривания нефтепродуктов, которые являются многотоннажной продукцией, поскольку процессы гидроочистки занимают ведущее место в современных схемах переработки нефти как в нашей стране, так и за рубежом. Срок службы катализаторов определяется количеством сырья, пропущенного через 1 кг катализатора, и зависит от условий эксплуатации.
Среди предполагаемых путей переработки отработанных катализаторов можно выделить методы восстановления каталитической активности или методы реактивации. В том случае если реактивация отработанных катализаторов невозможна, они могут быть использованы для выделения нужных металлов пирометаллургическими или гидрометаллургическими методами.
Для интенсификации перед выщелачиванием молибдена, отработанный катализатор необходимо обжигать для удаления с его поверхности отложений органических соединений [16,44]. Кроме того, для интенсификации выщелачивания молибдена предложена ультразвуковая обработка [52,57] и микроволновое излучение [57]. Из карбонатных растворов выщелачивания, в том числе и из отработанных катализаторов гидроочистки молибден предложено извлекать, жидкостной экстракцией [32,58-63], сорбцией на ионообменных смолах и активированных углях [64-66] и осадительными методами с получением молибдата кальция после нейтрализации карбонатного раствора HCl в присутствии CaCl2 [44], парамолибдата аммония при рН=11 [22], молибденовой кислоты при нейтрализации карбонатного раствора HNO3 [45,46,51,67] или трисульфида молибдена [68] Образующийся в результате выщелачивания алюмокобальтовый остаток, можно использовать для получения голубого пигмента [69].
Известно, что для разделения вольфрама и молибдена непосредственно из карбонатных растворов автоклавно-содового выщелачивания шеелитовых и вольфрамитовых концентратов используют жидкостную экстракцию солями ЧАО и, в частности, карбонатом МТАА [4].
Физико-химические основы экстракции молибдена из карбонатных растворов карбонатом МТАА описаны в работе [5]. При рН=7,6-12 экстракция молибдена протекает по анионообменному механизму с образованием молибдата МТАА (R4N)2MoO4, где: R4N - четвертичный аммониевый катион.
Примесные анионы, особенно однозарядные, оказывают депрессирующее влияние на анионообменное распределение МоО42--ионов, возрастающее с ростом их концентрации в ряду: MoО42->CrО42->SO42->СО32- и NO3->Сl->НСО3->>ОН-.
Перспективным вариантом выделения Мо из карбонатных растворов выщелачивания АКМ может быть экстракция Мо по полимеризационному механизму, особенностью которого является полимеризация полимолибдатов в органической фазе под действием протона минеральной кислоты, например угольной. Проведение экстракции по полимеризационному механизму позволяет в значительной степени повысить коэффициенты распределения полимерных соединений молибдена, что должно приводить к вытеснению других соэкстрагировавшихся примесей и очистке молибдена. В то же время облегчаются процессы реэкстракции, т.к. последняя протекает не по механизму анионного обмена, который затруднён в таких системах, а по реакции деполимеризации в присутствии щелочных реагентов, например NН4ОН. Полимеризационный механизм экстракции позволяет использовать в качестве экстрагента молибдат МТОА, который образуется на стадии реэкстракции полимолибдата МТОА водными растворами NH4OH.
Целью работы явилось: разработка метода экстракционного выделения Мо(VI) из карбонатных растворов выщелачивания отработанного алюмокобальтмолибденового катализатора солями метилтриоктиламмония.
Литературный обзор
Катализаторы гидроочистки
Для улучшения качества углеводородов используется процесс гидроочистки, заключающийся в обработке углеводородов водородом в присутствии катализатора [6,7]. В этом процессе применяются серостойкие гидрирующие катализаторы, представляющие собой сочетание оксидов, сульфидов – элементов VI и VIII групп Периодической системы элементов (Мо, W, Ti, Ni, Co), нанесенных на носитель – преимущественно γ – Al2O3, промотированных различными добавками [8]. Важным критерием оценки качества является обессеривающая активность и физико-механические свойства. В таблице приведены основные характеристики некоторых зарубежных промышленных катализаторов гидроочистки (таблица 1.1) [9].
Таблица 1.1
Характеристики некоторых зарубежных промышленных катализаторов
| Форма и марка катализатора | Показатели качества | |
| 1 | 2 | |
| Haldor Topsoe ТК - 551 TK - 581 | NiO - 3,4% MoO3 - 14,0% - - | Sуд. = 180 м2/г V = 740 кг/м3 Sуд. = 140 м2/г V = 740 кг/м3 |
| Pracatalyse HR - 345 HR - 346 | NiO - 3,0% WO3 - 15,0% NiO - 3,8% MoO3 - 16,8% | Sуд. = 170 м2/г Vпор = 0,45 cм3/г |
| Shokubai kasei koqyo CDS - DS(цеолитн.) CDS - D9 | СоO - 3,87% MoO3 - 12,8% СоO - 3,7% MoO3 - 14,0% | Sуд. = 276 м2/г Sуд. = 256 м2/г |
| Продолжение таблицы 1.1 | ||
| 1 | 2 | |
| American Cyanamid NDS - 20 NDS - 30 | СоO - 50% MoO3 - 16,2% NiO - 5,0% MoO3 - 16,2% | Sуд. = 230 м2/г V = 660 кг/м3 Sуд. = 230 м2/г V = 740 кг/м3 |
| Shell S - 424 | NiO - 3,9% MoO3 - 19,8% | Sуд. = 165 м2/г V = 750 кг/м3 |
| Ketjen KF - 124-3E (цеолитн.) | СоO - 50% MoO3 - 16,2% | Sуд. = 250 м2/г |
Выпускаемые зарубежными фирмами катализаторы гидроочистки, как видно из таблицы, отличаются достаточно низким содержанием активных компонентов (Со, Ni, Мо), высокой прочностью и удельной поверхностью. В то время как на отечественных заводах производят катализаторы гидроочистки не уступающие по физико-механическим и механическим характеристикам зарубежным аналогам (таблица 1.2) [10,11].
Таблица 1.2
Характеристики некоторых промышленных отечественных катализаторов гидроочистки
| Марка катализатора | Показатели качества |
| 1 | 2 |
| АКМ | Насыпная плотность - 0,64-0,74 г/см3 Коэффициент прочности - 2,1 кг/мм Диаметр гранул - 4,0-5,0 мм Химический состав в пересчете на сухое вещество, % масс. NiO - 3,0-4,0% CoO - не менее 4% MoO3 - не менее 12,0%, Fe2O3 - не более 0,20% |
| Продолжение таблицы 1.2 | |
| 1 | 2 |
| ГО-117 | Насыпной вес - 830 кг/м3 Коэффициент прочности - 1,2 кг/мм Удельная поверхность - 195 м2/г Диаметр гранул - 4,0мм Химический состав в пересчете на сухое вещество, % масс. NiO - 7,5% CoO - --- MoO3 - 21,0% |
| ГКД-202 | Насыпной вес - 820 кг/м3 Коэффициент прочности - 2,1 кг/мм Удельная поверхность - 220 м2/г Диаметр гранул - 1,3-2,1мм Химический состав в пересчете на сухое вещество, % масс. NiO - 4,5% CoO - 0,5-1,0% MoO3 - 14,0% |
| ГКД-202П | Насыпной вес - 760 кг/м3 Коэффициент прочности - 2,4 кг/мм Удельная поверхность - 225 м2/г Диаметр гранул - 1,5-2,1мм Химический состав в пересчете на сухое вещество, % масс. NiO - 3,0% CoO - --- % MoO3 - 9,5% |
| ГП-526 | Насыпной вес - 650 кг/м3 Коэффициент прочности - 1,4 кг/мм Удельная поверхность - 180 м2/г Диаметр гранул - 1,5-3,0мм Химический состав в пересчете на сухое вещество, % масс. NiO - 3,0-4,0% CoO - --- % MoO3 - 12,0-16,0% |
Каталитическую сложную систему представляет собой современный катализатор гидропереработки, состоящий из трех компонентов, имеющие различные функции: активных компонентов (АК), модификаторов (М) и структурообразующих компонентов (СОК) (рис. 1.1).
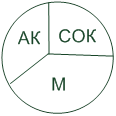
Рис. 1.1 Групповой состав катализаторов гидропереработки на основе Мо(W)
М – вещества неактивные, не способные играть роль СОК или АК, но улучшающие качество катализаторов ; AК – соединения Мо (W), стабильные в условиях катализа (сульфиды, оксиды, ксисульфиды), промотированные Со (Ni); СОК – вещества, которые могут быть получены в виде прочных гранул с развитой пористой структурой, включающей АК и М.
Активный компонент, который включает в себя оксид молибдена, вводимый в состав предшественника оксида алюминия влияет на термостабильность и структуру полученного носителя, и одновременно играя роль модификатора. Так же в качестве активных компонентов могут выступать модификаторы катализаторов гидроочистки – оксид кремния и цеолиты, при увеличении их содержания в составе такой системы резко увеличивается ее расщепляющая активность [12-14].
Для обессеривания прямогонного сырья обычно предпочитают использовать кобальт-молибденовые катализаторы, однако никель-молибденовые и кобальтникельмолибденовые катализаторы при определенных условиях также успешно удаляют серу из некоторых других видов сырья. Никель-молибденовые катализаторы могут быть даже более предпочтительными при удалении серы из высокоазотистого или крекированного сырья [1].
В большинстве случаев лучше удаляют азот и гидрируют ароматические углеводороды никель-молибденовые катализаторы.
Как правило, более чувствительны к изменениям парциального давления водорода никель-молибденовые катализаторы, следовательно работа с повышенными давлениями дает им преимущества перед кобальт-молибденовыми катализаторами при прочих равных условиях. Относительная эффективность никель-молибденового катализатора при высоких давлениях больше, чем при низких, но это не означает, что при повышенных давлениях водорода, никель-молибденовые катализаторы всегда эффективнее кобальт-молибденовых [15].
Методическая часть
Исходные вещества и реагенты
В настоящей работе использовали следующие неорганические соли: Na2МоO4, МоO3, NaOH, НСl, соль Мора, KCNS, CuSO4, квалификации «х.ч.». Кислоты: HNO3, H2SO4, HClO4 квалификации «х.ч.». В работе также использовали органические разбавители: ацетон и толуол квалификации «х.ч.». Все разбавители использовали без дополнительной очистки.
В качестве экстрагента использовали технический продукт - карбонат метилтриоктиламмония общей формулы: [(C8H17)3CH3N]+CH3СО3-. Содержание основного вещества в пересчёте на сухой продукт - не менее 96%. Содержание непрореагировавших аминов - не более 4%. Содержание физически растворённой воды - не более 15%.
В работе использовали молибдат МТОА, который получали из карбоната МТОА заменой аниона Мо на соответствующий по методикам, описанным в разделе 2.2.
Алюминий-кобальтового кека
Для выщелачивания кобальта навеску отмытого воздушно-сухого алюмо-кобальтового кека взвешенную на электронных аналитических весах с точностью ±0,01 г загружали в реактор (стеклянная круглодонная трехгорлая колба, объем которой составлял от 250 мл до 4000 мл) совместно с предварительно нагретым до необходимой температуры раствором требуемой концентрации выщелачивающего реагента, масса которого обеспечивала запланированное для данного опыта соотношение Т:Ж. Реактор был помещен в ванну термостата, нагретую до требуемой температуры. Время проведения процесса выщелачивания фиксировали с момента загрузки пробы алюмо-кобальтового кека. Эксперименты проводили при непрерывном перемешивании реакционной массы электромешалкой при числе оборотов равным 500-1000 об/мин.
Пробы растворов перед измерением количественного содержания кобальта и алюминия предварительно отделяли центрифугированием (при 1000 об/мин в течении 5 мин) или фильтрацией от взвешенных частиц твердой фазы. Содержание кобальта в пробах определяли методом атомно-эмиссионного спектрального анализа с индуктивно-связанной плазмой на оптическом плазменном спектрометре марки JY-38 (Jobin Yvon, Франция) в аналитическом центре ОАО «Институт «ГИНЦВЕТМЕТ».
2.12. Рентгенофазовый анализ твердых образцов
Рентгенофазовый анализ твердых образцов проводили на дифрактометре анализаторе марки D2 PHASER Bruker. Расшифровку полученных рентгенограмм проводили при помощи кристаллографической базы JCPDS-ICDD 1997.
Обсуждение результатов
ПРИЛОЖЕНИЕ
Таблица 25
Кинетика экстракции Мо из бикарбонатного раствора карбонатом МТАА при барботаже CO2.
Условия экстракции: барботаж СО2, О:В=1:1, t = 20±2°C, τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 700 об/мин.
Раствор: СМо = 13,2 г/л, СAl = 2,8 г/л, рН = 6,9.
Экстрагент: 100 % карбонат МТАА, С(R4N+) = 1,7M, C(CO32-) =0,7M.
| № п.п. | τК., мин | CMo В.Ф., г/л | CМо О.Ф., г/л | EMo(VI), % |
| 1 | 0 | 13,2 | 0,0 | 0,0 |
| 2 | 1 | 10,3 | 2,9 | 22,0 |
| 3 | 5 | 8,9 | 4,3 | 32,6 |
| 4 | 10 | 7,7 | 5,5 | 41,7 |
| 5 | 15 | 7,7 | 5,6 | 42,4 |
| 6 | 30 | 7,7 | 5,5 | 41,7 |
| 7 | 45 | 7,7 | 5,5 | 41,7 |
| 8 | 60 | 7,7 | 5,5 | 41,7 |
Таблица 26
Экстракции Мо из бикарбонатного раствора карбонатом МТАА при различных соотношениях О:В.
Условия экстракции: p(СО2)ИЗБ.=1,25 атм., t = 20±2°C, τК. = 15 мин., τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 700 об/мин.
Раствор: СМо = 13,2 г/л, СAl = 2,8 г/л, рН = 6,9.
Экстрагент: 100 % карбонат МТАА, С(R4N+) = 1,7M, C(CO32-) =0,7M.
| О:В | CMo(VI) В.РАВ., г/л | CMo(VI) О.РАВ., г/л | CAl В.РАВ., г/л | CАl О.РАВ., г/л | ЕMo(VI), % | EAl, % |
| 1:1 | 5,3 | 12,4 | 0,5 | 2,3 | 93,9 | 82,1 |
| 1:2 | 6,2 | 15,9 | 1,2 | 3,7 | 60,2 | 66,1 |
| 1:3 | 6,8 | 21,9 | 0,8 | 6,7 | 55,3 | 79,8 |
| 1:4 | 7,0 | 28,8 | 1,1 | 8,0 | 54,5 | 71,4 |
| 1:5 | 7,3 | 33,9 | 1,5 | 7,5 | 51,4 | 53,6 |
Таблица 27
Кинетика экстракции Мо из карбонатных и бикарбонатных растворов метилсульфатом МТОА.
Условия экстракции: t = 20±2°C, τК. = 15 мин., τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 700 об/мин.
Карбонатный раствор после выщелачивания: СМо = 23,2 г/л, СAl = 3,4 г/л, рН = 9,5.
Бикарбонатный раствор после карбонизации: СМо = 23,2 г/л, СAl = 2,8 г/л, рН = 7,3.
Экстрагент: 2,25 М метилсульфат МТОА.
| № п.п. | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| τК., мин | 0 | 5 | 10 | 20 | 30 | 45 | 60 |
| Карбонатный раствор после выщелачивания | |||||||
| CMo В.Ф., г/л | 23,2 | 21,6 | 21,6 | 21,6 | 21,4 | 21,5 | 21,5 |
| CМо О.Ф., г/л | 0,0 | 1,6 | 1,6 | 1,6 | 1,8 | 1,7 | 1,7 |
| ЕMo(VI), % | 0,0 | 6,9 | 6,9 | 6,9 | 7,8 | 7,3 | 7,3 |
| Бикарбонатный раствор после карбонизации | |||||||
| CMo В.Ф., г/л | 23,2 | 21,6 | 21,6 | 21,7 | 21,8 | 21,8 | 21,7 |
| CМо О.Ф., г/л | 0,0 | 1,6 | 1,6 | 1,5 | 1,4 | 1,4 | 1,5 |
| ЕMo(VI), % | 0,0 | 6,9 | 6,9 | 6,4 | 6,1 | 6,1 | 6,4 |
| Бикарбонатный раствор после карбонизации в автоклаве при p(СО2)ИЗБ.=1,25 атм. | |||||||
| CMo В.Ф., г/л | 23,2 | 22,5 | 22,2 | 22,2 | 22,2 | 22,2 | 22,2 |
| CМо О.Ф., г/л | 0,0 | 0,7 | 1,0 | 1,0 | 1,0 | 1,0 | 1,0 |
| ЕMo(VI), % | 0,0 | 3,0 | 4,3 | 4,3 | 4,3 | 4,3 | 4,3 |
Таблица 28
Экстракция Мо из карбонатных растворов карбонатом МТОА.
Условия экстракции: t = 20±2°C, τК. = 15 мин., τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 700 об/мин.
Карбонатный раствор после выщелачивания: СМо = 23,2 г/л, СAl = 3,4 г/л, рН = 9,5.
Экстрагент: 100 % карбонат МТОА С(R4N+) = 1,7M, C(CO32-) =0,7M.
| № п.п. | С(Na2CO3), М | CMo В.Ф., г/л | CМо О.Ф., г/л | CAl В.Ф., г/л | CАl О.Ф., г/л |
| 1 | 0,3 | 5,3 | 19,0 | 0,4 | 3,0 |
| 2 | 0,4 | 5,1 | 18,9 | 1,1 | 2,3 |
| 3 | 0,5 | 5,2 | 18,9 | 1,1 | 2,3 |
| 4 | 0,6 | 5,3 | 18,8 | 1,1 | 2,3 |
| 5 | 0,7 | 5,4 | 18,7 | 1,1 | 2,3 |
Таблица29
Изотерма экстракция Мо из карбонатного раствора карбонатом МТОА.
Условия экстракции: t = 20±2°C, τК. = 15 мин., τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 700 об/мин.
Карбонатный раствор после выщелачивания: СМо = 24,8 г/л, СAl = 3,4 г/л, С(Na2CO3) = 0,3 M, рН = 9,6.
Экстрагент: 100 % карбонат МТОА С(R4N+) =1,7M, C(СО32-) =0,7M
| № п.п. | О:В | CMo В.Р., г/л | CMo О.Р., г/л | CAl В.Р., г/л | CAl О.Р., г/л |
| 1 | 5:1 | 0,56 | 4,8 | 0,0 | 0,68 |
| 2 | 4:1 | 0,74 | 6,0 | 0,0 | 0,84 |
| 3 | 3:1 | 1,20 | 7,9 | 0,0 | 1,13 |
| 4 | 2:1 | 2,49 | 11,2 | 0,0 | 1,69 |
| 5 | 1:1 | 5,36 | 19,4 | 0,0 | 3,38 |
| 6 | 1:2 | 9,30 | 31,0 | 0,0 | 6,75 |
| 7 | 1:3 | 12,70 | 36,3 | 0,0 | 10,13 |
| 8 | 1:4 | 15,35 | 37,8 | 0,0 | 13,50 |
| 9 | 1:5 | 17,03 | 38,8 | 0,0 | 16,88 |
| 10 | 1:6 | 18,30 | 39,0 | 0,0 | 20,25 |
| 11 | 1:7 | 19,22 | 39,1 | 0,0 | 23,63 |
Таблица 30
Экстракция Мо из карбонатного раствора толуольными растворами карбоната МТОА.
Условия экстракции: О:В=1:5, t = 20±2°C, τК. = 15 мин., τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 700 об/мин.
Карбонатный раствор после выщелачивания: СМо = 24,8 г/л, СAl = 3,4 г/л, С(Na2CO3) = 0,3 M, рН = 9,6.
| № п.п. | CТОМАК в толуоле, % об. | CMo В.Р., г/л | CMo О.Р., г/л | ЕMo(VI),% | DMo(VI), % | lgDMo(VI) | lgC((R4N)2CO3 |
| 1 | 10 | 23,0 | 8,8 | 35,5 | 0,38 | -0,42 | 1,00 |
| 2 | 20 | 23,0 | 9,2 | 37,1 | 0,40 | -0,40 | 1,30 |
| 3 | 30 | 22,6 | 10,8 | 43,5 | 0,48 | -0,32 | 1,48 |
| 4 | 50 | 21,6 | 15,9 | 64,1 | 0,74 | -0,13 | 1,70 |
| 5 | 75 | 19,5 | 26,6 | 107,2 | 1,36 | 0,13 | 1,88 |
| 6 | 100 | 17,0 | 38,8 | 156,45 | 2,28 | 0,36 | 2,00 |
Таблица 31
Кинетика экстракции Мо из карбонатного раствора карбонатом МТОА в толуоле.
Условия экстракции: стальной автоклав, p(СО2)ИЗБ.=5 атм., О:В=1:1, t = 20±2°C, τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 1000 об/мин.
Карбонатный раствор после выщелачивания: СМо = 62,2 г/л, СAl= 7,6 г/л, С(Na2CO3) = 0,075 M.
Экстрагент: 50 % карбонат МТОА в толуоле С(R4N+) =0,97M, C(СО32-) =0,48M
| № п.п. | τК., мин | CMo(VI) В.Ф., г/л | CMo(VI) О.Ф., г/л |
| 1 | 0 | 62,2 | 0,0 |
| 2 | 5 | 30,6 | 31,6 |
| 3 | 10 | 28,6 | 33,6 |
| 4 | 15 | 26,3 | 35,9 |
| 5 | 20 | 25,3 | 36,9 |
| 6 | 30 | 24,4 | 37,8 |
| 7 | 45 | 23,2 | 39,0 |
| 8 | 60 | 23,9 | 38,3 |
Таблица 32
Кинетика реэкстракции Мо(VI) из органического экстракта молибдата МТОА в толуоле водным раствором NН4НCO3.
Условия реэкстракции: О:В=1:1, t = 20±2°C, τРАССЛАИВАНИЯ ФАЗ. = 15 мин. скорость перемешивания – 1000 об/мин.
Состав экстракта: молибдат МТОА в толуоле (С(R4N+) =0,9M, CМо =0,45M)
Состав реэкстрагирующего раствора: 1,0 М водный раствор NН4НCO3.
| № п.п. | τК., мин | CMо(VI) В.Ф., г/л | CMо(VI) О.Ф., г/л |
| 1 | 0 | 0,00 | 0,00 |
| 2 | 15 | 19,30 | 23,51 |
| 3 | 30 | 19,07 | 23,75 |
| 4 | 60 | 19,30 | 23,51 |
Таблица
Степень извлечения кобальта от температуры для системы выщелачивания 1,2М (NH4)2CO3, Т:Ж=1:50 по гравиметрии и спектрофотометрии.
| Система: 1,2М (NH4)2CO3, Ж:Т=1:50 | Температура | Гравиметрия | Спектрофотометрия | ||
| № п.п. | t, °С | С(Со), г/л | α(Со), % | С(Со), г/л | α(Со), г/л |
| 1 | 25 | 0,14 | 19,4 | 0,16 | 22,9 |
| 2 | 50 | 0,22 | 31,80 | 0,23 | 33,3 |
| 3 | 75 | 0,33 | 38,1 | 0,29 | 41,2 |
Таблица
| Система: NH4OH+(NH4)2CO3-1,25M, Ж:Т=1:50 | Температура | Гравиметрия | Спектрофотометрия | ||
| № п.п. | t, °С | С(Со), г/л | α(Со), % | С(Со), г/л | α(Со), г/л |
| 1 | 25 | 0,19 | 28,6 | 0,21 | 30,0 |
| 2 | 50 | 0,44 | 39,8 | 0,32 | 45,7 |
| 3 | 75 | 0,4 | 56,1 | 0,30 | 42,0 |
Кафедра технологии редких элементов и наноматериалов на их основе
Дата: 2019-04-23, просмотров: 427.