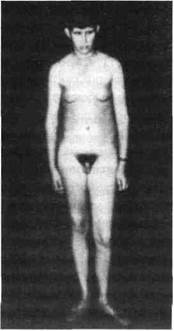
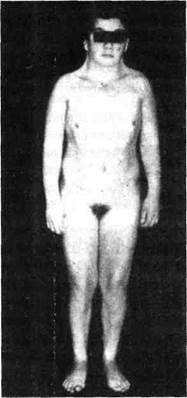
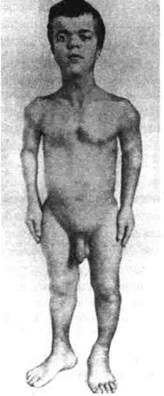
По критериям ВОЗ, подростком считается индивид в возрасте от 10 до 21 года, что примерно совпадает с моментом полного прекращения роста костей в длину. Само слово «подросток» указывает на характернейшую особенность юности — быстрый рост. Не удивительно, что нарушения ростовых и анаболических процессов часто встречаются в практике ювенильной эндокринологии.
Для более глубокого понимания патогенеза и клинической картины подобных заболеваний у подростков необходимо напомнить современные данные о гормоне роста — СТГ и его действии в норме и при патологии.
Гормон роста открыт Г.М. Ивенсом и Дж.А. Лонгом в 1921 году, но в чистом виде получен лишь через 35 лет. Из общего числа 160 аминокислот идентичны для СТГ, хорионического гонадотропина (ХГ) плаценты и для термином человека. Таким образом, СТГ и ХГ, гены которых находятся в 17-й хромосоме, — близкие гомологи (83 % структуры). Известную гомологию с ними проявляет и пролактин (16% структуры). В связи с этим у СТГ, кроме основной, имеется также слабая лактогенная активность. Более того, ХГ имеет выраженную ростостимулирующую активность, благодаря чему он широко применяется как препарат в лечении низкорослости. В плаценте экспреси-руется особый вариант СТГ—В-СТГ.
Гормон роста видоспецифичен. Так, у человека высокоактивен лишь соматотропин обезьян. Гипофиз выделяет СТГ в виде мономера и димера. Есть основания полагать, что плазминоподобные ферменты в организме должны активировать СТГ путём протеоли-за, вычленяя из него наиболее действенную часть. В таком случае гипофизарный СТГ можно рассматривать как прогормон.
Секреция СТГ сильно стимулируется гипоталами-ческим соматолиберином (он же — соматокринин), а также (в меньшей степени) — тиролиберином, в-эндорфином, допамином, серотонином, норадре-налином, ацетилхолином. Соматотропиногенез тормозится соматостатином (его нейроны в подбугорье реципрокно связаны с соматокрининовыми нейронами),
60
адреналином и неэтерифицированными жирными кис лотами.
Гормон роста выделяется импулъсно, причём в сутки бывает от 4 до 10 коротких периодов высокой сек реции, в том числе — при физических усилиях, стрес-се, гипогликемии, при приеме в пищу аминокислот (ocо-бенно аргинина, которым так богаты холодец и другие блюда, содержащие коллагеновые белки). Особенно любопытен научно доказанный пик секреции СТГ в медленноволновой фазе сна, когда возникают знакомые практически всем живущим на земле людям ощуще-ния «проваливания в бездну» или «падения с высоты), сопровождающиеся вздрагиванием всего тела. Xopо-шо известно народное поверье—«когда летаешь во сне, значит — растёшь», что, оказалось, действительно имеет отношение к пикам секреции соматотропина. Эстрогены, вазопрессин и глюкагон усиливают ос-вобождение СТГ, а прогестины — тормозят.
В клинике тесты на трансгипоталамическую прово-кацию секреции СГГосуществляются с помощью вве-дения тиролиберина, аргинина или индукции инсулино-вой гипогликемии. При беременности и кормлении соматотропиногенез резко возрастает, причём при бе-ременности большая часть СТГ— плацентарного про-исхождения. Время полужизни СТГ в плазме состав-ляет от 20 до 30 минут, а катаболизм гормона идет преимущественно в печени и в какой-то степени в поч-ках.
СТГ опосредует свое действие через рецепторы со-матомаммотрофного типа, которые стоят особняком от других ретрансляторов гормонального сигнала и име-ют, вероятно, пептидные внутриклеточные посредни-ки.
Метаболическое действие СТГ включает неболь-шое количество собственных и широкий спектр пептид-опосредованных эффектов этого гормона. Тканевыми аутокринными и паракринными посредниками, обяза-тельными для реализации большинства эффектов СТГ, служат инсулиноподобные факторы роста (сома-томедины).
Известно около семи соматомединов, но все они дей-ствуют путём понижения активности аденилатциклаз-ного механизма в различных клетках, но наибольшее физиологическое значение имеют соматомедин С (ин-сулиноподобный фактор роста I — ИФР- I ) и сома- томедин А (инсулиноподобный фактор роста II ИФР-11).
Соматомедин С (ИФР-1) — посредник всех основ-ных ростовых и метаболических эффектов СТГ в по-стнатальном периоде. Это — основной пептид из 70 аминокислот, кодируемый в 12-й хромосоме и напо-ловину гомологичный проинсулину ИФР- I может об-
разовываться всеми мезодермальными, многими эк-тодермальными и некоторыми энтодермальными клетками, но наиболее активно он продуцируется и выделяется в системный кровоток макрофагами печени, вследствие чего может рассматриваться как печёночный СТГ-зависимый гормон. Время полужизни ИФР-1 в плазме составляет до получаса, но он имеет белки-переносчики, продлевающие срок его существования в крови в 6-18 раз. Переносчик ИФР- I третьего типа поступает в плазму пропорционально уровню СТГ.
Секрецию ИФР- I стимулирует и ХГ плаценты. Кроме печени, ИФР-1 для паракринных и аутокринных нужд вырабатывается в почках, костях, мышцах, желудочно-кишечном тракте и даже в самом аденогипофизе. ИФР- I ингибирует продукцию соматокринина, замыкая обратную связь в системе центральной регуляции роста и анаболизма.
При ожирении уровень ИФР- I возрастает, вызывая снижение продукции СТГ. В то же время похудение и белковая недостаточность (включая начальные стадии алиментарной дистрофии, квашиоркор, нейрогеную ано-рексию и другие подобные состояния) понижают продукцию ИФР- I и растормаживают биосинтез СТГ. Кто из нас не помнит знаменитого родительского — «как ты похудел и вытянулся за время болезни!». Есть основания полагать, что это — не чисто кажущееся впечатление.
Наши наблюдения (Строев Ю.И. с соавт., 2003)
|
|
также показывают, что у подростков-призывников с гипотрофией (трофологической недостаточностью), рост, наоборот, часто опережает средние должные показатели. Можно полагать, что и здесь сказывается указанный соматомедин-зависимый эффект.
В периоде внутриутробного развития рост тела не определяется СТГ. Это доказывается нижеследующими наблюдениями: при наследственном дефиците СТГ матери рождают детей с дефицитом СТГ, но с нормальной длиной тела. Нормального размера и младенцы у африканских пигмеев Заира и Бурунди, хотя у них со-матомедин С-опосредованный эффект СТГ в постна-гальном онтогенезе нарушен в силу доминантной мутации. В дальнейшем их рост задерживается. Установлено, что количество ИФР- I y пигмеев сниже-но, хотя уровень СТГ у них выше, чем у здоровых европейцев.
Существуют этносы, у которых средний рост велик,
а процент лиц, формально подпадающих под критерий
гигантизма, намного выше, чем у большинства наро-
дов. Таково, например, племя тутси, населяющее Ру-
|
|
анду, Бурунди и Заир. Средний рост мужчин этого пле-
мени - 193 см, а средний рост женщин - 175 см, что
считается результатом генетической адаптации. Курьёзно, что тутси проживают территориально там же, где и пигмеи. Об удивительном соседстве племён гигантов и карликов писал еще Геродот! В определении роста это косвенно свидетельствует о преобладании генетических факторов над экологическими.
По имеющимся в литературе данным, среди достоверных, медицински освидетельствованных случаев гигантизма, одним из самых высокорослых из когда-либо живших на Земле людей был наш соотечественник Фёдор Махов (1880-1905), чей рост составлял 285 см (при весе 182 кг). Рост Джона Миддлтона из Ливерпуля (1578-1623) был 282 см. Человеком высокого документально зарегистрированного роста, страдавшим опухолью гипофиза, был Роберт Валдов (Штат Иллинойс, США). В 13 лет его рост составлял 214 см, а в в возрасте 22 лет, когда он умер (1940 г.), его рост достиг 286 см при массе тела 200 кг. Из хроник известны «ирландские гиганты» — Корнелиус Мегрэт (1742-1768) и Чарльз О'Брайен (1761-1783), у скелетов которых еще Дж. Хантер, поместивший один из них в музей Королевского Хирургического Колледжа в Лондоне, зафиксировал выраженное увеличение турецкого седла и необычную толщину костей.
Читатель несомненно заметил, что век Корнелиу-са, Чарльза, Джона, Роберта и Фёдора был, увы, недолог —они едва преодолели подростковый возраст. Аналогичный экспонат (скелет императорского слуги Буржуа, рост которого при жизни достигал 227 см) был включён в экспозицию петербургской Кунсткамеры Петром I Великим, который, впрочем, и сам был гигантом не только в историко-политическом, но и в биологическом смысле (204 см). Правда, император, по-видимому, не страдал гипофизарным гигантизмом. Вероятнее всего, у Петра Алексеевича Романова был синдром Марфана.
В истории зафиксированы случаи сверхгигантского роста (около 3 м), хотя эти исторические сведения могут быть недостоверными. Имена многих гипофизар-ных гигантов хранит история медицины и .. .баскетбола. Супергигант чеченец Увайс Ахтаев (рост—235 см, размер обуви — 58!) и латышский гигант-спортсмен Ян Круминьш заработали немало очков на баскетбольных аренах 60-х годов прошлого века, защищая цвета сборной СССР. Из приведённых примеров ясно, что сверхвысокий рост так же, как и гипофизар-ный нанизм, вполне совместимы с социальной активностью и интеллектуальной полноценностью. В настоящее время самым высокорослым представителем человечества, по-видимому, считается житель Мозамбика Габриэль Э. Моньяне (245, 7 см — с утра).
61
В качестве ростового фактора тканей плода действует соматомедин А — ИФР-П, продукция которого хотя и требует минимального уровня гормона роста, но к надфизиологическим концентрациям СТГ практически нечувствительна. ИФР-11 — нейтральный пептид из 67 аминокислот, закодированный в 11 -й хромосоме и гомологичный ИФР-1 почти на 70%. Соматомедин А известен в двух формах. Как паракринный и аутокринный регулятор он вырабатывается в тех же клетках, что и ИФР-1. В постэмбриональном периоде ростовое действие ИФР-11 ослабевает на протяжении первого года жизни и является актуальным только для зубных зачатков. Интересно, что у пигмеев относительный размер зубов крупнее, чем у представителей других народов, так как действие соматомедина А у них не нарушено. Вместе с тем у больных акромегалией и гипофизарным гигантизмом, когда усилено ИФР-/-опосредованное действие СТГ, характерным симптомом является наличие больших межзубных промежутков (диастема), а относительный размер зубов снижен.
Соматомедин В, объединяющий 4 разных кислых пептида, охарактеризованный хуже других сомато-мединов, по-видимому, участвует в СТ-зависимом усилении роста глиальных клеток. Так как СТГ сам стимулирует продукцию инсулина в В-клетках, формально инсулин вместе с сомтомединами тоже может быть причислен к кругу посредников действия СТГ, на рецепторы которых он способен влиять (Уил-сонДж., 1994).
Следует отметить, что соматомедины в свою очередь опосредуют те присущие им ростовые эффекты, которые связаны с ускорением деления клеток через стимуляцию клеточной орнитиндекарбоксилазы, генерирующей активаторы клеточной пролиферации — полиамины.
СТГ непосредственно стимулирует рост хондроци-тов и сам оказывает острые контринсулярные эффекты на метаболизм: снижает синтез липидов в адипоци-тах и поглощение глюкозы печенью и жировой тканью, усиливает освобождение жирных кислот в кровь. В то же время он способствует синтезу инсулина и сома-томединов, что позволяет, правда, в несколько отсроченном и пролонгированном режиме запустить через эти посредники более широкий круг пролиферативных процессов и, главное, осуществить продлённое инсу-линоподобное действие. Например, и СТГ, и инсулин оба стимулируют поглощение аминокислот рядом тканей. Вышеописанное замечательное двухфазное приспособление позволяет усиливать рост и анаболизм и в то же время не расплачиваться за это гипогликемией
62
и снижением процессов катаболизма (Лингаппа В. I,
1997)!
Из-за своеобразия взаимоотношений СТГ и инсу
линовой регуляции нарушения продукции СТГ небез
различны для углеводного метаболизма. Так, при
гипофизарном нанизме больные подвержены гипогли
кемии между приёмами пищи. При гигантизме и aк
ромегалии развивается инсулинорезистентность.В
норме гипергликемия тормозит продукцию СТГ. Но при
инсулинзависимом сахарном диабете концентрации
СТГ парадоксально повышены, как полагают, в свя-
зи с инсулиноподобным действием соматомединов
и в попытке оказать инсулинотропный эффект на В-
клетки островков Лангерганса. У гипофизарных кар-
ликов и гигантов сахарный диабет протекает при peз-
ко пониженной скорости развития микроангиопатии,
что свидетельствует об участии СТГ и соматоме-
динов в ее патогенезе. СТГ ускоряет разрушение ин-
сулина, являясь одновременно его прямым антагони-
стом, так как через активацию фосфорилазы СТГ
нарушает синтез глюкозо-6-фосфата в анаэробном
пути Мейергофа-Эмбдена. Наконец, гиперпродукция
СТГ способствует синтезу контринсулярного сома
тостатина, а при депанкреатизации и на фоне инсу-
линзависимого сахарного диабета СТГ ростостиму
лирующего действия не оказывает.
Через соматомедины и инсулин СТГ вызывает сле-дующие эффекты (рис. 21): усиление включения амино-кислот, уридина, тимидина и сульфата в клетки хряща ускорение синтеза белка, нуклеиновых кислот и проли-ферации хондроцитов и клеток всех других тканей; ин-дукция положительного азотистого баланса; снижение производства мочевины; усиление использования липи-дов; начальное понижение и последующие нормализа-ция и повышение уровня глюкозы, свободных жирных кислот и аминокислот в крови; увеличение синтеза гли-когена в мышцах и печени. СТГ благоприятствует син-тезу кетоновых тел, в связи с чем сахарный диабет у лиц с соматотропиномами может осложняться кетоацидо
ЗОМ.
СТГ также влияет на метаболизм других гормонов
ускоряет синтез ренина и альдостерона, активацию
кальциферола путём его гидроксилирования, которая
влечет за собой усиление всасывания и тканевого ис-
пользования кальция, а также повышает конверсию Т4
в ТЗ.
Нарушения функционирования системы «СТГ—со матомедины» приводят к различным расстройствам ростовых и анаболических процессов, особенно ярко выраженным у подростков. Поэтому при постпубер- татном угнетении продукции СТГ у взрослых лиц
| мерно в 5 раз чаще. Интересно, что среди гипофизар-ных гигантов соотношение мужчин и женщин — примерно равное, но среди пациентов с акромегалией женщины значительно преобладают. В подростковом возрасте заболевание чаще встречается у юношей, чем у девушек. Этиология и патогенез. С момента окостенения метаэпифизарных хрящей (примерно, к 21 -23 годам у юношей и к 23-25 — у девушек) кости более не растут в длину, хотя при периостальном росте могут продолжать утолщаться. Таким образом, патогенез и проявления нарушений, связанных с СТГ, зависят от длительности и времени начала дисфункции аденогипофиза. 63 |
 симптомов болезни может вообще не быть. Углубленное обследование взрослых лиц со сниженной продукцией гормона роста выявляет несколько сниженную толерантность к физической нагрузке, тенденцию к избыточной общей массе тела и к понижению соотношения массы мышц и жировой ткани. Смертность от сердечно-сосудистых заболеваний в этой группе увеличена, но частота злокачественных новообразований, напротив, снижена. В последнее время изучается возможность использования СТГ при различных метаболических расстройствах — в остром периоде травмы, после обширных хирургических вмешательств, при ожогах, для профилактики и лечения остеопороза, при сердечной деятельности вследствие идио-патической дилатационной кар-диомиопатии, в геронтологии (Дедов И.И., Тюльпаков А.Н., Петер- коваВ.А., 1998).
симптомов болезни может вообще не быть. Углубленное обследование взрослых лиц со сниженной продукцией гормона роста выявляет несколько сниженную толерантность к физической нагрузке, тенденцию к избыточной общей массе тела и к понижению соотношения массы мышц и жировой ткани. Смертность от сердечно-сосудистых заболеваний в этой группе увеличена, но частота злокачественных новообразований, напротив, снижена. В последнее время изучается возможность использования СТГ при различных метаболических расстройствах — в остром периоде травмы, после обширных хирургических вмешательств, при ожогах, для профилактики и лечения остеопороза, при сердечной деятельности вследствие идио-патической дилатационной кар-диомиопатии, в геронтологии (Дедов И.И., Тюльпаков А.Н., Петер- коваВ.А., 1998).
ГИГАНТИЗМ И АКРОМЕГАЛИЯ
| Рис. 21. Регуляция системы "СТГ — инсулиноподобные ростовые факторы" и биологическое действие СТГ (ИФР-1 — инсулинонодобный фактор роста, SCr — соматокрииин, ST— соматотрофы, SS — соматостатин) |
Определение. Гигантизм и акромегалия — единое заболевание, возникающее при хронически избыточной продукции клетками-сома-тотропами аденогипофиза гормона роста (соматотропного гормона, соматотропина, СТГ).
Если болезнь возникает рано, то есть при незакрытых зонах роста костей, то у подростков формируется чрезмерно высокий рост—гигантизм. Если болезнь развивается после закрытия зон роста костей в длину, то она проявляется толъко симптомами акромегалии.
Если же к моменту закрытия зон роста костей гиперсекреция СТГ не прекращается, то на гигантизм могут наслаиваться симптомы акромегалии. Такая со-четанная патология — гигантизм-акромегалия — может наблюдаться и у подростков.
Распространенность. Подавляющая часть больных представляет собой спорадические случаи, хотя имеются семейные формы этого синдрома. . Частота акромегалии невелика—порядка 5-7 случаев на 100000 населения. Гигантизм встречается при-
Как впервые показал К. Бенда (1900), в 99% случаев этиология болезни связана с соматотропиномой — опухолью из эозинофильных клеток, образующих СТГ. Соматотропиномы почти всегда доброкачественные, хотя изредка проявляют инвазивность. Аденогипофи-зарная локализация типична, хотя описаны эктопические соматотропиномы—в парафарингеальной области, синусах основной кости, желудочно-кишечном тракте, бронхах и даже в поджелудочной железе. В 1% случаев синдром гигантизма-акромегалии обусловлен гиперпродукцией соматокринина (соматолиберина) гипоталамуса и вторичной неопухолевой гиперплазией соматот-ропов. Фактором риска для гиперплазии эозинофильных клеток гипофиза считается и беременность.
В 90 % случаев причиной гигантизма является макроаденома, а в 9 % — микроаденома аденоги-пофиза. Еще реже гигантизм возникает на фоне синдрома «пустого турецкого седла». Как казуистика описана смешанная эозино-хромофобная аденома. В принципе гигантизму может способствовать повышенная чувствительность рецепторов тканей эпифи-зарных хрящей к СТГ (это отмечено в восстановительный период после инфекций).
Хорошо известна генетическая модель гипофизарно-го гигантизма, полученная собаководами. В патогенезе гигантизма ключевую роль играют соматическая мутация в соматотрофах и вызванный ею неопластический процесс.
Наследственными гипофизарными гигантами являются представители двух пород — бульдоги и ирландские волкодавы. Интересно, что представители породы карликовых бульдогов — не гипофизарные карлики, а нормальные родоначальники своих более знаменитых гигантских сородичей. У всех собак-моделей гигантизма и примерно у 40% пациентов с гигантизмом или акромегалией на почве соматотропиномы в клетках опухоли выявляется мутация а-субъединицы белка Gs, вследствие которой этот элемент пострецепторного ретранслятора сигнала со матокринина утрачивает способность к гидролизу ГТФ и «зависает» в хронически активном состоянии. Аденилатциклазный передаточный механизм пролонгирование активируется и заставляет соматотрофы вырабатывать избыток СТГ и ускоренно пролифери-ровать. В остальных случаях природа трансформации клеток соматотропиномы иная и пока не ясна. Избыток СТГ ускоряет рост не одних лишь костей, но и всех других, способных к росту, тканей и органов.
Поэтому было бы совершенно неправильным трактовать ростовые эффекты СТГ как ограниченные лишь соединительной тканью или опорно-двигательным ап-
64
паратом. СТГ также способствует росту практически всех мягких тканей. Достаточно указать на его лим-фопролиферативное (и иммуностимулирующее!) дей-ствие. Он способствует также гипертрофии миокарда и почек, эритропоэзу, заживлению ран (рис. 21). Харак-теризуя эффекты СТГ, А. Гайтон (1989) кратко и ёмко формулирует, что система «СТГ — соматомедины »
стимулирует рост «всего, что может расти».
ГИПОФИЗАРНЫЙ ГИГАНТИЗМ
Клиника. Подростки с гигантизмом жалуются на слабость, головокружения, почти постоянные головные боли, боли в конечностях, плохую память, сердцебие-ния. Девушек волнуют чрезмерные рост и размеры ноги, недоразвитие молочных желез, у юношей может быть гипосексуальность. Обращают на себя внимание высокий рост (выше 190 см у девушек и выше 200 см — у юношей, или превышающий среднепопуля-ционные значения на 2 и более сигмальных отклонения).
Иногда в клинике болезни на передний план высту-пают грубые черты лица при общей инфантильности У юношей может быть макрогенитализм. Масса тела обычно соответствует росту, конечности — относи-тельно длинные.
Несмотря на отдельные наблюдения гигантизма у ин-теллектуально выдающихся индивидов, следует отме-тить, что психика многих пациентов при этой патологии может быть недоразвитой: средние способности, peбя-чество, склонность к меланхолии, идеям преследования Подростки с гигантизмом все более обгоняют сверст-ников физически, что заметно при очередных профос-мотрах. Внутренние органы большие, но при высоком росте это не очень заметно. При отставании в скорости роста сердца от роста тела бывают головокружения, об-мороки.
Кроме ускоренного роста тела в длину, многие про-явления зависят от гиперплазии и гипертрофии мягких тканей. Как правило, имеются увеличение языка (глос-сомегалия, макроглоссия), гортани, диастема (редкие зубы). Все изменяет тембр голоса таких больных, и он становится низким, звучит как бы «из глубины».
Черты лица больных подростков грубеют, костные выступы подчёркиваются, имеется прогнатизм (ниж няя челюсть выступает вперед). Нос, губы и уши yве-личиваются. Из-за синусита и прогнатизма рот час-то полуоткрыт, периорбитальная гипертрофия мягких тканей, отмечаются выраженные кожные складки. Кожа маслянистая, влажная и тёплая. Бывают гипер-трихоз, акантоз, фиброзные кожные полипы, кисты сальных желёз. Увеличиваются стопы и кисти, раз-
меры головы. Нередко обнаруживается кифосколиоз. Кожа часто гиперпигментирована.
Все это делает внешний вид больных столь характерным, что, по выражению Дж. Дэниелса и Дж. Мартина (1994), они «похожи друг на друга больше, чем на членов собственных семей». Читатели, любители киноискусства, несомненно помнят акромегалоидный тип лица выдающегося французского комика Фернанделя и характерный клишированный облик чикагских мафиози из классического голливудского комедийного фильма «В джазе — только девушки».
Функция органов обычно сохранена, однако акромегалия-гигантизм, к сожалению, порождает иногда у пациентов не только косметологические, но и метаболические проблемы.
Изредка у пациентов возникает эутироидный зоб, но могут быть и аутоиммунный тироидит, и токсический зоб (редко). Чаще отмечается пониженная толерантность к глюкозе по типу симптоматического сахарного диабета как скрытого, так и явного, с резистентностью к обычным методам лечения и к инсу-линотерапии, в частности. И при гигантизме, и при акромегалии секреция СТГ гипергликемией не подавляется.
До 30% юношей — носителей синдрома гигантизма-акромегалии — имеют сниженные либидо и потенцию, а девушки — нарушение месячных, так как у тех и у других параллельно развивается гиперпролактине-мия. В запущенных, плохо леченных случаях может развиваться вторичный гипогонадизм.
Описаны парциальные формы акромегалии и геми-ги гантизм, когда ускоренный рост касается только отдельных частей тела или одной половины тела. Иногда увеличивается в размерах всего лишь один орган, например, сердце, печень и пр. Существуют спорадические и семейные формы этих состояний, связанные, предположительно, с региональными особенностями паракринно-го опосредования активности гормона роста (Бала- болкин М.И., 1974).
Осложнения. Гигантизм может вызвать общую гипофункцию гипофиза (пангипопитуитаризм), развитие явной акромегалии, сахарного диабета, сексуальных нарушений, дистрофии миокарда, артериальной гипертензии. В тяжелых случаях возможна потеря зрения. Соматотропинома может озлокачествляться (аденокарцинома гипофиза).
Классификация. Выделяют две формы гигантизма: евнухоидную (инфантильную) и акромегалическую (при наличии признаков акромегалии). Выделяют также парциальный (частичный) гигантизм отдельных
частей тела или органов, стабильную и прогрессирующую стадии заболевания.
Диагностика. Считается, что труднее установить причину гигантизма, чем его диагностировать. Анализы крови и мочи при гиперпродукции гормона рос та обычно нормальные. Выявляются гиперфосфате-мия, гиперкальцийурия, в крови и моче повышен уровень гидроксипролина. Рентгенограмма может обнаружить расширение, деформацию и остеопороз спинки турецкого седла, но нормальные размеры турецкого седла не исключают наличия микроаденомы, которую можно лучше выявить при использовании МРТ- исследования области гипофиза. Давление аденомы на оптическую хиазму может дать битемпо-ральную гемианопсию с признаками внутричерепной гипертензии. Гигантизм-акромегалия протекает с повышенным уровнем СТГ в крови и с отсутствием цир-кадного ритма (в норме СТГ выше ночью), иногда повышается уровень соматомединов. Проба на толерантность к глюкозе помогает выявить латентный сахарный диабет.
Критерии диагноза. Рост юношей более 200 см, а девушек — более 190 см, увеличивающийся размер обуви, постоянно повышенный уровень СТГ 'и соматомединов в крови, признаки объемного процесса в области гипофиза с характерными внешними акромегалоидны-ми симптомами — всё это весьма подозрительно на наличие у подростков гигантизма-акромегалии.
В сомнительных случаях показана проба с парло- делом (бромокриптином): после его приема при гигантизме уровень СТГ снижается, а в норме — повышается (Балаболкин М.И., 1974; Балаболкин М.И., Гаврилюк Л.И., 1984). Для этого натощак за 30 минут до пробы и перед пробой производят забор крови, а затем пациенту дают таблетку парлодела (0,0025 г). После этого через 2 и через 4 часа полного голодания вновь делают заборы крови. Тест на гигантизм-акромегалию считается положительным, если через 4 часа уровень гормона роста в крови падает на 50 % и более в сравнении с базальным уровнем. В норме после приема парлодела (бромокриптина) уровень СТГ повышается. То же наблюдается и при пробе с L -дофа.
Введение при гигантизме тиролиберина (500 мкг внутривенно) повышает продукцию СТГ в 2 и более раза, особенно на 30-60-й минутах теста.
При гигантизме-акромегалии имеется парадоксальное повышение СТГ через 60-90 минут после нагрузки глюкозой (в норме ожидается падение).
В стационарных условиях (во избежание гипогли-кемического шока) можно использовать и пробу с
65
 инсулином. Для этого внутривенно вводят простой инсулин в дозе 0,15-0,2 ЕД на 1 кг массы тела. Забор крови осуществляется за 15 минут до введения инсу лина, перед его введением и спустя 15, 30, 60, 90 и 120 минут после пробы. При гигантизме-акромегалии у большинства больных подростков может наблюдаться значительное повышение продукции СТГ. Однако проба с инсулином не отличается высокой специфичностью и используется редко.
инсулином. Для этого внутривенно вводят простой инсулин в дозе 0,15-0,2 ЕД на 1 кг массы тела. Забор крови осуществляется за 15 минут до введения инсу лина, перед его введением и спустя 15, 30, 60, 90 и 120 минут после пробы. При гигантизме-акромегалии у большинства больных подростков может наблюдаться значительное повышение продукции СТГ. Однако проба с инсулином не отличается высокой специфичностью и используется редко.
Пример диагноза. Эозинофильная макроаденома гипофиза. Гигантизм (инфантильная форма) в стадии прогрессирования. Эутироидный зоб III ст.
Дифференциальный диагноз. В дифференциально-диагностическом плане следует отметить, что высокий рост — не всегда результат гипофизарной гиперфункции.
Он может быть последствием удлинённого ростового периода. В этом случае даже при нормальных концентрациях СГГ высокорослость достигается путём задержки полового созревания и окостенения метаэпи-физарных хрящей. Именно поэтому многие носители раннего и врождённого гипогонадизма высокорослы. Так, высокий рост характерен для синдрома Кляйн-фелыпера, а также для евнухоидов при ранней кастрации. Выше уже упоминалось об ускорении роста при гипотрофии у подростков в связи с выпадением ингибирующего влияния ИФР-1 на центральные ростовые регуляторы. Однако нужно подчеркнуть, что причины высокорослости не так разнообразны, как карликовости (см. ниже), а гигантизм имеет исключительно гиперсоматотропное происхождение.
При диагностике гигантизма-акромегалии надо помнить о подростках-акселератах, когда уровень СТГ нормален. У некоторых высоких подростков в периоде полового созревания могут дурнеть черты лица, что может быть ошибочно расценено в качестве начальных проявлений гигантизма-акромегалии. Бывает наследственно-конституциональный гигантизм.
При болезни Марфана (рис. 22) и в некоторых случаях врожденной дисплазии соединительной ткани мар-фаноподобного фенотипа (за рубежом известной как MASS-фенотип) высокий рост сочетается с распространенными соединительнотканными аномалиями, высоким уровнем гидроксипролина в крови и в моче. Определяются деформации грудной клетки (воронкообразная или килевидная грудная клетка), различные сколиозы, паукообразные пальцы, «готическое» твердое небо, плоскостопие и разболтанность суставов. При УЗИ брюшной полости нередко выявляются нефроптоз, деформации желчного пузыря, при УЗИ сердца—пролапс митрального клапана, ложные хорды левого желудочка.
66
Рис. 22. Синдром Мар-фана (по Т. И. Кадуриной, 2000)
Часто бывают врожденная миопия с астигматизмом и амблиопией, реже — подвывих хрусталика. Больные с синдромом Марфана чаще высокоинтеллектуальны, та лантливы и работоспособны в силу гиперкатехоламине-мии (Эфроимсон В.П., 1982).
|
|
| Рис. 23. Синдром Кляйнфельтера (по С. Зографски, 1973) |
Синдром Кляйнфельтера (46XXY) отличается евнухоидностью, гипогонадизмом, из-за дефицита aн-дрогенов юноши не бреются. Половой хроматин от-сутствует (рис. 23).
При синдроме Сотоса высокий рост сочетается с большой головой от рождения, гипертелоризмом, антимонголоидным разрезом глаз, умственной отсталостью.
При евнухоидизме — несоразмерно длинные нижние конечности, женский таз, гипогонадизм (рис. 24).
Пубертатно- юношеский диспитуитаризм (ги-поталамический синдром пубертатного периода, болезнь Симпсона-Пейджа) также отличается высоким ростом, особенно у юношей (рис. 25). Но при нем имеется гиноидное ожирение с розовыми стрия-ми, в крови — некоторое повышение уровня АКТГ и кортизола, характерны базальная и стимулированная гиперинсулинемия.
Большой вес при рождении, а в дальнейшем — большой язык, гиперплазия почек и поджелудочной железы, а также клеток Лейдига, ускоренный рост костей, а еще позже — опухоли надпочечников и других органов говорят в пользу синдрома Бекуита-Виде- манна (Блунк В., 1981).
Но только при гигантизме-акромегалии выявляется повышенный уровень СТГ и соматомединов в крови, что является важнейшим критерием диагноза при синдромосходных с этой патологией болезнях.
Исходы заболевания и прогноз. Без радикального лечения прогноз при эозинофильной аденоме гипофиза (соматотропиноме) сомнительный, больные живут в среднем 20-21 год. Утяжеляет болезнь развитие аде-нокарциномы.
Больные могут погибать от обычных инфекций. Из-за развивающихся дефектов внешности (например, чрезмерно высокий рост, являющийся предметом насмешек сверстников, акромегалоидность черт лица, асимметричность) могут возникать дисморфофоби-ческие психозы (до суицидов).
Если гиперпродукция СТГ носит очень выраженный характер, то уже при незаконченном росте тела в длину на фоне гигантизма появляются признаки увеличения мягких тканей и внутренних органов — акромегалия. Такая акромегалия дебютирует чаще в среднем возрасте — в 40-45 лет, но может манифестировать и в позднем подростковом возрасте.
Хотя большинство пациентов компенсировано в отношении инсулиновой регуляции, у существенной их части со временем развивается явный сахарный диабет, нередко осложняемый кетоацидозом. ИФР-1 вызывает у пациентов гиперплазию щитовидной железы. От 3 до 7% имеют гипертироз, и гораздо большая часть больных проявляет признаки относительной избыточности тироидной функции, вероятно, за счёт усиленной конверсии Т4 в Т3 (повышение основного обмена, потливость,
непереносимость жары). Реп-родуктивность в редких случаях возможна.
У больных ускорено развитие сердечно-сосудистых заболеваний, имеется гипер-тензия при низком уровне ренина, связанная с неальдосте-роновой задержкой натрия и воды. Имеется кардиомега-лия, осложняемая миокарди-одистрофией и застойной сердечной недостаточностью по левожелудочковому типу.
Почки характеризуются гипертрофией и гиперфункцией, но, по-видимому, менее активны в отношении прессор-ного натрийуреза.
Висцеромегалия повышает внутрибрюшное давление и предрасполагает к грыжам.
Имеется дегенеративный остеоартрит, связанный с гиперплазией хрящей, синдром лучезапястного туннеля (карпалъный синдром), парестезии.
Повышена частота лим-фопролиферативных заболеваний, полипоза кишечника и карцином толстой кишки.
При большом размере и инвазивном росте соматотро-пиномы гипофиза, как и другие неоплазмы района турецкого седла, дают неврологические расстройства. Более значительные проявления включают ринорею (при распространении опухоли вниз), дефекты полей зрения (при сдавлении хиазмы зрительных нервов), офтальмоплегию (при прорастании в пещеристый синус), гидроцефалию, изредка (при латеральном распространении) — височную эпилепсию.
Лечение. В диете ограничивают белки и калораж. Ле-
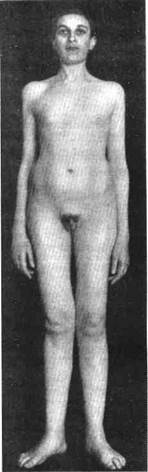
Рис. 24. Евнухоидизм (по В. Фальта, 1913)
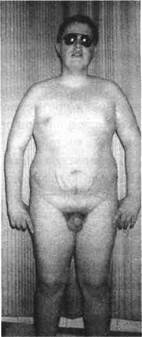
Рис. 25. Внешний вид подростка с гипоталамиче-ским синдромом пубертатного периода (собств. набл.)
67
чение может быть лекарственным, хирургическим и лучевым. Блокада продукции СТГ достигается антагонистами дофамина (бромокриптин, парлодел, дости-некс, метерголин, L -дофа, лерготрил, метисергид, лизургид) или аналогами соматостатина (сандоста- тин), которые должны применяться годами, возможно, пожизненно. При их отмене уровень СТГ опять возрастает, и заболевание вновь начинает прогрессировать.
Радикальная транссфеноидальная гипофизэк-томия или криогипофизэктомия жидким азотом показаны при аденокарциноме, угрозе слепоты, разрушении опухолью клиновидной кости.
Лучевое воздействие проводят пучком протонов, тяжелыми L-частицами, телегамматерапией, в последнюю очередь — рентгенотерапией гипофиза. Эффект дает вживление в гипофиз радиоигл из иттрия, иридия, золота.
При гигантизме без аденомы гипофиза можно закрыть зоны роста костей тестостероном. При развитии патологии щитовидной железы или сахарного диабета проводится соответствующая общепринятая терапия.
Профилактика. Первичная профилактика гигантизма-акромегалии неизвестна, хотя она была бы более важна, чем лечение этой патологии.
Избегают инфекций, травм черепа, использования анаболических стероидов и сомнительных по составу пищевых добавок при занятиях спортом, а также при искусственном наращивании мышечной массы. Детям и подросткам нежелательно злоупотребление мобильной связью.
Важен постоянный антропометрический контроль развития детей и подростков, особенно в возрасте от 13 до 16 лет.
При допубертатном развитии заболевания в целях остановки чрезмерного роста показаны андрогены (тестостерон) при рентгеновском контроле за зонами роста костей.
Диспансеризация. Диспансерная группа — Д-3. Показано постоянное наблюдение эндокринологом, неврологом и окулистом, с эндокринологического учета больные гигантизмом-акромегалией никогда не снимаются. С возрастом больные подростки передаются на диспансерный учет во взрослую поликлинику.
Беременным с гигантизмом-акромегалией делать аборты не рекомендуется. При развитии гигантизма и акромегалоидности во время первой беременности повторные беременности крайне нежелательны.
Важно подчеркнуть, что соматотропинома—это новообразование головного мозга. Она может спровоцировать внутричерепную компрессию. Так как любые
68
опухоли внутричерепной локализации прогностически неблагоприятны из-за опасности компрессионного синдрома, к больным гигантизмом-акромегалией следует относиться как к онкологическим.
Вопросы экспертизы. Группы здоровья — 5, реже — 4. При стабильном течении заболевания показана только ЛФК.
Субгиганты с умеренной дистрофией могут работать при малых нагрузках и без широких контактов с публикой (такие подростки особенно страдают от своей неполноценности). Нежелательна работа с постоянным использованием мобильной связи. Запрещается работа с токами высокой частоты, с различными ионизирующими излучениями, вибрацией и другими профвредностями.
При росте выше 200 см и при наличии аденомы гипофиза больные считаются инвалидами. К военной службе они не годны.
Подростки с данным заболеванием освобождаются от школьных экзаменов.
Впрочем, профессиональная карьера больных с гигантизмом-акромегалией может складываться достаточно успешно. Известны случаи, когда больные с этим заболеванием становились не только баскетболистами с мировыми именами, но и крупными учеными, артистами, общественными деятелями, бизнесменами.
АКРОМЕГАЛИЯ
Определение. Акромегалия — заболевание с утолщением костей, увеличением внутренних органов и нарушением обмена веществ в результате гиперпродукции СТГ, когда уже закрыты зоны роста костей в длину
Синонимы: эозинофильная аденома гипофиза, соматотропинома.
Распространенность. Акромегалия встречается реже гигантизма: 1 случай на 8-17 тыс. соматических больных. Подростки (чаще юноши) составляют до 7 % от всех больных акромегалией. Подростки заболевают акромегалией обычно после 18 лет. У них чаще бывает частичная, парциальная акромегалия.
Особенности этиологии и патогенеза. Название акромегалия происходит от греческого akron, которое переводится не только как «конечность», но и как «вершина» или «оконечность», то есть периферическая часть тела (выступающая или выдающаяся) — кисти, стопы, череп, затылочный бугор, надбровные дуги, нос, нижняя челюсть и т.д. При акромегалии эти периферические части тела становятся большими, так как они растут не только в длину, но и в ширину, а при гигантизме — только удлиняются.
Причины и механизмы акромегалии и гигантизма однотипны (см. выше). Описано развитие акромегалии после удара молнией, при врожденном сифилисе, во время беременности. Особенности патогенеза акромегалии состоят в том, что она развивается при избытке СТГ, когда уже закрываются зоны удлинения костей. Если акромегалия течет с отрочества до зрелости, то формируется гигантоакромегалия. Патогенез акромегалии обусловлен анаболическим влиянием на ткани избытка СТГ и соматомединов, а также повышенной к ним чувствительностью соответствующих рецепторов.
Клиника. Подростки с акромегалией жалуются на общую слабость, упорные, даже нестерпимые головные боли, рвоту (не снимающую головную боль, как обычно бывает при мигрени).
Возникают нарушения бокового зрения, потливость ладоней, обилие юношеских угрей и сальность кожи, прибавка веса, что чаще волнует девушек.
У юношей затягивается на годы физиологическая гинекомастия, ослабляются эрекции, исчезают поллюции, но наблюдаются признаки макрогенитализма. У девушек нарушаются месячные (до аменореи), их волнует явный гипертрихоз.
Нарушается прикус, что является поводом для посещения подростком врача-ортодонта. Родителей беспокоят частые внеплановые расходы на приобретение своему больному ребенку новой обуви, размер которой прогрессивно нарастает в длину и особенно в ширину. Девушкам-подросткам, помимо обуви, становятся малы кольца, перстни, браслеты, перчатки.
Подростки с акромегалией обычно сонливы, иногда слишком нервозны или даже безразличны, с легкой сменой настроения и даже эйфоричностью. Может извращаться обоняние. Внешне типичны диспропорции скелета, органов и мягких тканей с огрубением черт и угловатостью (крупные, грубые черты лица, большие нос и уши, прогнатизм, большой кадык).
Скелет раздается как бы в ширину: пальцы толстые. Из-за сдавления срединного нерва в карпальном туннеле могут неметь пальцы рук. Появляются лордоз и кифоз, общая неуклюжесть.
Кожа плотнеет и грубеет, нижняя губа может отвисать. Язык увеличивается в размерах, на нем появляются отпечатки от зубов. Зубы редкие (они остаются прежних размеров, а челюсти всё продолжают расти). Голос становится грубым, речь—невнятной. Часто увеличиваются щитовидная железа, сердце, печень. Из-за нарушения проходимости трахеи и бронхов подростки с акромегалией часто храпят во сне. Во сне у них иногда наступает синдром апноэ.
Может возникать жажда с полиурией и булимией.
Осложнения. Церебральная компрессия с поражением зрительной хиазмы дает сужение полей зрения и даже слепоту (особенно на красный цвет). Расстраивается обоняние. Могут развиться фронтальная или височная эпилепсия. Соматотропинома может озлока-чествляться (аденокарцинома).
Разрушение соматотропиномой основной кости и костей носа может приводить к назоликворее. Артериальное давление становится стойко повышенным. Нарушается психика. Часто развивается симптоматический сахарный диабет с кетоацидозом. Из-за реактивной гиперфукнции паращитовидных желез появляется остеопороз. Не является редкостью гипо-гонадизм.
Классификация. Различают следующие стадии акромегалии:
• преакромегалическую (симптомы заболевания в большинстве случаев отсутствуют или мало выражены);
• гипертрофическую (наблюдается усиленный рост скелета и мягких тканей);
• опухолевую (преобладают признаки повышения внутричерепного давления и нарушения зрения, связанные с ростом опухоли);
• кахектическую (терминальную).
Выделяют активную и стабильную фазы акромегалии. Признаками активности являются:
• периодическая или постоянная головная боль;
• ухудшение картины глазного дна и полей зрения;
• прогрессивное увеличение конечностей;
• появление сахарного диабета или ухудшение его течения;
• повышение выделения кальция с мочой;
• повышение уровня неорганического фосфора в крови;
• нарастание уровня СТГ в крови.
Выделяют гипоталамическую и гипофизарную формы. Последнюю отличает полная независимость от гипоталамуса, бесконтрольная гиперплазия и даже ма-лигнизация эозинофильных клеток аденогипофиза. Выделяется также парциальная (частичная) акромегалия. Половой инфантилизм при акромегалии порождает новую нозологическую форму болезни — инфантильный гигантизм.
Диагностика. Важную роль играет внешность больного подростка, но ее важно сравнивать с его прежними фотографиями.
В анализах периферической крови могут быть анемия, эозинофилия, моноцитоз, повышение уровней неорганического фосфора, свободных жирных кислот,
69
азота крови, а1-а2-глобулинов, фосфолипидов, в-липоп-ротеидов, щелочной фосфатазы и кальция.
Снижение утилизации глюкозы приводит к гипергликемии. Основной обмен повышается.
Выявляются кардиомегалия и асимметричная гипертрофия межжелудочковой перегородки, определяемая при ЭхоКГ-исследованиях. На ЭКГ обнаруживаются признаки ранней реполяризации миокарда, депрессия интервала S-T (Левина Л.И., 1989), наклонность к брадикардии. Артериальное давление повышается.
Рентгенография костей черепа выявляет его толстый свод, большой затылочный бугор, выраженные надбровные дуги, разрастание основной пазухи и, главное, — увеличение турецкого седла вплоть до разрушения основной кости и признаков компрессии мозга. Другие кости на рентгеновских снимках грубые, массивные, с гиперостозами (шпоры), тела позвонков утолщаются, ногтевые фаланги имеют вид катушек (рис. 26).
Окулист обычно обнаруживает битемпоральную ге-мианопсию, особенно на красный цвет, что считается почти патогномоничным признаком акромегалии. Уль-трасонография щитовидной железы часто выявляет ее увеличение и нередко — узлы.
При частичной акромегалии чрезмерно растут какая-либо часть тела или орган.
Мы наблюдали девушку-подростка, у которой парциальная форма акромегалии проявлялась лишь асимметричным ростом костей черепа (рис. 27), но с уровнем СТГ в крови, в 7 раз превышающим норму.
При характерных внешних признаках акромегалии диагноз подтверждает, как правило, повышенный уровень СТГв крови.
Критерии диагноза. Характерный внешний вид больного подростка в сочетании с инструментальными (рентген, КТГ, МРТ) признаками объемного процесса гипоталамо-гипофизарной области и повышенным уровням СТГв течение всего времени суток позволяют поставить диагноз акромегалии. В сомнительных случаях прибегают к функциональным пробам, которые аналогичны пробам, используемым в диагностике гигантизма (см. выше Гипофизарный гигантизм).
Пример диагноза. Эозинофильная аденома гипофиза. Акромегалия в активной фазе, гипертрофическая стадия. Кардиомегалия. Акромегалическая дистрофия миокарда. Битемпоральная гемианопсия. Аменорея.
Дифференциальный диагноз. Акромегалию дифференцируют с генетической акромегалоидной вне-
70
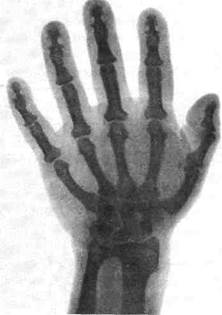
Рис. 26. Рентгенограмма кисти больного акромегалией. Ногтевые фаланги в виде катушек (по В. Фальта, 1913)
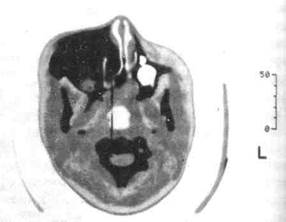
Рис. 27. Парциальная акромегалия. Томограмма костей черепа (собств. набл.)
шностъю. Для этого необходимо осмотреть родите-лей больного подростка.
Кроме того, при подозрении на акромегалию подростков следует проводить дифференциальную ди-агностику с карликовой акромегалоидностью, болезнью Педжета, болезнью Крузона, гаргоилиз-мом Гурлер-Пфаундлера, периостозом Пьера Мари-Бамбергера, синдромом Турена-Соланта-Голе.
При карликовой акромегалоидности обязательно наличие признаков нанизма — карликовости, которой не бывает при акромегалии.
Болезнь Педжета (деформирующая остеодистро-фия, постнатальный дистрофический процесс) чаще встречается у взрослых, но некоторые клиницисты выделяют юношескую форму болезни — ювенильный Педжет (гиперфосфатазию). Она отличается увеличением мозгового черепа при нормальном лицевом вследствие кортикального юношеского гиперостоза черепа, а также таза, позвоночника, спонтанными «банановыми» переломами костей. У великого Людвига Ван Бетховена была внешность, характерная для бо- хезни Педжета., которая привела его к ранней глухоте.
Болезнь Крузона может проявляться еще при рождении, но чаще формируется в первые два года жизни, до семи лет прогрессирует, а затем стабилизируется (рис. 28а). Основные симптомы болезни — деформации костей черепа (брахиоцефалия, гипоплазия верхней челюсти, гипертелоризм, высокое и узкое небо, толстый нос, неправильные верхние зубы из-за прогнатизма), экзофтальм с нистагмом и прогрессирующей слепотой, снижение слуха и обоняния вследствие сужения черепных отверстий соответствующих нервов.
Для гаргоилизма Гурлер-Пфаундлера (мукополи- сахаридоза, полидистрофии Гурлер, липохондро- дистрофии Вашингтона) характерны карликовость с дорсолюмбальным кифозом или кифосколиозом, слегка согнутыми в локтевых суставах руками, короткими и толстыми ладонями; гротескные черты лица с гипертелоризмом, толстым носом, большими ушами, толстыми и выдающимися вперед губами; круглый, выдающийся вперед живот с большим пупком, грыжами, гепатоспленомегалия; помутнение роговицы, прогрессирующая атрофия зрительных нервов, снижение слуха, психическое недоразвитие до степени полной идиотии (рис. 286).
Существуют напоминающие внешне акромегалию заболевания негипофизарной природы, при которых имеется гиперплазия мягких тканей конечностей и лица. Они, видимо, отражают аномалии паракринной со-матомединовой регуляции этих процессов и должны дифференцироваться с акромегалией по нормальному уровню и ритму секреции СТГ и отсутствию характерных для этого метаболических отклонений. Это, прежде всего, синдром Пьера Мари-Бамбергера — гипертрофическая пневмопатическая остеоартропатия. Хронические нагноительные заболевания лёгких и печени провоцируют у наследственно предрасположенных
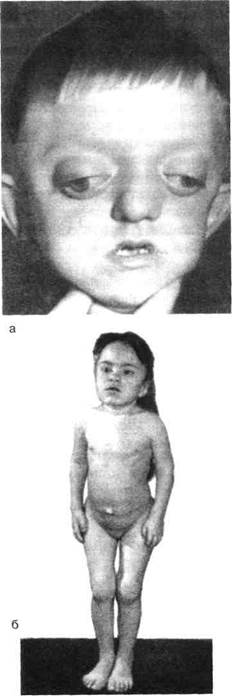
Рис. 28. а — болезнь Крузона, б — синдром Гурлер-Пфаундлера (по Н.А. Пучковской, 1981)
пациентов крайне подчеркнутые гиппократовы симптомы (толстые пальцы с «барабанными палочками», «часовыми стёклами»); отёк и артропатия дистальных отделов конечностей с артралгией по типу инфектарт-рита, гипергидроз и гипертрихоз.
При синдроме Турена-Соланта-Голе (пахидер-мопериостозе), который начинается обычно в пубертатном возрасте, имеется массивное утолщение кожи
71


 лица, кожи и костей дистальных отделов конечностей, гипергидроз и себорея. Также имеются симптомы «барабанных палочек», «часовых стёкол» и остеоартри-ты. Этиология и патогенез этого страдания, которое бывает и спорадическим, и семейным и поражает в основном мужчин, не совсем ясны, но при нем обнаружены дополнительная малая хромосома и трисомия половых хромосом.
лица, кожи и костей дистальных отделов конечностей, гипергидроз и себорея. Также имеются симптомы «барабанных палочек», «часовых стёкол» и остеоартри-ты. Этиология и патогенез этого страдания, которое бывает и спорадическим, и семейным и поражает в основном мужчин, не совсем ясны, но при нем обнаружены дополнительная малая хромосома и трисомия половых хромосом.
Исходы заболевания и прогноз. Прогноз при акромегалии зависит от своевременности удаления аденомы гипофиза—соматотропиномы. Иногда кровоизлияние в аденому приводит к самоизлечению.
Исходы заболевания зависят от направления роста аденомы и ее малигнизации. Могут нарушаться функции разных органов, развиться зоб, сахарный диабет. Дистрофия миокарда может дать сердечную недостаточность, особенно при стабильной артериальной ги-пертензии. Могут быть диплопия, птоз, даже слепота, снижение слуха, обоняния.
Подросткам свойственно злокачественное течение акромегалии с нередким развитием эпилепсии и психозов.
Репродуктивность весьма сомнительна. Даже после излечения аденомы акромегалоидные черты все равно сохраняются, что травмирует психику больных подростков.
Лечение. Принципы лечения акромегалии практически такие же, как и при гигантизме (см. стр. 67).
Терапия может дать стабилизацию болезненного процесса, однако костные изменения являются необратимыми. Иногда положительный эффект дает традиционное лечение выявленного при акромегалии сифилиса.
Профилактика. В целях профилактики акромегалии у подростков важно предупреждение травм черепа, острых и хронических инфекций, раннее выявление и лечение сифилиса.
Запрещен прием анаболических стероидов (ретабо-лил, метандростенолол, неробол и др.) без соответствующих показаний и тем более бесконтрольный.
Нежелательны непозволительно долгое пребывание детей и подростков у мониторов, злоупотребление мобильными телефонами, контакты с токами высокой частоты, которые могут быть непредсказуемыми в отношении патологии гипофиза, в частности, акромегалии.
Диспансеризация. Подростки с акромегалией относятся к диспансерной группе Д-3 с постоянным (1 раз в месяц) наблюдением эндокринологом, а по показаниям — неврологом, окулистом, онкологом. С диспансерного учета эти подростки никогда не снимаются, даже после радикального лечения акромегалии.
72
Вопросы экспертизы. Группа здоровья — 5. Ухуд-шение зрения приводит к инвалидности с обучением в школе для слабовидящих. Все подростки с акромегалией вследствие аденомы - соматотропиномы считаются инвалидами. На ранних стадиях акромегалии показано наблюдение ортодонтом. Во время лучевой терапии больные подростки освобождаются от учебы и от работы и являются нетрудоспособными.
Они не подлежат призыву в армию и снимаются с военного учета.
ГИПОФИЗАРНЫЙ НАНИЗМ
Определение. Гипофизарный нанизм — заболева-ние, возникающее при отсутствии или снижении сома-тотропной активности аденогипофиза в результате продукции аномального СТГ или из-за снижения тканевой чувствительности к нему.
Синонимы: карликовость, микросомия, наносомия. С легкой руки английского писателя Джонатана Свиф та, обессмертившего свое имя «Путешествиями Гулливера», в быту гипофизарных карликов называют обычно лилипутами (от скандинавского lille—маленький).
Распространенность. Частота гипофизарного нанизма невелика. Низкорослость — частое явление. Однако не более чем 1 на 1000 лиц с задержкой роста, которые обращаются к врачу, является истинным гипо-физарным карликом. -
В популяции частота гипофизарного нанизма от 1:15 000-1:20 000 в России до 1:4000 в Америке, Африке и на Ближнем Востоке. Гипофизарный нанизм чаще встречается у мальчиков и юношей. Наиболее частая форма гипофизарного нанизма (65-75 %) — идиопати-ческая.
Этиология и патогенез. Критерием карликовости считается рост, отстающий от среднепопуляционного возрастного роста на два-три сигмальных отклонения (как правило, менее 130 см—у мужчинименее 120см — у женщин).
Конечный рост таких пациентов может быть в пределах 90-120 см. Имеются сообщения о гипофизарных карликах ростом менее 70 см. Самой низкорослой жительницей Земли среди всех медицински освидетельствованных гипофизарных карликов считалась голландская цирковая артистка Полин Мастере (род. в 1895 г.), ее рост был 59 см при весе 4 кг, Самый известный миниатюрный мужчина — американец Кальвин Филиппе (1791-1812), чей рост не превышал 67 см. Среди ныне живущих людей «Книга рекордов Гиннеса» (1989) числит самым миниатюрным
доминиканца Нельсона де ла Роса (род. в 1968 г.) ростом 72 см при весе 6,8 кг.
Причиной гипофизарного нанизма могут быть травма черепа, инфекция или опухоль гипоталамо-гипофизар-ной области, синдром «пустого турецкого седла», генетический дефект СТГ, соматомединов и их рецепторов, дефицит соматолиберина (соматокринина).
Истинный гипофизарный нанизм всегда является гипосоматотропным. До половины больных имеют изолированную идиопатическую недостаточность СТГ, часто — вторичную по отношению к дефициту сома токринина.
До 35% имеют раннюю сочетанную недостаточность гипофизарных гормонов вследствие опухолевого разрушения аденогипофиза, аутоиммунного процесса, а также — облучения.
Около 15 % подростков с гипофизарным нанизмом страдают от изолированного дефицита СТГ, вызванного ранним воздействием указанных выше причин. Считается, что соматотропы аденогипофиза менее резистентны к ряду неблагоприятных факторов, чем другие его секреторные клетки.
Большинство форм гипофизарного нанизма являются приобретенными. Имеется созданная собаководами модель наследственного гипофизарного нанизма в виде карликовых пород декоративных собак. Существует наследственный гипофизарный нанизм и у человека, притом в аутосомно-рецессивной (дефект гена СТГ) ив сцепленной с Х-хромосомой разновидности.
Особая форма гипофизарного нанизма, сочетанно-го с гипогонадотропным гипогонадизмом, — «питуи- тарный инфантилизм» — вызывается краниофарин-гиомами или аутоиммунным процессом, разрушающим соответствующие клетки-регуляторы. Именно эта форма встречается у подростков весьма часто.
Патогенез гипофизарного нанизма связан с замедленным постнатальным ростом. Родившись нормальными, больные с гипофизарным нанизмом до 3-4 лет хорошо развиваются, но затем их рост резко замедляется, и они на всю жизнь сохраняют детские пропорции. В случаях врожденной недостаточности СТГ задержка роста замечается буквально с первых месяцев жизни, а для детей и подростков с дефицитом СТГ органического происхождения (при опухолях ги-поталамо-гипофизарной области, при травме мозга) характерны более поздние сроки симптоматики заболевания. Одновременное снижение секреции адено-гипофизом и тиротропина (ТТГ) может вызывать гипотироз.
Если нет сопутствующего дефицита других гипофизарных гормонов, то гипостатура носит пропорциональ-
ный характер (голова, однако, может иметь слегка больший относительный размер, а лоб — выступать). Гипостатура сопровождается уменьшением внутренних органов (микроспланхнией) и чаще сопряжена с отклонениями в психомоторном или половом развитии: ведь у многих пациентов имеется не только дефицит СТГ, но и относительная нехватка гонадотропинов.
Гипофизарный нанизм нередко сопровождается некоторым избытком жировых отложений (за счет дефицита липотропина) и гипогликемиями натощак (вследствие недостаточности контринсулярных гормонов).
Высокий, пронзительный голос многих гипофизарных карликов не должен восприниматься как симптом гипогонадизма, а связан с особенностями миниатюрной гортани как резонатора. Н.А. Зарубина (1985) указывает на такой характерный признак, как удлинённые ресницы.
У гипофизарных карликов ускорено старение кожи (геродерма), что связано с замедлением её обновления и иногда—вторичным гипотирозом. Но при гипо-физарном нанизме нет достоверных данных о скорости общего старения.
Клиника. Задержка роста — ведущая жалоба больных гипофизарным нанизмом, что рано приводит их к врачу. Главный признак — маленький рост с общей миниатюрностью, мелкими чертами «кукольного» лица с западающим носом. Относительно большой лоб может вызвать подозрение на врожденную гидроцефалию. Характерны малые размеры кистей и стоп (акромикрия), иногда—с гипоплазией ногтей.
Тембр голоса — детский, что связывают не только с гипоплазией гортани, но и со слабостью мышц. Кожа бледноватая, нежная, тонкая, рано увядает, благодаря чему на лице карликов появляются морщинки, придающие им вид сказочных старичков-гномов. В лобно-височной области может наблюдаться разрежение тонких волос. Общее ожирение встречается крайне редко, чаще наблюдается избыточное отложение жира на туловище.
Больные гипофизарным нанизмом быстро устают. Это отчасти связано с выраженной слабостью скелетной мускулатуры. Они замкнуты, негативны, переживают свою неполноценность, плохо контактируют со сверстниками. Самооценка у них снижена. Появляется повышенная потребность в постоянной родительской опеке. Нередко отмечается плохая школьная успеваемость.
У них всегда обнаруживается относительный гипо-гонадизм со слабыми проявлениями или отсутствием вторичных половых признаков. У юношей с гипофизар-
ным нанизмом нередки крипторхизм, гипоплазия яичек, микропенис, а у девушек — нарушения месячных (до аменореи), при этом матка и яичники часто недоразвиты. У большинства подростков с гипофизарным нанизмом половое созревание наступает с большим опозданием. С возрастом они могут создавать семьи, но эти семьи обычно бездетны.
Они всегда обижаются на прозвище «лилипут» и предпочитают именоваться «маленькими». Им свойственно сочетание зрелости суждений с инфантильным поведением, резонерством, поучением окружающих. При этом они капризны, как дети. При генетических формах гипофизарного нанизма психика более устойчива.
Больные одержимы в попытках подрасти любым путем.
Осложнения. При гипофизарном нанизме опухоль как его причина за счет компрессии мозга может обусловить серьезные осложнения, при этом может развиться даже идиотия. Иногда возникает гипотироз.
В головном мозге могут выявляться кальцинаты (что, возможно, связано с последствиями врожденного токсоплазмоза как причинного фактора нанизма).
Классификация. В клинике различают следующие формы карликовости:
• гипофизарный нанизм (при первичной патологии гипофиза);
• гипоталамический нанизм (при дефиците соматот-ропин-рилизинг-гормона гипоталамуса).
Существует клиническая форма нанизма в результате тканевой резистентности к СТГ при патологии его рецепторов в тканях-мишенях. Сюда относится нанизм Ларона с повышенной продукцией СТГ, но с низкой чувствительностью к нему.
Выделяют также питуитарный инфантилизм. Редко наблюдается нанизм вследствие врожденного отсутствия гипофиза.
Диагностика. Карликовостью считают отставание роста на 20 % и более для соответствующего возраста (юноши — ниже 130 см, девушки — ниже 120 см). Задержка дифференцировки и окостенения скелета может дать отставание от паспортного возраста до 10 лет!
Диагноз не труден, сложнее уточнить форму гипофизарного нанизма, что определяет индивидуальные подходы к его лечению.
Рутинные анализы обычно нормальные. АД чаще снижено, бывают функциональные шумы сердца. На ЭКГ — низкий вольтаж и склонность к брадикардии. ЭЭГ сохраняет черты, свойственные детскому возра-
74
сту. При развитии гипотироза возникают свойственные ему зябкость, запоры, гиперхолестеринемия, анемиза-ция.
Уровни СТГ и соматомединов крови явно снижа-ются. Для распознавания гипофизарного нанизма важны внешний вид больных и наличие признаков гипого-надизма.
Критерии диагноза. В диагностике важен анам-нез страдающего низкорослостью подростка. При этом В.А. Петеркова и О.В. Фофанова (2000) обращают внимание на следующие признаки:
• сроки появления задержки роста;
• перинатальную патологию (асфиксия, фетальный дистресс, наложение щипцов, вакуум-экстракция, стремительные или длительный роды), типичный для идиопатического нанизма дефицита СТГ;
• эпизоды гипогликемии (они характерны для детей и подростков с врожденным дефицитом СТГ);
• семейный анамнез (у подростков с преходящим де-фицитом СТГв семейном анамнезе имеются случаи низкорослости и задержек полового развития);
• наличие хронических заболеваний;
• предшествующий прием гормональных и других препаратов.
Окончательный диагноз гипофизарного нанизма базируется на исследовании секреции СТГ.
Определяется его базальный уровень и циркадный ритм продукции, реакция на стимуляторы — инсулин, глюкагон, тиролиберин (Балаболкин М.И., Гаври-люк Л.И., 1984; Дедов И.И. с соавт., 1998).
В норме после стимуляции выброс СТГ составляет 7-10 нг/мл, а при гипофизарном нанизме — не выше 5 нг/мл. Положительная проба с тиролиберином говорит о первичной недостаточности гипоталамуса. От-рицательная проба с инсулином и тиролиберином указывает на поражение аденогипофиза.
При нанизме Ларона снижен уровень соматоме динов при высокой продукции СТГ.
В диагностике необходимо обязательное использование рентгеновских снимков зон роста костей, вы-являющих при гипофизарном нанизме задержку окостенения. КТГ и МРТ-методики помогают обнаружить объемные процессы гипоталамо-гипофизар-ной области. Окулист выявляет признаки компрессии мозга и внутричерепной гипертензии.
Пример диагноза. Краниофарингиома. Гипофизарный нанизм. Внутричерепная гипертензия. Гипотироз легкой степени. Гипогонадизм.
Дифференциальный диагноз. Задержка роста чаще всего имеет причины, не связанные с дефици-
том его гипоталамических и гипофизарных стимуляторов.
Поскольку рост — аддитивно-полигенный признак с пороговым эффектом, определяемым комплексом экзогенных факторов, эти причины многочисленны. Некоторые руководства насчитывают до 60 разновидностей нанизма и гипостатуры.
Образно говоря, карликовость — проблема гигантская. Поэтому эрудиция в вопросах нарушений ростовых и анаболических процессов у человека необходима подростковому врачу и эндокринологу для успешной дифференциальной диагностики гипофизарного нанизма.
Самая частая причина нанизма—конституциональная задержка роста (98%). Полигенность контроля роста делает предсказания ненадёжными, но имеется корреляция между ростом обоих родителей и ребёнка. При оценке зависимости роста подростка от роста родителей суммируют рост матери и отца, сумму делят пополам и у юношей прибавляют 5 см, а у девушек — столько же вычитают. Эта цифра примерно соответствует ожидаемому росту подростка (Блунк В., 1981). Для наследственного гипофизарного нанизма типичны его повторные случаи в семье, при этом чувствительность тканей-мишеней к СТГ сохранена.
Задержка роста бывает в периоде полового созревания, при наличии преходящего дефицита гонадотро-пинов. Хотя дефицит андрогенов в период полового созревания может повлечь отсутствие пубертатного ростового скачка, но нанизм вызвать он не способен.
Примордиальный нанизм (болезнь Палътауфа) возникает еще внутриутробно, при этом вес при рождении — не более 2 кг. Плод доношен, но черты лица мелкие, клювовидные, голос писклявый, далее костный возраст нормальный, пациенты обычно репродук-тивны.
Питание, особенно в грудном периоде раннего детства и в подростковом периоде, небезразлично для реализации генетически детерминированной потенции роста. Рост может тормозиться при нехватке белка в питании маленьких детей, при дефиците незаменимых аминокислот, витамина D, цинка и, возможно, других алиментарных факторов.
При раннем и врождённом гипотирозе — спорадическом гипотирозе с кретинизмом (болезни Фагге) рост также значительно тормозится (гипотироидный нанизм). Частота его примерно вдвое выше, чем нанизма гипофизарного (рис. 29).
Тироидные гормоны необходимы для влияния ИФР-1 на хондроциты. Они усиливают продукцию СТГ в ответ на различные стимулы, активизируют амино-ацил-т-РНК-синтетазы и процессы трансляции. Всё это

Рис. 29. Болезнь Фагге (спорадический кретинизм) у 16-летней девушки (по А. Попову, 1968)
приводит к тому, что без тироидных гормонов линей ный рост у животных практически полностью останавливается.
Гипотироидная карликовость сопровождается нарушением психомоторного развития детей и подростков и умственной отсталостью, выраженной тем более, чем раньше сформировался дефицит тироидных гор монов. Сами признаки гипотироза могут присутствовать и у гипофизарных карликов как следствие гипопи-туитаризма, но они не бывают столь выраженными.
Макрогенитосомия и другие причины раннего гипер-гонадизма (адреногенитальный синдром) из-за избытка тестостерона могут вызывать раннее закрытие зон роста костей, вследствие чего ребёнок быстро растет в раннем детском возрасте, но рост его преждевременно останавливается и бывает ниже среднего.
Выраженная низкорослость наблюдается в подавляющем большинстве, при дизгенезии гонад, в частности, у девушек-подростков при синдроме Шере-шевского-Тернер а, причём уровень СТГ в этих случаях не снижается, но чувствительность к нему уменьшается, что, однако, можно преодолеть применением больших доз биосинтетических препаратов гормона роста человека. Для синдрома Шерешевс-кого-Тернера типичны не только низкорослость, но и вальгусные локтевые суставы, складки кожи на шее, короткие первые фаланги больших пальцев, отсутствие полового хроматина, первичная аменорея, врожденные пороки сердца и сосудов (рис. 30).
Так как инсулин в известной степени также явля ется соматомедином, то при тяжелом раннем инсулин-зависимом диабете подростков может развиваться низ-
75
 корослость в сочетании с такими признаками, как стеа-тоз печени, инфантилизм, остеопороз, что входит в так называемый синдром Мориака.
корослость в сочетании с такими признаками, как стеа-тоз печени, инфантилизм, остеопороз, что входит в так называемый синдром Мориака.
Весьма редко встречается, но представляет определенный теоретический интерес не чувствительный к лечению гормоном роста синдром Ларона (ауто-сомно-рецессивная карликовость при высоком уровне СТГ, но дефекте пострецепторной передачи его сигнала, что делает невозможным адекватную продукцию ИФР-1). Выше уже шла речь о аутосомно-доминантном дефиците ИФР-1 у африканских пигмеев (рис. 31).
Низкорослость с диспропорциями и дизгенезией скелета, искривлением конечностей может сопровождать некоторые наследственные тезаурисмозы (болезни накопления). Наконец, наследственный дефицит лептина у детей сопровождается ожирением и низкорослостью с антимарфаноидным фенотипом, лептинотерапия корректирует рост (Дж. Матарезе, 2003).
Хондродистрофия отличается малым ростом вследствие коротких конечностей и седловидным носом (рис. 32).
Нанизм бывает при раннем синдроме Иценко-Ку-шинга, для которого характерна типичная внешность с гиперкортизолизмом (рис. 33).
Выше уже упоминалось о психосоциальной гипо-таламической карликовости (до 1 % всех случаев задержки роста у подростков). Такая форма задержки роста бывает при тяжелых болезнях печени, почек, при голодании, у воспитанников детдомов, интернатов, детских исправительно-трудовых колоний {психосо циальный нанизм).
Только истинная гипофизарная карликовость сопровождается понижением содержания в плазме крови СТГ, а также ИФР-1 и третьего ИФР-переносящего белка крови и реагирует на терапию рекомбинантным человеческим гормоном роста.
Исходы заболевания и прогноз. При церебральных формах гипофизарного нанизма исход заболевания обусловлен первичной патологией.
При позднем гипофизарном нанизме прогноз лучше. Своевременное лечение ускоряет физическое развитие. Больные живут обычно долго, до старости. Прогноз лучше при наследственных формах нанизма. При бесконтрольном лечении анаболическими стероидами возможно развитие желчнокаменной болезни.
Могут быть расстройства психики. Возможны тяжелые психозы, но суициды крайне редки.
Артистизм и талант многих пациентов с гипофизар-ным нанизмом лишний раз подчеркивают, что микро-сомия в принципе не означает какой-либо формы умственной либо социальной неполноценности. Нередко
76
они совершают успешную артистическую и циркоъвую карьеру.
По свидетельству современников, один из самых миниатюрных гипофизарных карликов планеты был ге-нералом эфиопской армии. Авторы сожалеют о невоз-можности опубликовать фото этой исторической лич-ности в парадном мундире или во время руководства боевыми действиями.
Описаны уникальные случаи гипофизарных карли-ков, имевших потомство.
При самолечении анаболическими препаратами больные могут прийти к плачевным результатам вслед-ствие преждевременного закрытия зон роста костей,
Лечение. Лечение — индивидуальное, длительное, требующее терпения пациента и врача.
Пища должна быть богатой белками, витаминами, кальцием, йодом, цинком.
Основное в терапии гипофизарного нанизма— ща-жение зон роста костей.
Гормон животных для лечения гипофизарного наниз-ма оказался малоэффективным, поэтому длительно (с 1956 года) существовала практика лечения гипофизар-ного нанизма трупным человеческим гормоном роста. В 80-х годах XX века обнаружился повышенный риск за-болеть прионовой губчатой энцефалопатией (болезнъю Крейцфелъдта-Якоба), передаваемой будто бы с пре-паратами трупного гипофиза. Это—неизлечимое деге-неративное заболевание центральной нервной системы, близкое к болезням куру, скрепи, синдрому Герстман- на-Штраусслера-Шейнкера и спонгиоформной энцефалопатии овец и коров («коровье бешенство). Поэтому применение человеческого трупного гормона роста с 1984 года в мире обоснованно запрещено. Осно-ванием для этого послужили публикации в медицинской прессе с описаниями нескольких случаев болезни Kpe й цфельдта-Якоба, которые в детстве и юности получа-ли трупный гормон роста по поводу нанизма. Опублико-вано 57 подобных случаев. Первый случай гибели от болезни Крейцфелъдта-Якоба — 20-летний мужчи-на, который с 3 до 17 лет получал трупный гормон роста. В нашей стране еще не зарегистрировано ни одного слу-чая ятрогенной формы этого опасного заболевания, хотя полностью исключить их трудно. По рекомендации Де-партамента здравоохранения Великобритании весь ин-струментарий, использовавшийся при операциях на го-ловном мозге и на глазах у лиц, получавших когда-либо трупный гормон роста, должен обязательно уничтожать-ся во избежание его повторного использования.
В настоящее время рекомбинантньш гормон рос-та признан как средство выбора при лечении СТГ-не достаточности. Используют или рекомбинантный
|
|
|
|
Рис. 30. Синдром Шерешевского-Тернера (по П. Коларову. С Докумову, 1968)
Рис. 32. Хондродистрофия (по В. Фальта, 1913)
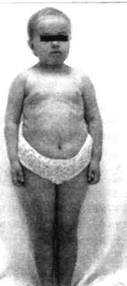
Рис. 31. Синдром Ларона (по И. И. Дедову с соавт., 1998)
человеческий гормон роста, или его аналоги (сомато- ген, генотропин, хуматроп, сейзен, нордитропин). Ре-ко мбинантный гормон роста стал доступным с 1985 г. В настоящее время получают аутентичный гормон роста с полностью соответствующей человеческому гормону последовательностью аминокислот (Дедов И.И. с соавт., 1998).
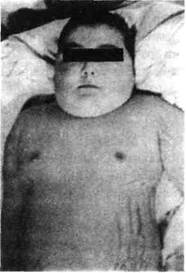
Рис. 33. Синдром Иценко-Кушинга (по М. Юлесу и И. Холло, 1967)
У детей и подростков особенно удобно использовать жидкий препарат гормона роста, что исключает при инъекциях процедуру смешивания и делает инъекцию проще и безопаснее. Единственным жидким препаратом человеческого СТГ, поставляемым в Россию, является в настоящее время Нордитро-пин® Симплекс®
77
При раннем начале такой терапии эффект гораздо выше. Большим технологическим достижением в области терапии гормоном роста явилось создание новых систем для его дозированного введения — шприц-ручек. Первая система, содержащая жидкий препарат человеческого гормона роста (НордиПен®), была разработана фирмой Ново Нордиск А/С. Как и ее усовершенствованный аналог — НордиПенМэйт ® (шприц-ручка) облегчает самостоятельное пользование препаратом гормона роста, что особенно важно у детей и подростков.
Вообще показанием к терапии гормоном роста является не любая задержка роста, но именно соматотроп-ная недостаточность. В противном случае пока весь ма дорогостоящее лечение не даёт никакого эффекта. Впрочем, имеется опыт успешного лечения гормоном роста подростковой низкорослости при синдроме Шерешевского-Тернера и при хронической почечной недостаточности, когда дефицит СТГ носит относительный характер.
Терапия гормоном роста должна по возможности имитировать его физиологический ритм секреции. Это достигается подбором оптимальной дозы, способа, частоты и времени введения препарата. В настоящее время рекомендуется подкожный метод введения гормо на роста (наиболее удобная область инъекций - бедро), что позволяет подросткам при наличии устройств, описанных выше, делать такие инъекции самостоятельно.
При введении его постоянно в одни и те же области могут возникать осложнения — липоатрофии, подкожные инфильтраты, поэтому места инъекций желательно менять.
Более частое введение гормона роста оказывает более выраженный лечебный эффект. В настоящее время стандартом являются ежедневные однократные подкожные инъекции. Так как пик естественной секреции СТГ наступает в первую фазу глубокого сна, введение препарата рекомендуется делать на ночь, перед сном, что более физиологично. Кроме того, для больного подростка это время более удобно.
Рекомендуются следующие дозы рекомбинантно- го СТГ.
Суточная доза должна колебаться от 0,07 до 0,1 ME на 1 кг массы тела или 2-3 ME на 1 м2 поверхности тела, которую рассчитывают по общепринятым номограммам (см. Приложение).
Недельная доза должна составлять, таким образом, от 0,5 до 0,7 ME на 1 кг массы тела или 14-20 ME на 1 м2 поверхности тела.
Так как при успешном лечении гормоном роста параметры роста и массы тела должны изменяться, то его доза должна корригироваться в зависимости от этих по-
78
казателей. Во время позднего пубертата в целях дости-жения адекватного ростового скачка дозу гормона следует индивидуально увеличить.
Встречаемость побочных эффектов от терапии ре-комбинантным человеческим гормоном роста чрезвычайно низкая.
Критерием прекращения лечения гормоном является достижение конечного роста, который считался бы оптимальным для данной популяции. Этот вопрос решается индивидуально. В качестве ориентира считают, что достижение конечного роста происходит при показателях костного возраста 16 лет у юношей и 14 лет —у де-вушек.
При гипофизарном нанизме длительно применяют ретаболил.
До использования анаболиков нельзя применять гонадотропины и половые гормоны, иначе возникает угроза закрытия зон роста костей.
У юношей 15-16 лет для стимуляции клеток Лей-дига используют хорионический гонадотропин, а у девушек — эстрогены, чем достигается имитация месячных. Для поддержания либидо, половой потенции и внешних половых признаков желателен пожизненный прием половых стероидов.
По показаниям назначают тироидные гормоны (ле-вотироксин, эутирокс, тиреотом) в адекватных дозах, под контролем уровней свободных Т3, Т4 и ТТГв крови.
Профилактика. В профилактике гипофизарного нанизма важны предупреждение инфекций у беремен ных; исключение травм головы новорожденного в инт-ра-, пери- и постнатальном периодах.
Детям необходимо обеспечить нормальные условия быта, полноценное питание, ласки, здоровую обстанов-ку в семье и в школе.
Важна своевременная санация очагов латентной инфекции.
Диспансеризация. При гипофизарном нанизме дис-пансерная группа — Д-3. С учета подростки с этой патологией никогда не снимаются.
Посещение эндокринолога необходимо осуществлять каждые 2-3 мес, а при поддерживающий тера-пии — 1 раз в 6 мес.
Периодически больные с гипофизарным нанизмом осматриваются окулистом, неврологом и психологом, а по показаниям — нейрохирургом.
Вопросы экспертизы. Группы здоровья при гипофизарном нанизме— 5 или 4.
При выборе профессии учитывают обычно свойственный больным гипофизарным нанизмом достаточ-но высокий интеллект с правом выбора специальности, Однако психологические особенности и инфантилизм
являются неподходящими для занятия такими пациентами руководящих должностей.
Больные нанизмом могут заниматься любым умственным трудом по интересам, но без физических нагрузок.
Часто они становятся актерами и в коллективах себе равных (ансамбли лилипутов, цирковые группы и др.) чувствуют себя комфортнее.
Известны случаи, когда люди с гипофизарным нанизмом были выдающимися личностями.
Призыву в армию они не подлежат, хотя выше приводился случай, когда карлик был генералом.
ГИПОТАЛАМИЧЕСКИЙ СИНДРОМ
ПУБЕРТАТНОГО ПЕРИОДА
( ОЖИРЕНИЕ С РОЗОВЫМИ СТРИЯМИ )
Определение. Гипоталамический синдром пубертатного периода — нейро-эндокринный синдром возрастной перестройки организма с дисфункцией гипоталамуса, гипофиза и других эндокринных желез.
Синонимы: ожирение с розовыми стриями, болезнь Симпсона-Пэйджа, пубертатный базофилизм, базофи-лизм до полового созревания, юношеский гиперкорти-цизм, пубертатный гиперкортизолизм, юношеский ку-шингоид, функциональный кушинг, пубертатно-юношеский диспитуитаризм, транзиторный ювенильный диэнцефальный синдром.
Распространенность. Частота заболевания в последние годы нарастает. Это не только самая частая форма ожирения подросткового периода, но и самая частая эндокринно-обменная патология подростков вообще. Заболевание чаще дебютирует в препубер-татном или раннем пубертатном периоде на фоне начинающегося полового созревания, а наблюдается в возрасте от 10 до 18 лет. Средний возраст больных — 16-17 лет.
По нашим данным (Строев Ю.И. с соавт., 2003) средний возраст манифестации ожирения при этом заболевания составил 8,2±0,36 года. Общепризнанно, что мальчики болеют чаще, чем девушки. По данным Р.Ф.Рудаковой-Суворовой с соавт. (1980), гипоталамический синдром пубертатного периода составил 3,3% от всех лечившихся эндокринных больных и 19 % от всех больных с патологией гипоталамуса.
Этиология и патогенез. Ставим в известность читателей, интересующихся подростковым ожирением вообще, что рассмотрение этой проблемы, важной для эндокринологов, но не сводящейся только к нарушению эндокринной регуляции жирового обмена, вынесено нами в отдельную монографию (Ю.И. Строев с соавт. «Ожирение у подростков», СПб: ЭлБи, 2003). В связи с
этим в данной главе специальной характеристики ожирения не приводится.
Гипоталамический синдром пубертатного периода — заболевание, при котором, как правило, формируется вторичное, то есть не связанное с лептиновой не достаточностью, ожирение (Строев Ю.И. с соавт., 2003). Однако, абстрагируясь от природы ожирения при данном синдроме, надо отметить, что сам по себе этот симптомокомплекс не сводится только к вторичному ожирению. Он может развиваться как первично (у подростков с изначально нормальной массой тела), так и вторично (у подростков, уже имеющих первичное леп-тинзависимое ожирение). В последнем случае «лепти-новое» и «нелептиновое» звенья в патогенезе тучности могут сосуществовать.
Факторами риска первичного гипоталамическо-го синдрома пубертатного периода являются:
• Патология беременности (хроническая фетопла-центарная недостаточность).
• Перинатальная энцефалопатия.
• Нейротоксикоз у детей раннего возраста.
• Черепно-мозговые травмы в детском возрасте.
• Нейроинфекции (менингоэнцефалиты, арахноидиты и васкулиты) у детей.
• Частые инфекции верхних дыхательных путей, в том числе — частые ангины.
• Хронические очаги инфекции в носоглотке и придаточных пазухах носа.
• Стрессы в детском и подростковом возрастах.
• Употребление гормональных контрацептивов
девочками-подростками.
• Беременности и аборты у несовершеннолетних
девушек.
• Аутоаллергические заболевания центральной
нервной системы.
• Злоупотребление анаболическими стероидами.
Приведенные многочисленные факторы риска позволяют сделать вывод о том, что при желании в анамнезе всегда можно найти возможную причину этого синдрома.
Вторичный гипоталамический синдром пубертатного периода развивается на фоне лептинового (алиментарно-конституционально-гиподинамиче-ского ожирения, по классической терминологии).
Перечисленные факторы риска, вероятно, приводят к повреждению диэнцефальной области головного мозга в детском возрасте (например, к вялотекущему ди-энцефалиту и к латентной аутоиммунной гипоталамо-патии) с формированием скрытой неполноценности гипоталамуса без каких-либо клинических проявлений.
79
Аналогичная ситуация у взрослых, по некоторым представлениям (Цыган В.Н. с соавт., 2001), складывается при развитии так называемого синдрома хроничес кой усталости.
В пубертатном периоде на фоне нейроэндокринной и морфофункциональной перестройки организма подростка значительно повышается нагрузка на гипотала-мо-гипофизарную систему. Это приводит к развитию дисфункции гипоталамо-гипофизарной системы с клинической манифестацией описываемого синдрома.
По другим данным, при этой патологии в 100 % случаев вовлечен аденогипофиз, но могут страдать и ги-поталамические ядра.
Заболевание характеризуется дисфункцией гипота
ламуса с нарушением продукции аденогипофизотропных
гормонов — кортикотропин-рилизинг
фактора (КРФ), соматокринина и люлиберина. Следствием этого является дисфункция аденогипофи-за — диспитуитаризм с нарушением секреции тройных гормонов—АКТГ, СТГ и ЛГ. При этом нарушается также синтез ряда аминов и нейропептидов головного мозга — дофамина, серотонина, эндорфинов.
Для подростков с гипоталамическим синдромом пубертатного периода характерна гиперфункция ги-поталамо-гипофизарно-адреналовой системы с гиперпродукцией кортикотропин-рилизинг-гормо-на в гипоталамусе, АКТГ— в аденогипофизе и кор-тикостероидов — в коре надпочечников. Под действием АКТГ усиливается стероидогенез в пучковой и сетчатой зонах коры надпочечников, и повышается секреция глюкокортикоидов и надпочечниковых ан- дрогенов. Клинические проявления синдрома у подростков определяются в основном гиперпродукцией кортизола и дегидроэпиандростерона (ДЭА).
Кортизол как мощный контринсулярный регулятор стимулирует у таких больных глюконеогенез в печени и вызывает развитие инсулинорезистентности. Усиление процессов глюконеогенеза объясняет отчасти появление на коже, в местах повышенного разрушения мобильных запасов жира, розовых полосок — стрий. Следствием инсулинорезистентности являются ги-перинсулинемия (гиперинсулинизм) и относительная инсулиновая недостаточность. Гиперинсулине-мия возникает в результате инсулинотропного действия на островки Лангерганса АКТГ.
Таким образом, механизм ожирения при гипоталами-ческом синдроме пубертатного периода связан как с собственным липогенетическим эффектом АКТГ и глюко кортикоидов, так и с инсулинотропным действием АКТГ на В-клетки островков Лангерганса. Определенное значение имеет повышение под действием глюко кортикоидов аппетита.
80
Глюкокортикоиды угнетают экспрессию рецептора ЛПНП, что сопровождается выраженной атероген-ной гиперлипопротеидемией. Инсулин также играет в этом важную роль. Известно, что инсулин сти-мулирует биосинтез холестерина и атерогенных ли-поротеидов в печени, способствует инфильтрации холестерином сосудистой стенки, потенцирует формирование атеросклеротических бляшек. Таким образом, инсулин является сильным атерогенным гор- моном. Поэтому ожирение с розовыми стриями сопровождается выраженной атерогенной гиперли-попротеинемией.
Для подростков с этим заболеванием типичны фун- кциональный базофилизм (гиперфункция базофиль-ных клеток аденогипофиза без их гипертрофии и ги-перплазии) и функциональный гиперкортицизм (гиперфункция железистых клеток пучковой и сетча-той зон коры надпочечников также без их гипертро-фии и гиперплазии). В отличие от болезни Иценко-Кушинга, при нем в гипофизе нет клона аномальных соматически мутировавших кортиколипотропоцитов, Поэтому не формируются базофильные аденомы аде-ногипофиза (кортикотропиномы), а размеры и масса надпочечников не увеличены.
Результатами наших исследований, проведенных в эндокринологическом отделении Мариинской больницы Санкт-Петербурга, у всех подростков с гипоталамичес-ким синдромом пубертатного периода выявлена адре- нокортикотропная гиперфункция аденогипофиза и глюкокортикоидная гиперфункция коры надпочечников.
В отличие от болезни Иценко-Кушинга, при этом заболевании существенно не нарушен физиологический циркадный ритм секреции гормонов гипоталамо-гипо-физарно-адреналовой системы (КРФ, АКТГ и корти- зола).
Для гипоталамического синдрома пубертатного пе-риода характерна соматотропная гиперфункций аденогипофиза. При этом у подростков повышается продукция соматолиберина в гипоталамусе и СТГ-в аденогипофизе. Следствием этого является ускоре-ние их роста и физического развития (характерная вы-сокорослость и «дородность»).
При этой патологии нарушается также функция ги-поталамо-гипофизарно-гонадной системы, особенно — аркуатного ядра, являющегося и составным эле-ментом центра насыщения, и звеном центральной регуляции гонадотропной активности. У девочек повы-шена выработка люлиберина в аркуатном ядре гипо-таламуса и ЛГ— в аденогипофизе. Поэтому для девочек с этим заболеванием характерно раннее половое созревание и раннее менархе. Под действием гиперсек-
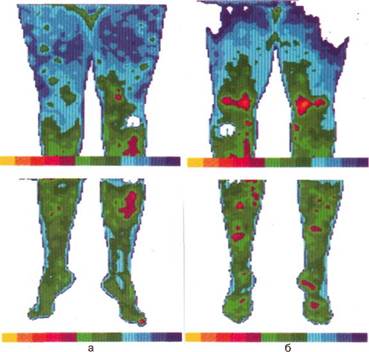
Рис. 35. Термограммы нижних конечностей у тучного полростка с нсйроциркуляторной дистонией, а — вид спереди; б — вид сзади (собств. набл.)
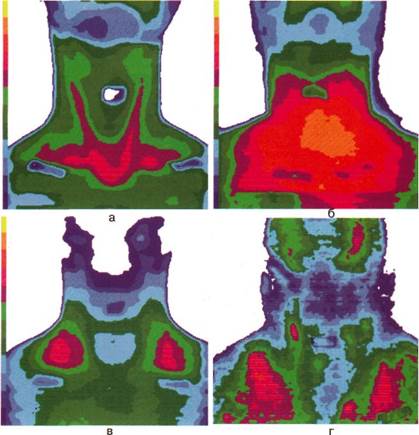
Рис. 36. Термограммы щитовидной железы у подростков: а — нормальная; б — при диффузном токсическом зобе: в — при гипотирозе; г -при аутоиммунном тироидите (собств. набл.)
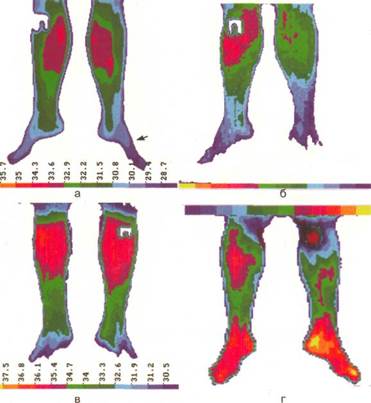
Рис. 37. Термограммы нижних конечностей у подростков; а — нормальная; б — при атеросклерозе периферических артерий с асимметричной "термоампутацией"; в — диабетическая микроангиопатия с симметричной "термоампутацией"; г — венозный застой (собств. набл.)
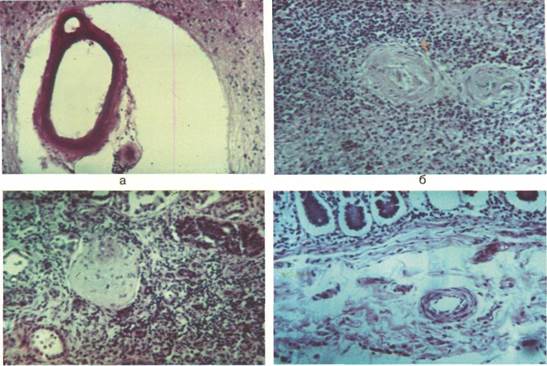
В Г
Рис. 85. Диабетическая микроангиопатия внутренних органов, а — срез головного мозга; отложение резко PAS-положительных веществ в стенках сосудов, периваскулярный отек; окраска по Мак Манусу.х 120. б — срез селезенки; резко выраженный гиалиноз, периваскулярный склероз, значительное сужение просвета сосудов; гематоксилин-эозин, х 120. в — срез почки; тотальный гиалиноз почечного клубочка; гематоксилин-эозин, х 120. г — срез стенки тонкого кишечника; гиалиноз и склероз сосуда; гематоксилин-эозин, х 120 (собств. набл.)
реции ЛГ в яичниках развивается кистозная атрезия фолликулов с нарушением стероидогенеза и усилением синтеза андрогенов.
У мальчиков также нарушается продукция гонадо-л иберинов в гипоталамусе и гонадотропинов — в аденогипофизе. Следствием этого являются нарушения полового созревания (раннее или, напротив, позднее).
Заболеванию свойственна дисфункция гипотала- мо-гипофизарно-тироидной системы с нарушением продукции тиролиберина в гипоталамусе, ТТГ — в аденогипофизе и йодтиронинов {Т3 и Т4) — в фолликулах щитовидной железы. При этом нередко выявляются антитироидные аутоантитела (Строев Ю.И. с соавт., 2003).
Вследствие нарушения синтеза дофамина в головном мозге и частичного снятия пролактостатического влияния подбугорья на аденогипофиз, у подростков с ги-поталамическим синдромом пубертатного периода в аденогипофизе усиливается секреция пролактина с развитием гиперпролактинемии. Поэтому у девочек хорошо развиты молочные железы, часто развивается мастопатия. Для мальчиков с этим заболеванием характерна гинекомастия (чаще — ложная, вследствие ганоидного ожирения; редко—истинная). Гипер- пролактинемия стимулирует биосинтез андрогенов в сетчатой зоне коры надпочечников и является при этой патологии одной из причин гиперандрогении у девочек — гирсутизм по мужскому типу, нарушение менструального цикла вплоть до аменореи, кистозное перерождение яичников.
Созревание гипоталамических структур, регулирующих секрецию рилизинг-гормонов, замыкает на фоне гиперандрогении порочный круг патогенеза этого синдрома.
Гиперпродукция АКТГ, кортизола, повышение активности ренин-алъдостероновой системы являются одной из ведущих причин нередкой для таких подростков артериальной гипертензии.
Важным звеном ее патогенеза является гиперин-сулинемия. Инсулин, стимулируя реабсорбцию натрия и воды в нефронах, повышает чувствительность коры надпочечников к ангиотензину II и увеличивает секрецию алъдостерона. Это приводит к задержке натрия и воды, увеличению объема циркулирующей плазмы крови и минутного объема кровообращения. Инсулин также повышает активность симпатической нервной системы. Инсулин, действуя на гладкомы-шечные клетки в стенках резистивных сосудов (ар-териолы), повышает в них внутриклеточное содержание ионов кальция и стимулирует их пролиферацию. Все это приводит к росту периферического сосудис-
того сопротивления и к возникновению артериальной гипертензии.
Таким образом, гормональные нарушения при гипоталамическом синдроме пубертатного периода проявляются гиперсекрецией СТГ, АКТГ, ГКС, гипер- пролактинемией, гиперинсулинизмом. У девочек развивается гиперандрогения и относительная ги-перэстрогения, снижена секреция гестагенов. Для юношей характерна гиперэстрогения, содержание тестостерона в крови вариабельно. Причиной гормональных нарушений при этом является первичное повреждение гипоталамуса. Строгой хронологической последовательности развития гормональных нарушений при этом синдроме обычно не наблюдается.
Клиника. Всех подростков прежде всего беспокоит ожирение—постоянный объект насмешек сверстников и дурно воспитанных взрослых, увеличение молочных желез, появление на коже живота, плеч и бедер розовых полос — «растяжек» (рис 34). Обычно родственники и окружающие отмечают у больных подростков булимию (прожорливость) — результат гиперинсулинизма, особенно во вторую половину суток, к ночи, когда повышается активность вагуса, стимулирующая продукцию инсулина. Неуемный волчий аппетит приводит к тому, что больные подростки часто украдкой едят по ночам. По утрам эти же подростки обычно едят мало, некоторые вообще не завтракают. Реже бывает отказ от еды.
Могут быть жажда и полиурия. Для этого синдрома вообще характерно нарушение толерантности к углеводам (причина—инсулинорезистентность). Уже в
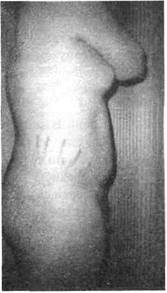
Рис. 34. Розовые стрии у подростка с гипоталамическим синдромом пубертатного периода (собств. набл.)
81
пубертате может развиваться инсулиннезависимый сахарный диабет 2-го типа. Проба на толерантность к глюкозе бывает патологической более чем у половины подростков, а примерно у каждого пятого-шестого подростка выявляется скрытый сахарный диабет.
Практически все жалуются на почти постоянные головные боли, быстро устают. Физическая работоспособность у них снижена.
Эти подростки отличаются замкнутостью, забывчивостью, плохой успеваемостью. Часты вспыльчивость, грубость из-за колких выпадов досужих окружающих, гораздых на различные обидные прозвища. Может быть плаксивость. Бывают депрессивные состояния.
Половое развитие может быть ускоренным. У юношей часто наблюдаются псевдо-евнухоидные черты телосложения с широким тазом, херувимоподобность или матронизм. Характерно отложение жира по женскому типу. Феминизация юношей связана с дисметаболизмом андрогенов. Гинекомастия чаще ложная, без железистой ткани. У юношей наблюдается гиперсексуальность, они склонны к ранней половой жизни. Для девушек это не характерно. У них бывают ранняя легкая вирилизация, угловатость, гипертрихоз, почти всегда расстраиваются месячные, пигментируются соски, клитор, малые половые губы.
Основной симптом синдрома— ожирение, которое возникает обычно еще в раннем детстве, но особенно они полнеют в 11-13 лет, поэтому выглядят старше своих лет и производят впечатление отменно здоровых. Лишний вес для каждой возрастной группы при этом достигает 35-40 кг. В наших наблюдениях масса тела у таких подростков колебалась от 67 до 140 кг ( в среднем —108,4±0,78 кг).
Формируется равномерное гиноидное ожирение (по женскому типу), иногда — евнухоидное (с широким тазом). Верхние и нижние конечности в отличие от синдрома Иценко-Кушинга — всегда также ожирелые, полные.
Рост, как правило, высокий. В наших личных наблюдениях рост обследованных подростков с гипоталами-ческим синдромом пубертатного периода колебался от 162 до 195 см, составив в среднем 180±0,78 см. Костный возраст обгоняет паспортный на 2-3 года.
Практически все подростки с гипоталамическим синдромом пубертатного периода имеют чаще поперечные, не западающие полосы не коже живота, внутренней поверхности плеч и бедер, верхнего наружного квадранта ягодиц, реже — в области поясницы, что является предметом тревоги больше родителей, чем самих больных. Полосы могут возникать быстро, в течение нескольких недель, но они не имеют экстрава-
82
затов. Характерной особенностью стрий при описыва-емом синдроме является их обратимость при успеш-ном лечении ожирения — снижение массы тела приво-дит к обесцвечиванию стрий, они становятся белыми и очень часто вообще исчезают.
На коже могут обнаруживаться липомы, бородав-ки, витилиго, кондиломы, гиперпигментация складок, Дермографизм обычно красный, быстро исчезает Кожа может быть нежной, не загорающей, почему та-кие юноши чаще белокожие, с мраморным оттенком (херувимоподобные). Атрофии кожи, как при синдро-ме Иценко-Кушинга, не бывает. Кожа задней поверхности плеч и кожа ягодиц обычно шершавая («с пупы-рышками»). Волосы сальные, склонны к выпадении (мы наблюдали трех подростков с гнездной и даже то-тальной алопецией — с выпадением бровей, ресниц и т. д.). Ногти тонкие и ломкие. На фоне жирной себо-реи часто выявляются юношеские угри, особенно у де-вушек в результате гиперандрогении и повышенной к ней чувствительности волосяных фолликулов.
Руки нежные, мягкие, с длинными пальцами и гипер-мобильностью суставов, напоминающими кисти боль-ных с соединительнотканной дисплазией марфаноподоб-ного фенотипа (Кадурина Т.И.,2000). Нередка наблюдаются акроцианоз и «ледяные» наощупь кисти Гипергидроз кистей может быть настолько выражен-ным, что подростки стесняются подавать руку при ветре-че.
Внешне подростки эутироидны, но функция щито-видной железы может снижаться, появляются признаки гипотироза (зябкость, дневная сонливость, заторможенность, степенная медлительность, сухости! гиперкератоз кожи локтей и пяток, нередки запоры), Изредка возникает легкий гипертироз (тремор пальцев, потливость, тахикардия).
Температура тела обычно нормальная, но часто асимметричная, реже — субнормальная, что может co-провождаться зябкостью (по-видимому, из-за гипофункции щитовидной железы).
Часто обнаруживается артериальная гипертензия, Ей обычно предшествует нейроциркуляторная дисто-ния (Строев Ю.И. с соавт., 2003), хорошо проявляющаяся при термографических исследованиях нижних конечностей (рис. 35, цв. вклейка). В наших наблюде-! ниях повышенное артериальное давление выявлялось более чем у 70 % юношей с гипоталамическим синдромом пубертатного периода, при этом истинная артериальная гипертензия (по критериям ВОЗ) диагностировалась у 38 %, пограничная — у 33 %. Для этих подростков был характерным гипокинетический тип гемодинамики с низкими показателями сердечного выброса и высоким периферическим сосудистым сопротив-
лением, что является у них основным механизмом артериальной гипертензии (Бельгов А.Ю., 1994).
Осложнения. При стрессах (например, экзамены, тяжелые виды спорта в целях похудения, резкая смена климата в виде модных краткосрочных вояжей в Турцию или Египет и пр.) гипоталамический синдром пубертатного периода может обостряться и даже прогрессировать. Истинный синдром Иценко-Кушинга развивается при этом крайне редко.
Артериальное давление может повышаться до ги-пертензивных кризов. Отмечается повышение внутричерепного давления с микросимптоматикой.
У девушек может возникать поликистоз яичников с аменореей, фиброаденоматоз молочных желез, галак-торея. При беременности в первой ее половине бывают отеки и невынашивание, а во второй половине — токсикозы беременности (гестозы) с повышением артериального давления и массы тела.
У юношей иногда прогрессирует гинекомастия. Больные склонны к кандидомикозам.
Классификация. Гипоталамический синдром пубертатного периода разделяют по течению на легкий, среднетяжелыи и тяжелый, что определяется не столько степенью тяжести ожирения, сколько тяжестью эндокринных и сердечно-сосудистых расстройств.
Диагностика. Вид больных (равномерное гиноид-ное ожирение) достаточно типичный, а розовые стрии для этого синдрома почти патогномоничны (рис. 34).
Анализы крови обычно нормальные. Патология мочи (у 35-40 % больных) чаще обусловлена аномалиями почек, хроническим пиелонефритом или нефролитиазом. Но зато у большинства больных имеются атерогенные нарушения обмена липидов с ростом коэффициента ате-рогенности.
Секреция гормонов отличается умеренным повышением в крови АКТГ и кортизола с нарушением циркад-ного ритма последнего (повышение в вечерние и ночные часы), ренина и алъдостерона, инсулина. Повышенные уровни АКТГ, кортизола, инсулина, ренина и алъ достерона в крови у больных подростков положительно коррелируют с цифрами артериального давления (Бельгов А.Ю., 1994).
Всем подросткам, страдающим ожирением с розовыми стриями, необходимо проводить рутинный тест на толерантность к глюкозе (ГТТ), а при сомнительных его результатах—повторить исследование на фоне кор тизола или преднизолона (проба Конна).
Уровень тестостерона у юношей слегка снижается. Концентрации катехоламинов и серотонина нормальные или даже умеренно снижены.
Определение концентраций тироидных гормонов обнаруживает у большинства этих подростков некоторое
снижение Т4, увеличение Т3 и тиротропина (ТТГ), что свидетельствует у них о тенденции к нарастанию гипофункции щитовидной железы. Нередкое выявление ан-титироидных аутоантител в сочетании с типичной для аутоиммунного тироидита ультрасонографической и термографической (рис. 36, цв. вклейка) картинами щитовидной железы (гипоэхогенность ткани органа и неоднородность его как ультрасонографической, так и термографической структур) позволяют диагностировать у подростков с гипоталамическим синдромом пубертатного периода аутоиммунный тироидит, что дает основание для включения в терапию этой формы ожирения синтетические тироидные гормоны.
Границы сердца слегка расширяются влево, левый желудочек нередко гипертрофирован из-за артериальной гипертензии. У 1/3 подростков выявляется гипертоническая ангиопатия сетчатки глаз. Тип гемодинамики— чаще гипокинетический, с ростом периферического сосудистого сопротивления. Сократительная функция миокарда снижается, на ЭКГ могут быть признаки местных блокад.
Часто выявляются тепловизионные признаки мик-роциркуляторных расстройств в нижних конечностях по типу микроангиопатии (рис. 37, цв. вклейка), возможно, за счет частого для этих подростков скрытого сахарного диабета (10-15 %) и поголовной гиперин-сулинемии после нагрузки глюкозой (рис. 38). Гликемические кривые при глюкозо-толерантном тесте нередко имеют признаки пониженной толерантности к глюкозе и даже выраженного гиперинсулинизма. Признаки периферического атеросклероза встречаются редко и то — при сочетании выраженной дислипо-
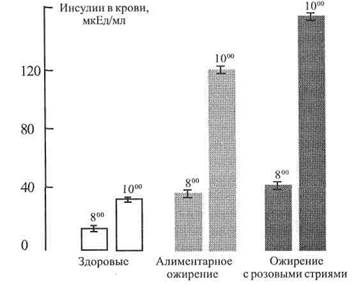
Рис. 38. Базальная (800 утра) и стимулированная перорально глюкозой (1000 утра)инсулинемия у подростков с разными формами ожирения (собств. данные)
83
протеидемии, гиперинсулинемии и артериальной ги-пертензии.
Данные ЭЭГ свидетельствуют о диффузных изменениях биоэлектрической активности головного мозга на фоне дисфункции мезодиэнцефальных структур со снижением порога судорожной готовности и совпадением волн с ЭКГ. На ЭЭГ после пробы с гипервентиляцией часто (до 75 %) нарастает индекс медленных волн (рис. 74). Последнее может быть обусловлено гипокальциемией, которая, по нашим наблюдениям, нередко сопутствует аутоиммунному ти-роидиту с гипофункцией щитовидной железы (Стро ев Ю.И. с соавт., 2002)
На рентгенограммах поясничного отдела позвоночника вследствие избыточной массы тела обнаруживается слабо выраженный остеопороз. Могут быть признаки внутричерепной гипертензии. Турецкое седло чаще нормальное, встречаются гиперостозы черепа и кальциноз твердой оболочки мозга.
Критерии диагноза. Патогномоничен внешний вид подростков с розовыми стриями на животе, ягодицах, внутренней поверхности бедер и плеч и диффузным ожирением по женскому типу, гипоталамической дисфункцией, сопровождающейся умеренным повышением уровня кортизола в крови в течение суток.
Пример диагноза. Гипоталамический синдром пубертатного периода. Ожирение III степени с розовыми стриями в области живота и внутренней поверхности бедер. Функциональный гиперинсулинизм. Артериальная гипертензия. Мочекислый диатез. Ложная гинекомастия.
Дифференциальный диагноз. Важно подчеркнуть, что ожирение с розовыми стриями, несмотря на внешнее сходство с картиной синдрома Иценко-Кушинга (см. ниже) и многими формами диэнцефального ожирения, протекает преимущественно доброкачественно. При этом расстройстве нет опухолей и повреждений, обусловливающих необратимые нарушения в гипотала-мо-гипофизарном нейросекреторном аппарате.
Поэтому ожирение, зависящее от преходящей ги перпродукции АКТГ и соматотропного гормона, не сопровождается стойким гипогонадизмом, задержкой психического или физического развития. Напротив, рост и созревание таких подростков ускорены, а раннее начало половой жизни даже благотворно влияет на их жировой обмен и способствует нормализации веса.
Ожирение носит смешанный или гиноидный характер, однако и гиноидность контуров фигуры, и ложная гинекомастия у юношей не свидетельствуют о каких-либо аномалиях полового развития, так как сохраняется в основном нормальная продукция гонадотропинов и андрогенов.
84
Так как в подкожно-жировой клетчатке происходит повышенный катаболизм мобильных жировых депо в результате глюконеогенеза, отмечаются разрывы co -единительно-тканных прослоек и формирование жиро-вых кист, появляются обратимые розовые полосы -стрии.
Подростки с гипоталамическим синдромом пубер- татного периода имеют несколько повышенную про-дукцию АКТГ и кортикостероидов всех трёх групп. Hо ожирение не характеризуется типичной для синдрома Иценко-Кушинга строгой зональностью. Конечности всегда остаются ожирелыми, полными. В плане диффе-ренциальной диагностики с иными формами ожирения важно учесть ложный характер гинекомастии и розовый (а не фиолетовый или багрово-синюшный, как при син- дроме Иценко-Кушинга) цвет поверхностных, не запа-дающих, тонких стрий.
При синдроме Иценко-Кушинга рост и дифферен-цировка скелета всегда отстают от паспортного воз-раста, всегда выражены остеопороз и атрофия мышц, почему конечности всегда выглядят худыми. Подрос-тки-юноши феминизируются, бреются очень редко или вообще не бреются. Девушки явно маскулинизируют-ся, что приводит к аменорее, атрофии яичников и вы-раженному гирсутизму. Лицо, как правило, лунообразное, синюшно-багровые полосы на коже атрофичные, западающие, с петехиями и экстравазатами, никогда са-мостоятельно не регрессируют. Лучевые методы при этом часто выявляют объемную патологию гипоталамуса или гипофиза, опухоли или гиперплазию коры над-почечников, что сопровождается патологически высоким уровнем кортизола в крови в течение суток и высоким содержанием 17-ОКС в моче. Подростковое ожирение с розовыми стриями с возрастом обычно проходит, синдром Иценко-Кушинга без лечения никогда не исчезает. Наличие розовых стрий позволяет отличить гипоталамический синдром пубертатного периода от алиментарно-конституционального ожирения, при котором обычно не бывает ни стрий, ни явных отклонений уровней гормонов в крови от нормы.
Исходы заболевания и прогноз. При гипоталами-ческом синдроме пубертатного периода прогноз чаще удовлетворительный. При рациональной коррекции он исчезает быстрее (к 20-25 годам), в синдром Иценко-Кушинга переходит в единичных случаях.
Заболевание может перейти в хроническую форму с периодами ремиссий и обострений.
Наибольшую опасность представляет транзитор- ная гипертензия как проявление подростковой веге-то-сосудистой дистонии. Она может персистировать и переходить в истинную артериальную гипертензию, то
есть артериальная гипертензия может стабилизироваться. Артериальную гипертензию при ожирении с розовыми стриями следует, по нашему мнению, рассматривать как симптоматическую (вследствие гиперкортизолизма, гиперальдостеронизма и гиперренинемии).
Репродуктивная функция, особенно у подростков мужского пола, обычно не страдает.
В катамнезе у подростков, перенесших гипоталами-ческий синдром пубертатного периода, может, по-видимому, в зрелые годы формироваться метаболический Х-синдром Камю. Девушки с гипоталамическим синдромом пубертатного периода, очевидно, могут в дальнейшем развивать синдром поликистозных яичников (синдром Лесного-Штейна-Левенталя), так как эти два заболевания имеют патогенетически много общего.
На основании собственных данных и сопоставления известных сведений о патогенезе этих расстройств мы предлагаем гипотезу о том, что гипоталамический синдром пубертатного периода (ожирение с розовыми стриями) представляет собой своего рода предболезнь или пубертатный дебют синдрома Камю и синдрома Лес ного-Штейна-Левенталя, имеющих, по-видимому, общую с ним генетическую основу. В будущем вполне возможно появление прямых свидетельств, позволяющих сблизить или объединить эти нозологические формы (Ю.И. Строев, Л.П. Чурилов с соавт., 2003).
Лечение. Лечение должно быть длительным и комплексным. Оно требует большого терпения не только у больного и его родствнников, но и у врача. Оно во многом зависит от информированности подростка и его родных об ожирении с розовыми стриями и о его исходах (Терещенко И.В., 1994).
Цель лечения—нормализация функции гипоталамо-гипофизарной системы, коррекция гормонально-обменных, а также вегетативных и гемодинамических нарушений.
Первоочередной задачей являются устранение обострения заболевания и профилактика его рецидивов.
Основной метод лечения—редукционная диета, направленная на снижение массы тела и на нормализацию углеводного и липидного обменов. Цель диетотерапии — создание в организме тучного подростка отрицательного энергетического баланса.
Диета должна быть субкалорийной, с малым содержанием углеводов и животных жиров (стол 8 б). Этот стол содержит 80-90 г белка, 70-80 г жира и 80-120 г трудноусвояемых углеводов. Запрещаются сахар, сладо- стии мучные изделия. Важны разгрузочные дни, но без сладких фруктов, которые богаты углеводами. Запреща-
ется виноград как источник чистой глюкозы. В настоящее время в продаже имеются многочисленные саха-розаменители и изделия, их содержащие, которые можно использовать при ожирении с розовыми стриями (сахарин, сластилин, сукралайф, сукрадайет, сорбит, ксилит, аспартам, фруктоза и др.).
Животные жиры полностью исключать нельзя, так как они являются источником холестерина, необходимого для синтеза всех стероидных гормонов, в том числе половых, и витамина D . Холестерина растительные жиры вообще не содержат. При резком ограничении жиров обязательно назначать жирорастворимые витамины — A , D 3 ( o к cu д e в um , вигантол), К и Е в нужных дозах.
Подростка нужно постепенно приучать к субкалорийной диете. По И.В. Терещенко (1994), больному подростку следует установить 5-разовое питание, при этом завтрак должен укладываться в 30 % суточного калоража, второй завтрак—в 15%, обед—в 3 5 %, полдник — в 10%, у жин — также в 10 %. На время лечения в семье необходимо прекратить приготовление сладких и мучных блюд или, по крайней мере, не употреблять их в присутствии больного подростка. Лечение идет успешнее при поддержке и поощрении не только со стороны врачей, но и со стороны родных и друзей.
Дата: 2019-02-02, просмотров: 530.