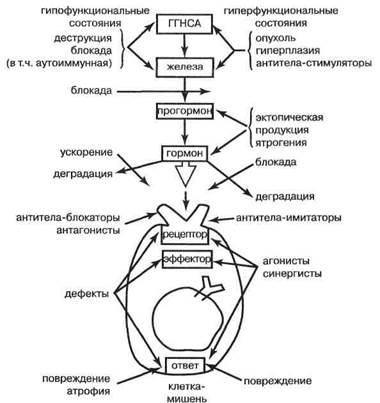
Патология эндокринной системы затрагивает все виды метаболизма, а также рост, размножение, регенерацию, индивидуальное развитие организма, его онтогенетическое становление. Классические представления о патогенности недостатка или избытка того или иного гормона сложились уже на заре эндокринологии. В XX веке к ним добавилось понимание того, что тканевая резистентность или гиперчувствительность к действию гормона могут вызвать картину болезни даже при его адекватной продукции. Современные представления о том, чем и как могут быть вызваны эндокринопатии, отражены на рис. 12.
Эндокринопатии всегда сопровождаются избыточным или недостаточным эффектом какого-либо гормона на те или иные мишени, что и порождает клиническую картину. Известны, правда, и исключения. Так, дефицит тирокальцитонина у человека бессимптомен, так как кальций-фосфатный гомеостаз при этом эффективно поддерживается компенсаторными изменениями, связанными с его антагонистами паратгор- моном и кальциферолом. Избыток тестостерона у
|
|
мужчин, а прогестерона у лиц обоего пола также не дает клинических симптомов.
Недостаточное действие гормона может быть следствием нескольких типовых причин, так или иначе затрагивающих железу, где он производится.
• Нарушение выделения гормона в кровь эндокрин
ной железой происходит либо при деструкции, либо
при информационной блокаде гормонообразующих
клеток. Причиной деструкции могут быть различ
ные процессы.
S Негормонообразующие опухоли, как это происходит, например, при хромофобных (нуль-клеточных) опухолях гипофиза, вызывающих гипопитуитаризм. К этой же этиологической группе может быть отнесена гипофункция железы при метастазах в нее неэндокринных опухолей и инфильтрации лейкозными бласта-ми (например, аддисонова болезнь в результате метастазов опухоли в надпочечники).
S Инфекция и последующее воспаление с альтерацией железы (примером служит острый тироидит, туберкулёз надпочечников как причина болезни Аддисона и т.д.).
S Неинфекционое воспаление, главным образом — аутоаллергической природы (например, аутоиммунный тироидит Хаси-мото*, аутоиммунный гипопаратироз, аутоиммунный гипофизит). Известны случаи деструкции эндокринных органов при их воспалении, вызванном травмой. В Мариин- ской больнице Санкт-Петербурга в 1995 г. авторы наблюдали случай вторичного сахарного диабета, развившегося после боевого (в Афганистане) огнестрельного ранения в брюшную полость, сопровождавшегося обширной травмой поджелудочной железы.
S Острое нарушение кровообращения, приводящее к ишемическому некрозу или тром-боэмболической апоплексии эндокринного органа (примером служит синдром Уотер-хауза-Фридериксена — острая надпо-чечниковая недостаточность при двусторонней тромбоэмболической апоплексии мозгового вещества надпочечников, возникающей на фоне диссеминированного внут-
* В русскоязычной литературе и в устной речи эта фамилия
пишется и произносится как «Хашимото», что не совсем пра
вильно, так как в японском языке звука «ш» вообще не существует.
Таким искажением фамилия Н. Hashimoto обязана английскому
произношению. Поэтому правильнее писать и говорить — Хаси-
мото.
рисосудистого свёртывания крови в результате менингококкового сепсиса).
S Генетически обусловленный дефект синтеза гормона, приводящий к его недостатку или ненормальной структуре (как при наследственных формах гипотироза и в эсквизит-ных случаях инсулиннезависимого сахарного диабета).
S Дефицит компонентов, из которых производится гормон (гипотироз при геохимической недостаточности йода; иммунодефицит при нехватке цинка, входящего в состав тимули- на; гипофункция щитовидной железы и мозгового вещества надпочечников при наследственном нарушении окисления тирозина, из которого синтезируются их гормоны).
S Интоксикации, избирательно нарушающие продукцию гормонов. Сюда относятся как случаи ятрогенного подавления продукции гормонов при лечении и самолечении (например, индукция гипокортицизма метирапо-ном, гипотироза — мерказолилом), так и случаи влияния пищевых факторов. Родани- ды и цианиды репы, редьки, кабачковых, краснокочанной капусты, маниоки и тапиоки
Рис. 12. Возможные механизмы эндокринопатий. ГГНСА — ги-поталамо-гипофизарный нейросекреторный аппарат
29
в больших дозах могут вызывать понижение продукции тироидных гормонов. Так, подсчитано, что килограмм репы по антитироид-ному действию приближается к половине таблетки мерказолила. S Важно отметить, что в некоторых случаях блокада рецепторов тропных гормонов на эндокриноцитах антирецепторными аутоан-тителами ведет к неэффективности стимуляции железы ее физиологическими регуляторами и к отсутствию продукции гормона интактными в других отношениях эндокри-ноцитами, несмотря на метаболическую в нем потребность. Так как многие тропные гормоны (гормоны-стимуляторы гормонооб-разования) служат для своих мишеней и секреторными, и митогенными сигналами (Пав- ликовски М., 1982), то такой информационный блок ведет не просто к недостаточности гормонов регулируемой железы, но и к ее атрофии, без признаков воспалительного или иного деструктивного процесса. Примерами могут служить атрофия коры надпочечников при наличии блокирующих аутоантител к рецепторам АКТГ (Давидай М. с соавт., 1984), гипергонадотропный гипогонадизм из-за аутоаллергии против рецепторов ФСГ (Диас X . с соавт., 1982) и аутоиммунный атрофический гипотироз, вызванный иммуноглобулинами, блокирующими рецептор ТТГ (Де Сент Ж.П., Вемо Ж. Л., 1982). Во многих случаях недостаточное действие того или иного гормона имеет внежелезистое происхож дение.
S Недостаточный переход прогормона в гормон вызывает симптомы дефицита его активности, даже при не нарушенном синтезе. Примерами могут служить подавление перехода проренина в ренин при сахарном диабете, связанное с механизмами диабетической нефропатии, а также витамин D-резистентные формы рахита, рассматриваемые ниже в разделе, посвященном нарушениям функций паращитовидных желез. При дефекте фермента 5а-редуктазы ткани-мишени не превращают тестостерон в дигидротестостерон, что ведет к частичному гипоандрогенизму, ибо собственная андрогенная активность предшественника намного ниже, чем дигидроформы этого стероида.
30
S Циркулирующие антагонисты гормона могут снизить его эффективные концентрации. В роли таких антагонистов нередко выступают антитела к гормону (вазопресси-ну — при неопухолевых формах несахарного диабета, инсулину — при вторичной инсули-норезистентности). Неиммунологическими циркулирующими антагонистами, вызывающими понижение эффективности действия гормона, могут быть и другие гормоны (симптоматический вторичный сахарный диабет при гиперкортизолизме, феохромоцитоме, глюкагономе), а также ятрогенно введённые лекарства (гипоандрогенизм и импотенции под влиянием противоязвенного гистаминово-го блокатора циметидина и его аналогов, ги-потироз при передозировке мерказолила) иле метаболиты (избыток свободных жирных кислот снижает эффективность действия ин сулина). S Как уже отмечалось выше, при нормальном функционировании сервомеханизмов обрат ной связи одно только усиление связывания гормона с белком-переносчиком, как и изоли-рованное ускорение деградации гормона, не могут вызвать стабильного дефицита действия гормона. Преходящие изменения будут ком пенсироваться. Но в условиях нарушенного механизма обратной связи как увеличение степени связывания, так и скорости разруше ния гормона способны отразиться на его эффек тивной концентрации. Это хорошо проясняю следующие примеры. Повышение содержани тестостерон-связывающего глобулина способ но вызвать снижение действия тестостеро на у женщин, поскольку у них нет механизм обратной связи, контролирующего уровень это го стероида. Высокий уровень транстирети на и тиросвязывающего глобулина плазмы не ведет к гипотирозу у здоровых людей, но ва-жен для больных, находящихся на экзогенном тироксине. Поскольку тироидные гормоны ускоряют катаболизм глюкокортикоидов, ги пертироз способен вызвать переход скрытого гипокортицизма в явный или обусловить рези-стентность к лечению кортикостероидами, хотя сам по себе не ведет к гипокортицизму, если только резервы коры надпочечников и ги-пофиза адекватны. Периферическая резистентность к гормонам -важная внежелезистая причина понижения эффек-
тивности их действия. Такая резистентность часто связана с рецепторными механизмами. Это может подразумевать:
S наследственный дефект внутриклеточных рецепторов по типу одиночных аминокислотных замен или отсутствия их экспрессии (как это наблюдается в отношении рецепторов ан-дрогенов при тестикулярной феминизации— синдроме Морриса, псевдогипоалъдосте-ронизме, наследственной резистентности к кортизолу); S наследственный дефект мембранных поверхностных рецепторов {почечный питрессин- резистентный несахарный диабет, синдром карликовости Ларона, некоторые формы тяжелого наследственного инсулинорезис-тентного сахарного диабета); S блокаду рецепторов аутоантителами (как это отмечено при myasthenia gravis — в отношении Н-холинергических, а при acantosis nigricans—в отношении инсулиновых рецепторов); S подавление экспрессии генов рецепторов эпигенетическими воздействиями (считается, что подобным образом переедание и ожирение могут способствовать развитию гиперин- сулинемических форм сахарного диабета). Не менее важен пострецепторный механизм гор-монорезистентности. При псевдогипопаратирозе имеет место дефект сопряжения рецептора паратгор- мона и рецепторов ряда других регуляторов с адени-латциклазами за счет наследственного дефекта гуа-нилнуклеотид-связывающего регуляторного белка. Многие формы инсулиннезависимого сахарного диабета зависят от наличия пострецепторных дефектов в опосредовании действия инсулина на его мишени.
Иногда рецепторная нечувствительность к гормону связана с неспособностью ткани выработать под его влиянием тканевой белковый гормон-посредник. Так, при карликовости Ларона продукция СТГ адекватна, но ткани из-за дефекта рецептора СТГне образуют под действием гормона роста нужного количества одного из соматомединов — инсулиноподобного фактора ро ста I (соматомедина С). Важно подчеркнуть, что тканевая резистентность бывает не только к пептидным или тирозиновым гормонам, но и к стероидам. Так, А. Вингерхёдс с соавт. (1976) описали пациента с вы-раженым гиперкортицизмом, но без признаков синд рома Иценко-Кушинга.
• Наконец, если сами клетки-мишени атрофированы или повреждены, они могут не отвечать
даже на сильный гормональный сигнал. Так, глю-кагон перестает вызывать гипергликемию при тяжелой печёночной недостаточности. В условиях истощения адипоциты прекращают отвечать выработкой лептина на инсулин и глюкагоноподоб-ный пептид — и перестает тормозиться аппетит. Вазопрессин, например, не эффективен при выраженном нефросклерозе. Избыточное действие гормона также может иметь несколько типовых причин.
• Недостаточность физиологического сервомеханизма, контролирующего продукцию гормона по типу обратной связи (например, снижение чувствительности В-клеток островков Лангерганса к глюкозе при некоторых формах ин- сулиннезависимого сахарного диабета или клеток гипоталамуса, вырабатывающих корти-колиберин, к глюкокортикоидам и АКТГ— при болезни Иценко-Кушинга).
• Обход физиологического механизма обратной связи из-за появления избытка стимуляторов гормонообразующих клеток, не включённых в сервомеханизм. Данная группа гиперфункциональных эндокринопатий имеет почти исключительно аутоиммунную природу и вызвана имму-ноглобулинами-агонистами рецепторов тропных гормонов. Типичным примером служит базедова болезнь, при которой гиперплазия и гиперфункция щитовидной железы вызываются, в обход гипоталамо-гипофизарной регуляции, аутоантите-лами к ганглиозидной и белковой частям рецепторов ТТГ. Подобные аутоантитела могут вызвать изолированную гиперфункцию железы, но чаще обусловливают ее гиперплазию и гиперфункцию. Хронические неэндокринные заболевания могут создавать неиммунологические сигналы, стимулирующие продукцию того или иного гормона с развитием вторичной гиперпродукции последнего. Примером служит вторичный гипе-ралъдостеронизм, закрепляющий механизм системных отёков при сердечной недостаточности. В роли сигнала, побуждающего в конечном итоге к гиперфункции «ренин-ангиотензин-алъ- достероновой системы», выступает снижение объема сердечного выброса.
• Утечка гормона из железы вследствие ее деструкции (примером служат эпизоды гипертироза при развитии аутоиммунного подострого тироиди- та Де Кервена).
• Нерегулируемая гиперпродукция гормона относительно высокодифференцированной доброкачественной эндокринной опухолью в пределах той
31
железы, которая служит его основным источником (таков гипертироз при токсической аденоме щитовидной железы, персистирующая галакто-рея-аменорея при пролактиноме аденогипофи-за). Изредка гормонообразующими являются злокачественные опухоли эндокринных желез.
• Метаболический блок во взаимопревращени
ях гормонов может вызвать не только недоста
ток гормона, являющегося конечным звеном цепи
превращений, но и избыток промежуточного гор
монально-активного продукта. Характерным при
мером служит врождённая гиперплазия коры
надпочечников, вызванная дефицитом 21-гидро-
ксилазы. При дефиците этого фермента страдает
биосинтез минералокортикоидов, а избыток
предшественников превращается в андрогены.
Поэтому гипоалъдостеронизм и солътеряющий
синдром может сочетаться с гиперандрогениз-
мом и вирилизацией девочек, либо с макрогени-
тосомией и с преждевременным половым со
зреванием мальчиков.
Синдром избыточной эффективности действия гормона может иметь также внежелезистое происхождение. Основные формы этого явления следующие.
• Эктопическая, автономная от сервоконтроля, продукция избытка гормонов вне основных эндокринных желез. Этот вариант эндокринной гиперфункции связан, как правило, с образованием гормонов, кодируемых одним-двумя генами, в опухолевых, чаще злокачественных, клетках апудоцитарной природы (синтез АКТГ и паратгормона овсянокле-точными карциномами бронхов, а также серото- нина и энтериновых пептидов — карциноидами желудочно-кишечного тракта, гормонообразова- ние в тимомах). Изредка опухоли неапудоцитарной природы могут осуществлять подобный эктопический синтез (продукция тироидных гормонов в опухолях яичника).
• Продукция избытка активного гормона из про-гормонов в неопухолевых периферических тканях. Примером служат гиперэстрогенизм при ожирении и при печеночной патологии из-за избыточной конверсии андростендиона в эстрогены адипоцитами или гепатоцитами, а также эндогенный гипервитаминоз D при саркоидозе из-за образования макрофагами гранулём избытка высокоактивной формы кальциферола.
• Ятрогенный избыток гормона или его аналога может быть результатом лечения или самолечения. Часто это относится к избыточному приему адреномиметиков, тироидных гормонов, анд-
32
рогенов и кортикостероидов. Интересно, что некоторые растительные пищевые продукты содержат действенные аналоги животных гормонов. Такова солодка, имеющая в своём составе аналоги алъдостерона (глицерризиниевую кислоту). Злоупотребление лакричными конфетами и усиленное траволечение солодкой вызывает картину, сходную с первичным гиперальдостеронизмом, провоцируя артериальную гипертензию.
• Аутоантитела к гормональным рецепторам периферических тканей-мишеней могут имитировать избыточное действие соответствующих гормонов. Как правило, они образуются по иди- отип-антиидиотипическому механизму в ответ на антитела к гормону. Инсулиномиметичес-кие аутоантитела обнаружены у подростков, больных «криптогенной» гипогликемией и лабильным инсулинзависимым сахарным диабетом, а также получены экспериментально, Связываясь с инсулиновым рецептором, они временно воспроизводят часть эффектов гормона, нарушая соотношение между уровнем глюкозы и активностью В-клеток (Ди Марио В. с соавт. 1977; Шехтер Й. с соавт., 1982).
• Тканевая гиперчувствительность к гормонам встречается реже, чем резистентность. Однако описаны почечная гиперчувствительность к мине- ралокортикоидам {псевдогиперальдостеро-низм с низким уровнем ренина и альдостерона и задержкой натрия), а также глюкокортикоидная глаукома у больных, которые особенно чувстви-тельны к влиянию кортикостероидов на внутриглазное давление. Широко известна индукция ти роидными гормонами экспрессии рецепторов катехоламинов в сердце и сосудах, участвующая в патогенезе артериальной гипертензии и миокар диодистрофии при гипертирозе.
• Изолированные понижение связывания гормона в крови и ускорение его деградации, как пра вило, недостаточны для индукции его избыточного действия в силу нивелирующего эффекта нормаль-ных механизмов обратного контроля. Но эндокри нологи традиционно не оставляют без внимания возможность появления стабильного внежелези стого избытка гормона, связанного с особеннос тями его транспорта и катаболизма. Дело в том что при нарушениях нормальных взаимоотноше ний тропных и периферических гормонов или в со четании с действием других факторов данный механизм приобретает известное значение. Так при голодании, печёночной недостаточности и не-
фротическом синдроме дефицит альдостеронсвя-зывающих белков плазмы и недостаточный распад алъдостерона в печени вносят свой вклад в развитие вторичного гипералъдостеронизма и отёков, которые обусловлены прежде всего другим фактором — понижением онкотического давления плазмы. Эндокринопатии бывают моногланду лярными, то есть поражающими одну эндокринную железу. Но встречаются и плюригландулярные поражения. В случае вовлечения в дисфункцию многих желез необходимо учесть возможность системных причин такого поражения. Плю ригландулярные синдромы бывают гипоталамо-гипо-физарными, аутоиммунными, рецепторными и наследственными.
При центральной этиологии плюригландулярное поражение является вторичным по отношению к панги- попитуитаризму (тироидная, надпочечниковая не достаточность и гипогонадизм).
При аутоиммунном плюригландулярном синдроме аутоантитела поражают несколько желёз внутренней секреции, имеющих общие или сходные антигены. Известен аутоиммунный синдром Шмидта {инсулин-зависимый сахарный диабет, аутоиммунный тиро-идит, гипопаратироз и гонадо-надпочечниковая недостаточность).
При наличии аутоантител к 17-а-гидроксилазе ауто-аллергия поражает стероидопродуцирующие клетки в коре надпочечника и в гонадах. Аутоиммунные плю ригландулярные синдромы часто сопровождаются неэндокринными аутоиммунными расстройствами {ар трит, бронхиальная астма, витилиго, атрофичес-кий гастрит с В1-дефицитной анемией), а также другими признаками нарушенного иммунитета (например, кандидоз).
Рецепторная плюригландулярная аномалия развивается при дефекте гуанидин-связывающей части гормональных рецепторов семейства G-белков. Наблюдается неэффективность действия многих гормонов на их мишени {псеедогипопаратироз, гипергонадот-ропный гипогонадизм, первичный гипотироз).
Описаны три различных плюригландулярных на следственных синдрома, характеризующихся аномалией экспресии онкогенов и неопластическими процессами в разных гормонообразующих клетках { MEN - I , 11 а, 11в — от англ. Multiple Endocrine Neoplasiae ).
Это аутосомно-доминантные растройства с варьирующей пенетрантностью. Носитель синдрома MEN наследует один из двух аллельных генов дефектным, а во втором на протяжении онтогенеза имеет место соматическая мутация. Если она предоставляет клеткам-
мутантам селективные преимущества, формируется доброкачественная или злокачественная опухоль.
При синдроме MEN I имеется дефект гена под аналогичным названием из 11 -й хромосомы, который служит антионкогеном. При других типах MEN -синдро- ма генетический дефект, вероятно, связан с протоонкогеном RET из 10-й хромосомы, онкобелок которого является мембранной тирозин-протеинкиназой со свойствами ростового рецептора (Зайчик А.Ш., Чурилов Л.П., 2002).
Синдром MEN -1 (он же множественный эндокринный аденоматоз или синдром Вермера) включает доброкачественную аденому паращитовидной железы, а также доброкачественную либо злокачественную гормонообразующую опухоль островковых клеток поджелудочной железы (это, в порядке убывания частоты, может быть гастринома, инсулино-ма, значительно реже — глюкагонома или ВИПома). Гастриномы обусловливают у таких больных тяжёлые язвы желудка {синдром Цоллингера-Эллисона). Для синдрома MEN I характерны также гипофизар-ные аденомы (соматотропинома, пролактинома, реже— кортикотропинома). Бывают карциноиды из диффузных эндокриноцитов желудочно-кишечного тракта, липомы и аденомы коры надпочечников. Клиника некоторых гормонально-активных опухолей у подростков подробно описывается ниже.
Синдром MEN II отличается присутствием медул лярной карциномы С-клеток щитовидной железы и доброкачественной либо злокачественной феохромо- цитомы.
Он имеет две разновидности. При синдроме MEN 11а (синдроме Сиппла) добавляется гиперпаратироз, а при синдроме MEN 11в (он же —MEN III ) — гиперпаратироз не типичен, зато бывают невриномы кожи и слизистых, ганглионевромы, а внешний вид пациентов может напоминать синдром Марфана (арахнодактилия, высокий рост, длинные конечности).
Подростковый возраст —
Дата: 2019-02-02, просмотров: 395.