1. Введение антител одного типа, т.е. моноклональных антител, может вызывать появление в сыворотке антиидиотипических антител (анти-Id), определяемых по их связыванию только с индуцирующим моноклоном (Id).
2. Некоторые анти-Id подавляют связывание между Id и антигеном, его индуцирующим, показывая, что они направлены против фактического антигенсвязывающего участка.
3. Нормальный прирост количества антител при иммунном ответе ингибируется для любого Id инъекцией соответствующего анти-Id (но не всегда; см. пункт 9).
4. На поздней стадии иммунного ответа анти-Id появляются спонтанно именно в то время, когда уменьшается количество соответствующих им Id.
НЕКОТОРЫЕ ПРОБЛЕМЫ
5. Эксперименты показывают, что идиотип-антиидиотипическая сеть не бесконечна, а скорее состоит из небольших серий сцепленных идиотипов. Вероятно, некоторые В-клетки связаны через сеть идиотипов со «своими» антигенами, а другие В-клетки отвечают на чужеродные антигены.
6. Некоторые анти-Id распознают Id вне антигенсвязывающего участка и не подавляют присоединение антигена, причём такие Id могут находиться на других молекулах Ig с отличающейся специфичностью для антигена. В этом случае регуляция анти-Id будет специфичной для Id и не окажет существенного влияния на фактический иммунный ответ.
7. Подобные Id, синтезированные в ответ на конкретный антиген, например бактериальный, способны через сеть иммуногло-булинов или Т-клеточных рецепторов клеток-хелперов стиму-лировать синтез других антител, несущих Id, но со специфичностью к совершенно другому антигену. Возможно, это один из путей индукции аутоантител (рис. 36).
8. Отношение между Id и анти-Id сходно с взаимодействием гормонов и их рецепторов. Антитела к гормону, например к инсулину, могут быть подобием рецептора и индуцировать антитела к нему, что будет уже двойной дозой аутоиммунитета.
9. В экспериментах по регуляции показано, что введение анти-Id иногда ингибирует, а иногда стимулирует соответствующий Id. Объяснения этому пока не найдено, но класс или подкласс иммуноглобулина и способ введения могут иметь значение.
ПРАКТИЧЕСКОЕ ПРИЛОЖЕНИЕ
10. Если подавление продукции Id введением анти-Id будет надёжно воспроизводимым, то откроется новый подход к лечению аутоиммунных заболеваний, аллергии и др. Это особенно важно, если окажется, что аутоантитела имеют особые идиотипы, как в случае с некоторыми анти-ДНК-антителами.
11. Наиболее впечатляющее применение сетевой теории, но, возможно, успешно реализуемое только в будущем, связано с «внутренним образом» анти-Id, который подобен индуцирующему антигену. В некоторых случаях, когда антиген происходит из патогенных организмов и может быть применён в качестве вакцины, но его по разным причинам трудно получить в адекватном количестве, возможно применение антиидиотипических антител, имеющих «внутренний образ» антигена вакцины. Этот процесс достаточно сложен и требует сначала синтеза моноклональных Id, а затем моноклональных анти-Id, несущих заданный тип «внутреннего образа», что даёт обнадёживающие результаты, особенно с углеводными антигенами. Нет необходимости для антигена и анти-Id иметь ту же структуру, поскольку они имеют сходную конфигурацию. Другое преимущество состоит в том, что такие анти-Id-вакцины, будучи белками и являясь тимусзависимыми антигенами, способны индуцировать иммунную память, что нехарактерно для самих углеводов.
51
23. ЦИТОКИНОВАЯ СЕТЬ
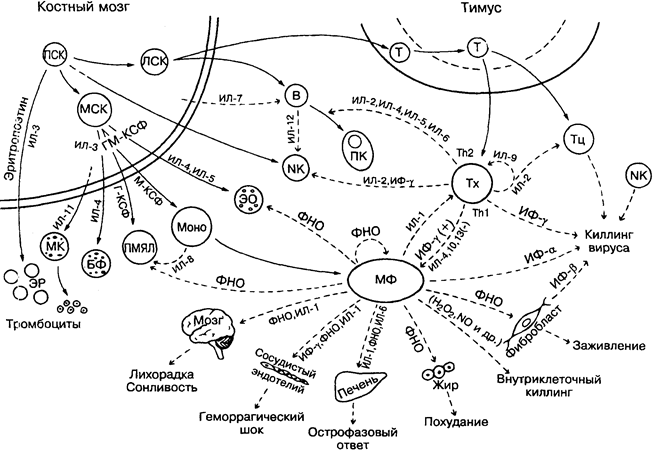
В предыдущих разделах упоминались продуцируемые клетками небольшие белковые молекулы, активно участвующие в межклеточных взаимодействиях и неспецифичные к антигену. Это колониестимулирующие факторы (рис. 4), интерлейкины (рис. 14, 18, 20), а также молекулы, о которых будет сообщена в разделах об инфекциях и опухолях, — интерфероны (рис. 26) и факторы некроза опухоли (рис. 31). Вместо устаревшего разделения на лимфокины и монокины (в зависимости от секретирующей клетки) все они обозначаются сейчас как цитокины.
Одно время считалось, что каждая из этих молекул имеет свою определённую функцию (ингибиция вирусов, стимуляция дифференцировки В-клеток и т.д.), но после того, как по крайней мере 20 цитокинов удалось клонировать и получить в чистом виде, стало ясно, что каждый из них выполняет несколько раз-
личных, явно не связанных, часто перекрывающихся синергических или, напротив, антагонистических функций, имеющих как благоприятные, так и нежелательные последствия при разных заболеваниях.
Производство и продажа цитокинов и их ингибиторов уже стали обширным бизнесом, приносящим хорошие прибыли. Обнаруживаются всё новые молекулы. Представленный рисунок сильно упрощает ситуацию, показывая лишь наиболее достоверные взаимодействия. Пунктирными линиями обозначены продукция и активность, сплошными — развитие клеточных линий. Для ответа на цитокины клетка должна обладать специализированными поверхностными рецепторами, многие из которых уже идентифицированы и клонированы. Возможно, они найдут применение в качестве конкурентных ингибиторов активности цитокинов.
52
ИНТЕРЛЕЙКИНЫ
ИЛ-1 (м. м. 17 500). Известен также как фактор, активирующий лимфоциты, или эндогенный пироген. Существует в двух формах — альфа и бетта, действие которых имеет много общего с ФНО.
ИЛ-2 (м. м. 15 500). Первоначально обозначенный как фактор роста Т-лимфоцитов, ИЛ-2 в действительности способен стиму-лировать многие, в том числе и секретирующие его клетки через рецептор, состоящий из 3 цепей.
ИЛ-3 (м. м. 15 000), или мульти-КСФ. Стимулирует рост предше-ственников большинства типов клеток костномозгового происхождения, возможно, как дополнительный регуляторный элемент.
ИЛ-4 (м. м. 20000). Первоначальное название «фактор роста В-лимфоцитов I». Выделяется Т-хелпером типа 2 для антительного отзета.
ИЛ-5 (м. м. 45 000) — ещё один выделяемый Т-хелпером типа 2 фактор роста В-лимфоцитов; стимулирует также созревание эозинофилов.
ИЛ-6 (м. м. 26 000), или фактор дифференцировки В-лимфоцитов. Требуется для секреции антител. Важный медиатор острой фазы воспалительного процесса.
ИЛ-7 (м. м. 25 000) продуцируется стромальными клетками костного мозга и тимуса и стимулирует рост ранних Т- и В-лимфоцитов.
ИЛ-8 (м. м. 8500), или фактор хемотаксиса нейтрофилов, выделяемый макрофагами. В последнее время включается в семейство хемокинов (см. ниже).
ИЛ-9 (м. м. 40 000) — Т-клеточный ростовой фактор для Т-лим-фоцитов.
ИЛ-101м. м. 40 000) — продукт Т-хелперов типа 2, ингибирую-щий клеточный иммунный ответ.
ИЛ-11 (м. м. 23 000) — продуцируемый в костном мозге фактор, влияющий на стволовые клетки, выработку тромбоцитов и участвующий во многих воспалительных процессах.
ИЛ-12 (м. м. 70 000) — фактор макрофагального и В-клеточно-го происхождения, стимулирующий функцию Т- и NK-клеток.
ИЛ-13 (м. м. 12 000) — подобный ИЛ-4 продукт Т-хелперов типа 2, ингибирующий макрофагальный ответ.
ИНТЕРФЕРОНЫ
Более видоспецифичны, чем остальные цитокины.
ИФ-альфа (м. м. 20 000), или лейкоцитарный ИФ. Существует около 20 сходных подтипов ИФ-альфа, индуцирующих синтез противовирусных белков.
ИФ-бетта (м. м. 20 000), или фибробластный ИФ. Как и ИФ-а, устойчив к действию кислот, и для него имеется такой же рецептор. Оба ИФ обозначаются как ИФ типа I.
ИФ-гамма (м. м. 45 000; обычно в форме димера), или ИФ типа II, иммунный ИФ, ИФ, чувствительный к кислотам. Выделяется Т-хел
пером типа 1, многофункционален и существенно отличается от ИФ-а и р. Среди его важнейших функций — активация макрофагов. Более видоспецифичен, чем большинство других цито-кинов.
Дата: 2018-12-28, просмотров: 444.