Антигенсвязывающий участок антитела представляет собой щель размером примерно 3х1х1 нм (размер 5 или 6 углеводных единиц), но известно, что антигены способны связываться с большими или даже отдельными частями вариабельной области. Связывание основывается на тесном трехмерном контакте, так что слабые межмолекулярные силы преодолевают нормальное отталкивание.
Ван-дер-Ваальса силы притягивают все молекулы через облако электронов, но действуют только на очень коротких расстояниях.
Водородные связи (Н-связи) (например, между -NH2- и -ОН-группами) — другой вариант слабых сил.
Электростатическое притяжение молекул антигена и антитела, несущих оппозитные заряды, может быть достаточно сильным.
Гидрофобные области антигена и антитела притягиваются в жидкой среде. Возможно, это наиболее сильная связь в иммунном комплексе.
Аффинитет выражается константой равновесия (на рисунке слева вверху). Значение, например, 103 л/моль считается низким, а у высокоаффинных антител оно может достигать 1010 л/моль и выше, что на несколько порядков больше, чем в большинстве взаимодействий фермент-субстрат. На практике чаще измеряют авидность, поскольку антитела имеют как минимум 2. активных участка и с моновалентными антигенами антисыворотка может реагировать с аффиннитетом средней степени. После антигенной стимуляции аффиннитет антител постепенно повышается, особенно в результате клеточной селекции снижающимся количеством антигена и частично соматической мутации генов иммуноглобулинов. В большинстве случаев высокоаффинные антитела гораздо эффективнее, но поскольку антитела с низким аффиннитетом тоже существуют, они могут иметь определённые преимущества (многоразовость, отсутствие толерантности).
ИММУННЫЕ КОМПЛЕКСЫ
При избытке антигена или антител образуются преимущественно мелкие (растворимые) комплексы. При почти одинаковых количествах антигена и антител (зона эквивалентности) формируются преципитаты (образования решётчатой структуры). В присутствии комплемента (т.е. в свежей сыворотке) образуются только растворимые комплексы: СЗ способен растворять крупные комплексы (рис. 34).
Блокирование киллерной активности, опосредованной Т-лим-фоцитами или антителами, иммунными комплексами при избытке антигена или антител (соответственно) может стать причиной нео"вечаемости на опухоли или паразитарные заболевания.
Clq — первый компонент комплемента. Связывается с Fc-фраг-ментом антител в иммунном комплексе, и, возможно, это происходит после конформационных изменений в молекуле Ig, хотя
некоторые исследователи считают достаточным условием на-груженность антигеном обоих активных участков (IgG). Связывание Clq с иммунным комплексом вызывает активацию комплемента по классическому пути.
Воспаление. Продукты расщепления СЗ и С5, воздействуя на тучные клетки, нейтрофилы и др., вызывают повреждение сосудов, характерное для болезней, связанных с иммунными комплексами (рис.34).
Лизис (например, бактерий) требует полного каскада компонентов комплемента. Иногда комплекс С5,6,7 удаляется от первоначального участка связывания антитела, активирует С8 и С9 и вызывает лизис нормальных клеток (например, эритроцитов) — процесс, известный как реактивный лизис.
Фагоцитоз. Чаще всего иммунные комплексы фагоцитируют-ся макрофагами, нейтрофилами, эозинофилами и др. Обычно классы и подклассы антител, соединяющиеся с Fc-рецепторами фагоцитов, связываются и с комплементом, давая более высокий эффект опсонизации. Действие через Fc- и СЗ-рецепторы происходит по разным механизмам. IgM, например, в большей степени связывает комплемент, чем взаимодействует с фагоцитарными клетками. Большинство иммунных комплексов, циркулирующих в крови, связывается через рецепторы комплемента с эритроцитами (рис. 5), попадает с ними в печень или селезёнку, где удаляется местными фагоцитарными клетками.
Цитотоксичность. Антитела, связанные с поверхностью клетки или микроорганизма, через Fc-рецепторы могут опосредовать киллинг, а не фагоцитоз. Макрофаги, моноциты, нейтрофилы, эози-нофилы и лимфоцитоподобные К-клетки способны осуществлять антителозависимую клеточно опосредованную цитоток-сичность (рис. 9). Данные о значении этого типа цитотоксич-ности in vivo противоречивы.
В-клеточная память. Фолликулярные дендритные клетки имеют рецепторы к комплементу, которые позволяют им удерживать иммунные комплексы и представлять антиген В-лимфоци-там с высокоаффинными свойствами рецепторов, обеспечивая тем самым усиление антительного ответа.
Выявление растворимых комплексов
Иммунные комплексы осаждают ультрацентрифугированием или в градиентах плотности и преципитируют в полиэтиленгликоле (ПЭГ), а также на холоде (криопреципитация). Имея в своём составе иммуноглобулины, комплексы выявляются анти-Ig-aн-тителами (например, ревматоидный фактор). Для обнаружения иммунных комплексов часто используют чувствительную реакцию их связывания с Clq. Выявление компонента СЗ основано на применении анти-СЗ-сывороток (иммуноконглютинин) и использовании клеток линии Raji с рецепторами комплемента. Некоторые комплексы не фиксируют комплемент, но преципи-тируются ПЭГ. Отдельные тесты могут выявлять также другие крупные молекулы. Поэтому для определения иммунных комплексов необходимо сочетание нескольких тестов.
45
20. КЛЕТОЧНЫЙ ИММУННЫЙ ОТВЕТ
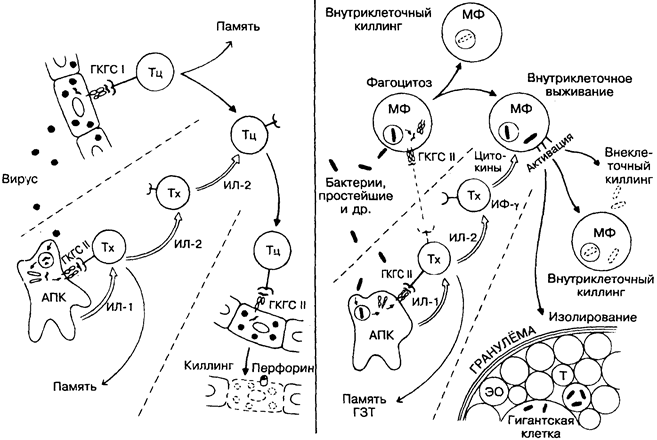
Многие варианты иммунного ответа опосредуются Т-лимфоцитами, проходят без участия В-лимфоцитов, проявляя при этом характерные для адаптивного иммунитета специфичность и память. Первоначально была выявлена их роль в иммунитете к возбудителю туберкулёза, а позже установлено, что они вовлекаются в контактную чувствительность, отторжение трансплантата, противовирусный и противоопухолевый иммунитет, хроническое воспаление и др. Во всех случаях речь идёт о клеточном иммунитете. Этот вариант иммунитета проявляется в двух направлениях: генерации специфических цитотоксических Т-лимфоцитов против внутриклеточных вирусов (на рисунке слева) и стимуляции Т-лимфоцитами активности неспецифических клеток, таких как макрофаги, в отношении внутриклеточных бактерий и других паразитов (справа). Примером последнего типа
ответа является гиперчувствительность замедленного типа, определяемая в кожном тесте.
Клеточный иммунный ответ имеет много общего с гуморальным, а именно взаимодействие с участием Т-хелперов и представление антигена в ассоциации с молекулами ГКГС (рис. 13,14,17). Нежелательными последствиями клеточного иммунитета могут быть повреждение тканей и отторжение трансплантата (рис. 35,37).
Как и антительный ответ, клеточный иммунитет регулируется различными супрессорными клетками и факторами (на рисунке не показаны), которые в норме, вероятно, ограничивают повреждающие побочные эффекты, но при некоторых заболеваниях подавляют защитные свойства иммунной системы.
46
Вирусы. Не способны к длительному выживанию вне клеток хозяина, в которых они размножаются, покидают их, и в то же время многие из них разрушают клетку (подробно см. рис. 26).
ГКГС I — молекулы ГКГС класса I (А, В, С у человека, К, D, L у мыши; рис. 13) играют существенную роль в распознавании вирусных антигенов рецептором цитотоксических Т-лимфо-цитов. Молекулы CD8 также участвуют в этом процессе (рис. 14,17).
Тц — цитотоксический Т-лимфоцит (Т-киллер), в функцию которого, в частности, входит распознавание и уничтожение инфицированных вирусом клеток. Их рецепторы распознают собственные антигены ГКГС класса I плюс «не свой» вирусный антиген. Распознавание высокоспецифично, т.е. имеются разные Т-лимфоциты для различных вирусов, которые отбираются и клонально пролиферируют подобно В-клетке (на рисунке этот этап не показан).
АПК — антигенпредставляющие клетки. Представляют сочетание антигена вируса и молекулы ГКГС II Т-хелперу так же, как в антительном ответе, и секретируют ИЛ-1.
ИЛ-1 — интерлейкин-1 (м. м. 17 500). Белок, секретируемый АПК и макрофагами. Стимулирует Т-хелперы к продукции ИЛ-2 и пролиферации. ИЛ-1 ранее был известен как LAF — фактор, активирующий лимфоциты (интерлейкины; рис. 23).
Тх — Т-хелпер. Т-лимфоцит-хелпер для клеточного иммунитета во многом сходен и, возможно, подобен Т-хелперу для антительного ответа (см. Th1- и Th2-клетки; рис. 9). Вызывает пролиферацию и дифференцировку цитотоксических Т-клеток в зрелые киллерные клетки главным образом с помощью секре-тируемого им ИЛ-2.
ИЛ-2 — интерлейкин-2 (м. м. 15 500). Гликопротеин, секретируемый Т-хелпером и значительно варьирующий у разных биологических видов. Действует только на клетки, несущие соответствующий рецептор. На Т-лимфоцитах рецепторы к ИЛ-2 появляются в процессе созревания. ИЛ-2 ранее был известен как фактор роста Т-лимфоцитов — TCGF (рис. 23).
Цитолитическое действие. После полного созревания ци-тотоксические Т-клетки способны лизировать любую клетку, на поверхности которой распознают сочетание антигена вируса и молекулы ГКГС класса I. Цитолитическое действие осуществляется в два этапа: присоединение киллера к поверхности клетки-мишени с помощью антигенспецифического рецептора и последующий Ca2+-зависимый лизис её. Лизис происходит после отсоединения киллера, что позволяет одному киллеру лизировать несколько клеток-мишеней. В процессе лизиса участвуют секретируемые лимфоцитом перфорины, которые являются небольшими порообразующими молекулами, сходными с литичес-ким комплексом конечных компонентов комплемента. Интересно, что естественные клетки-киллеры (NK), несмотря на отличие их распознающих механизмов, используют для лизиса мишеней те же способы, что и Т-киллеры (рис. 26). Кроме того, под влиянием клеток-киллеров запускаются механизмы апоп-тоза в клетке-мишени, что ведёт к её гибели.
Бактерии. Некоторые бактерии, простейшие, грибы и многие вирусы, будучи фагоцитированными макрофагами (МФ), избега
ют обычного внутриклеточного киллинга (рис. 8) и выживают в фаголизосомах или в свободном состоянии в цитозоле. В отсутствие помощи от Т-лимфоцитов возможно развитие прогрессирующей, не поддающейся лечению инфекции. Помощь Т-хелпе-ров (ТЫ) заключается в секреции ИФ-гамма и некоторых других факторов, активирующих макрофаги.
Цитокины. Большое семейство молекул, продуцируемых лимфоидными и миелоидными клетками с различным действием на макрофаги. Они неспецифичны по отношению к антигену, и активность некоторых из них подавляется естественными ингибиторами, ограничивающими их нежелательные эффекты. Ниже представлены некоторые из наиболее известных цитокинов (подробнее см. рис. 23):
ИЛ-2 — см. выше.
МИФ — фактор, ингибирующий миграцию макрофагов, ограничивает их подвижность и концентрирует в окружении Т-лимфоцита.
МАФ — фактор, активирующий макрофаги, повышает многие их функции, включая внутриклеточный киллинг и секрецию различных цитотоксических факторов, способных поражать микроорганизмы вне клетки.
Интерферон (иммунный или у) — крайне важная противовирусная и регуляторная молекула, возможно, главный компонент МАФ.
Лимфотоксин, возможно, важен в киллинге некоторых опухолевых клеток (рис 30).
Фактор роста В-лимфоцитов (рис. 18).
КСФ — колониестимулирующий фактор. Стимулирует дифференциацию моноцитов и, возможно, секрецию ИЛ-1.
Гранулёма. Не подвергающиеся перевариванию материалы (например, туберкулёзная палочка, клеточные стенки стрептококка, тальк) могут быть изолированы плотными скоплениями макрофагов. Там же часто содержатся Т-лимфоциты, эозииофи-лы (ЭО) и гигантские клетки, образованные слиянием нескольких макрофагов. О роли гранулём при хронических воспалениях см. рис. 35.
Память. Все Т-лимфоциты, вовлечённые в клеточный иммунитет, способны формировать клетки памяти, обеспечивая тем самым возможность иммунного ответа по вторичному типу (более эффективный и ускоренный ответ). В иммунных реакциях, где эффекторные функции выполняют макрофаги, память создаётся исключительно Т-хелперами.
ГЗТ — гиперчувствительность замедленного типа. Впервые этот тип реагирования описал Р. Кох в 1891 г. При подкожном введении туберкулина больным туберкулёзом на следующий день или позже в месте инъекции наблюдались покраснение и отёк. При наличии у больных антител соответствующая реакция развивается через несколько часов. Соответственно появились термины «гиперчувствительность замедленного типа» и «гиперчувствительность немедленного типа». ГЗТ зависит от Т-клеток памяти и реализуется в месте инъекции антигена, сопровождаясь повышенной сосудистой проницаемостью (справа внизу). Таким образом, ГЗТ является моделью нормального клеточного иммунитета, а также удобным тестом на Т-клетки памяти.
47
21. ТОЛЕРАНТНОСТЬ
Эволюция распознающих механизмов, вызывающих уничтожение чужеродного материала, могла происходить только одновременно с совершенствованием механизмов, защищающих от повреждения «своих» тканей. Факторы естественной защиты, такие, как фагоцитоз, лизоцим, С-реактивный белок, активирован-ный по альтернативному пути комплемент и т.д., нормально ак-тиьны лишь против ограниченного спектра субстанций, включая микроорганизмы и «свои» уже повреждённые ткани. Механизмы адаптивного иммунитета, т.е. Т- и В-лимфоциты с их огромным напором рецепторов, явно нуждаются в ограничении активности тех рецепторов, которые способны распознавать «своё». Такая агрессивность не может быть обеспечена на генетическом уровне. так как «свои» молекулы и рецепторы, способные их распознать, наследуются совершенно отдельно. Например, у носителей группы крови А вырабатываются анти-В-антитела, и наоборот. Таким образом, АВ-ребёнок от А-отца и В-матери наследует способность продуцировать анти-А- и анти-В-антитела, но для нормальной жизнедеятельности не должен производить ни одно из них, т.е. быть толерантным к А- и В-антигенам эритроцитов.
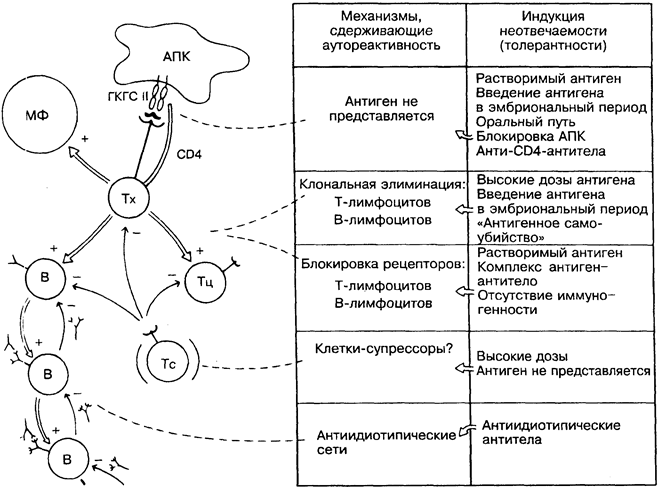
В иммунной системе аутореактивность (т.е. реактивность против «своего») сдерживается на нескольких уровнях. В ле
вой части рисунка представлены три основных типа адаптивного ответа (рис. 18 и 20), в центре — механизмы, сдерживающие аутореактивность. Кроме клональной элиминации аутореактив-ных клонов, всегда считавшейся основной причиной неотвечае-мости иммунной системы на «свои» ткани, обнаружено множество других регулирующих механизмов, нарушение любого из которых может привести к аутоиммунному ответу (рис. 36).
В определённых условиях (справа на рисунке) сдерживающие механизмы могут быть запущены нормальным антигенным «не своим» материалом. Иммунная система воспринимает эти вещества как «свои» и не отвечает на них — состояние, названное толерантностью. Это может оказаться полезным при пересадке органов, но может привести к очень тяжёлым последствиям при некоторых инфекциях. Толерантность подразумевает специфичность по отношению к тому антигену, который её вызвал, и в корне отличается от неспецифической неотвечаемо-сти, вызванной поражением иммунной системы в целом (рис. 38). В литературе толерантность часто ставят в прямую зависимость от клональной элиминации. К сожалению, в большинстве случаев клональная элиминация слишком труднодоказуема, чтобы говорить об этом с уверенностью.
48
Дата: 2018-12-28, просмотров: 470.