38. Иммуносупрессия ........................................................82
39. Иммунодефицита ........................................................84
40. ВИЧ и СПИД ..............................................................86
41. Иммуностимуляция и вакцинация ..............................88
Приложение
42. Сравнительные величины............................................ 90
Сравнительная молекулярная масса ..........................90
43. Вехи истории иммунологии .........................................91
Нерешённые вопросы.................................................. 91
44. Классификация СО...................................................... 92
Указатель...........................................................93
1. ОПРЕДЕЛЕНИЕ ИММУНОЛОГИИ
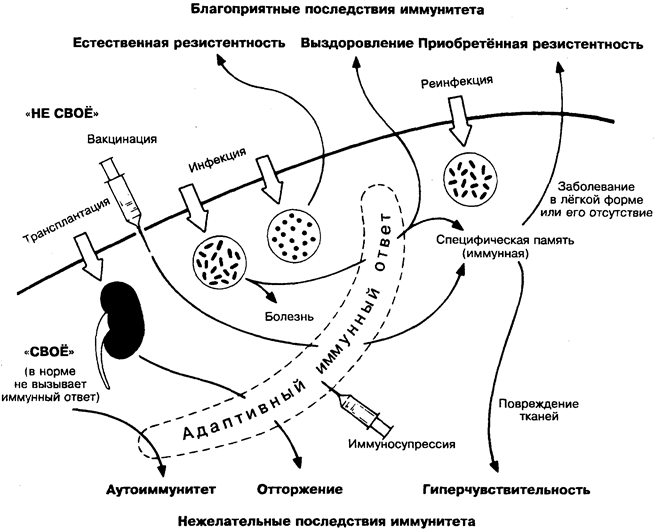
Среди основных причин смерти — травмы, инфекции, рак и дегенеративные болезни. Из них только инфекции и травмы регулярно вызывают гибель особей до достижения репродуктивного возраста, ослабляя тем самым генофонд вида. Поэтому защищающие от их последствий механизмы — иммунитет и заживление — особенно важны для выживания.
Иммунитет выполняет функцию распознавания и устранения чужеродного («не своего») материала, который поступает в организм обычно в виде опасных для жизни патогенных микроорганизмов, но в то же время в форме жизненно необходимого трансплантата, например почки. Устойчивость к инфекции может быть естественной (т.е. врождённой и неизменяющейся) или приобретённой в результате адаптивного иммунного ответа. Иммунология — наука об органах, клетках и
молекулах, составляющих иммунную систему, ответственную за обнаружение и удаление чужеродных веществ. Иммунология изучает структуру и функцию иммунной системы, её реакцию на возбудителей заболеваний, последствия иммунного ответа и способы влияния на них.
Наиболее опасный чужеродный материал, который необходимо распознать и удалить, — это микроорганизмы, вызывающие инфекционные заболевания. Строго говоря, иммунное реагирование начинается после их проникновения в организм, но попасть в него и спровоцировать иммунный ответ микроорганизмы могут, лишь преодолев ряд защитных механизмов, которые можно рассматривать как первую линию обороны иммунной системы.
8
Чужеродность («не своё») — распространённый в иммунологии Теркин, означающий генетическое различие между веществами. Чаще всего чужеродными для организма материалами являются патогенные микроорганизмы и ткани других особей, хотя медицинские препараты и даже пища тоже чужеродны и способны вызывать иммунный ответ.
Инфекция. Вероятно, необходимость в иммунном ответе возникла в связи с обилием бактерий, вирусов, простейших, червей и грибов, проникающих в организм. Животные с нарушениями иммунной системы часто гибнут от инфекций, безопасных для здоровых особей.
Внешняя защита. Неповреждённые слизистые оболочки и кожный покров сами по себе представляют серьёзное препятствие для болезнетворных микроорганизмов и, кроме того, вырабатывают множество антимикробных (в основном бактерицидных) секретов. Более специализированная защита включает высокую кислотность (рН около 2,0) в желудке, слизь и подвижные реснички бронхиального дерева. Благодаря факторам внешней защиты большая часть микробов так и не попадает в организм.
Естественная резистентность. Чужеродные организмы, проникшие в тело, быстро (минуты, часы) уничтожаются механизмами естественной (врождённой) защиты. В противном случае начинается адаптивный иммунный ответ.
Адаптивный иммунный ответ — выработка или активация защитных механизмов против определённого (специфического) возбудителя, например болезнетворного микроорганизма. В результате происходит уничтожение возбудителя и прекращение болезни, а организм приобретает способность усиленно реагировать на повторную встречу с этим возбудителем — явление, называемое иммунной памятью. К сожалению, иммунная система распознаёт не патогенность микроба или вещества, а его чужеродность и поэтому способна реагировать на безвредные, но «чужие» вещества, например на пыльцу.
Вакцинация — метод, позволяющий стимулировать иммунный ответ и создавать иммунитет к возбудителю в отсутствие заболевания. Название произошло от препарата vaccina (коровья оспа — variola vaccina), который Дженнер использовал для защиты от натуральной оспы.
Трансплантация. Клетки или органы, пересаженные другой особи, обычно выдерживают действие факторов естественной защиты, но отторгаются в результате адаптивного иммунного ответа.
Аутоиммунитет. В норме ряд механизмов постоянно поддерживает иммунную систему в состоянии толерантности к тканям своего организма и иммунного ответа на них не происходит. Аутоиммунитетом, или аутоиммунным заболеванием, называется состояние, при котором иммунная система начинает воспринимать «свои» ткани как чужеродные и атакует их.
Гиперчувствительность. Благодаря иммунной памяти при повторной встрече с тем же стимулом иммунная система реагирует по вторичному (усиленному) типу, и в этих случаях возможно повреждение даже «своих» тканей. Это явление получило название «гиперчувствительность». Например, аллергия (поллинозы) и некоторые болезни почек — все это проявления гиперчувствительности. Некоторые иммунологи, однако, применяют термин «аллергия» вообще по отношению ко всем изменениям ответных реакций, включая и приобретённую резистентность.
Иммуносупрессия. Нежелательные последствия иммунного ответа, такие как аутоиммунитет, гиперчувствительность и отторжение трансплантата, часто приходится подавлять медика-ментозно или другими способами.
9
2. ЕСТЕСТВЕННЫЕ И АДАПТИВНЫЕ ИММУННЫЕ МЕХАНИЗМЫ
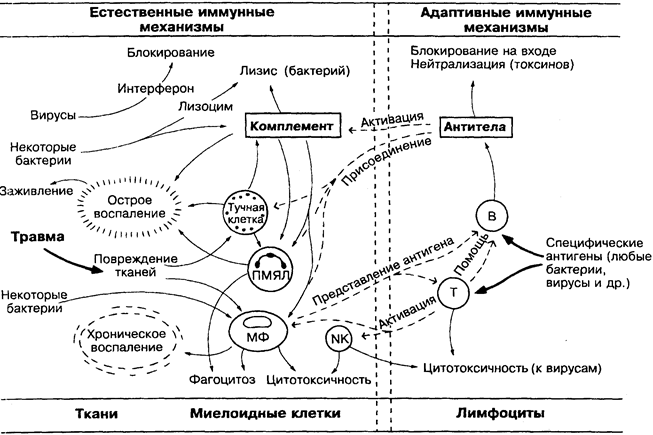
Так как резистентность к заболеванию может быть естественной (врождённой) или приобретённой, то определяющие её механизмы подразделяются на естественные (слева на рисунке) и адаптивные (справа), каждый из которых имеет как клеточные (нижняя часть рисунка), так и гуморальные (сыворотка или другая биологическая жидкость; верхняя часть рисунка) элементы. Адаптивный механизм, появившийся эволюционно позднее, выполняет многие свои функции, взаимодействуя с более старыми факторами естественной защиты.
Основа естественного иммунитета — это действие неспецифических механизмов, в большинстве своём реагирующих на повреждение тканей воспалительными реакциями (левая часть рисунка). Некоторые клетки (макрофаги — МФ) и гуморальные факторы (комплемент, лизоцим) всё-таки обладают ограниченной способностью узнавать и уничтожать бактерии. Многие клетки секретируют интерферон, который действует против вирусов, но не оказывает воздействия на другие микроорганизмы.
Таким образом, термин «неспецифический», часто применяемый как синоним термина «естественный», не вполне точен.
Адаптивный иммунитет основан на свойствах Т- и В-лимфоцитов избирательно отвечать на тысячи чужеродных веществ (антигенов) с образованием специфической памяти и реагирования, индивидуального для каждого конкретного антигена (адап-тирование к окружающей среде). Против некоторых антигенов адаптивные механизмы способны действовать автономно. В большинстве случаев происходит взаимодействие с элементами естественного иммунитета: антител — с комплементом и фагоцитарными клетками, Т-лимфоцитов — с макрофагами. Адаптивный иммунный ответ, активирующий факторы естественной защиты, часто проявляется острым или хроническим воспалением, которое может развиться до состояния гиперчувствительности.
Составляющие этого сложного механизма будут подробно рассмотрены в следующих разделах.
10
ЕСТЕСТВЕННЫЙ ИММУНИТЕТ
Интерфероны (ИФ) — семейство белков, вырабатываемых клетками в ответ на вирусную инфекцию и другие стимулы. Блокируют репликацию вируса в других клетках и участвуют во взаимодействии между клетками иммунной системы (см. рисунок в разделе 23*).
Лизоцим (мурамидаза) — выделяемый макрофагами фермент, атакующий клеточные мембраны бактерий. Лизоцим и интер-ферон часто называют природными антибиотиками.
Комплемент — группа сывороточных белков, которые при активации вызывают широко распространённые воспалительные эффекты, а также лизис бактерий и др. Комплемент может быть активирован непосредственно бактериями, но обычно для этого необходимо присутствие антител (рис. 5).
Лизис — распад клетки, необратимое истечение её содержимого через повреждённую мембрану.
Тучные клетки — большие тканевые клетки. При повреждении или под действием антител выделяют медиаторы воспалительных процессов, которые повышают проницаемость сосудов, позволяя комплементу и клеткам поступать из кровотока в ткани (рис. 6).
Полиморфно-ядерные лейкоциты (ПМЯЛ) Короткожи-вущие клетки-«мусорщики» крови, содержащие мощные бактерицидные ферменты.
Макрофаги (МФ). Большие тканевые клетки, удаляющие из организма повреждённые ткани, клетки, бактерии и другие материалы. Макрофаги и полиморфно-ядерные лейкоциты называют также миелоидными клетками, подчеркивая их общее происхождение в костном мозге.
Фагоцитоз — поглощение частиц клеткой. Наиболее важные фагоцитарные клетки, уничтожающие большую часть попавшего в организм чужеродного материала, — макрофаги и полиморфно-ядерные лейкоциты (микрофаги).
Цитотоксичность. Макрофаги способны убивать некоторые клетки (возможно, и опухолевые), не фагоцитируя их, но подобная цитотоксическая активность лучше развита у других клеток (лимфоцитов).
Естественные киллеры (NK) — лимфоцитоподобные клетки, способные уничтожать некоторые мишени (в основном инфицированные клетки), но без рецепторов и узкой специализации, характерных для истинных лимфоцитов.
АДАПТИВНЫЙ ИММУНИТЕТ
Антиген — вещество, стимулирующее любую форму адаптивного иммунного ответа. Обычно в роли антигенов выступают чужеродные частицы (клетки, бактерии и др.) или крупные молекулы (белки, полисахариды) чужого организма, но в ряде случаев мелкие молекулы (гаптены) и даже «свои» компоненты могут быть антигенными. Основное, но далеко не единственное условие антигенности — наличие поверхностных структур, генетически отличных от тканей организма-хозяина (рис. 17-20).
Специфичность, специфичный — термины, обозначающие избирательность иммунного ответа к вызвавшему его возбудителю, т.е. выработку антител и лимфоцитов, специфических к этому возбудителю. Так, антитела к вирусу кори не будут связываться ни с каким другим вирусом.
Лимфоцит — мелкая клетка крови, из которой она рецирку-лирует через ткани и обратно (через лимфу) в поисках чужеродных веществ. Её способность распознавать индивидуальные антигены с помощью специализированных поверхностных рецепторов и продуцировать большие клоны подобных клеток с идеальной специфичностью и длительным жизненным сроком отвечает задачам адаптивного иммунитета. Различают Т- и В-лимфоциты (рис. 9).
В-лимфоциты (В-клетки, от лат. bursa). Участвуют в выработке антител — гуморальных факторов адаптивного иммунитета.
Т-лимфоциты (Т-клетки, от лат. thimus). Делятся на несколько субпопуляций, которые взаимодействуют с В-лимфоцитами, убивают заражённые вирусом клетки, активируют макрофаги и выполняют многие другие функции.
Антитела — сывороточные глобулины с широким спектром специфичности к различным антигенам. Обладают свойством специфически связываться с антигеном, активировать комплемент, усиливать фагоцитарную активность макрофагов и нейт-рализовывать бактериальные токсины.
Представление. В большинстве случаев для реализации иммунного ответа макрофаг должен в особой форме представить антиген Т- и В-лимфоцитам — один из частых случаев кооперации адаптивного и естественного защитных механизмов.
Помощь. Для синтеза большинства антител необходимо взаимодействие В-лимфоцита и Т-хелпера (помощника). Существуют также Т-лимфоциты, которые подавляют выработку антител.
*Далее до всей книге указан номер рисунка, относящегося к разделу, в котором он помещен.
11
3. ЭВОЛЮЦИЯ ИММУННЫХ МЕХАНИЗМОВ
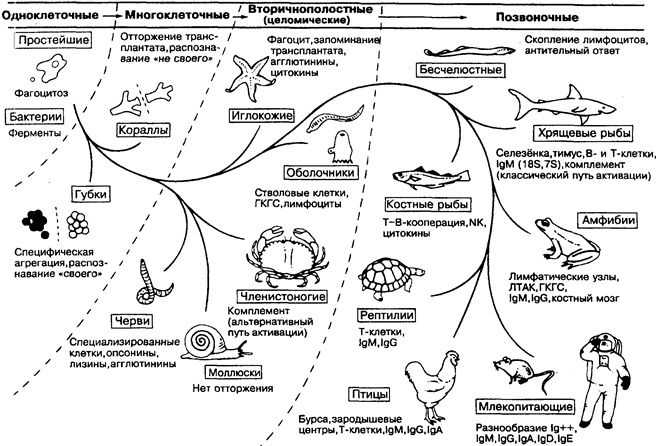
От способности амёбы распознавать свою пищу (на рисунке вверху слева) до сложнейшего гуморального и клеточного иммунитета млекопитающих (внизу справа) механизмы распознавания «своего» и «чужого» неуклонно совершенствовались, следуя всё возрастающей потребности организма поддерживать генетическое постоянство своего состава. Поэтому следует говорить не о возникновении иммунитета, а о его становлении, развитии.
На рисунке показаны основные этапы, когда предположительно произошли и сохранились наиболее важные изменения защитных механизмов. Сведения о примитивных животных по большей части основаны на изучении их весьма отдалённых потомков, имевших иммунную систему, адаптированную к новой среде обитания.
На рисунке видно, что в начале эволюции речь могла идти только о клеточном распознавании «своего» и «чужого», а значит, Т-зависимая система должна быть значительно старше гуморальной, впервые появившейся у позвоночных. У современных млекопитающих сосуществуют 3 отдельные системы распознавания на молекулярном уровне. Это поверхностные молекулы В-клеток (антитела), рецепторы Т-лимфоцитов и мо
лекулы главного комплекса гистосовместимости (ГКГС), причём кодирующие их гены, по-видимому, произошли от общего примитивного предшественника (рис. 12). Возможно, фагоцитарные клетки содержат иной набор рецепторов (рис. 8), но подтверждения этому пока не найдено ни на генетическом, ни на молекулярном уровне.
Возникновение адаптивного иммунитета стало возможным только с появлением лимфоцитов, обладающих специфичностью и способностью создавать и хранить иммунную память о возбудителе заболевания. Впервые лимфоциты обнаруживаются у ранних позвоночных, с которыми и принято связывать зарождение адаптивного иммунитета. Очевидно, одновременное резкое изменение размеров, продолжительности жизни, температуры тела и среды обитания потребовало новых, более действенных иммунных механизмов, но прямой причинной связи между позвоночником и лимфоцитами до сих пор не найдено. Возможно, её прояснят более совершенные методы изучения ДНК древних животных и окаменелостей. Кроме того, еще только начинается систематическое исследование иммунных механизмов растений.
12
БЕСПОЗВОНОЧНЫЕ
Простейшие. Лишённые хлорофилла, эти примитивные животные должны питаться. Мало известно о том, как они распознают пищу, но поверхностные белки их находятся под очень сложным генетическим контролем.
Бактерии — паразиты, хотя не самые мелкие, так как в свою очередь могут быть инфицированы особыми вирусами — бактериофагами. Предполагается, что ставшие уже незаменимыми в генной инженерии рестриктазы в природе служат для распознавания и уничтожения ДНК вируса без вреда для ге-нома самой бактерии. В свою очередь многие вирусы выработали против этого свои защитные механизмы, что хорошо иллюстрирует возможности и ограничения естественного иммунитета.
Губки способны жить как отдельно, так и в колониях, используя видоспецифические гликопротеины, чтобы распознавать «своё» и предотвращать образование гибридных колоний. Созданные искусственно, такие колонии подвергаются некрозу в коятактной зоне и усиленно разрушаются при попытке воссоздания.
Кораллы принимают генетически идентичные (сингенные) трансплантаты, но слабо отторгают чужеродные (аллогенные) с обоюдным разрушением. Есть свидетельства, что при этом создаётся специфическая память о предварительном отторжении, т.е. адаптивный иммунитет.
Черви. У вторичнополостных червей уже наблюдается специализация клеток. В целомической полости земляного червя обнаружено по меньшей мере 4 типа фагоцитарных клеток с различными функциями: одни осуществляют отторжение аллот-рансплантата, другие выделяют бактерицидные факторы.
Членистоногие и моллюски любопытны тем, что не отторгают трансплантат. Впрочем, это связано не с отсутствием распознающих механизмов, а скорее с малой гетерогенностью их ГКГС (рис. 13). Явно преобладают гуморальные факторы, среди которых возможны и компоненты комплемента (альтернативный путь активации), защищающие от некоторых паразитов.
Иглокожие. Ещё в 1882 г. И.И. Мечников использовал морскую звезду для демонстрации специализированных фагоцитарных клеток. Иглокожие отторгают трансплантат (клеточный инфильтрат), имеют развитую иммунную память и молекулы, сходные с цитокинами (интерлейкин-1 — ИЛ-1, фактор некроза опухоли).
Оболочники (например, асцидия). Эти предшественники позвоночных обладают такими прогрессивными особенностями, как самоподдерживающаяся гемопоэтическая клетка и единая главная система гистосовместимости, контролирующая отторжение чужеродных трансплантатов. Имеют клетки, сходные с лимфоцитами.
ПОЗВОНОЧНЫЕ
Бесчелюстные (круглоротые, например миноги). Переломный момент в истории иммунитета. Первые выжившие позвоночные, у которых лимфоциты организованы в центры в области глотки и в других местах, и впервые определяются антительные иммуноглобулины — лабильные молекулы из 4 цепей, специфически вырабатываемые в ответ на различные антигены. Некоторые другие молекулы (например, адгезивные) суперсемейства иммуноглобулинов присутствуют у беспозвоночных, как и у членистоногих.
Хрящевые рыбы (например, акулы). Впервые появляются тимус, плазматические клетки (антителопродуценты) и гуморальный ответ по вторичному типу. В молекулах иммуноглобулинов появляются дисульфидные связи, а также лёгкие и тяжёлые цепи, означающие пока скорее полимеризацию, чем различия по классам. Присутствуют также молекулы комплемента (классический путь активации).
Костные рыбы. Различия в ответе на митогены и клеточная кооперация в продукции антител знаменуют начало разделения функций между Т- и В-лимфоцитами. Обнаруживаются МК-клетки, цитокины (например, интерлейкин-2, интерферон), наблюдается реакция лимфоцитов в смешанной культуре. Ещё отсутствует ГКГС, характерный для млекопитающих.
Амфибии. Впервые появляются другой класс иммуноглобулинов (IgG; рис. 16) и явно выраженные антигены ГКГС. В процессе морфогенеза (например, головастик—лягушка) возможно развитие специфической толерантности к антигенам взрослой особи. Впервые на данной стадии появляются лимфатические узлы, гемопоэз в костном мозге, лимфоидная ткань, ассоциированная с кишечником (ЛТАК).
Рептилии. Ранее считалось, что клетки тимуса у рептилий несут молекулы, сходные с сывороточными иммуноглобулинами. Более вероятно, что эти молекулы — предшественники Т-клеточных рецепторов, и антисыворотка, использованная для их выявления, перекрёстно реагировала с иммуноглобулинами. Это одна из проблем иммунологии.
Птицы замечательны тем, что имеют специальный орган для выработки В-лимфоцитов —фабрициеву сумку (или бурсу), представляющую собой мешковидный выступ заднего отдела клоаки. У птиц имеется большой многодольчатый тимус, но отсутствуют типичные лимфатические узлы. Система комплемента отличается от таковой у млекопитающих, например фактор В замещает компоненты С2 и С4 (рис. 5).
Млекопитающие характеризуются большим разнообразием классов и подклассов иммуноглобулинов и антигенов ГКГС, чем дальнейшим развитием эффекторных функций. Различия между млекопитающими достойны изумления. Например, у крыс чрезвычайно развит естественный иммунитет, а у китов и сирийских хомячков необычно низкий полиморфизм ГКГС. То, что среди такого разнообразия есть мыши, иммунологически сходные с человеком, можно считать счастливой для него случайностью.
13
4. КЛЕТКИ, УЧАСТВУЮЩИЕ В ИММУНИТЕТЕ. ГЕМОПОЭТИЧЕСКАЯ СИСТЕМА
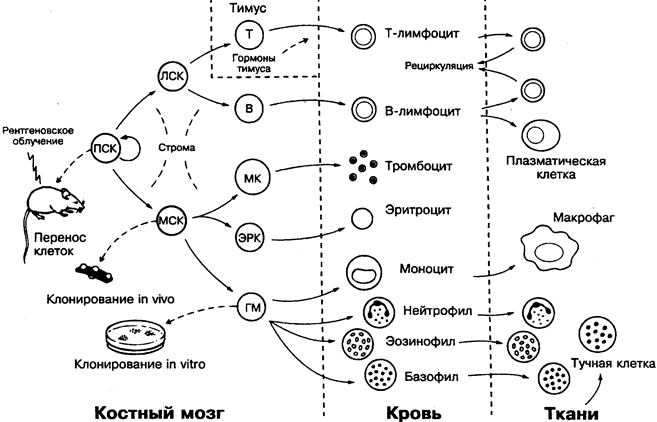
Образование большинства клеток, вовлекаемых в иммунитет млекопитающих, происходит из предшественников в костном мозге (левая половина рисунка). Они циркулируют в крови, при необходимости проникая и на некоторое время задерживаясь в тканях.
Существование полипотентной стволовой клетки у взрослых особей, сохраняющей эмбриональную способность к дифференцировке во все типы клеток крови, установлено в опытах по переносу клеток костного мозга и хромосомному анализу у облучённых мышей (слева в центре).
В постнатальном периоде стволовые клетки обнаруживаются только в костном мозге и периферической крови и встречаются очень редко (примерно 1 на 100000 ядерных клеток). У эмбрионов полипотентные клетки присутствуют в печени. В ответ на введение облучённой мыши большого количества костномозговых клеток в селезёнке развиваются дискретные клеточные колонии, или клоны, in vivo. Их морфология и дифференцировка могут быть изучены в более или менее естественных условиях.
Эксперименты с культивированием клеток костного мозга в полужидких средах in vitro дают возможность изучить в изолированных условиях образование клонов из отдельных родоначальных клеток (внизу слева).
Основываясь на этих методах, гематологи ввели такие понятия, как «колониеобразующая единица» (КОЕ), «бурстообразующая единица» (БОЕ). Пролиферация и дифференцировка всех этих клеток регулируются факторами роста, выделяемыми самими клетками или стромой костного мозга (рис. 23).
В отличие от других гемопоэтических клеток, лимфоциты начинают активно делиться только после стимуляции, и для формирования лимфоцитарных клонов необходимо повторное воздействие антигена и факторов роста, что ведёт к селекции специфически реагирующих клеток. Поэтому для изучения многочисленных свойств лимфоцитов используют гибридомы — бессмертные клетки, получаемые слиянием Т- или В-лимфоцита с опухолевой клеткой (рис. 9).
14
О ТЕРМИНОЛОГИИ
Процесс дифференцировки стволовой клетки разделён гематологами на множество этапов (например, для эритроцитов: про-эритробласт, эритробласт, нормобласт, эритроцит). Суффикс "бласт" обычно означает начальную стадию деления, относительно недифференцированную клетку, но может применяться для описания лимфоцита, который был простимулирован, например, антигеном и начал делиться (термин «бластотрансформация»).
Строма — эндотелий и другие клетки, непосредственно не участвующие в гемопоэзе, но составляющие основу ткани и секретирующие многие факторы роста для гемопоэтических клеток.
Полипотентная стволовая клетка (ПСК) — самоподдерживающаяся стволовая клетка костного мозга, существование которой доказано, но морфология которой недостаточно изучена.
Лимфоидная стволовая клетка (ЛСК) обладает способностью дифференцироваться в Т- и В-лимфоциты.
Миелоидная стволовая клетка (МСК) — предшественник селезёночных колоний и всех клеток нелимфоидной линии: гранулоцитов, эритроцитов, моноцитов и мегакариоцитов; её часто называют КОЕ-ГЭММ (колониеобразующая единица гранулоцитов-эритроцитов-моноцитов-мегакариоцитов).
Эритроидная родоначальная клетка (ЭРК) — предшественник эритроцитов. В гематологии различают БОЕ и КОЕ на основании образцов их роста in vitro. ЭРК могут быть стимулированы к дифференцировке как местными факторами роста, так и эритропоэтином — гликопротеиновым гормоном, который вырабатывается в почках при гипоксии. Это классический пример отрицательной обратной связи в организме: потребность в кислороде компенсируется возросшим количеством кисло-роднесущих эритроцитов.
Дата: 2018-12-28, просмотров: 469.