Зрачковые нарушения используют в качестве индикатора повреждений ствола мозга, приводящих к возникновению коматозных состояний, так как области ствола мозга, поражение которых приводит к нарушению сознания, находятся в анатомической близости от зон, участвующих в иннервации зрачков. Кроме того, зрачковые пути относительно устойчивы к нарушениям метаболизма, поэтому отсутствие зрачковой реакции на свет - важный признак, позволяющий отличить коматозное состояние, обусловленное структурными повреждениями, от метаболического (Plam F., Posner J., 1986).
ЗРАЧКОВЫЕ НАРУШЕНИЯ
Следующие зрачковые нарушения позволяют определить локализацию очага поражения (рис. 2-1):
• умеренный миоз с сохраненной реакцией на свет как элемент синдрома Горнера - поражение задневентральных отделов гипоталамуса (начальные проявления транстенториальной дислокации) или латеральных отделов продолговатого мозга и спинного мозга на шейном уровне;
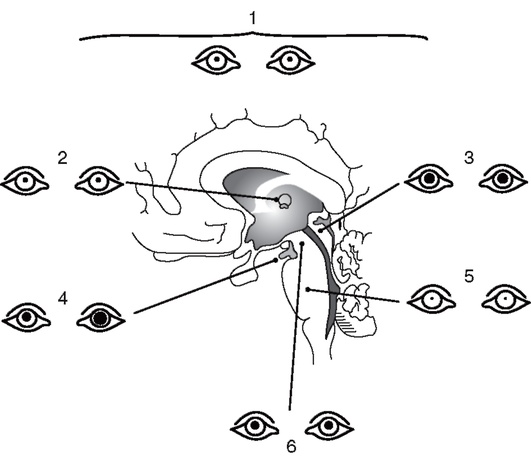
Рис. 2-1. Состояние зрачков у больных в коматозном состоянии при различной локализации поражения структур мозга (по Plam F., Posner J., 1986): 1 - нарушения метаболизма (узкие зрачки, реагирующие на свет); 2 - диэнцефальное поражение (узкие зрачки, реагирующие на свет); 3 - тектальное поражение (широкие фиксированные зрачки, гиппус); 4 - височно-тенториальная дислокация (поражение III нерва, широкий фиксированный зрачок на стороне поражения); 5 - поражение моста (точечные зрачки); 6 - поражение среднего мозга (фиксированные умеренно расширенные зрачки)
• умеренный мидриаз, отсутствует реакция на свет - поражение покрышки моста и области ядер среднего мозга;
• резкое двустороннее сужение зрачков - поражение покрышки моста, обычно при кровоизлиянии;
• односторонний фиксированный мидриаз - поражение III нерва, прижатие его крючком гиппокампа к краю намета мозжечка при височно-тенториальной дислокации.
ГЛАЗОДВИГАТЕЛЬНЫЕ НАРУШЕНИЯ
При исследовании движений глаз у способных к контакту больных сопоставляют произвольные и рефлекторные движения глаз и век. У больных в коматозном состоянии исследуют только рефлекторные движения глаз и век.
Оценка положения век
В состоянии комы и во сне глаза закрыты в результате тонического напряжения круговых мышц глаз (лицевой нерв, ретикулярная формация ствола мозга). Тонус мышц век оценивают, приподнимая и освобождая их. У больных в коме после освобождения поднятые веки постепенно закрываются. Неполное смыкание свидетельствует о нарушении функции лицевого нерва на этой стороне. Выраженное сопротивление открыванию глаз или быстрое смыкание век может наблюдаться при психической ареактивности (истерия) и блефароспазме «органического» генеза. Иногда при коматозном состоянии отмечается широкое, тоничное открытие глаз при отсутствии мигательных движений. Очаг поражения при таком состоянии локализуется в мосту мозга.
Мигательный рефлекс
Наличие спонтанных мигательных движений свидетельствует о сохранности ретикулярной формации моста мозга, а наличие мигательных движений в ответ на свет и звук - о сохранности соответствующих афферентных путей. Отсутствие мигательных движений на одной из сторон отмечается при нарушении функций лицевого нерва, на двух сторонах - при структурном или метаболическом нарушении функций ретикулярной формации.
Птоз (опущение) верхнего века
Птоз верхнего века наблюдается при нарушении функции m. levator palpebrae, которая иннервируется глазодвигательным нервом (ядро в среднем мозге). Поражение глазодвигательного нерва в орбите и на основании черепа, его волокон и ядра в стволе проявляется односторонним птозом с расширением зрачка и нарушением его реакции на свет на той же стороне. Двусторонний птоз наблюдается при поражении оральных отделов среднего мозга. При нарушении симпатической иннервации глаза также возникает птоз, входящий в этом случае в состав синдрома Горнера (птоз, миоз, энофтальм). При этом птоз, как правило, бывает неполным (сужение глазной щели) и сопровождается сужением зрачка с живой реакцией на свет. При церебральной патологии птоз наблюдается в основном при поражении нижних отделов моста и продолговатого мозга.
Нарушения взора (содружественных движений глаз)
Корковый центр взора находится в лобной доле и обеспечивает содружественный поворот глазных яблок в противоположную сторону. Повреждение коркового центра или его связей с медиальным продольным пучком приводит к парезу взора в сторону. Так, при повреждении левой лобной доли развивается парез взора вправо: глазные яблоки отклоняются влево, невозможен взор в сторону гемипареза конечностей. При раздражении коркового центра взора (эпилептический припадок, первые часы кровоизлияния) взор обращен в противоположную сторону. Например, при раздражении левой лобной доли глазные яблоки отклонены вправо.
Существует также центр горизонтального взора в мосту мозга в области ядра отводящего нерва. При поражении мостового центра, в отличие от коркового, возникает паралич взора в сторону очага, глаза обращены в сторону парализованных конечностей. Также при этом нарушается окулоцефалический рефлекс.
Окулоцефалический рефлекс (феномен головы и глаз куклы)
Рефлекс вызывают, быстро поворачивая и кратковременно удерживая голову больного то вправо, то влево, а также разгибая и сгибая шею (рис. 2-2). При этом глаза отклоняются в противоположном направлении (например, при повороте головы влево глаза отклоняются вправо). Исследовать этот рефлекс можно только при отсутствии травмы шейного отдела позвоночника. У пострадавших с тяжелой ЧМТ голову можно поворачивать только в горизонтальной плоскости. Нормальный окулоцефалический рефлекс отражает сохранность лабиринтов, проприорецепторов шеи, вестибулярных ядер и их связей с ядрами глазодвигательных нервов, медиальным продольным пучком. Если при поворотах головы глазные яблоки остаются в прежнем положении, то повреждение локализуется на уровне ядер отводящих нервов, вестибулярных ядер и их связей. Если при поворотах головы сохранено отведение глаза, но нарушено приведение, то очаг поражения расположен на уровне медиального продольного пучка, осуществляющего связи между ядрами отводящего и глазодвигательного нервов. Асимметричное несодружественное отклонение глаз и несодружественные движения глаз при оценке окулоцефалического рефлекса свидетельствуют о структурном повреждении ствола мозга.
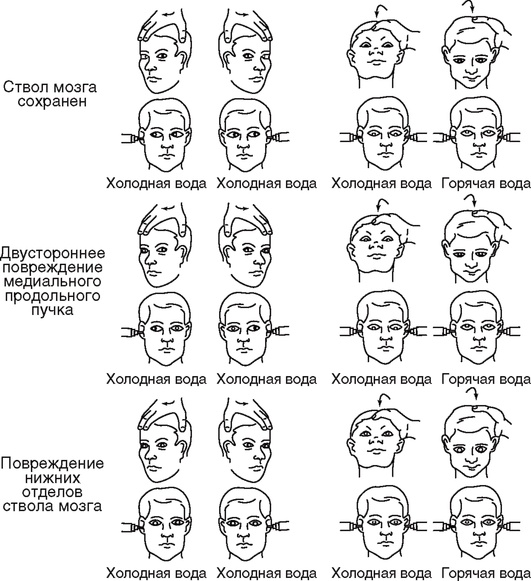
Рис. 2-2. Глазодвигательные рефлексы у больных в бессознательном состоянии. Движения глазных яблок во время оценки окулоцефалического (верхний ряд каждого рисунка) и окуловестибулярного (нижний ряд каждого рисунка) рефлексов при различных повреждениях головного мозга (по Plam F., Posner J., 1986)
Окуловестибулярный рефлекс (холодовая проба)
Пробу проводят в тех случаях, когда при оценке окулоцефалического рефлекса не удалось выявить каких-либо движений глазных яблок, а также в случае предположительной травмы черепа или шейного отдела позвоночника. Перед проведением пробы необходимо произвести отоскопию и убедиться в целости барабанных перепонок. При сохранном стволе мозга от варолиева моста до среднего мозга введение ледяной воды в слуховой проход вызывает отклонение глазных яблок в сторону раздражаемого слухового прохода. Вертикальные отклонения глазных яблок можно оценить с помощью одновременной стимуляции обеих барабанных перепонок. Так же как и рефлекс «глаз куклы», положительный окуловестибулярный рефлекс наблюдается при коматозном состоянии, развившемся вследствие двустороннего поражения полушарий головного мозга или угнетения их функций метаболического генеза. Отсутствие окуловестибулярного рефлекса указывает на поражение среднего мозга или моста.
Парез взора вверх
Парез взора вверх возникает при поражении на медиодиэнцефальном уровне (претектальная зона, область задней комиссуры) или при двустороннем поражении медиального продольного пучка. У больных в состоянии сопора и комы оценить вертикальный взор можно, раздражая роговицу глаза (при этом должно происходить отклонение глаз вверх), а также исследуя окулоцефалический рефлекс. Содружественное отклонение глаз вниз может отмечаться при аксиальной дислокации головного мозга вследствие сдавления среднего мозга.
Разностояние глазных яблок по вертикали
Разностояние глазных яблок по вертикали (симптом Гертвига-Мажанди) наблюдается при поражении дорсолатеральных отделов моста и медиального продольного пучка. Симптом возникает при дислокации ствола мозга и возникновении патологических процессов в задней черепной ямке.
Поплавковые движения глаз
Поплавковые движения глаз - периоды быстрых содружественных движений глаз вниз с последующим возвращением в исходное положение отмечаются при повреждениях каудальных отделов моста.
Плавающие движения глазных яблок
Плавающие движения глазных яблок у больных в коматозном состоянии напоминают таковые при сне у здорового человека и свидетельствуют о сохранности стволовых структур. Такие движения глазных яблок наблюдаются при двустороннем полушарном или диффузном повреждении мозга.
Корнеальный рефлекс
Корнеальный рефлекс - смыкание век при легком прикосновении к роговице глаза. Дуга рефлекса включает первую ветвь тройничного нерва, основное чувствительное ядро тройничного нерва, ядро и волокна лицевого нерва (уровень средней и нижней части моста мозга). Смыкание век обычно сопровождается отклонением глазных яблок вверх (феномен Белла), которое обеспечивается связями с ядрами глазодвигательного нерва (покрышка среднего мозга). Корнеальный рефлекс снижается или исчезает при поражении ствола мозга в области задней и средней черепных ямок. Постепенное угасание рефлекса может свидетельствовать о нарастании аксиальной дислокации.
НАРУШЕНИЯ ДВИГАТЕЛЬНОЙ СФЕРЫ
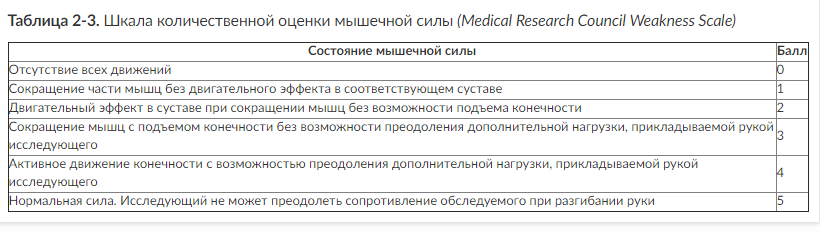
У больных с ОЦН, находящихся в коматозном состоянии, исследование двигательных функций проводят для топической диагностики и определения динамики течения заболевания. Оценивают двигательные реакции, возникающие при нанесении болевых раздражений на различные части тела (грудина, супраорбитальные точки, ногтевое ложе) с обеих сторон. Нормальная реакция проявляется отталкиванием раздражителя, отдергиванием конечностей, отстранением тела и может сопровождаться гримасой на лице и стоном. Оценивают симметричность движений и мышечную силу. Для оценки мышечной силы следует использовать шкалу количественной оценки мышечной силы (табл. 2-3).
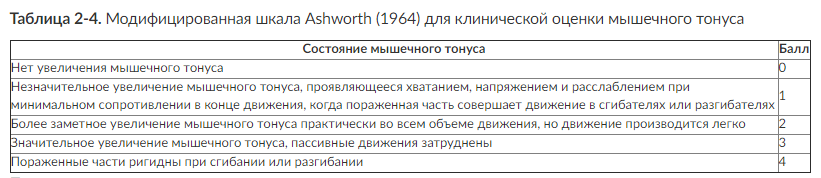
Особое внимание следует обращать на симметричность мышечного тонуса. Пассивными движениями во всех конечностях последовательно проверяют наличие сгибательного (декортикационный) и разгибательного (децеребрационный) гипертонуса. Гипертонус указывает на топический уровень первичного повреждения и стадию дислокационного процесса. Количественно мышечный тонус можно измерить в баллах модифицированной шкалы Ashworth, 1964 (табл. 2-4).
Патологическими считают следующие двигательные реакции.
• Сгибание рук и разгибание ног (декортикационная ригидность). При нанесении раздражения развивается медленное сгибание рук, запястий и пальцев с приведением рук в сочетании с разгибанием, поворотом внутрь и подошвенным сгибанием ног. Фрагментарные проявления этой реакции имеют такое же локально-диагностическое значение, как и полные, и отражают меньший размер и меньшую степень воздействия патологического очага. Патологические сгибательные реакции рук с разгибанием или без разгибания ног наблюдаются при преобладании поражения полушарий мозга и редко сочетаются с глазодвигательными нарушениями.
• Разгибание рук и ног (децеребрационная ригидность). Руки разогнуты, приведены и пронированы; ноги разогнуты, приведены, подошвенное сгибание стоп. Такая двигательная реакция характерна для вовлечения в патологический процесс среднего мозга и оральных отделов моста при массивном двустороннем полушарном поражении, патологическом процессе в задней черепной ямке со сдавлением ствола мозга и прогрессирующей дислокации на тенториальном уровне. Глазодвигательные нарушения отмечаются у большинства больных. Спонтанные, возникающие без воздействия внешнего раздражителя тонические спазмы, преимущественно разгибательные, но также чередующиеся со сгибанием в руках, С.Н. Давыдов (1919) назвал горметонией (от греческого horme - приступ и tonos - напряжение). Горметонические спазмы цикличны, обладают определенным ритмом и продолжительностью и могут иметь тетра-, пара- и моноплегическое распределение. Они часто совпадают с дыхательными движениями. Н.К. Боголепов (1953), изучая двигательные нарушения у больных с кровоизлияниями в мозг, выделил симптомы, позволяющие определить сторону поражения при наличии горметонии у больного, находящегося в коматозном состоянии:
— меньшее смыкание глазной щели на стороне паралича;
— на стороне паралича ощущается меньшее сопротивление (напряжение) при попытке пассивно раскрыть веки;
— пассивно поднятое верхнее веко на здоровой стороне опускается и закрывает глаз быстрее, чем на парализованной;
— при постукивании по скуловым дугам на здоровой стороне сокращается лицевая мускулатура, на стороне паралича сокращение отсутствует;
— при вызывании рефлексов орального автоматизма (хоботкового, губного, ладонно-подбородкового) выявляется асимметрия: мышцы рта и подбородка не сокращаются на стороне паралича;
— иногда снижается роговичный рефлекс на стороне паралича;
— поворот головы и глаз в сторону очага поражения;
— рефлекторное отведение нижней челюсти в сторону паралича и частичный спазм жевательной мускулатуры при вызывании корнеального рефлекса на здоровой стороне;
— меньшая выраженность менингиального симптома Кернига на стороне паралича в силу развивающейся гипотонии;
— наличие двигательного беспокойства и насильственных движений в конечности на стороне очага;
— изменение рефлексов: большая выраженность сухожильных и защитных рефлексов, меньшая выраженность суставных и кожных рефлексов на стороне паралича;
— положение стопы: на стороне паралича - поворот кнаружи, на стороне очага - тоническое вращение внутрь;
— рано возникающий цианоз дистальных отделов ноги на стороне паралича;
— отставание при дыхании половины грудной клетки на стороне паралича;
— редко - эпилептические припадки, начинающиеся с противоположных очагу конечностей;
— при повороте головы в сторону очага исчезает тонус разгибателей предплечья противоположной руки и одновременно на руке, к которой обращен подбородок, развивается тоническое сгибание, усиливается тонус разгибателей предплечья;
— патологический разгибательный рефлекс большого пальца ноги в начальной стадии комы появляется раньше на стороне паралича, в конечной стадии комы он угасает раньше на стороне паралича;
— иногда у больных на стороне, противоположной параличу, возникают избыточные движения в руке и ноге, чаще флексорного типа.
Горметонию часто сопровождают вегетативные нарушения: гипергидроз, гиперемия лица, гипертермия, артериальная гипертензия, сердечные и дыхательные аритмии, острые эрозии желудочнокишечного тракта (ЖКТ).
• Разгибательные реакции рук с атонией или слабой сгибательной реакцией ног возникают у больных с поражением ствола мозга на уровне покрышки моста, вестибулярных ядер.
• Мышечная атония, или отсутствие двигательных реакций, может возникать как при поражении периферического двигательного нейрона (например, при полинейропатии), так и при нарушении двигательных путей на уровне нижних отделов моста и продолговатого мозга. Исследование тонуса мышц в остром периоде поражения головного мозга у больных, находящихся в коматозном состоянии, позволяет установить наличие паралича и сторону поражения мозга. Для этого используют следующие приемы (Боголепов Н.К., 1962).
— Исследуют симптомы гипотонии век (см. выше).
— Поднимают обе вытянутые руки больного и отпускают их. На стороне паралича вследствие резкой гипотонии рука падает как плеть, причем не ощущается того минимального напряжения, которое остается даже в коматозном состоянии в непарализованной конечности.
— Сгибают обе руки в локтевом суставе на 90° и отпускают их. На стороне паралича кисть и предплечье падают более пассивно.
— Пытаются насильно разводить пальцы на руках. На стороне паралича отмечается меньшее тоническое напряжение, чем на здоровой стороне.
— Сгибают бедра под прямым углом к туловищу, а голени под прямым углом к бедрам. На стороне паралича нога, пассивно разгибаясь, больше отпадает кнаружи.
— Путем осмотра и пальпации определяют состояние мышц бедра. На стороне паралича отмечается уплотнение бедра и кажущееся увеличение (расширение) его вследствие потери тонуса бедренных мышц.
— Исследуют симптом Кернига. На стороне паралича напряжение сгибателей голени выражено слабее и отсутствует содружественное сгибание парализованной ноги при исследовании нижнего симптома Брудзинского.
— Сгибают голову вперед для определения ригидности мышц затылка. Парализованная нога при этом остается неподвижной, в то время как другая сгибается (верхний симптом Брудзинского).
— Разгибают ногу в коленном суставе, поднимая стопу за пятку и прижимая колено к постели (симптом Оршанского).
— Исследуют симптом ротированной стопы: обе стопы пассивно поворачивают кнаружи до крайнего предела, затем руки быстро убирают. При этом стопа парализованной ноги не возвращается окончательно в исходное положение вследствие нарушения тонуса и силы мышц, вращающих ногу.
— Нарушенные двигательные реакции свидетельствуют как об уровне, так и о стороне максимального повреждения мозга. Наличие патологических сгибательных реакций рук при наличии или отсутствии разгибательных реакций ног позволяет сделать предположение о более распространенном и менее тяжелом супратенториальном поражении. Наличие разгибательной реакции рук и ног указывает на более глубинные и тяжелые, но все же преимущественно супратенториальные повреждения. Разгибательная реакция рук, сочетающаяся со сгибанием ног, наблюдается при нарушении функций ствола мозга в области моста. Диффузная мышечная атония с отсутствием реакций на стимуляцию обычно коррелирует с повреждением ствола на нижнем понтомедуллярном уровне или дистальнее его (Plam F., Posner J., 1986).
МЕНИНГИАЛЬНЫЕ СИМПТОМЫ
К основным менингиальным симптомам относят:
• ригидность мышц затылка;
• симптом Кернига (тоническое напряжение мышц-сгибателей тазобедренных и коленных суставов);
• тризм (тоническое напряжение жевательных мышц);
• тоническое сокращение лицевых мышц, возникающее на стороне раздражения при перкуссии по скуловой дуге (симптом Бехтерева), давлении на переднюю стенку слухового прохода, супраорбитальную точку.
Основными причинами возникновения менингиальных симптомов у больных с ОЦН являются:
• раздражение мозговых оболочек при САК и вентрикулярном кровоизлиянии, а также при оболочечной гематоме;
• вовлечение мозговых оболочек в воспалительный процесс при менингите, менингоэнцефалите и т.п.;
• раздражение оболочек мозга вследствие внутричерепной гипертензии, увеличения объема мозга при отеке и острой гидроцефалии;
• нарушение функций подкорково-стволовых тоногенных образований при дислокации, ушибе мозга.
Нередко наблюдается сочетание нескольких факторов. Увеличение выраженности менингиальных симптомов может свидетельствовать о развитии менингита, повторного кровоизлияния, внутричерепной гипертензии, окклюзионной гидроцефалии и дислокационного синдрома. Диссоциация менингеальных симптомов по оси тела наблюдается при поражении и дислокации стволово-подкорковых структур (преобладание симптома Кернига над ригидностью мышц затылка) и при локализации патологического процесса (кровоизлияние, травматическая гематома) в задней черепной ямке (преобладание ригидности затылочных мышц над симптомом Кернига). Симптом Кернига может иметь латерализационное значение: он более выражен на стороне оболочечной гематомы, асимметричного САК и абсцесса мозга и менее выражен на стороне центрального паралича (при полушарном кровоизлиянии).
ДИСЛОКАЦИЯ СТВОЛА ГОЛОВНОГО МОЗГА
Один из факторов, определяющих тяжесть состояния больного с ОЦН, - дислокация и сдавление ствола мозга. Ствол мозга на уровне среднего мозга окружен плотным краем мозжечковой вырезки, а на границе продолговатого и спинного - краем большого затылочного отверстия (рис. 2-3).
При увеличении объема содержимого супратенториального пространства в зависимости от расположения патологического очага и направления смещения мозга наблюдаются следующие виды дислокации головного мозга (рис. 2-4):
• вклинение поясной извилины под большой серповидный отросток (боковая дислокация);
• вклинение диэнцефальной области в тенториальное отверстие и смещение ствола вниз (каудально) по оси - центральная или транстенториальная дислокация;
• вклинение крючка гиппокампа между краем мозжечкового намета и ножкой мозга, приводяшая к боковому смещению и сдавлению среднего мозга (височно-тенториальная дислокация).
При увеличении объема содержимого субтенториального пространства, которое в норме занимает ствол мозга и мозжечок, развивается вклинение части червя мозжечка в тенториальную вырезку со сдавлением верхних отделов среднего и промежуточного мозга (мозжечково-тенториальная дислокация) или/и направленная вниз дислокация миндаликов мозжечка в большое затылочное отверстие со сдавлением и смещением продолговатого мозга (см. рис. 2-4). Непосредственное давление на покрышку моста и среднего мозга приводит к ишемии и отеку этих структур.
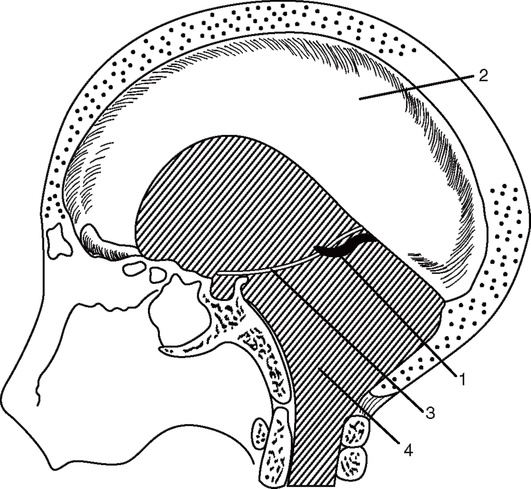
Рис. 2-3. Большой серповидный отросток и намет мозжечка на саггитальном распиле черепа: 1 - большая вена мозга (вена Галена); 2 - большой серповидный отросток; 3 - свободный край мозжечкового намета; 4 - большое затылочное отверстие (по Блинкову С.М., Смирнову Н.А., 1967)
При супратенториальных объемных поражениях мозга патологические изменения проявляются вазомоторным параличом, полнокровием, отеком, распространяющимся на соседние участки мозга сначала радиально от очага, а затем рострокаудально (сверху вниз). Этот процесс непрерывно прогрессирует. Патологические изменения распространяются в рострокаудальном направлении, напоминая неуклонно продвигающуюся волну, которая создает серию последовательных срезов функциональных нарушений. Этот процесс наблюдается даже тогда, когда тенториальное вклинение и смещение вниз в конечном итоге приводят к повреждению ствола мозга, и отражается в определенной последовательности появления клинических симптомов. Последовательно возникают дыхательные, офтальмологические и двигательные нарушения, указывающие на угнетение функций сначала диэнцефальной области, затем среднего мозга, моста и продолговатого мозга (Plam F., Posner J., 1986).
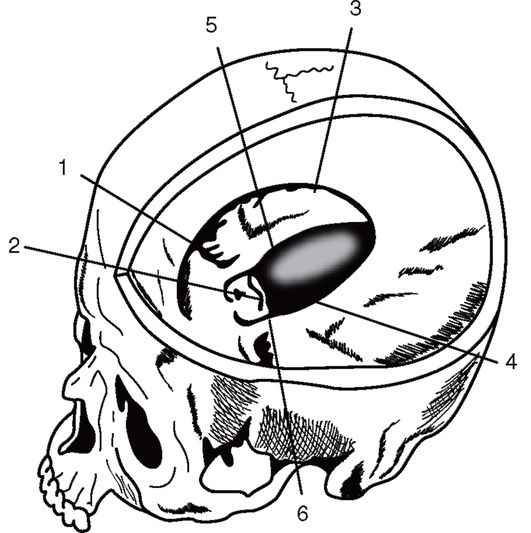
Рис. 2-4. Большой серповидный отросток и намет мозжечка: 1 - край малого крыла основной кости; 2 - спинка турецкого седла; 3 - свободный край большого серповидного отростка; 4,5 - свободный край намета мозжечка; 6 - каменисто-клиновидная связка (по Блинкову С.М., Смирнову Н.А., 1967)
Боковая дислокация (рис. 2-5) возникает при поражениях полушарий головного мозга, преимущественно в лобных и теменных долях. Отмечается смещение поясной извилины под большой серповидный отросток. Почти всегда диагностируют смещение промежуточного мозга через вырезку намета мозжечка.
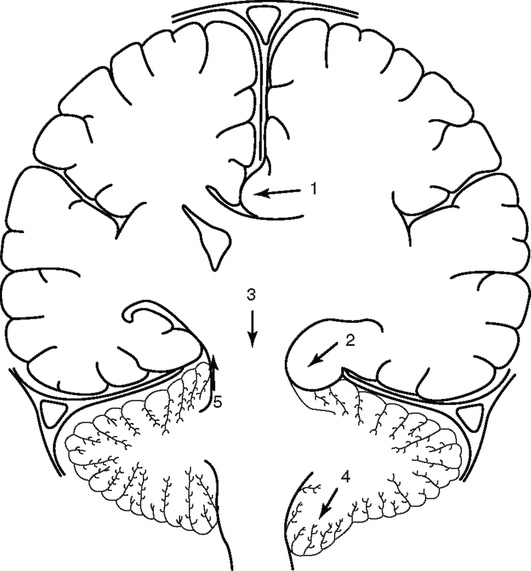
Рис. 2-5. Основные виды дислокации головного мозга: 1 - боковая - под большой серповидный отросток; 2 - височно-тенториальная (вклинение крючка гиппокампа через вырезку мозжечкового намета); 3 - центральная транстенториальная или аксиальная; 4 - дислокация миндаликов мозжечка в большое затылочное отверстие; 5 - мозжечково-тенториальная или направленная вверх транстенториальная дислокация при изолированном повышении субтенториального давления
При центральной транстенториальной дислокации выделяют следующие стадии.
• Диэнцефальная стадия. Нарушается концентрация внимания и память, возникает состояние возбуждения или сонливости. Затем (ранняя диэнцефальная стадия) дыхание прерывается зевотой, глубокимим вдохами, паузами, иногда по типу Чейна-Стокса. Зрачки сужены, фотореакции вызываются только сильным светом. Глазные яблоки в состоянии содружественного покоя или совершают содружественные плавающие движения. Окулоцефалические рефлексы не нарушены. Адекватные двигательные реакции на болевое раздражение; двусторонний рефлекс Бабинского; возможно паратоническое сопротивление (противодержание).
• Стадия среднего мозга - верхних отделов моста. Кома. Тахипноэ. Возможны колебания температуры и развитие несахарного диабета. Зрачки расширяются до 3-5 мм и фиксируются. Трудно вызывается окулоцефалический рефлекс. В покое - обездвиженность. При болевом раздражении - децеребрационная ригидность, особенно на стороне, противоположной полушарному очагу.
• Стадия нижних отделов моста - верхних отделов продолговатого мозга. Кома. Дыхание поверхностное, частое (20-40 в минуту) или атактическое. Зрачки средней величины, на свет не реагируют. Окулоцефалический рефлекс отсутствует. Обездвиженность и мышечная атония. Отсутствие реакции на боль. Двусторонний рефлекс Бабинского, иногда - защитный рефлекс сгибания ног при раздражении стопы.
• Стадия продолговатого мозга (терминальная). Дыхание замедленное, нерегулярное по частоте и глубине, периоды гаспинга. Пульс меняется от замедленного до учащенного, артериальная гипотония. В итоге происходит остановка дыхания. Зрачки максимально расширяются. Мышечная атония.
При височно-тенториальной дислокации выделяют следующие стадии.
• Ранняя стадия глазодвигательного нерва. Сознание может быть ненарушенным (или наблюдается оглушение). Умеренная анизокория с ослаблением реакции расширенного зрачка на свет. Двигательные нарушения обусловлены полушарным очагом. Дыхание, движения глаз, окулоцефалические рефлексы не нарушены. Состояние больного может изменяться в течение нескольких часов от ясного сознания до глубокой комы.
• Поздняя стадия глазодвигательного нерва. Быстрое прогрессирование симптомов вклинения. Гипервентиляция. Резкая анизокория с мидриазом на стороне вклинения. Фотореакция расширенного зрачка отсутствует, затем полная офтальмоплегия. Нарушение, затем отсутствие окулоцефалического рефлекса. Гомолатеральный полушарному очагу гемипарез вследствие сдавления противоположной ножки мозга вырезкой намета мозжечка. Двусторонние патологические симптомы, затем децеребрационная ригидность.
• Стадия среднего мозга - верхних отделов моста. Кома. Зрачок, противоположный ранее расширенному, расширяется и фиксируется. Гиперпноэ. Нарушение или отсутствие окулоцефалических рефлексов. Двусторонняя децеребрационная ригидность. С этого момента клинические признаки вклинения крючка гиппокампа соответствуют клиническим признакам центрального вклинения.
Дислокация миндаликов мозжечка в большое затылочное отверстие приводит к компрессии продолговатого мозга и полному прекращению функции дыхания и кровообращения.
Мозжечково-тенториальная, или направленная вверх транстенториальная, дислокация представляет собой смещение мозжечка и промежуточного мозга через тенториальную вырезку. Данный вид дислокации возникает при увеличении объема структур задней черепной ямки. Происходит сдавление дорсальной поверхности промежуточного мозга, прилежащих сосудов и водопровода мозга, развивается обструктивная гидроцефалия. Зрачки сужены и фиксированы по средней линии, отмечается децеребрационная или, реже, декортикационная ригидность. При оценке окулоцефалических и окуловестибулярных рефлексов диагностируют паралич взора вверх при живых латеральных движениях.
Глава 3. Нейромониторинг
Мониторинг - важная часть интенсивной терапии больных с ОЦН, находящихся в критическом состоянии.
По объему используемых методов обследования можно выделить несколько уровней мониторинга.
• Уровень 1. Постоянный мониторинг частоты сердечных сокращений (ЧСС) и ритма сердца, пульсоксиметрия, определение концентрации углекислого газа в выдыхаемом воздухе (EtCO2), центрального венозного давления (ЦВД), газового состава артериальной и венозной крови. Дискретное неинвазивное измерение артериального давления (АД).
• Уровень 2. Постоянный мониторинг ЧСС и ритма сердца, пульсоксиметрия, определение EtCO2, ЦВД, газового состава артериальной и венозной крови. Постоянное инвазивное измерение АД. Определение внутричерепного давления (ВЧД) и насыщения гемоглобина кислородом в луковице яремной вены (SvjO2).
• Уровень 3. Постоянный мониторинг ЧСС и ритма сердца, пульсоксиметрия, определение EtCO2, ЦВД, газового состава артериальной и венозной крови. Постоянное иназивное измерение АД. Определение ВЧД и SvjO2. Оценка напряжения кислорода в веществе головного мозга и биохимического состава интерстициальной жидкости мозга. Электрофизиологический мониторинг. Измерение объемного МК.
У больных с САК вследствие разрыва артериальной аневризмы головного мозга, находящихся в критическом состоянии, следует ежедневно исследовать линейную скорость МК при помощи транскраниальной допплерографии.
В данной главе не имеет смысла останавливаться на рутинных методах мониторинга, повсеместно используемых в реанимационной практике, поэтому здесь будут рассмотрены методы оценки системной гемодинамики, внутричерепного давления, мозгового кровотока, оксигенации, метаболизма и функции мозга.
МОНИТОРИНГ ГЕМОДИНАМИКИ
В настоящее время в распоряжении реаниматолога существует множество методов оценки системной гемодинамики. Среди инвазивных методик наиболее удобна и точна транспульмональная термодилюция, среди неинвазивных - чрезпищеводная допплерография.
ИНВАЗИВНОЕ ИЗМЕРЕНИЕ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ
Инвазивное измерение позволяет в непрерывном режиме оценивать АД и вовремя диагностировать и лечить эпизоды артериальной гипотензии. При одновременном измерении ВЧД мониторы автоматически рассчитывают церебральное перфузионное давление (ЦПД) (рис. 3-1, см. цв. вклейку).
Для проведения инвазивного мониторинга АД катетеризируют лучевую артерию и через соединительную трубку, заполненную физиологическим раствором, к катетеру подсоединяют датчик давления. Перед катетеризацией лучевой артерии необходимо оценить сохранность коллатерального кровотока по артериальной ладонной дуге. Для этого проводят пробу Аллена. Одновременно пережимают как лучевую, так и локтевую артерии, прекращая кровоснабжение кисти. Затем отпускают локтевую артерию, сохраняя компрессию лучевой артерии, и оценивают время, за которое кисть становится розовой. Если цвет кожных покровов восстанавливается в течение 5 с, то коллатеральное кровообращение в кисти считают сохранным. Если же бледность кожных покровов сохраняется, то коллатеральное кровообращение считают нарушенным. В этом случае катетеризация лучевой артерии может привести к ишемическим расстройствам.
В клинических условиях провести пробу Аллена не всегда возможно. В таких случаях на большой палец кисти больного надевают датчик для пульсоксиметрии и оценивают амплитуду плетизмографической кривой и показатель сатурации. Пережимают лучевую артерию и определяют динамику амплитуды волны и данных сатурации. Если указанные параметры не изменились, то коллатеральный кровоток считают сохранным.
Для правильной оценки ЦПД датчик для измерения АД следует фиксировать на уровне отверстия Монро, проецируя его на середину расстояния между наружным углом глазницы и наружным отверстием наружного слухового прохода (рис. 3-2, см. цв. вклейку).
ТРАНСПУЛЬМОНАЛЬНАЯ ТЕРМОДИЛЮЦИЯ
Для проведения измерений катетеризируют одну из подключичных или внутренних яремных вен, а также устанавливают специальный катетер с термистором в бедренную артерию в проксимальном направлении (рис. 3-3, см. цв. вклейку). Артериальный доступ позволяет осуществлять постоянный мониторинг показателей системной гемодинамики, температуры крови и забор проб артериальной крови. В катетер, установленный в центральную вену, вводят холодный раствор, температуру которого фиксирует специальный термодатчик. После прохождения малого круга кровообращения холодовую метку улавливает термодатчик, расположенный в бедренной артерии. По полученным данным монитор выстраивает кривую термодилюции и рассчитывает параметры системной гемодинамики. Методика транспульмональной термодилюции позволяет оценивать сердечный выброс, преднагрузку, периферическое сосудистое сопротивление, содержание внесосудистой воды в легких и другие важные параметры системной гемодинамики.
Для улучшения индивидуальной оценки измеряемых параметров их принято оценивать в отношении к площади поверхности тела, выраженной в м2 (табл. 3-1).
Таблица 3-1. Нормальные значения основных показателей системной
гемодинамики, определяемых при помощи транспульмональной термодилюции

ЧРЕСПИЩЕВОДНАЯ ДОППЛЕРОГРАФИЯ
Для проведения измерений в пищевод вводят специальный зонд с ультразвуковым датчиком на конце. Монитор регистрирует скорость кровотока в нисходящей аорте и рассчитывает сердечный выброс, ударный объем сердца и периферическое сосудистое сопротивление (рис. 3-4, см. цв. вклейку).
ИЗМЕРЕНИЕ ВНУТРИЧЕРЕПНОГО ДАВЛЕНИЯ
Внутричерепное давление представляет собой разницу между давлением в полости черепа и атмосферным давлением. Измерение ВЧД позволяет выявить внутричерепную гипертензию, оценить ее выраженность и рассчитать ЦПД.
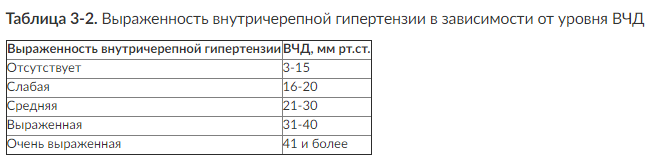
У взрослого человека в положении на спине нормальные значения ВЧД составляют 7-15 мм рт.ст. (табл. 3-2). Показанием к терапии считают стойкое увеличение ВЧД выше 20 мм рт.ст.
Показаниями для мониторинга ВЧД у пострадавших с ЧМТ считают угнетение уровня бодрствования по ШКГ до 8 баллов и менее при наличии изменений на КТ головного мозга в виде:
• гематом;
• очагов ушибов;
• отека;
• аксиальной дислокации.
При отсутствии изменений на КТ головного мозга решение о начале мониторинга ВЧД принимают при наличии двух или более факторов:
• возраст более 40 лет;
• появление одноили двусторонних познотонических реакций. Познотонические реакции свидетельствуют о наличии функционального разобщения ствола и полушарий головного мозга и представляют собой сгибательную или разгибательную реакцию в конечностях (декортикационная и децеребрационная ригидность) в ответ на болевое раздражение;
• систолическое АД менее 90 мм рт.ст.
Показанием для установки датчика измерения ВЧД у больных с нетравматическими внутричерепными кровоизлияниями считают угнетение уровня бодрствования до 10 и менее баллов по ШКГ.
Показанием для мониторинга ВЧД у пациентов с ишемическим инсультом является развитие злокачественной формы массивного ишемического инсульта в бассейне средней мозговой артерии с угнетением уровня бодрствования по ШКГ до 9 баллов и менее.
Определение ВЧД проводят с помощью различных устройств. Возможно измерение ВЧД в субдуральном, субарахноидальном и эпидуральном пространствах. К достоинствам такого измерения относят простоту установки датчиков и низкую вероятность травматизации вещества мозга. Однако применение данных устройств часто не обеспечивает необходимой точности. Показания датчика могут искажаться при избыточном локальном давлении на него, например, костных выступов.
Чаще всего используют мониторинг внутрижелудочкового давления. Преимущество использования данного метода заключается в возможности одновременного измерения ВЧД и удаления цереброспинальной жидкости. Для внутрижелудочкового измерения ВЧД используют различные способы:
• вентрикулярный дренаж, подключаемый к тензометрическому датчику измерения давления (гидравлические системы, монитор «Liquoguard»);
• двухпросветный пневматический датчик. Один просвет датчика необходим для измерения ВЧД с помощью раздутого воздухом баллончика, расположенного на конце датчика, второй просвет - для сброса ЦСЖ (монитор «Spiegelberg»);
• интегрированный в вентрикулярный дренаж датчик микродеформации (микрочип) или фиброоптический датчик (мониторы «Codman», «Camino», «MPRO2», «Sophyssa»).
В клинической практике для внутрижелудочкового измерения ВЧД наиболее часто используют гидравлические системы и монитор Шпигельберга.
Гидравлическая система
Принцип работы гидравлической системы основан на передаче давления столба цереброспинальной жидкости на тензометрический датчик давления. После установки вентрикулярного катетера к нему в стерильных условиях присоединяют измеряющую систему. Проводят калибровку измеряющего устройства по атмосферному давлению, после чего открывают вентрикулярный катетер и начинают регистрацию ВЧД (рис. 3-5, см. цв. вклейку). Для правильного измерения ВЧД датчик давления должен быть закреплен на уровне отверстия Монро. Если датчик расположен ниже уровня отверстия Монро, то значение ВЧД будет завышено, а если выше, то занижено. Использование гидравлических систем имеет ряд недостатков. Основные из них - опасность развития инфекционных осложнений и большая вероятность блокирования катетера из-за нарастающей компрессии желудочков и обтурации его просвета сгустком крови. Необходима периодическая калибровка внешнего измерительного устройства из-за колебаний атмосферного давления. При тяжелом поражении головного мозга установка вентрикулярного катетера часто невозможна из-за небольших размеров спавшихся желудочков. В настоящее время существуют одноразовые системы для одновременного измерения внутричерепного давления и контролируемого сброса цереброспинальной жидкости. Использование таких систем позволяет не только эффективно контролировать ВЧД, но и уменьшать частоту развития инфекционных осложнений, связанных с вентрикулостомией.
Монитор Шпигельберга
Для проведения измерений в желудочек мозга устанавливают специальный двухпросветный вентрикулярный катетер (рис. 3-6, см. цв. вклейку). На конце катетера расположен баллончик, соединенный с измерительным устройством. Второй канал катетера предназначен для удаления цереброспинальной жидкости. После проведения вентрикулостомии монитор заполняет баллончик воздухом и по степени давления цереброспинальной жидкости на стенки баллончика определяет ВЧД.
Разделение каналов для регистрации ВЧД и сброса цереброспинальной жидкости позволяет измерять внутричерепное давление даже в условиях обтурации или дислокации вентрикулярного катетера, что невозможно при применении гидравлических систем (рис. 3-7). При использовании прибора не требуется ручной калибровки измерительного устройства по атмосферному давлению.
Помимо измерения ВЧД монитор Шпигельберга позволяет определять церебральную податливость, или комплаенс мозга (рис. 3-8, см. цв. вклейку). Для этого к каналу катетера, по которому удаляют цереброспинальную жидкость, присоединяют тензометрический датчик давления. Монитор нагнетает 0,2 мл воздуха в баллончик и одновременно фиксирует изменение ВЧД. Отношение введенного объема к изменению ВЧД называют податливостью, или комплаенсом, мозга.
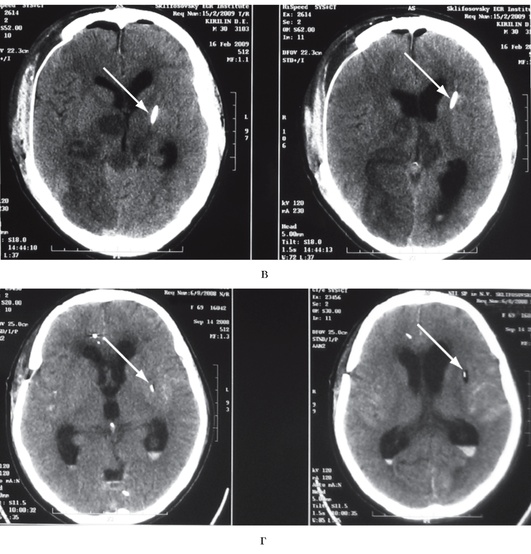
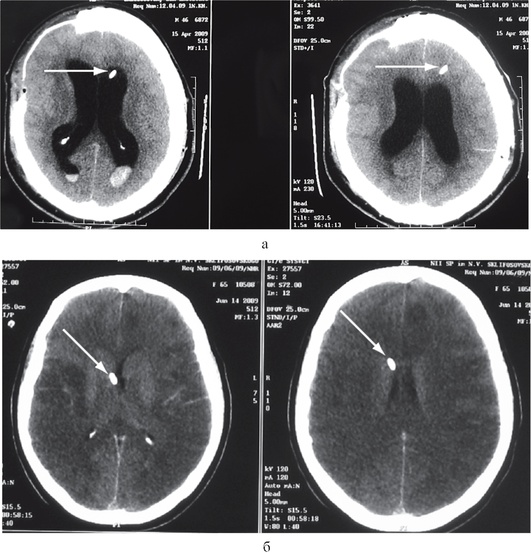
Рис. 3-7. Примеры внутрижелудочкового измерения ВЧД при помощи гидравлической системы (а, б, в)и монитора Шпигельберга (г): а - правильная установка катетера в передний рог левого бокового желудочка (стрелка), ВЧД можно измерять; б - катетер установлен в правый боковой желудочек (стрелка), однако в связи с выраженным отеком мозга боковые желудочки значительно сужены, что не позволит измерять ВЧД при помощи гидравлической системы; в - неудачная попытка дренирования переднего рога левого бокового желудочка: катетер установлен в вещество мозга (стрелка), измерение ВЧД невозможно; г - неудачная попытка дренирования переднего рога левого бокового желудочка: датчик монитора Шпигельберга установлен в вещество мозга (стрелка), однако баллончик на конце датчика позволяет определять ВЧД интрапаренхиматозно
Альтернатива внутрижелудочковому определению ВЧД - использование паренхиматозных датчиков. К достоинствам паренхиматозного измерения относят низкий риск травматизации вещества мозга и развития инфекционных осложнений, простоту установки и отсутствие необходимости в перекалибровке. Датчики устанавливают либо через фрезевое отверстие, либо через специальные устройства для фиксации в вещество лобной или височной доли, противоположной очагу основного поражения, на глубину 1-1,5 см (рис. 3-9). Для правильного измерения ВЧД локализация датчика в веществе мозга должна быть приближена к уровню отверстия Монро.
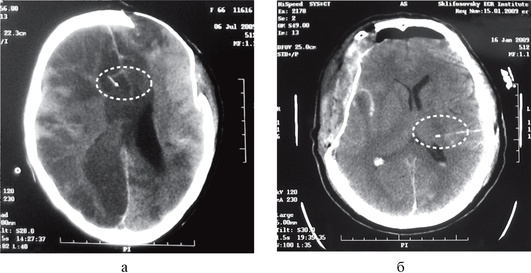
Рис. 3-9. Паренхиматозное измерение внутричерепного давления (положение датчиков для измерения ВЧД отмечено пунктирной линией): а - правильная установка паренхиматозного датчика; б - датчик установлен ниже отверстия Монро, что может привести к завышению значений ВЧД
В настоящее время для паренхиматозного измерения ВЧД используют различные датчики:
• пневматический датчик с раздуваемым воздухом баллончиком на конце (монитор «Spiegelberg»);
• датчик микродеформации (микрочип) (мониторы «Codman», «MPRO2», «Pressio», «Liquoguard»);
• фиброоптический датчик (монитор «Camino»).
В клинической практике для паренхиматозного измерения ВЧД наиболее часто используют мониторы Шпигельберга, «Codman» и «MPRO2».
Монитор Шпигельберга
Методика измерения принципиально не отличается от внутрижелудочкового измерения ВЧД. В вещество мозга устанавливают однопросветный катетер с баллончиком на конце. После установки катетера монитор заполняет баллончик воздухом и по степени давления ткани мозга на стенки баллончика определяет ВЧД.
Монитор «Codman»
Принцип работы датчика «Codman» основан на регистрации ВЧД специальным измерительным устройством (микрочипом), расположенным на конце датчика (рис. 3-10, см. цв. вклейку). Полученная с микрочипа информация выводится на экран прикроватного монитора. Особенность монитора заключается в необходимости калибровки датчика на границе водной и воздушной сред перед установкой в вещество мозга.
Монитор «MPRO2»
Для измерения ВЧД используется специальный фиброоптический катетер (рис. 3-11, см. цв. вклейку). Датчик не требует специальной калибровки перед установкой в вещество мозга и позволяет одновременно определять ВЧД, напряжение кислорода в веществе головного мозга и температуру мозга. Катетер можно устанавливать как через специальное фиксирующее устройство, так и через фрезевое отверстие с помощью подкожного туннеля.
В настоящее время в процессе исследования находятся отоакустические методы измерения ВЧД. Они основаны на изменении комплаенса барабанной перепонки в ответ на изменения давления перелимфы в лабиринте улитки при колебаниях ВЧД. Одна из перспективных разработок - оценка ВЧД по диаметру зрительного нерва, определяемому с помощью ультразвукового исследования глаза (рис. 3-12, см. цв. вклейку).
Для точной оценки степени внутричерепной гипертензии следует сначала устанавливать датчик ВЧД, а затем приступать к основному этапу операции. Измерение ВЧД прекращают, если в течение 24-48 ч ВЧД находится в нормальных пределах, не превышая 20 мм рт.ст.
МЕТОДЫ ОЦЕНКИ МОЗГОВОГО КРОВОТОКА
Существующие в настоящее время методы мониторинга позволяют определять глобальный и регионарный объемный кровоток, а также оценивать линейную скорость кровотока в основных артериях головного мозга.
В клинической практике наиболее часто используют следующие методы оценки МК:
• метод Кети-Шмидта;
• позитронно-эмиссионную томографию;
• однофотонную эмиссионную компьютерную томографию;
• термодиффузию;
• транскраниальную допплерографию.
Метод Кети-Шмидта позволяет с высокой точностью проводить количественную оценку МК в мл/мин на 100 г вещества мозга. Метод разработан в 1948 г. S. Kety и C. Shmidt и основан на ингаляции оксида азота (N2O) с последующим измерением его концентрации в периферической артериальной крови и в луковице внутренней яремной вены. По полученным данным на основании принципа Фика рассчитывают МК. Принцип Фика основан на том, что концентрация в ткани мозга вещества, которое не метаболизируется мозгом и легко диффундирует в него, пропорциональна разнице концентрации этого вещества в притекающей артериальной и оттекающей венозной крови. Таким образом, при увеличении МК артерио-венозная разница в концентрации N2O будет уменьшаться, а при его снижении - увеличиваться. Метод Кети-Шмидта был модифицирован для использования не только оксида азота, но и других газов (например, криптона и ксенона). Метод позволяет определять только общий МК и не дает возможности измерения кровотока в различных областях головного мозга.
Позитронно-эмиссионная томография (ПЭТ) позволяет одновременно получать томографические срезы и осуществлять регионарные исследования метаболизма и МК. Метод основан на внутривенном или ингаляционном введении включающихся в биологические процессы меченых изотопов (11С, 18F, 15O и др.), с последующей их индикацией в веществе мозга. ПЭТ позволяет определять регионарный объемный МК, то есть объемный кровоток в различных отделах головного мозга (рис. 3-13, см. цв. вклейку). Следует отметить, что метод не может быть применен непосредственно у кровати больного и требует транспортировки пациента в отделение томографии. Возможности использования ПЭТ ограничиваются также дороговизной таких томографов и необходимостью размещения их вблизи циклотрона для производства препаратов, содержащих быстрораспадающиеся изотопы.-
Однофотонная эмиссионная компьютерная томография (ОФЭКТ) позволяет определять регионарный мозговой кровоток по распределению радиоактивных изотопов (133Xe, 99Tc) в веществе мозга. Захват изотопов клетками мозга происходит в течение 5 мин после их внутривенного введения, а полное удаление из вещества мозга - в течение 24 ч. ОФЭКТ не позволяет проводить достоверную количественную оценку объемного мозгового кровотока. Определить изменения кровотока в различных областях мозга можно только при сравнении интенсивности накопления изотопов при повторных исследованиях. Таким образом, ОФЭКТ может быть использована только для динамической оценки МК с интервалами между исследованиями не менее суток.
Термодиффузия - единственный метод, позволяющий количественно оценивать регионарный объемный МК в постоянном режиме непосредственно у кровати больного (рис. 3-14, см. цв. вклейку). В вещество головного мозга устанавливают специальный датчик с двумя термисторами. Проксимальный (пассивный) термистор определяет температуру мозга, а дистальный - активно нагревается. МК рассчитывают по следующей формуле:
МК (мл/мин на 100 г вещества мозга)=Кх(1/V-1/V0),
где К - константа теплопроводности головного мозга; V - разница электрического напряжения между двумя термисторами; V0 - разница электрического напряжения между двумя термисторами при отсутствии кровотока.
Транскраниальная допплерография (ТКДГ) - неинвазивный метод оценки линейной скорости кровотока по магистральным сосудам шеи и головного мозга (рис. 3-15, см. цв. вклейку). Принцип ТКДГ основан на феномене изменения частоты ультразвуковой волны при отражении от движущихся форменных элементов крови. Допплерограмма - графическое представление распределения линейных скоростей эритроцитов в исследуемом участке артерии за сердечный цикл. Дуплексная (двойная) допплерография позволяет одновременно проводить эхотомографию и допплерографию, что обеспечивает визуализацию на экране монитора не только функциональных показателей мозгового кровотока, но и структурно-морфологического изображения экстра- и интракраниальных сосудов.
ТКДГ у больных с внутричерепными кровоизлияниями проводят с целью:
• диагностики и динамической оценки ангиоспазма, развивающегося после разрыва артериальных аневризм головного мозга;
• оценки состояния ауторегуляции МК;
• неинвазивой диагностики внутричерепной гипертензии.
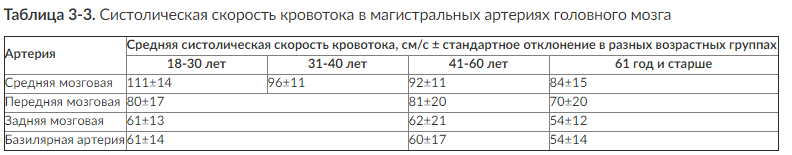
Стандартный протокол транскраниальной допплерографии включает в себя определение систолической (ЛСКс), диастолической (ЛСКд) и средней (ЛСКср) линейных скоростей кровотока (ЛСК) во внутренних сонных, средних, передних, задних мозговых и базилярной артериях (табл. 3-3). Рассчитывают полушарный индекс кровотока (индекс Линдегаарда), который представляет собой отношение средней скорости кровотока в средней мозговой артерии к средней скорости кровотока в экстракраниальном сегменте внутренней сонной артерии (в норме до 3,0). При ангиоспазме вследствие субарахноидального кровоизлияния после разрыва артериальной аневризмы индекс Линдегаарда увеличивается до 6-9.
остояние ауторегуляции мозгового кровотока оценивают при помощи компрессионного теста по коэффициенту овершута (КО) (отношение ЛСКср первого пика после прекращения компрессии ипсилатеральной общей сонной артерии к ЛСКср в покое) (рис. 3-16, см. цв. вклейку). Нормальные значения КО составляют 1,2-1,5. При значениях КО, близких к 1,0, констатируют нарушение ауторегуляции мозгового кровотока. В качестве косвенного признака внутричерепной гипертензии используют пульсационный индекс, который рассчитывают как отношение разности между ЛСКс и ЛСКд к ЛСКср (в норме 0,8-0,9) (рис. 3-17, см. цв. вклейку).
Следует отметить, что методика допплерографии не позволяет определять объемные показатели кровотока и обладает высокой «операторзависимостью» (например, полученные значения скорости кровотока зависят от угла наклона датчика). При динамическом наблюдении за линейной скоростью кровотока желательно, чтобы все исследования выполнялись одним специалистом.
МЕТОДЫ ОЦЕНКИ ОКСИГЕНАЦИИ И МЕТАБОЛИЗМА МОЗГА
К методам оценки оксигенации и метаболизма головного мозга относят: определение насыщения гемоглобина кислородом в яремной вене, прямое определение напряжения кислорода в ткани мозга, церебральную оксиметрию и микродиализ вещества головного мозга.
ЮГУЛЯРНАЯ ОКСИМЕТРИЯ
Метод основан на определении насыщения гемоглобина кислородом в оттекающей от головного мозга венозной крови. Датчик для измерения SvjO2 устанавливают ретроградно в луковицу внутренней яремной вены. Возможно использование как обычного катетера для катетеризации центральных вен (рис. 3-18, см. цв. вклейку), так и специального фиброоптического катетера (рис. 3-19, см. цв. вклейку). Установка центрального венозного катетера позволяет измерять SvjO2 дискретно в пробах крови, забираемых несколько раз в сутки.
Фиброоптический катетер дает возможность осуществлять постоянную югулярную оксиметрию с периодической калибровкой по данным SvjO2 в пробах венозной крови. Использование постоянного мониторинга улучшает выявляемость эпизодов ишемии и качество лечения больных.
После установки необходимо верифицировать положение катетера при помощи рентгенографии шейного отдела позвоночника в боковой проекции. Кончик катетера должен проецироваться на уровень сосцевидного отростка височной кости (рис. 3-20). При смещении катетера в дистальном направлении результаты измерений искажаются из-за примеси экстрацеребральной крови.
Существуют данные о неравномерности венозного оттока от головного мозга и отличии показателей SvjO2 в правой и левой внутренних яремных венах. В связи с этим существует три подхода к выбору стороны для проведения югулярной оксиметрии.
• Катетер устанавливают в ипсилатеральную по отношению к основному поражению вену.
• Определяют доминантную яремную вену либо при помощи допплерографии (оценивают диаметр левой и правой яремных вен и считают доминантной вену большего диаметра), либо по изменению ВЧД при поочередном пережатии обеих яремных вен. Катетер устанавливают на стороне большего увеличения ВЧД. Если давление увеличивается одинаково с обеих сторон, то катетеризируют правую яремную вену, так как в подавляющем большинстве случаев именно она доминантна.
• При невозможности проведения допплерографии и измерения ВЧД катетеризируют правую яремную вену.
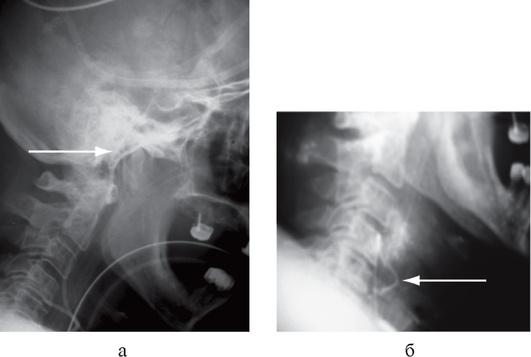
Рис. 3-20. Рентгенографический контроль положения катетера для измерения SvjO2(положение катетеров показано стрелками): а - правильное положение катетера; б - неправильное положение катетера
Показатель SvjO2 отражает соотношение доставки и потребления кислорода в головном мозге.
Доставку кислорода (DO2) вычисляют как произведение сердечного выброса (СВ) и содержания кислорода в артериальной крови (СаО2):
DO2 =CВxCaO2.
Содержание кислорода в артериальной (СаО2) и оттекающей от мозга (СvjО2) крови рассчитывают по формуле:
CO2=Hbx1,39xSO2+0,0031xPO2,
где Hb - концентрация гемоглобина; SO2 - насыщение гемоглобина кислородом; PO2 - напряжение кислорода.
Потребление кислорода (VO2) определяют путем умножения СВ на артерио-венозную разницу по кислороду:
VO2 =CВx(CaO2-CvjO2).
Количество кислорода, которое потребляет головной мозг, называют коэффициентом экстракции кислорода (O2ER) и определяют по отношению потребления кислорода к его доставке:
O2ER=VO2/DO2 или O2ER=(CaO2-CvO2)/CaO2.
Учитывая идентичность концентрации гемоглобина в артериальной и венозной крови, а также ничтожный вклад напряжения кислорода в содержание кислорода в крови, часто используют упрощенную формулу:
O2ER=(SaO2-SvjO2)/SaO2.
Поскольку больным с поражением головного мозга проводят искусственную вентиляцию легких дыхательными смесями с повышенным содержанием кислорода, у таких пациентов гемоглобин в артериальной крови всегда насыщен кислородом на 100% (или 1). Таким образом, коэффициент экстракции кислорода для головного мозга представляет собой:
O2ER=1-SvjO2.
Нормальными считают показатели SvjO2, находящиеся в пределах 55-75% при условии достаточной оксигенации артериальной крови. Таким образом, нормальные значения коэффициента экстракции кислорода для головного мозга составляют 25-45%. Снижение насыщения гемоглобина кислородом в оттекающей от мозга крови - один из первых признаков развивающейся церебральной ишемии. Уровень SvjO2 ниже 55% считают проявлением выраженной ишемии головного мозга. При снижении SvjO2 ниже 45% появляются симптомы спутанности сознания, а при уровне 24% и менее происходит утрата сознания. Наиболее частые причины эпизодов десатурации - низкое ЦПД, внутричерепная гипертензия, гипервентиляция, вазоспазм, анемия и гипоксемия.
Увеличение SvjO2 выше 75% (O2ER менее 25%) может свидетельствовать о развитии гиперемии головного мозга. Под гиперемией понимают избыточный объемный МК, составляющий более 60 мл/мин на 100 г вещества мозга (феномен «роскошной перфузии»). Однако для более точной диагностики гиперемии необходимо в совокупности оценивать уровень ВЧД и объемную скорость МК (при гиперемии будет отмечаться увеличение ВЧД и объемного МК). SvjO2 может повышаться при наличии патологического артерио-венозного сброса (например, при артерио-венозных мальформациях и травматическом каротиднокавернозном соустье), при увеличении фракции кислорода во вдыхаемой смеси, выраженном ограничении кровотока в ишемизированных областях головного мозга и при смерти мозга.
Югулярная оксиметрия позволяет оценивать глобальную церебральную оксигенацию, но не всегда отражает нарушения регионарной оксигенации головного мозга. Необходимо помнить, что проведение югулярной оксиметрии может сопровождаться осложнениями, связанными с выполнением пункции и катетеризации яремной вены. К ним относят повреждение сонной артерии, нервных стволов шейного сплетения, гнойно-септические осложнения и тромбоз яремной вены.
ПРЯМОЕ ОПРЕДЕЛЕНИЕ НАПРЯЖЕНИЯ КИСЛОРОДА В ВЕЩЕСТВЕ ГОЛОВНОГО МОЗГА (РbrO2)
В настоящее время в России существуют два вида приборов для определения PbrO2: «Licox» и MPRO2.
Монитор «Licox» определяет напряжение кислорода при помощи специального полярографического электрода Кларка непосредственно в веществе головного мозга. Этот метод был описан в 50-х годах прошлого столетия. Работа монитора основана на раздельной установке полярографического электрода и температурного датчика в вещество мозга (рис. 3-21, см. цв. вклейку). Принцип полярографического метода основан на диффузии кислорода через О2-проницаемую мембрану в электролитный раствор с последующим превращением О2 в гидроксильные ионы. Указанная реакция приводит к появлению электрического тока, величина которого прямо пропорциональна концентрации кислорода в электролитном растворе.
Работа монитора MPRO2 основана на измерении PbrO2 и температуры головного мозга при помощи специального фиброоптического катетера, устанавливаемого в вещество мозга. Помимо измерения напряжения кислорода и температуры монитор позволяет определять уровень внутричерепного давления.
Показатель PbrO2 соответствует напряжению кислорода во внеклеточном пространстве и отражает соотношение между доставкой и потреблением кислорода. В метаболически активной ткани существует градиент между артериальным и венозным концом капилляра, отражающий экстракцию кислорода тканью. В нормальных условиях концентрация кислорода в венозном конце капилляра и внеклеточном пространстве мозга практически одинакова, и PbrO2 отражает напряжение кислорода в венозном конце капилляра. Нормальные значения PbrO2 составляют 25-48 мм рт.ст. при напряжении кислорода в артериальной крови 80-120 мм рт.ст. Критически низкими значениями PbrO2 считают 8-15 мм рт.ст. Снижение PbrO2 ниже 10 мм рт.ст. значительно увеличивает риск летального исхода.
Важно проводить мониторирование PbrO2 в зоне, примыкающей к месту первичного повреждения (penumbra), так как основная цель интенсивной терапии заключается в улучшении оксигенации именно этих отделов мозга. Определение напряжения кислорода в веществе мозга имеет большое значение в подборе уровня ЦПД и определении резервов ауторегуляции мозгового кровотока (рис. 3-22).
Однако нужно помнить, что этот метод относится к регионарным, поэтому полученные результаты следует оценивать только в совокупности с данными о глобальной оксигенации головного мозга, полученными при югулярной оксиметрии. Напряжение кислорода в веществе мозга может зависеть от расположения датчика. Смещение его к корковым отделам или нахождение рядом с крупной артериолой может привести к завышению показателя PbrO2.
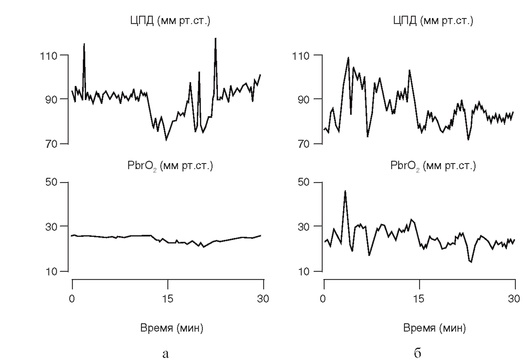
Рис. 3-22. Определение ауторегуляции мозгового кровотока при помощи мониторинга тканевого напряжения кислорода: а - пример интактной ауторегуляции МК: при изменении ЦПД напряжение кислорода в веществе мозга (PbrO2) не меняется; б - пример нарушенной ауторегуляции МК: изменения ЦПД приводят к однонаправленной динамике PbrO2 (по Dohmen С. et al., 2007)
ЦЕРЕБРАЛЬНАЯ ОКСИМЕТРИЯ
Церебральная оксиметрия (rSO2) - неинвазивный способ оценки регионарной оксигенации головного мозга. Принцип метода основан на детекции параинфракрасного излучения (длина волны 730 нм и 810 нм) двумя фотодиодами. Этот технический прием - разделение фотодиодов - используют для детекции сигнала от мозга, не смешанного с сигналами от экстрацеребральных тканей. Параинфракрасное излучение поглощается гемоглобином и его восстановленной фракцией. Поскольку в корковых отделах головного мозга 70-80% крови составляет венозная кровь, показания церебрального оксиметра отражают в основном насыщение кислородом гемоглобина венозной крови мозга. Датчик церебрального оксиметра располагают на коже лобной области на границе волосистой части головы. После подключения датчика к прибору на экран в постоянном режиме выводится показатель rSO2.
Используют как одноканальные, так и двухканальные церебральные оксиметры. Как и для SvjO2, нормальные значения rSO2 находятся в пределах 55-75% при условии нормальной оксигенации артериальной крови. Уровень rSO2 ниже 55% расценивают как проявление ишемии, а выше 75% - как развитие гиперемии головного мозга. Однако, как и в случае с югулярной оксиметрией, для точной установки диагноза гиперемии необходимо в совокупности оценивать уровень ВЧД и объемную скорость МК. Следует учитывать, что показатели rSO2 также могут увеличиваться при наличии патологического артерио-венозного сброса и увеличении фракции кислорода во вдыхаемой смеси.
Основное преимущество церебральной оксиметрии перед другими методами оценки церебральной оксигенации - неинвазивность. Этот простой в использовании метод позволяет осуществлять контроль регионарной оксигенации головного мозга при проведении различных кратковременных манипуляций (интубация трахеи, трахеостомия, санация трахеобронхиального дерева, фибробронхоскопия).
Однако этот метод часто дает артефактные результаты вследствие диспозиции датчиков и примеси экстрацеребральной крови. В связи с этим в настоящее время церебральную оксиметрию практически не используют для мониторирования оксигенации головного мозга у больных с ОЦН, находящихся в критическом состоянии.
ТКАНЕВОЙ МИКРОДИАЛИЗ
Динамическое исследование обмена веществ головного мозга - один из основных методов диагностики вторичных ишемических повреждений головного мозга у больных с поражением головного мозга, находящихся в критическом состоянии. Оценка церебрального метаболизма позволяет диагностировать вторичные повреждения головного мозга раньше, чем другие методы мониторинга.
Единственным прикроватным методом исследования метаболизма головного мозга является тканевой микродиализ, основанный на пассивной диффузии веществ, находящихся в интерстициальной жидкости головного мозга, через полупроницаемую мембрану (рис. 3-23, см. цв. вклейку).
Для проведения микродиализа используют специальные двухполостные катетеры, конечный отдел которых представлен полупроницаемой мембраной. Катетер устанавливают непосредственно в вещество головного мозга, а к его внутреннему каналу подключают специальный инфузионный насос с раствором, близким по электролитному составу к тканевой жидкости мозга. Когда раствор достигает полупроницаемой мембраны, происходит диффузия метаболитов из интерстициальной жидкости в полость катетера по градиенту концентрации. После прохождения полупроницаемой мембраны перфузионный раствор оттекает по наружной части катетера и накапливается в микроампуле. Для накопления достаточного количества диализата требуется 17-20 мин, после чего микропробирку помещают в специальный биохимический анализатор, позволяющий определять концентрации интересующих метаболитов.
Тканевой микродиализ используют у больных с внутричерепными нетравматическими кровоизлияниями и у пострадавших с тяжелой черепно-мозговой травмой, требующих мониторирования ВЧД.
Установку катетера в паренхиму мозга осуществляют либо через фрезевое отверстие, либо через специальное устройство для фиксации датчиков - bolt, которое закрепляют во фрезевом отверстии (рис. 3-24, см. цв. вклейку). У больных с субарахноидальным кровоизлиянием вследствие разрыва артериальной аневризмы головного мозга катетер устанавливают в отделы мозга, находящиеся в зоне кровоснабжения пораженной артерии. У больных с тяжелыми ушибами мозга один катетер устанавливают в зону, непосредственно прилежащую к очагу ушиба, а второй - помещают в неповрежденную область мозга. У пациентов с гипертензивными гематомами один катетер устанавливают в зону, непосредственно прилежащую к внутримозговой гематоме, а второй помещают в неповрежденную область мозга.
Катетеры для микродиализа содержат золотой фрагмент в дистальном конце, который легко идентифицируется при КТ мозга (рис. 3-25). Важно отметить, что не имеет смысла проводить микродиализ непосредственно в зоне ушиба или ишемическом очаге, так как они представляют собой зону уже состоявшихся некротических изменений.
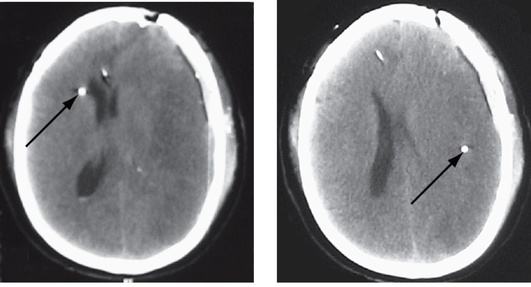
Рис. 3-25. Визуализация катетеров для тканевого микродиализа на компьютерной томограмме головного мозга (катетеры отмечены стрелками)

Микродиализ позволяет определять концентрацию глюкозы, глицерола и глутамата и отношение лактат/пируват в интерстициальной жидкости мозга (табл. 3-4). Глюкоза - единственный питательный субстрат для головного мозга. Основное количество глюкозы изначально поступает в астроциты. Доминирующим процессом, обеспечивающим образование АТФ в астроцитах, является гликолиз. Утилизация одной молекулы глюкозы приводит к образованию двух молекул пирувата и двух молекул АТФ. АТФ используется для поддержания трансмембранных ионных градиентов, обеспечивая работу АТФ-зависимых ионных помп (в основном К+-Ка+-АТФазы). Основное количество пирувата, образующегося в результате гликолиза в астроцитах, в дальнейшем не поступает в цикл трикарбоновых кислот и не подвергается окислительному фосфорилированию, а преобразуется в лактат, который выделяется в интерстициальное пространство и поступает в нейроны. В настоящее время появляется все больше доказательств того, что основной субстрат для питания нейронов именно лактат, а не глюкоза. В нейроне происходит преобразование лактата в пируват, который включается в цикл Кребса и дыхательную цепь, приводя к образованию 18 молекул АТФ на 1 молекулу пирувата. Таким образом, распад 1 молекулы глюкозы с учетом гликолиза и окислительного фосфорилирования приводит к образованию 38 молекул АТФ. Снижение концентрации глюкозы в интерстициальной жидкости головного мозга у больных с ОЦН свидетельствует о недостаточном кровоснабжении головного мозга и повышает риск летального исхода и вероятность развития выраженного неврологического дефицита.
тношение лактат/пируват позволяет выявить соотношение между анаэробным и аэробным метаболизмом в веществе мозга. В норме отношение лактат/пируват составляет 20-25. В нормальных условиях при наличии достаточного количества кислорода образование лактата в головном мозге невелико. В условиях ишемии нарушаются процессы окислительного фосфорилирования в митохондриях, происходит преобразование пирувата в лактат, в результате чего соотношение лактат/ пируват повышается. Повышение отношения лактат/пируват в остром периоде внутричерепного кровоизлияния у больных с разрывами церебральных аневризм считают предиктором летального исхода. Следует отметить, что увеличение концентрации лактата и отношения лактат/ пируват может происходить даже при достаточной доставке кислорода к тканям мозга. Такая ситуация может быть связана с развитием митохондриальной дисфункции в нейронах.
Концентрация глицерола прямо коррелирует со степенью повреждения клеточных мембран. Глутамат считают маркером эксайтотоксичности. Увеличение его концентрации также свидетельствует о выраженном клеточном повреждении.
ЭЛЕКТРОЭНЦЕФАЛОГРАФИЯ (ЭЭГ)
ЭЭГ - метод исследования головного мозга, основанный на регистрации его спонтанных электрических потенциалов (рис. 3-26, см. цв. вклейку).
Интерпретация ЭЭГ основана на анализе структуры соотношения основных ритмов (табл. 3-5).
Таблица 3-5. Частотно-амплитудные диапазоны ЭЭГ
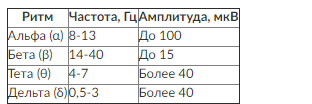
У больных с ОЦН ЭЭГ используют для:
• диагностики причины и глубины нарушения сознания;
• прогнозирования исхода комы;
• регистрации эпилептиформной активности и подбора противосудорожной терапии;
• анализа структуры цикла сон-бодрствование (полисомнография);
• подтверждения смерти мозга;
• оценки глубины седации.
В отделении неотложной нейрохирургии НИИСП им. Н.В. Склифосовского была создана классификация типов ЭЭГ у больных с САК вследствие разрыва артериальных аневризм, позволяющая предполагать прогноз лечебных мероприятий у каждого конкретного больного. Выделяют четыре типа ЭЭГ.
• I тип. Наличие минимальных изменений ЭЭГ (нерегулярность альфа-ритма) на фоне физиологической нормы, снижение амплитуды активности, медленная активность в диапазоне 5-7 Гц.
• II тип. Более выраженные изменения ЭЭГ. По всем отведениям доминирует полиморфная активность альфа-тета диапазона, сохранены зональные различия. В затылочных отведениях регистрируется полиморфный нерегулярный альфа-ритм. Патологическая активность медленного диапазона носит преимущественно диффузный характер.
• III тип. Альфа-ритм отсутствует. Регистрируются лишь отдельные группы волн альфа-диапазона. Преобладает активность тета-диапазона. Активность медленного диапазона носит преимущественно генерализованный характер, на фоне которого может регистрироваться межполушарная асимметрия.
• IV тип. Регистрируются грубые нарушения электрической активности с доминированием активности дельта-диапазона диффузного и билатерально-синхронного характера.
Чем выше тип ЭЭГ, тем хуже прогноз лечения. Наличие у больного ЭЭГ III-IV типа считают фактором риска при проведении оперативного вмешательства по выключению аневризмы из кровотока в остром периоде кровоизлияния.
Главное ограничение применения ЭЭГ - ее недостаточная надежность при изучении функциональных изменений мозга ниже коры, поскольку ЭЭГ-сигнал отражает преимущественно кортикальную активность.
ВЫЗВАННЫЕ ПОТЕНЦИАЛЫ (ВП)
ВП - метод исследования головного мозга, основанный на регистрации электрических реакций нервной системы на предъявляемый стимул. В зависимости от места стимуляции выделяют соматосенсорные, зрительные и акустически вызванные потенциалы. Их совокупность дает представление о сохранности восходящих проводящих путей. Оценить нисходящий пирамидный тракт позволяют двигательные потенциалы, получаемые при транскраниальной магнитной стимуляции коры. Основные изменения ВП состоят либо в увеличении времени прохождения сигнала (латентный период), либо в уменьшении амплитуды возбуждаемых волн.
ВП используют в комбинации с ЭЭГ для разрешения следующих задач:
• топическая диагностика повреждения спинного мозга;
• диагностика причины и глубины нарушения сознания;
• оценка глубины наркоза;
• прогнозирование исхода комы.
Из-за высокой стоимости и технической сложности ВП обычно используют только в специализированных отделениях нейрореанимации и нейрохирургических центрах.
Дата: 2018-12-21, просмотров: 634.