Возможные причины массовых поражений
Пульмонотоксикантами
В силу либо высокой токсичности, либо масштабности использования в народнохозяйственной деятельности наибольшую опасность представляют химические соединения следующих групп:
- галогены: хлор, фтор.
- ангидриды кислот: оксиды азота, оксиды серы.
- аммиак.
- галогенпроизводные угольной кислоты: фосген, дифосген.
- изоцианаты (метилизоцианат) и многие др.
Основные причины массовых поражений населения пульмонотоксикантами:
1. Разрушение промышленных объектов
- станции по хлорированию воды - содержат большие запасы газообразного хлора, хранящегося под давлением;
- большие промышленные хладокомбинаты - в холодильных агрегатах таких комбинатов используют как хладоген аммиак (в отличие от бытовых холодильников, в которых используется фреон);
- объекты химической промышленности, осуществляющие синтез полимерных материалов, производство лакокрасочных материалов, производство азотистых удобрений (содержат большие запасы хранения аммиака, летучих кислот, хлора и проч.);
- фармацевтические производства (кислоты, метилизоционат и проч.);
2. Применение боевых отравляющих веществ (ОВ) из класса «удушающих ОВ»: фосген, дифосген, фосгеноксим, хлорпикрин.
3. Воздействие продуктов горения полимерных материалов. При термической деструкции из многих материалов выделяются продукты, способные вызвать токсический отек легких. К таким продуктам термодеструкции относятся, прежде всего, оксиды азота.
4. Воздействие продуктов пиролиза средств объемного пожаротушения. Для тушения пожаров в больших зданиях используют так называемые средства «объемного пожаротушения» - фреоны (аналогичны по строению фреонам в холодильнике). Горение фреоны не поддерживают, но одним из продуктов пиролиза (термической деструкции в огне пожара) фреонов является фосген, т.е. «классический» пульмонотоксикант.
4. Воздействие веществ раздражающего действия в больших концентрациях или при длительной экспозиции. К веществам раздражающего действия относятся, например, так называемые «полицейские газы». При большой дозе эти вещества способны вызвать отек легких.
Фосгены
Источники контакта фосгена и дифосгена - табельные боевые ОВ.
Фосгены относятся к группе галогенпроизводных угольной кислоты. Помимо фосгена в качестве ОВ рассматривается трихлорметиловый эфир угольной кислоты - дифосген. Вещества обладают практически одинаковой биологической активностью. Принято считать, что действие дифосгена обусловлено расщеплением его молекулы на две молекулы фосгена при контакте с тканями легких.
Фосген применялся широко как ОВ в Первую мировую войну всеми странами. Впервые применен в 1915 г. Германией.
Фосген и его производные являются важным исходным продуктом синтеза пластмасс, синтетических волокон, красителей, пестицидов. Поэтому производство этого вещества во всех странах с развитой химической промышленностью неуклонно возрастает.
Фосген является одним из токсичных продуктов термической деструкции хлорорганических соединений (фреоны, поливинилхлоридный пластик, тефлон, четыреххлористый углерод), что также необходимо учитывать при организации оказания помощи в очагах аварий и катастроф.
Физико-химические свойства.
Фосген в обычных условиях бесцветный газ. Обладает характерным фруктовым запахом, который описывается как «запах герани», «запах гнилых яблок» или «запах прелого сена».
Газообразный фосген в 2,48 раза тяжелее воздуха.
В воде растворяется плохо.
Токсикокинетика.
Фосген действует только ингаляционно, оказывает специфическое «удушающее» действие: отек легких. В момент контакта раздражающим действием практически не обладает (немой контакт).
Во внутренние среды фосген не проникает, разрушаясь в крови малого круга.
Токсичность.
Концентрация 1 г/м при экспозиции уже 5 мин более чем в 50% случаев ведет к смерти.
Токсикодинамика (механизм токсического действия).
Вызывает отек легких «медленного» типа. Фосген не задерживается в дыхательных путях вследствие низкой гидрофильности. Поражение легких является следствием прямого повреждения веществом клеточных структур аэрогематического барьера. Обусловливает повреждение белковых структур, в первую очередь - мембран, эндотелиоцитов, альвеолоцитов. Взаимодействуя с альвеолоцитами II типа, токсикант повреждает их, угнетая активность ферментов синтеза сурфактанта.
Хлор
Источники контакта.
Хлор был первым веществом, примененным на войне в качестве ОВ.
Хлор сохраняется и транспортируется в сжиженном виде под повышенным давлением. В случае аварий на объектах производства, хранения, транспортировки и использования возможно массовое поражение людей.
Поэтому хлор, дети,-это АОХВ (!) (аварийно химически опасное вещество).
Нередки случаи групповых отравлений хлором при нарушениях в системах обеззараживания воды в бассейнах и аквапарках.
Физико-химические свойства.
Хлор - газ желтовато-зеленого цвета с характерным удушливым запахом, примерно в 2,5 раза тяжелее воздуха.
Химически очень активен. Хорошо адсорбируется активированным углем.
Токсичность.
Обладает выраженным раздражающим и прижигающим действием. Пребывание в атмосфере, содержащей хлор в концентрациях 1,5-2 г/м3, сопровождается быстрым (через 2 - 4 часа) развитием отека легких.
Токсикокинетика.
Путь поступления - только (!) ингаляционный.
Токсикодинамика: развитие отека «быстрого» типа.
Механизм повреждающего действия хлора на клетки дыхательной системы связывают с его высокой окислительной активностью, способностью при взаимодействии с водой образовывать соляную и хлорноватистую кислоты.
Клиника острого поражения.
При ингаляции чрезвычайно высоких концентраций развивается молниеносная форма: смерть может наступить уже при первых вдохах зараженного воздуха. Причина смерти - рефлекторная остановка дыхания и сердечной деятельности.
При ингаляции высоких концентраций развивается химический ожег слизистой дыхательных путей («ожег легких»). Практически с начала воздействия появляется надрывный, мучительный кашель, позже присоединяется одышка, причем в дыхании участвуют добавочные дыхательные мышцы. Одновременно отмечается крайняя слабость. Нередко отравленные падают и лишаются возможности покидать пораженную зону. Пострадавший погибает через 20-30 мин после вдыхания хлора в больших концентрациях.
В случаях менее тяжелого отравления в момент воздействия пострадавший ощущает резкое жжение в области глаз и верхних дыхательных путей, стеснение дыхания. Через некоторое время после выхода из зоны поражения может наступить некоторое облегчение состояния (скрытый период), однако в отличие от поражения фосгеном полная ремиссия не наступает: сохраняется упорный лающий кашель, болезненные ощущения по ходу трахеи.
Через некоторое время (от нескольких часов до суток) состояние вновь ухудшается, усиливаются кашель и одышка до 40-50 дыханий в минуту. Пострадавший теряет сознание и погибает при явлениях острой дыхательной недостаточности.
Удалить из очага поражения
2. Оксигенотерапия (не выше 60% в теории, но на практике и до 100%)
Введение диуретиков
4. ГК (преднизолон) - мембраностабилизирующее действие
5. Введение коллоидных растворов (реополиглюкин, желатиноль) - разгрузить малый круг кровообращения
6. Интубация трахеи - > перевод на ИВЛ (при ухудшении показателей).
Проявления интоксикации.
Фосген – вещество, вызывающее «замедленный» отек – скрытый период от 6-8 ч до 1-2 суток). Отсроченное действие, латентный период.
В момент действия затруднение дыхания, слезотечение, кашель, головокружение, слабость. В скрытом периоде(6 часов) течение благополучное. Стадия токсического отека проявляется инспираторной одышкой(50-60). Кашель с выделением пенистой мокроты. Выслушиваются влажные хрипы. В стадии разрешения высок риск вторичной инфекции (пневмонии что и определяет летальные исходы). Патогенез отека: снижается жизнеспособность и метаболитическая активность эндотелиальных клеток кровеносных капилляров легких, повышается содержание вазоактивных веществ в малом кругу кровообращения, спазм, повышение гидростатического давления, увеличение транссудации жидкости, увеличение транссудации форменных элементов крови в интерстиций, снижение лимфооттока в 5-10 раз, сдавление малого круга кровообращения, интерстициальный отек легких, снижение оксигенации крови и снижение общего метаболизма организма.
Медицинская защита . Использование индивидуальных технических средств защиты в зоне заражения. Противогаз – фактически единственный способ избежать поражения фосгеном. Своевременное выявление пораженных. Применение средств патогенетической и симптоматической терапии состояний, угрожающих жизни. Подготовка и проведение эвакуации.
Оказание помощи.
Для прекращения дальнейшего поступления токсикантов в организм надевают противогаз. Необходимо немедленно эвакуировать пораженных из очага. За всеми лицами, доставленными из зон поражения, устанавливается активное врачебное наблюдение на срок не менее 48 ч. Периодически проводятся клинико-диагностичемкие исследования.
Местное действие
Поражение кожи развивается при воздействии ипритом как в парообразном, так и в капельно-жидком состоянии. Наиболее чувствительны места с нежной кожей и большим содержанием потовых протоков (паховая область, внутренняя поверхность бедер, подмышечные впадины). Выраженные поражения кожи возникают и в местах плотного прилегания одежды: пояс, воротник, голенища сапог.
Стадии: 1) эритематозная: появление разлитой эритемы на фоне выраженного отека тканей;
2) буллезная: появление по краю эритемы мелких пузырей, сливающихся затем в один большой пузырь;
3)язвенно-некротическая: изъязвление на месте пузыря.
Поражение органов дыхания происходит при ингаляции паров иприта.
1) токсический ринит: сильная ринорея и саднение в носовых ходах;
2) токсический фарингит: затруднение при глотании;
3) токсический ларингит: осиплость голоса, а иногда и полная потеря его (афония);
4) токсический трахеобронхит: саднение за грудиной, мучительный кашель, в первые дни кашель сухой, малопродуктивный, а затем — с обильной гнойной мокротой
Поражение глаз наблюдается при воздействии как парообразным, так и капельно-жидким ипритом. При легком поражении развивается конъюнктивит. После скрытого периода (4—5 ч) появляются признаки раздражения: ощущение «песка в глазах», чувство жжения и рези, светобоязнь, слезотечение, гиперемия и отек слизистой оболочки век. При воздействии вещества в высокой концентрации или при длительной экспозиции поражается роговица: все указанные выше симптомы выражены более интенсивно, развивается помутнение роговицы, носящее поверхностный характер. В случаях тяжелых поражений с присоединением вторичной инфекции возможно глубокое изъязвление роговицы вплоть до ее прободения.
Резорбтивное действие
ü По окончании скрытого периода развиваются нарушения со стороны центральной нервной системы — токсическая энцефалопатия. Дисфункциия ЦНС обусловлена «первичной токсемией»: в кровь поступают токсичные продукты метаболизма иприта, биологически активные вещества, образующиеся в результате цитолиза. К числу ранних проявлений относятся общая слабость, головная боль, головокружение, апатия
ü действием токсиканта на систему кроветворения. Поражаются все ростки: лейкоцитарный, эритроцитарный и тромбоцитарный. В периферической крови развивается лейкопения, которая быстро прогрессирует.
ü глубокое нарушение обмена веществ, в результате которого развивается истощение, описываемое как «ипритная кахексия». Нарушается белковый обмен: анаболические процессы замедляются, катаболические — резко интенсифицируются – ипритная кахексия
Патогенетическая терапия
СПЕЦИФИЧЕСКИХ АНТИДОТОВ НЕТ!
1) Предотвратить поступление в организм
2) Уменьшить всасывания
Местная антивоспалительная терапия
Предупреждение и устранение вторичной инфекции.
Смягчение и устранение явлений резорбции яда.
Серосодержащие препараты в терапии ипритных поражений:
- тиосульфат Na 30% в/в 75 мл сразу (за 10 мин) по 25 мл через 1, 3, 5 ч
- смесь «тиоцит»: равные количества 30% тиосульфата (гипосульфата) Na + 5% цитрата Na
5 мл/кг, V = 1 мл/мин
- унитиол
5% 5-10 мл/сут в/в, в/м
По Александрову:
ü Для дегазации иприта на коже человека рекомендуется применение 2—5% водных растворов препаратов «активного хлора» (хлораминов). Также для дегазации иприта на коже могут применяться растворы марганцевокислого калия, перекиси водорода и йода, поскольку при окислении иприт теряет свои токсические свойства.
ü Для обработки слизистых глаз применяют 1—2% растворы двууглекислой соды или борной кислоты.
ü В случае попадания иприта в желудок необходимо вызвать рвоту и провести промывание желудка 0,05% раствором марганцевокислого калия. По окончании промывания в желудок вводится активированный уголь.
ü Для уменьшения явлений резорбтивного действия иприта используется 30% раствор гипосульфита натрия в количестве 10-15 мл внутривенно.
Для защиты органов дыхания и кожных покровов от действия иприта используются соответственно противогаз и специальная защитная одежда. Поскольку иприт обладает способностью диффундировать в сложные органические соединения, следует помнить, что ОЗК и противогаз не гарантируют полную защиту кожных покровов. Время нахождения в зоне поражения ипритом не должно превышать 40 минут, во избежание проникновения ОВ через средства защиты к коже.
В состав билета не входит, но давайте вспомним про РИЦИН
(его аналог – абрин, в составе бус, четок)
ü Рицин — растительный белок (гликопротеид), токсин растительного происхождения, белый, не имеющий запаха, легко диспергируемый в воздухе и растворимый в воде порошок, малоустойчив в водных растворах и при хранении постепенно теряет токсичность.
ü Рицин способен проникать в организм через легкие (инфляционно),через желудочно-кишечный тракт. Через неповрежденную кожу рицин проникать не способен.
ü Основной “точкой приложения” А-цепи рицина являются рибосомы, а именно их 60-S (большие) субъединицы. Рицин связывается с рибосомами в той их области, где указанные активные молекулы взаимодействуют с факторами элонгации (ФЭ-1 и ФЭ-2). В результате удлинение формируемых на рибосомах полипептидных цепей прекращается - нарушается синтез белка в клетке и она погибает.
ü Рицин инактивирует эндогенные ингибиторы протеолиза в клетках, тем самым активируя протеолитические процессы, что ведёт к разрушению клеточных белков и в конечном итоге к гибели клеток.
ü Рицин, активирует Т-киллеры и другие фагоцитирующие элементы иммунной системы, что также приводит к клеточной гибели.
Местное действие рицина обусловлено повреждением клеточных структур на месте проникновения в организм. При ингаляционном поступлении повреждаются альвеолоциты и эндотелиоциты, при алиментарном пути поступления — эпителий желудочно-кишечного тракта. Резорбтивное действие проявляется выраженным нарушением проницаемости сосудов и деструктивными процессами (цитолизом) в печени, почках, миокарде. В основе нарушения сосудистой проницаемости также лежит повреждение эндотелиоцитов.
Патогенетическая терапия
Специальные антидотные средства отсутствую!
Помощь пораженным оказывается симптоматическая. Перспективным направлением разработки антидотов может быть создание антитоксических сывороток, содержащих антитела к белку-рицину.
ФОС
Лекарственные препараты: армин
Отравляющие вещества (ФОВ): зарин, зоман, табун, VX
Интсектициды (ФОИ): карбафос, хлорофос, дихлофос, лептофос.
Физико-химические свойства
Большинство ФОС в нормальных условиях — бесцветные жидкости, обладают слабым фруктовым запахом. Хорошо растворимы в жирах, плохо растворимы в воде. ФОС хорошо сорбируются пористыми материалами без потери токсичности.
ФОС являются производными кислот пятивалентного фосфора. В молекуле ФОС группа Р=0 поляризована за счет смещения электронных облаков. Атом фосфора становится электрофильным, что имеет принципиальное значение для механизма действия ФОС.
Среди реакций, в которые могут вступать ФОС, особое значение имеют реакции фосфорилирования, гидролиза и окисления. Эти реакции обусловливают механизм токсического действия, биотрансформацию данных токсикантов в организме, а также некоторые принципы дегазации и антидотной терапии.
ФОС фосфорилируют аминокислоты. В организме фосфори- лированные таким образом ферменты теряют свою активность. Основу механизма токсического действия ФОС составляет фосфорилирование холинестеразы на постсинаптической мембране холинергических синапсов нервной системы.
Все ФОС хорошо подвергаются гидролизу с образованием нетоксичных продуктов. Данная реакция значительно ускоряется в присутствии щелочей, поэтому для дегазации этих ОВ используют растворы, содержащие щелочи (КОН, NaOH), аммиак. Особенно эффективно кипячение в щелочных растворах, используемое, например, для дегазации обмундирования, зараженного зарином или зоманом.
Некоторые ФОС подвержены процессу летального синтеза. Биоокисление ферментами печени тионовых соединений (фосфотионатов) ведет к образованию более токсичных веществ — токсификации ксенобиотика. Примером такого «летального синтеза» может служить превращение в организме паратиона в высокотоксичный параоксон.
Токсикокинетика
ФОС могут проникать в организм:
· через кожу и слизистые оболочки
· ингаляционно
· через желудочно-кишечный тракт
(!) Способны проникать через ГЭБ (об этом нам говорит высокий коэффициент распределения в системе «масло—вода» (коэффициент Овертона—Мейера).
Токсикодинамика
3 механизма действия: (по лекции)
· необратимое ингибирование ХЭ
· взаимодействие с рецептором
· повышение чувствительности к АЦХ
По учебнику:
1. АНТИХОЛИНЭСТЕРАЗНОЕ ДЕЙСТВИЕ:
Иммуносупрессивное действие
Как осуществляется ингибирование ХЭ:
ФОС фосфорилируют серин, входящий в активный центр ХЭ:
На первой стадии образуется фермент-ингибиторный комплекс (фермент-ФОС). При этом каталитическая активность фермента теряется. Впоследствии происходит фосфорилирование фермента. Оно заключается в формировании ковалентной связи между фосфором и гидроксилом серина. Осуществление такой атаки становится возможным вследствие формирования на атоме фосфора дефицита электронов и некоторого положительного заряда. Образовавшийся комплекс отличается высокой прочностью: дефосфорилирование происходит очень медленно.
В процессе ингибирования холинэстеразы ФОС возможность реактивации фермента убывает пропорционально времени угнетения. Это явление носит название «старение холинэстеразы». Считается, что в процессе старения происходят конформационные изменения молекулы фермента, исключающие как спонтанную, так и индуцированную реактивацию фермента. Активность восстанавливается пропорционально ресинтезу фермента de-novo.
Как осуществляется взаимодействие с рецептором и повышение чувствительности к АЦХ:
 Тоже через фосфорилирование: холинергические неантихолинэстеразные эффекты могут быть связаны со способностью ФОС фосфорилировать активные участки холинорецептора, поскольку и ацетилхолинэстераза и холинорецепторы взаимодействуют с одним и тем же субстратом — ацетилхолином. Прямое холиномиметическое действие характерно для М-холинорецепторов. Холиносенсибилизирующее действие — повышение чувствительности М-холинорецепторов к ацетилхолину — также приводит к холиномиметическому действию. Холинолитическое действие считается характерным для нервно-мышечной передачи, т. е. для Н-холинорецепторов. Немного о пианино: между холиномиметическим и холинолитическим действием ФОС на рецепторы противоречие кажущееся. Образно можно сравнить рецептор с клавишей. Но рецептор — это клавиша пианино, а не клавиша органа. Длительное «давление» на клавишу не дает длительного звучания, звук постепенно гаснет, но рецептор остается оккупированным и не способен отвечать на действие ацетилхолина. Миметическое действие сменяется литическимL
Тоже через фосфорилирование: холинергические неантихолинэстеразные эффекты могут быть связаны со способностью ФОС фосфорилировать активные участки холинорецептора, поскольку и ацетилхолинэстераза и холинорецепторы взаимодействуют с одним и тем же субстратом — ацетилхолином. Прямое холиномиметическое действие характерно для М-холинорецепторов. Холиносенсибилизирующее действие — повышение чувствительности М-холинорецепторов к ацетилхолину — также приводит к холиномиметическому действию. Холинолитическое действие считается характерным для нервно-мышечной передачи, т. е. для Н-холинорецепторов. Немного о пианино: между холиномиметическим и холинолитическим действием ФОС на рецепторы противоречие кажущееся. Образно можно сравнить рецептор с клавишей. Но рецептор — это клавиша пианино, а не клавиша органа. Длительное «давление» на клавишу не дает длительного звучания, звук постепенно гаснет, но рецептор остается оккупированным и не способен отвечать на действие ацетилхолина. Миметическое действие сменяется литическимL
Нехолинергические эффекты:
А) Нарушения других нейромедиаторных систем, которые возникают в результате нарушения межмедиаторного баланса, прежде всего в ЦНС. Воздействие ФОС сопровождается нарушениями содержания в мозге норадреналина, дофамина, серотонина, нейромедиаторных аминокислот, ГАМК, нейропептидов.
Б) Изменение активности ряда ферментов: трипсина, тромбина, липазы, альдолазы, нейротоксической эстеразы, АТФ-азы и др.
В) Мембранотоксическое действие (усиление перекисного окисления липидов мембран).
Г) Угнетение иммунитета: возможной причиной этого является ингибирование эстераз иммунокомпетентных клеток, как следствие, отравления ФОС нередко сопровождаются инфекционными осложнениями (пневмониями, ангинами, ОРЗ, бронхитами).
ИТОГО:
Итак, анализ механизмов токсического действия антихолинэстеразных ядов показывает, что основным механизмом, безусловно, является ингибирование ацетилхолинэстеразы синапсов. По мере ингибирования активности ацетилхолинэстеразы во всех холинергических синапсах начинает накапливаться ацетилхолин. Это приводит к возбуждению постсинаптических М- и Н-холинергических структур. Соответственно выделяют мускарино- и никотиноподобное действие ФОС. При этом М-холиномиметическое действие определяется преимущественно антихолинэстеразным эффектом ядов (непрямое холиномиметическое действие), а Н-холиномиметическое — сенсибилизацией Н-холинорецепторов. Однако при купировании проявлений острейшего и острого периодов интоксикации все большее значение приобретают нарушения структуры биологических мембран, изменения межмедиаторных взаимоотношений.
Периферические и центральные эффекты антихолинэстеразных ядов:
1. Периферические мускариноподобные эффекты:
— бронхоспазм —бронхорея
— брадикардия
— саливация
— усиление моторной и секреторной функции ЖКТ
— миоз, спазм аккомодации
— усиление потоотделения
2. Периферические никотиноподобные эффекты:
— мышечные подергивания
— параличи — в подостром периоде (развитие нервно-мышечного блока) 3. Центральные мускари но подобные эффекты:
—судорожный синдром
— гипокинезия и каталепсия
— тремор (возбуждение Н-холинергических структур лимбической
системы мозга)
— нарушения сознания (психоз— при средней степени тяжести,
Антидотная терапия
Холинолитики как антидоты ФОС. Ингибирование ацетилхолинэстеразы, развивающееся при отравлении ФОС, приводит к накоплению ацетилхолина в холинэргических синапсах («интоксикация эндогенным ацетилхолином»). Такое действие ФОС может быть описано как непрямое холиномиметическое действие. Поэтому при интоксикации ФОС с целью лечения должны использоваться холинолитики. Холинолитики (антихолинэргические средства) являются физиологическими антагонистами ФОС в действии на холинэргические синапсы. Они связываются с постсинаптическими рецепторами, защищая их от гиперактивации ацетилхолином, накапливающимся в избытке в синаптической щели.
Как известно, вещества имеют неодинаковую способность проникать через гематоэнцефалический барьер (ГЭБ). Поэтому все холинолитики подразделяются на «центральные», проникающие через ГЭБ: амизил, тропацин и др., и периферические, не проникающие через ГЭБ. Неодинаково и сродство холи политиков к рецепторам разных типов. По этому показателю антихолинэргические препараты, как известно, разделяют на М-холинолитики (атропин, скополамин, метацин и др.) и Н-холинолитики (пентамин, бензогексо- ний, мекамиламин и др.).
Принципы антидотной терапии холинолитиками отравлений ФОС:
1. Использование многокомпонентных рецептур. Холинолитики различных групп не являются полными антагонистами ФОС, так как, блокируя лишь определенный тип рецепторов, устраняют эффекты, инициируемые возбуждением только рецепторов этого типа. Поэтому должны использоваться многокомпонентные рецептуры, состоящие из холинолитиков различных групп (центральных и периферических, М-и Н-холинолитиков),
2. Использование доз, превышающих максимально разрешенные. При тяжелом отравлении в условиях гипоксии чувствительность к холинолитикам резко снижается. Для получения антидотного эффекта препараты следует вводить в дозах, во много раз превосходящих фармакопейные. Атропин вводят до появления признаков переатропинизации: сухость и гиперемия кожных покровов, прекращение саливации, расширение зрачка, тахикардия.
3. Частое повторное введение холинолитиков. Продолжительность действия холинолитиков в организме на фоне тяжелой интоксикации ФОС резко сокращается и составляет не более 1-3 ч. Это делает необходимым повторное назначение холинолитиков при отравлениях.
Антидоты само- и взаимопомощи представляют собой комплексные рецептуры, состоящие из центральных и периферических холинолитиков. Эти препараты должны быть использованы максимально быстро с момента отравления (поражения), поэтому в угрожаемый период они выдаются населению или санитарным дружинникам. Антидоты первой помощи изготавливаются в виде шприца-тюбика объемом 1,0 мл. Пострадавший вводит себе содержимое самостоятельно в большие мышечные массивы (бедро, плечо, ягодица) при появлении первых признаков отравления ФОС.
Врачебным антидотом (препаратом, который может применять только врач) в течение длительного времени является атропин. Будучи М-холинолитиком преимущественно периферического действия, атропин устраняет такие проявления интоксикации, как бронхоспазм, бронхорея, брадикардия, рвота, диарея, гиперсаливация и пр. Атропин обладает слабой противосудорожной активностью.
Как вводим атропин:
ü легкая интоксикация – внутримышечно 2 мг (т. е. доза превышает максимально разрешенную фармакопейную дозу в 1 мг)
ü средняя степень тяжести – внутримышечно 4 мг, затем каждые 10 мин по 2 мг до полного исчезновения симптоматики и появления признаков легкой переатропинизации.
ü тяжелая интоксикация – внутривенно (или внутримышечно) 4—6 мг атропина, затем через каждые 5—10 мин по 2 мг. В течение первых суток может потребоваться до 100 мг и более атропина.
(!) Введение атропина лицам без поражения ФОС сопровождается тяжелым отравлением.
Для максимально быстрого оказания помощи пораженным должны использоваться антидоты первой помощи: рецептуры, достаточно эффективные, но и относительно безопасные при неадекватном ошибочном использовании. К таким препаратам относятся АФИН, БУДАКСИМ, ТАРЕН. Тарен — комплексный препарат на основе холинолитиков и обратимого ингибитора холинэстеразы. Тарен расположен в аптечке индивидуальной АИ-2.
Реактиваторы холинэстеразы
Это фармакологические вещества, восстанавливающие каталитическую активность холинэстеразы, ингибированную ФОС. Реактиваторы холинэстеразы являются биохимическими антагонистами ФОС. К числу наиболее известных реактиваторов холинэстеразы относятся КАРБОКСИМ, ПРАЛИДОКСИМ, ДИПИРОКСИМ, ТОКСОГОНИН.
В результате нуклеофильной атаки оксимной группы на фосфорилированный энзим разрывается ковалентная связь между атомом фосфора ФОС с кислородом серина активного центра холинэстеразы и образуется новое соединение — фосфорилированный оксим и свободный энзим.
Таким образом, оказывают эффекты:
· дефосфорилирование холинэстеразы и восстанавление ее активности
· десенсибилизирующее действие на холинорецепторы и восстанавление их функции
· нейтрализация ФОС, циркулирующих в крови.
Под влиянием реактиваторов холинэстеразы ускоряется восстановление сознания у пораженных, ослабляется выраженность бронхоспазма, спазма кишечника, ослабляются или прекращаются фибриллярные мышечные подергивания, предупреждается развитие мышечной слабости и восстанавливается деятельность дыхательной мускулатуры, что, в свою очередь, приводит к ослаблению гипоксии. При лечении острых отравлений ФОС реактиваторы холинэстеразы применяются в сочетании с холинолитическими веществами.
Диэтиламид лизергиновой кислоты (ДЛК, LSD)
*диэтиламид d-лизергиновой кислоты
Актуальность.
ДЛК часто используется с токсикоманическими целями, возможны случаи массовых отравлений. Долгое время ДЛ рассматривали как потенциальное ОВ. Не исключено использование ДЛК как диверсионного агента. (жопой чую, это не к добру)
Физико-химические свойства.
ЛСД — белый кристаллический порошок без запаха. Плохо растворим в воде, растворяется в органических растворителях. Соли ЛСД хорошо растворимы в воде.
Пути поступления. ДЛК способен быстро проникать в организм через желудочно-кишечный тракт, а также через слизистые дыхательных путей при ингаляции в форме аэрозоля. Основной путь поступления при использовании с токсикоманическими целями — через слизистую ротовой полости (марки). Максимальная концентрация в крови отмечается через 5 -15 мин после приема.
При приеме вещества внутрь человеком в дозе 0,005 мг/кг развиваются выраженные психозы. Летальная доза оценивается в 20 -30 мг/кг.
Механизм токсического действия ДЛК остается гипотезой. В основе токсических эффектов, развивающихся при действии ДЛК на нервную систему, лежат:
1) серотонинолитическое действие (истощение запасов серотонина);
2) дофаминомиметическое действие — активируется процесс синтез нейромедиатора, ускоряется его оборот в стриатуме, гипоталамусе, лимбических ядрах;
3) активация других катехоламинергических систем и их истощение.
Клиника острого отравления ДЛК складывается из нарушений психики, соматических и вегетативных нарушений.
· Нарушения психики проявляются расстройствами восприятия
по типу иллюзий, а при большой дозе — развитием зрительных и
слуховых (реже) галлюцинаций. Как правило, иллюзии носят яркий
характер («расширение сенсорного входа»), что вызывает прилив по
ложительных эмоций. Впоследствии возможны смена настроения,
эмоциональная напряженность, озлобленность. Контакте поражен
ным затруднен, но возможен. Тяжелые интоксикации сопровожда
ются нарушениями мышления вплоть до помрачения сознания.
· Вегетативные расстройства протекают по типу адренергическо
го синдрома: мидриаз, тахикардия, гипергликемия, пиломоторные
реакции, гипертония. Соматические нарушения сопровождаются
головокружением, слабостью, тремором рук, атаксией (неустойчи
востью позы и движений), дизартрией (нарушением речи).
Общая продолжительность интоксикации составляет 6—12,
реже до 24 ч. По выходе из острого состояния пострадавший хорошо
помнит пережитое.
Частичными специфическими антагоннотами ДЛК (физиологические антагонисты) являются нейролептики.
Как известно, в основе антипсихотического действия препаратов этой группы лежит способность блокировать рецепторы дофамина, а также а-рецепторы норадреналина и 5 НТ2-рецепторы. К числу нейролептиков относятся производные фенотиазина (аминазин, тиоридазин, трифлюоперазин и т. д.), тиоксантена(тиотикрен), бутирофенона (галоперидол), бензамида (метоклопрамид, диметпрамид) (снова это говно)и т. д. Используются для оказания первой помощи и купирования психических расстройств.
12. Делириогены. Токсикологическая характеристика BZ и фенциклидина. Механизм действия. Проявление интоксикации. Медицинская защита. Оказание помощи.
(бОльшая часть инфы из интернета, потому что ни в презентации, ни в учебнике толком почти ничего нет)
Делирий способны вызывать все вещества, обладающие центральной М-холинолитической активностью. Наиболее токсичным представителем группы является вещество BZ - производное хинуклединилбензилата, находившееся на снабжении армий некоторых государств в качестве ОВ несмертельного действия. Остальные представители группы менее токсичны, но так же представляют опасность: атропин, скополамин, дитран, фенциклидин, фторацизин и др.
К числу делириогенов так же могут быть отнесены лекарственные препараты из группы нейролептиков (производные фенотиазина) и некоторые трициклические антидепрессанты (фторацизин и др.), которые в высоких дозах также проявляют свойства холинолитиков. Основными симптомами интоксикации являются:
- спутанность сознания;
- нарушение оценки своего состояния;
- эйфория;
- беспокойство;
- нарушение координации движений;
- галлюцинации;
- нарушение контакта с внешним миром;
- гиперрефлексия;
- гипертермия;
- судороги;
- кома;
- амнезия.
BZ
Твердое кристаллическое вещество без цвета и запаха, устойчивое в водных растворах. Как ОВ применяется в виде аэрозоля или дыма. Проникает в лёгкие и ЖКТ, легко преодолевает ГЭБ. Прочно и длительно(до 72ч) связывается с М-холинорецепторами мозга à нарушение психической деятельности: нарушения кратковременной памяти, сценоподобные галлюцинации, психомоторное возбуждение, агрессия; вегетативные нарушения: тахикардия, сухость и гиперемия кожных покровов, мидриаз, гипертермия. Возможен смертельный исход.
Важно помнить, что поскольку в ЦНС существует тесное функционально-морфологическое взаимодействие нейронов, передающих нервный импульс с помощью различный нейромедиаторов, помимо нарушений холинэргических механизмов мозга при отравлении BZ, как и другими холинолитиками, отмечаются нарушения в системе норадренергической, дофаминергической, серотонинергической медиации.
Фенциклидин
Это вещество, один из аналогов кетамина, впервые синтезировано в 50-е годы, как средство для наркоза. В процессе испытаний была выявлена его высокая психодислептическая активность. Проявления интоксикации фенциклидином:
5 - 10 мг - атаксия, нистагм, деперсонализация, нарушение чувства времени, ухудшение настроения, галлюцинации, парестезии, тошнота, рвота. Начало: 1 - 2 часа; продолжительность: 4 - 8 часов
10 - 20 мг - ступор, гиперрефлексия, гипертензия, стереотипии, нистагм, миоз. Начало: 0,5 - 1 час; продолжительность: 8 - 24 часа
более 50 мг - нистагм, гипотензия, брадикардия, затруднение дыхания, судорожные приступы, кома. Продолжительность: до 4 суток
более 100 мг - гипертермический криз, угнетение дыхания, смерть в течение 3 - 10 суток от остановки дыхания
В основе токсического действия фенциклидина лежит способность блокировать проведение нервных импульсов в глютаматергических синапсах центральной нервной системы. Однако при действии больших доз токсиканта отмечаются нарушения со стороны и других нейромедиаторных систем.
В зависимости от действующей дозы токсикантов можно выделить несколько степеней тяжести острого отравления:
| Степени тяжести | Основные проявления | Фазы течения |
| Субпсихотическая | Снижение работоспособности, ухудшение самочувствия | Не прослеживаются |
| Легкая | Оглушенность, маниакально- и галлюцинозоподобные комплексы | Астения с резидуальными состояниями |
| Средняя | “Субделирий” | - Оглушенность - “Субделирий” - Критический сон - Астения |
| Тяжелая | Делирий, делириозноаментивные состояния | - Оглушенность - Делирий - Критический сон - Астения (возможна энцефалопатия) |
| Сверхтяжела | Делирий, сопор, кома, | - Оглушенность - Делирий - Кома (при недостаточности лечения) - Астения (возможна энцефалопатия) |
Медицинские средства защиты
Специфическими противоядиями (функциональными антагонистами) при отравлении холинолитиками вообще и BZ в частности являются непрямые холиномиметики - обратимые ингибиторы холинэстеразы, способные проникать через гематоэнцефалический барьер, например галантамин, эзерин, аминостигмин и т.д.
Недостатком обратимых ингибиторов, как антидотов BZ, является непродолжительность их действия. Вещества угнетают активность энзима всего на несколько часов, в то время как токсикант связывается с рецепторами синапсов очень прочно и на долго (до нескольких суток). В этой связи однократного введения антидотов бывает недостаточно - развиваются ремиссии интоксикации. Повторное введение обратимых ингибиторов с каждым разом становится все менее эффективным. Это дало повод рекомендовать для устранения психозов необратимые ингибиторы ХЭ (ДФФ, фосфорилтиохолины). Однако высокая токсичность и малая терапевтическая широта веществ, препятствует их применению в клинической практике.
Исходная доза и продолжительность введения обратимых ингибиторов ХЭ определяются степенью тяжести интоксикации. Препараты целесообразно назначать как можно раньше, желательно при появлении первых признаков интоксикации. Однако при этом важно установить, что нарушения психики обусловлены именно действием холинолитиков, а не психодислептиков с иным механизмом действия (например, ДЛК) или нейротоксикантов смертельного действия в малых дозах (ФОС, карбаматы, ГАМК-литики). Поскольку сделать это быстро практически невозможно, перед введением антидота, следует понаблюдать за пострадавшим и убедится, что в основе процесса лежит антихолинэргическое действие (ориентируясь в основном на характер вегетативных нарушений и особенности нарушения психики. Таблица с различиями адреномиметического и холинолического синдромов есть в Александрове на стр. 100).
При легкой степени поражения BZ для восстановления нормальной психической деятельности препараты вводят внутримышечно: аминостигмин – 2 мл 0,1% раствора внутримышечно; галантамин - 2 мл 0,5% раствора; эзерин - 2 мл 0,05%. Если лечебный эффект недостаточно полный, препараты следует вводить повторно через 30-60 мин до исчезновения симптомов отравления.
При средних и тяжелых формах отравления показано раннее многократное введение обратимых ингибиторов холинэстеразы дробными дозами. Так, аминостигмин в первые-третьи сутки следует вводить 3 – 5 раз; галантамин вначале следует вводить внутримышечно или внутривенно в 1% растворе по 2-3 мл. В последующем через каждые 30-40 мин по 1-2 мл 0,5% раствора до получения позитивного эффекта.
Поскольку помимо холинэргических механизмов в действии BZ на мозг присутствует и другие механизмы (в частности активация катехоламинэргических механизмов) при тяжелых отравлениях устранить патологические эффекты с помощью только холиномиметиков не представляется возможным. Чрезвычайно сложным, но вместе с тем и ответственным мероприятием при интоксикации является борьба с психомоторным возбуждением. Из медикаментозных средств для этой цели, прежде всего, рекомендуют нейролептики, лишенные холинолитической активности, например трифтазин (0,2% - 1,0 мл).
Кроме нейролептиков для борьбы с психомоторным возбуждением могут быть использованы симптоматические средства: бензодиазепины (диазепам) и наркотические аналгетики (промедол: 2 мл 2% раствора внутримышечно).
Для устранения нарушений, обусловленных периферическим холинолитическим действием ОВ (тахикардия, сухость кожи, нарушение функции кишечника, задержка мочевыделения и др.) и усиления действия антидотов, показано применение ингибиторов ХЭ не проникающих через ГЭБ, например прозерина в виде 0,05% раствора по 3-5 мл внутримышечно
При выраженной тахикардии (порой угрожающей жизни) показаны препараты с -адреноблокирующим действием, например анаприлин (пропранолол), который следует вводить внутримышечно в дозе 2 мл 0,25% раствора. Блокируя -рецепторы синусного узла и обладая мембраностабилизирующим действием, эти препараты устраняют активирующее влияние на сердце симпатической иннервации и адреналина и нормализуют сердечный ритм.
После купирования (по возможности) проявлений острого психоза, пораженные должны быть эвакуированы в специализированные медицинские учреждения, и оставаться под наблюдением психиатра не менее недели. Длительность наблюдения определяют индивидуально в зависимости от тяжести перенесенной интоксикации
13.Галлюциногены. Токсикологическая характеристика диэтиламида лизергиновой кислоты. Механизм действия. Проявления интоксикации. Медицинская защита. Оказание помощи.
Итак, галлюциногены относятся к группе психодислептиков (см. также вопрос 11)
* сейчас будет немного информации из учебника С.А. Куценко "Основы токсикологии"(хороший учебник, кстати), ибо в Александрове информации и не особо по классификации и проч.
Пару слов о психодислептиках:
Психодислептики - это вещества, способные в минимальных дозах, в сотни - тысячи раз
меньше тех, в которых они вызывают угнетение сознания или соматические расстройства,
извращать психические процессы восприятия, эмоций, памяти, обучения, мышления, делать
поведение неадекватным реальной ситуации
Есть несколько классификаций:
I . По химическому строению (я сомневаюсь, что это нужно знать, но для общего развития почему бы и нет)
1. Производные триптамина
- диметилтриптамин
- буфотенин
- псилоцин
- псилоцибин
- диэтиламид длизергиновой кислоты (ДЛК) !!
- гармин
2. Фенилалкиламины
- мескалин
- 2,5-диметокси-4метиламфетамин
- 2,5-диметокси-4этиламфетамин
- триметоксифенизопропиламин
3. Пиперидилгликоляты
- атропин
- скополамин
- хинуклединилбензилат
- ВZ
4. Разные
- фенциклидин (сернил)
-тетрагидроканнабинол
II . Механизм действия
В основе токсических эффектов, развивающихся при интоксикации ДЛК, лежит способность блокировать центральные серотонинергические рецепторы. Однако далеко не все серотонинолитики обладают свойствами психодислептиков, поэтому этот механизм, вероятно не является единственным.
Особенностями действия ДЛК являются:
· способность угнетать спонтанную активность серотонинергических нейронов мозга и повышать уровень серотонина в ЦНС. 10 - 20 тысяч клеток (менее 0,1% нейронов), компактно залегающие в ядрах шва головного мозга, иннервируют все структуры ЦНС, особенно плотно - образования зрительного анализатора, лимбической системы, гипоталамуса. ДЛК не только блокирует проведение нервных импульсов в синапсах, образуемых окончаниями аксонов этих нейронов, но и подавляет их активность. В результате в нервных окончаниях накапливается нейромедиатор (в норме содержание серотонина в структурах мозга составляет 5 - 30 нг/мг белка) ATTENTION, mes amis!! ДЛК конкурентно с серотонином связывается практически со всеми серотониновыми рецепторами => серотонина всё больше и больше (как написано выше) , НО Александров пишет, что ДЛК вызывает истощение запасов серотонина, что по-моему (после всего прочитанного в других источниках скорее, а не "по-моему") не совсем правильно. Поэтому, вы уж выбирайте сами, что вам больше нравится...
· дофаминомиметическое действие; ДЛК активирует ДА-ергические нейроны нигростриальной, мезолимбической, тубероинфундибулярной систем мозга, при этом активируется процесс синтеза нейромедиатора, ускоряется его оборот в стриатуме, гипоталамусе, лимбических ядрах.
· слабое центральноле холинолитическое действие
· активация других катехоламинергических систем и их истощение
В общем, есть противоречия, поэтому как пишет Александров "Механизм токсического действия ДЛК остаётся более или менее вероятной гипотезой"
Механизм действия
«Структурой-мишенью» для ирритантов являются рецепторы рефлексогенных зон защитно-приспособительных рефлексов. Выделяют два механизма действия химических веществ на рецепторный аппарат:
1) Прямое действие на мембранные структуры (ингибирование арсинами SH-групп структурных белков; действие капсаицина на ионные каналы электровозбудимой мембраны)
2) Опосредованное действие: активация образования в покровных тканях медиаторов воспаления (брадикинина, простагландинов, серотонина и др.), которые вторично возбуждают рецепторный аппарат
Активация рецепторного аппарата → передача мощного афферентного потока на нейроны желатинозной субстанции, чувствительные ядра спинного мозга, ядра тройничного и языкоглоточного нервов → поступление сигнала с вышеперечисленных структур в вегетативные и двигательные ядра среднего и продолговатого мозга → формирование безусловных рефлексов (кашель, насморк, чихание, слезотечение, блефароспазм). Смысл этих реакций понятен – организм пытается «смыть» со слизистых вещество, вызвавшее мощную афферентацию.
Также возникает интенсивная боль или её патофизиологические аналоги (жжение, зуд). Болевые ощущения возникают в результате трёх процессов:
1) Возбуждение ноцицепторов
2) Чрезмерное возбуждение любого афферентного канала
3) Ослабление действия антиноцицептивной системы
Действие ирритантов – классический вариант рефлекторного действия «яда».
Основные клинические симптомы острого поражения веществами раздражающего действия в подавляющем большинстве случаев купируются достаточно быстро без каких-либо остаточных явлений. Клиническая картина острого отравления возникает при действии больших доз раздражающих веществ.
При поражении лёгкой степени развивается транзиторная токсическая реакция. Поражение сопровождается выраженным ощущением жжения в глазах, иногда чувством боли, блефароспазмом, редко – светобоязнью. При выходе из заражённой атмосферы явления раздражения сохраняются 2-4 минуты, затем прекращаются.
При более сильном поражении (средней степени тяжести) к явлениям раздражения глаз присоединяются проявления раздражения дыхательных путей: жжение во рту, носоглотке, в груди, обильная ринорея (насморк), саливация, мучительный сухой кашель, иногда кашель настолько упорный, что провоцирует рвоту. После выхода из очага поражения признаки поражения редуцируются в течение 20-30 минут.
Непереносимые субъективные ощущения, вызванные действием раздражающих веществ на слизистые глаз и дыхательных путей, объективно выражаются в слабой гиперемии гортани и полости носа, инъекция склер и сосудов слизистой оболочки зева.
При более длительной ингаляции развивается тяжёлое поражение, в процесс вовлекаются более глубокие отделы дыхательных путей, субъективно это выражается чувством удушья. Развиваются интенсивные загрудинные боли, боль иррадиирует в спину, голову, может развиться бронхоспазм. Большие дозы и длительная экспозиция могут вызывать рефлекторную остановку дыхания и сердечной деятельности. Причиной смерти, как правило, является токсический отёк лёгких.
Мероприятия медицинской защиты. Оказание помощи.
Современный (общевойсковой или гражданской обороны) фильтрующий противогаз надёжно защищает органы дыхания и глаза от воздействия ОВ раздражающего действия. При угрозе отравления АОХВ, обладающих выраженным раздражающим действием, следует применять противогазы со специальными фильтрующими элементами.
Для оказания первой помощи используется летучий анестетик фицилин. Он выпускается в ампуле в ватно-марлевой оплётке. Одна ампула содержит 0,894 г фторотана, 0,621 г циклогексана, 0,598 г бутилацетата и 0,04 г ментола. Ампула раздавливается, содержимое пропитывает оплётку, которую помещают под шлем-маску противогаза поражённого. Испаряясь, анестетик поступает в органы дыхания и прекращает поток афферентной импульсации. После выхода из зоны заражения необходимо промыть глаза и полость рта 2% раствором соды, при отсутствии – чистой водой. При стойком болевом синдроме пострадавший госпитализируется в лечебные учреждения для оказания врачебной помощи (используются различные летучие анестетики, при мучительном некупируемом кашле – вплоть до наркотических анальгетиков). Учитывая угрозу развития отёка лёгких, больные с тяжелыми формами поражений должны находиться под врачебным наблюдением не менее 48 часов.
16. Общеядовитое действие. Классификация отравляющих и высокотоксичных веществ общеядовитого действия. Ингибиторы цепи дыхательных ферментов. Токсикологическая характеристика синильной кислоты и ее соединений. Механизм действия. Проявления интоксикации. Медицинская защита. Оказание помощи.
(Описала подробно, может, даже чересчур, учебник + презентация)
Общеядовитое действие – токсическое действие химических веществ на механизмы биоэнергетического обмена в организме. Вещества, первичным механизмом которых является нарушение энергетического обмена, объединяются в группу веществ общеядовитого действия.
Деление энергетического обмена на внешнее дыхание (транспорт газов через аэрогематический барьер и газотранспортную функцию крови) и тканевое дыхание (биологическое окисление субстрата и окислительное фосфорилирование в митохондриях) обспечивает деление веществ общеядовитого действия на «яды» крови и тканевые «яды»
Яды гемоглобина
Гемолитические яды
Тканевые яды (тканевая гипоксия)
Ингибиторы цикла Кребса
Механизм действия.
«Структура-мишень» для циан-иона – хромопротеиды, содержащие железо в третьей валентности (с Fe 2+ цианиды НЕ взаимодействуют!). Взаимодействие цианидов с трёхвалентной формой железа цитохрома а3-цитохромоксидазы обеспечивает утрату способности цитохромоксидазы переносить электроны на молекулярный кислород (короче говоря, система летит к чертям).
Таким образом, цианиды угнетает цепь дыхательных ферментов → блокируется вся дыхательная цепь → развивается тканевая гипоксия. Кислород из артериальной крови не усваивается тканями и переходит в неизменном виде в венозную кровь → венозная кровь высокооксигенирована → падение артериовенозной разницы по кислороду до нуля → розовая окраска слизистых и кожных покровов.
Взаимодействие с другими биомишенями:
- Блокада металлсодержащих ферментов (металлы переменной валентности). Блокада ферментов антиоксидантной защиты (КТ, ГР, ГП, СОД).
- Угнетение пиридоксалевых ферментов (глутаматдекарбоксилазы), что ведет к дефициту ГАМК и глутамата. Активирование гуанилатциклазы, что ведет к увеличению концентрации цГМФ в ткани мозга и объясняет судорожную активность.
- Взаимодействие с элементами системы регуляции внутриклеточного Са+2, что ведет к нарушению поддержания необходимого уровня ассиметричности концентрации его внутри клетки и, следовательно, к тяжелым дезинтеграционным процессам в клетках.
Медицинская защита
-использование индивидуальных технических средств защиты (средства защиты органов дыхания) в зоне химического заражения; участие медицинской службы в проведении химической разведки; проведение экспертизы воды и продовольствия на зараженность; запрет на использование воды и продовольствия из непроверенных источников.
Основные направления антидотной терапии:
· Связывание цианидов с образованием нетоксичных соединений
· Поставка ложного субстрата в виде метгемоглобина крови
· Стимуляция метаболизма цианидов (детоксикация)
· Активация тканевого дыхания
Глюкоза → образует с цианидами стойкие малотоксичные соединения – циангидрины (химический механизм антидотного действия). Вводят в/в 20-25 мл 40% раствора.
Метгемоглобинообразователи – вещества, которые окисляют двухвалентное железо гемоглобина до трёхвалентного состояния → метгемоглобин является «донором» трёхвалентного железа для цианидов. Следует помнить о том, что метгемоглобин с кислородом не связывается, поэтому нужно применять строго определённые дозы метгемоглобинобразователей, изменяющие не более 25-30% гемоглобина. К их числу относятся нитрит натрия, амилнитрит, антициан, метиленовый синий.
Амилнитрит – антидот первой помощи, ампулу в ватно-марлевой обёртке следует раздавить и заложить под маску противогаза, при необходимости повторить. Наиболее доступным метHbобразователей является нитрит натрия (готовят ex tempore). Вводят в/в 10-20 мл 1-2% раствора. Но при этом нитрит натрия является врачебным антидотом. Антициан – врачебный антидот, первое введение при отравлении производится в объёме 1 мл в/м или 0,7 мл в/в. При внутривенном введении препарат разводят в 10 мл 25-40% раствора глюкозы или 0,85% раствора NaCl. Скорость введения 3 мл в минуту. При необходимости через 30 мин антидот может быть введен повторно в дозе 1,0 мл (только внутримышечно). Еще через 30 мин можно провести третье введение.
Частичным метHbобразующим действием обладает метиленовый синий. Основное его действие – активация тканевого дыхания. Вводят в/в в виде 1% раствора в 25% растворе глюкозы по 50 мл.
Цианид в организме вступает в реакцию конъюгации с эндогенными серосодержащими соединениями с образованием малотоксичных роданистых соединений (CNS-). При введении тиосульфата натрия скорость конъюгации возрастает в 15-30 раз, что является обоснованием использования вещества в качестве дополнительного антидота на фоне применения метHbобразователей. Вводят в/в по 50 мл 30% раствора.
Препараты, содержащие кобальт, образуют прочные связи с циан-ионом. Однако неорганические соединения кобальта сами обладают высокой токсичностью. Показана активность гидроксикобаламина (витамина В12), но препарат очень дорог. Наименее токсичным и эффективным оказалась кобальтовая соль этилендиаминтетраацетата (ЭДТА), но в РФ он не используется
Отравляющие и высокотоксичные вещества, образующие карбоксигемоглобин. Токсикологическая характеристика оксида углерода. Механизм действия. Проявления интоксикации. Медицинская защита. Оказание помощи
Механизм действия
«Структурой-мишенью» для оксида углерода являются хромопротеиды, содержащие двухвалентное железо. Оксид углерода активно взаимодействует с многочисленными гемсодержащими протеидами: гемоглобином, миоглобином, цитохромами дыхательной цепи и др. (рис. 13). С трехвалентным железом вещество не взаимодействует.
В первую очередь оксид углерода, проникший в кровь, вступает во взаимодействие с двухвалентным железом гемоглобина (НЬ) эритроцитов, образуя карбоксигемоглобин (НЬСО). Относительное сродство гемоглобина к оксиду углерода (СО) примерно в 300-350 раз выше, чем к кислороду. Карбоксигемоглобин не способен транспортировать кислород. Развивается гемический тип гипоксии.

Дополнительным механизмом токсического действия СО на гемоглобин является механизм нарушения кооперативного взаимодействия. Молекула гемоглобина состоит из четырех субъединиц. Присоединение кислорода к одной единице облегчает присоединение к трем остальным. Этот феномен описывается как кооперативное взаимодействие гемоглобина, которое объясняет «S-образный» характер «кривой Холдена», описывающей насыщение кислородом гемоглобина (рис. 14). В диапазоне концентраций кислорода 20—30 мм рт. ст. происходит не линейное, а лавинообразное насыщение гемоглобина кислородом.
 |
Как было показано Дж. Холденом в его классических опытах по физиологии дыхания, угарный газ нарушает так называемое гем-гем-взаимодействие. Присоединение СО хотя бы к одной субъединице гема резко повышает сродство кислорода к железу гема. В результате процесс диссоциации НЬО в тканях резко затрудняется, т. е. остальные три субъединицы гема «не работают». При взаимодействии CO с двухвалентным железом гемоглобина валентность последнего не изменяется, зато происходит перестройка характера связей железа, т.е. ионные связи кислорода с Hb становятся ковалентными. Затруднение диссоциации гемоглобина при интоксикациях угарным газом получило название эффекта Холдена.
Угарный газ взаимодействует не только с гемоглобином, но также с цитохромами цепи дыхательных ферментов, угнетая тем самым биоэнергетические процессы в тканях. Цитохромы становятся уязвимыми в состоянии Fe+I, в котором они находятся в условиях гипоксии. Так замыкается «порочный круг»: инактивация гемоглобина приводит к гипоксии, которая усугубляется ингибированием цепи дыхательных ферментов.
Угарный газ активно взаимодействуете миоглобином. Миоглобин — мышечный аналог гемоглобина, состоящий из одной молекулы глобина, связанной с гемом, в поперечно-полосатой мускулатуре выполняет функцию депо кислорода. Взаимодействие оксида углерода с миоглобином приводит к образованию карбоксимиоглобина. Нарушается обеспечение работающих мышц кислородом. Этим объясняют развитие у отравленных такого типичного для отравлений угарным газом симптома, как брутально выраженная мышечная слабость. Образованием карбоксимиоглобина на объясняют другой типичный симптом: розовое окрашивание кожных покровов. Однако следует иметь в виду, что этот симптом выражен, как правил о, при ингаляции «чистого» угарного газа, например при нарушении правил пользования печами.
Проявления интоксикации
Раздражающим действием оксид углерода не обладает, поэтому контакт с веществом остается незамеченным («немой контакт»).
Тяжесть клинической картины отравления угарным газом определяется:
Ø содержанием СО во вдыхаемом воздухе
Ø длительностью воздействия
Ø интенсивностью физической активности пострадавшего
Ø Потребностью организма в кислороде.
Существует корреляция между уровнем карбоксигемоглобина в крови и выраженностью клинической картины отравления (табл. 19).

По степени тяжести острое отравление принято подразделять на легкое, среднее и тяжелое.
Легкая степень отравления формируется при действии относительно невысоких концентраций угарного газа. Она характеризуется сильной головной болью, головокружением, шумом в ушах потемнением в глазах, ощущением «пульсации височных артерий». Пораженные постепенно теряют сознание. Развиваются тахикардия, повышение артериального давления, одышка как компенсаторные реакции на гипоксию. При прекрашении поступления яда в организм все перечисленные симптомы в течение нескольких десятков минут-часа проходят без каких-либо последствий.
При продолжительном поступлении оксида углерода в организм (при утрате сознания или во сне) или при действии более высоких концентраций развивается отравление средней степени тяжести. Сознание «затемняется», угнетается до уровня оглушения — сопора (больной в ответ на внешние стимулы может лишь издавать нечленораздельные звуки и выполнять некоординированные движения). Появляется выраженная мышечная слабость. Слизистые оболочки и кожа приобретают розовую окраску. Одышка усиливается, пульс учащается. Артериальное давление после кратковременного подъема, связанного с возбуждением симпатико-адреналовой системы и выбросом катехоламинов из надпочечников, снижается. При отравлении средней степени тяжести в большинстве случаев через несколько часов после прекращения действия яда состояние пострадавших практически полностью нормализуется. Могут в течение 2 -3 сут сохраняться головная боль, сонливость, головокружение, лабильность пульса и артериального давления (развивается астенический синдром).
Тяжелое отравление характеризуется быстрой потерей сознания вплоть до комы (больной не реагирует на внешние стимулы и болевые раздражения). На высоте гипоксии могут развиться судороги клонико-тонического характера (некоординированные сокращения больших мышечных групп). Кожные покровы и слизистые оболочки могут приобрести ярко-розовый цвет: признак высокого содержания карбоксигемоглобина в крови и образования карбоксимиоглобина. Если в этот период пострадавший не погибает, то он длительное время (до 12-24 ч) находится в коме. При длительности комы более трех суток прогноз становится неблагоприятным. При отсутствии эффективной помощи и лечения больной может погибнуть от нарастающей дыхательной и сердечно-сосудистой недостаточности. При благоприятном течении отравления и своевременном оказании медицинской помощи симптомы интоксикации исчезают и через 3—5 дней состояние пострадавшего нормализуется.
В случае высокого содержания во вдыхаемом воздухе оксида углерода (1 -3 об.%) на фоне пониженного парциального давления кислорода (до 9 -1 2 об.%) — ситуация, возникающая при больших пожарах — может развиваться молниеносная форма отравления. Пораженный быстро (практически мгновенно) теряет сознание, происходит рефлекторная остановка дыхания, реже — сердечной деятельности. Развиваются генерализованные судороги. Наступает смерть. Механизм остановки дыхания при молниеносной форме рефлекторный. Сверхбольшая концентрация СО вызывает перевозбуждение хеморецепторов каротидного гломуса. Избыточная афферентация из каротидного гломуса вызывает запредельное торможение в стволовых центрах — дыхательном и сосудодвигательном. Дыхание останавливается. .
В презентации выделяются также:
Синкопальная форма отравления – характеризуется наличием нарушений сердечно-сосудистой системы: падением АД и обморочным состоянием. Дыхание частое, прерывистое, поверхностное. Резко выражена бледность кожных покровов (белая асфиксия).
Эйфорическая форма отравления – пострадавший возбужден, может совершать немотивированные поступки.
Медицинская защита
В качестве технических средств защиты от угарного газа используют противогазы. Обычный фильтрующий противогаз не «задерживает» (не сорбирует) угарный газ. Для защиты органов дыхания используется специальный гопкалитовый патрон, который содержит катализатор — гопкалит — смесь двуокиси марганца (60%) и окиси меди (40%), на поверхности которого оксид углерода окисляется до двуокиси углерода. Гопкалитовый патрон по форме напоминает обычный противогазный фильтр. Гопкалитовый патрон присоединяется через гофрированную трубку к шлем-маске противогаза, что и обеспечивает защиту. Гопкалитовый патрон не эффективен при концентрации оксида углерода более 1 об. %. При больших концентрациях угарного газа должен использоваться изолирующий противогаз.
Также для профилактики используется ацизол (см. ниже).
Оказание помощи
Антидотная терапия
Транспорт кислорода от легких к тканям осуществляется двумя способами: 1) гемоглобином в форме оксигемоглобина (НЬО) и 2) плазмой свободно растворенного кислорода. Кислородная емкость крови складывается из оксигемоглобина и растворенного кислорода. В форме оксигемоглобина переносится 20 мл на 100 мл крови. В растворенном состоянии плазмой крови переносится около 0,2 мл 0 2 на 100 мл крови, В нормальных условиях эта величина не имеет практического значения. Однако растворимость кислорода как любого газа прямо пропорционально зависит от давления газа над жидкостью: чем больше давление, тем больше газа растворяется в жидкости. Оказывается, что при увеличении давления воздуха до 1,5 атм кислорода, растворенного в плазме, становится достаточно для поддержания нормального уровня дыхания. Такой метод «подачи» кислорода получил название «оксигенобаротерапия (ОБТ)»: терапия кислородом (оксигено-) под повышенным давлением (баро-). Синонимичный термин — «гипербарическая оксигенация» (ГБО).
Таким образом, кислород является антидотом угарного газа. Механизм антидотного действия кислорода складывается из следующих процессов:
1)транспорт к тканям и замещение ингибированного гемоглобина — физиологический механизм; 2) ускорение диссоциации карбоксигемоглобина — биохимический механизм;
3) стимуляция цитохромоксидаз тканевого дыхания.
В идеале кислород должен подаваться под давлением, но это не всегда возможно. При отсутствии технической возможности провести ОБТ необходимо обеспечить ингаляцию кислорода при обычном давлении.
Современным антидотом угарного газа является препарат «Ацизол» (бис-(1-виниламидазол)-цинкдиацстат) — комплексное соединение цинка, которое при действии на гемоглобин способствует восстановлению кооперативного взаимодействия гемов, уменьшает сродство гема к оксиду углерода. Также он ослабляет ближайшие последствия выраженного кислородного голодания тканей и жизненно важных органов, уменьшает осложнения и отдаленные последствия интоксикации.
Препарат рекомендуют применять внутримышечно в форме 6% раствора на 0,5% растворе новокаина в объеме 1,0 мл на человека в возможно более ранние сроки после воздействия СО. В случае тяжелого отравления допускается повторное введение анизола в той же дозе не ранее чем через 1 ч после первой инъекции.
Применение ацизола не заменяет проведения оксигенотерапии. Неоспоримым преимуществом ацизола является возможность его профилактического использования. При угрозе острого воздействия угарного газа препарат может быть введен профилактически за 10—15 мин до входа в аварийную зону (например, такое применение препарата возможно личным составом аварийно-спасательных партий при планируемом входе в зараженную атмосферу). Назначение средств, возбуждающих дыхание и сердечную деятельность (дыхательных н сердечных аналептиков типа кордиамина, кофеина, бемегрида, этимизола и пр.) на фоне гипоксии и угнетения дыхания противопоказано! В условиях гипоксии введение таких средств у тяжело пораженных вызывает после небольшого «пробуждающего действия» более глубокое угнетение ЦНС и ухудшение состояния.
18. Спирты. Токсикологическая характеристика. Механизм действия. Проявления интоксикации. Профилактика отравлений. Оказание помощи.
Учебник: (в презентах нет ничего)
СПИРТЫ относятся к неэлектролитам (немного общей инфы, но можно листать сразу к этанолу и тд).
Неэлектролиты: 1) предельные углеводороды (бензин, керосин, природный газ и пр.); 2 )спирты (метанол, этанол, пропанол, этиленгликоль и др.); 3)галлогенированные (хлорированные) углеводороды (дихлорэтан, фреоны и др.); 4) непредельные углеводороды (ацетон).
Все эти вещества имеют различное химическое строение, но обладают рядом сходных свойств: 1)они либо не растворяются в воде, либо их водные растворы не проводят электрический ток — являются неэлектролитами; 2) обладают высокой растворимостью в жирах и, следовательно, в липидах биомембран; 3)при поступлении в организм проявляют свойства наркотиков — вызывают угнетение ЦНС, что выражается выключением сознания вплоть до комы — так называемое неэлектролитное действие; 4) неэлектролитное действие носит дозозависимый характер — чем больше доза неэлектролита, тем глубже угнетение ЦНС: в зависимости от тяжести отравления развиваются сонливость — оглушение — сопор — кома
Причины массовых поражений неэлектролитами:
1) разрушение химических заводов по производству полимерных пластмасс, азотистых удобрений, лакокрасочных материалов и пр
2) нарушение техники безопасности (ТБ) на химических пред приятиях
3) использование средств объемного пожаротушения на основе фреонов
4) аварии на газопроводах
5) аварийные ситуации при эксплуатации современной автотракторной техники (бензин, тосол, тормозная жидкость, антифризы, гидравлические жидкости, омыватели стекол)
6) острые отравления при употреблении ЯТЖ («ядовитые технические жидкости» - омывайку выпить) с целью опьянения. = «суррогаты алкоголя».
Механизм токсического действия неэлектролитов складывается из двух процессов:
1)действие целой молекулы — собственно неэлектролитное действие: дозозависимое угнетение ЦНС вплоть до комы; 2)специфическое органотоксическое действие метаболитов
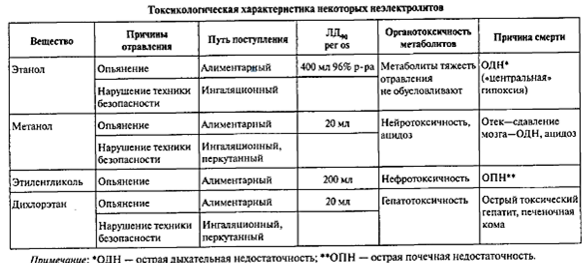
Основной системой метаболизма неэлектролитов является система цитохром Р-450-зависимых оксидаз смешанных функций печени. В результате окисления из исходных веществ образуются высокотоксичные метаболиты. = «токсификация» или «летальный синтез». Для некоторых веществ — метанол, этиленгликоль — важную роль в токсификации играет алкогольдегидрогеназа печени.
 Причины смерти: либо (1) в чрезмерном угнетении ЦНС и угнетении (остановке) дыхания — развитие острой гипоксической («центральной») гипоксии; либо 2) при дозах, не вызывающих столь глубокого угнетения ЦНС, — в результате специфического органотоксического действия метаболитов.
Причины смерти: либо (1) в чрезмерном угнетении ЦНС и угнетении (остановке) дыхания — развитие острой гипоксической («центральной») гипоксии; либо 2) при дозах, не вызывающих столь глубокого угнетения ЦНС, — в результате специфического органотоксического действия метаболитов.
Этанол
*можно сказать про то, что используют алкоголь и его суррогаты для повышения настроения и можно лить любую другую «воду» про то, как это влияет на популяцию.
Этиленгликоль.
Источники контакта: современные технические средства, автотракторная техника, теплоносители в некоторых системах отопления.
Причина отравления: ошибочное употребление вещества с целью алкогольного опьянения.

Физико-химические свойства: этиленгликоль это двухатомный спирт, входит в состав антифризов, гидравлических, тормозных жидкостей. Сиропообразная сладковатая жидкость без запаха (!). Хорошо растворим в воде и спиртах. Малолетуч, соответственно, ингаляционное поступление маловероятно.
Абсолютно смертельная доза – 100-150 мл.
Токсикокинетика: отравления этиленгликолем возможны лишь при приёме его внутрь в качестве суррогата алкоголя или по ошибке. Этиленгликоль очень быстро адсорбируется в желудке и распределяется в тканях организма. Наибольшее количество накапливается в печени и почках.
Основной путь превращения этиленгликоля – ферментативное окисление, происходящее с участием алкогольдегидрогеназы. В результате метаболизма этиленгликоля накапливаются кислые продукты – щавелевая кислота, гликолаты.
Период полудетоксикации = 3 часа, но при приёме большого количества этиленгликоль определяется в крови на протяжении суток.
Механизм токсического действия: 1. Неэлектролитное действие целой молекулы 2. Токсические метаболиты (щавелевая кислота, гликолевый и глиоксалевый альдегид) → метаболический ацидоз. Ключевой метаболит – щавелевая кислота, которая образует нерастворимые соли – оксалаты кальция. Они, выпадая в осадок в виде кристаллов октаэдрической формы в почечных канальцах, вызывают повреждение почек. Аналогичные процессы идут в печени, при больших дозах – в мозге.
Пути формирования ацидоза аналогичны тем, которые формирует метанол. В крови рН при тяжёлом отравлении этиленгликолем может быть 6,9 и менее, это очень опасно…
Основные проявления интоксикации:
1. начальный период – отчётливое опьянение (дозозависимый эффект). При тяжёлых отравлениях опьянение переходит в оглушение, затем – в кому. На данном этапе больной может умереть от дыхательной недостаточности.
2. токсическая энцефалопатия – пациент засыпает на высоте опьянения, просыпается через 2-12 часов с головной болью, головокружением, тошнотой, повторной рвотой, обшей слабостью, ознобом и т.д.
3. почечная недостаточность – неукротимая жажда, отёки, анурия. Нарушения электролитного баланса. Угнетение сознания, кома (уремическая?)
Причины смерти: некомпенсируемый ацидоз, острая почечная недостаточность.
Лечение: мероприятия аналогичны таковым, как при отравлении метанолом. При оказании первой помощи вызвать рвоту, промыть по возможности желудок, +сорбенты (активированный уголь). Гемодиализ, форсированный диурез, перитонеальный диализ.
Антидот – этанол (1 г/кг*ч).
Еще желательно вводить MgSO4 25% в/в (уменьшает кристаллообразование).
Добавления по лекции и по практике:
Гликоли относятся к спиртам (I-III класс неэлектролитов) → их коэффициент Овертона-Мейера составляет менее 10-3 – 100. (чем выше коэффициент, тем сильнее наркотическое действие).
Этиленгликоль – специфическое нефротоксическое действие. До 50% отравлений заканчиваются летальным исходом. Относится ко второй группе суррогатов алкоголя (без примесей этанола, но с похожим действием).
Дифференциальная диагностика от отравления метанолом – нет нарушений зрения.
При выпадении в осадок оксалатов кальция → снижение уровня кальция в крови → аритмии. Соответственно при лечении таких отравлений, нужно бы ещё препараты кальция добавлять в инфузию.
20. Галогенированные углеводороды. Токсикологическая характеристика дихлорэтана. Механизм действия. Проявления интоксикации. Профилактика отравлений. Оказание помощи.
Начнем с тог, что дихлорэтан относится к неэлектролитам.
Источники контакта: лакокрасочные материалы, растворители, клеи, смолы и проч.
Причины острых отравлений дихлорэтаном:
1) ошибочное употребление вещества с целью алкогольного опьянения;
2) нарушение техники безопасности при работе с веществами, содержащими дихлорэтан: а) покрасочные работы в плохо вентилируемом помещении б) чрескожное отравление при случайном разливе на кожу и длительном контакте с дихлорэтаном.
Физико-химические свойства. Дихлорэтан – бесцветная жидкость с характерным резким эфирным запахом. Высоколетуч (быстро испаряется при нормальных условиях). В воде практически не растворяется. Хорошо растворяется в жирах и органических растворителях – хорошо проникает через гистогематические барьеры. Все перечисленные свойства дихлорэтана обусловливают его универсальный характер с точки зрения путей поступления: может поступать ингаляционно, алиментарно, перкутанно.
Смертельная доза дихлорэтана для человека составляет 10-25 мл.
Токсикокинетика. Основной путь превращения — ферментативное окисление, которое происходит при участии цитохром Р-450- зависимых оксигеназ смешанных функций в печени. В процессе биотрансформации образуются активные радикалы и достаточно стабильны химические вещества: хлорэтанол, монохлоруксусная кислота и др. Эти вещества превышают токсичность дихлорэтана в 2-10 раз - «летальный синтез».
Механизм токсического действия дихлорэтана имеет фазный характер. На первом этапе отравление обусловлено незначительным неэлектролитным действием целой молекулы. На втором этапе клиника отравления определяется цитотоксичным поражением печени и в меньшей степени почек, что связано действием токсичных метаболитов.
Основные проявления интоксикации. В течении отравления дихлорэтаном основное значение занимает острая печеночная недостаточность (острый токсический гепатит). Больные погибают на высоте печеночной комы.
Следующая информация из методички Ставропольского меда... Много и довольно коряво... Но вот...
Начальный период обусловлен наркотическим действием яда, выраженность которого определяется концентрацией ДХЭ и временем пребывания человека в загазованном помещении. В начале пострадавшие ощущают своеобразный запах и сладковатый привкус во рту, одновременно могут отмечаться явления раздражения дыхательных путей (кашель, чихание) и слизистых оболочек глаз. Наркотическое действие яда в легких случаях проявляется в виде астенического синдрома (головная боль, общая слабость, головокружение), состояния, напоминающего опьянение; нередко возникает тошнота и рвота.
В более тяжелых случаях наблюдается дезориентация, агрессивность, немотивированные действия, сопор и кома.
При легких интоксикациях астенический и гастроинтестинальный синдромы длятся в течение 3-7 суток. На 2 или 3 сутки можно выявить незначительные изменения, указывающие на поражение печени и почек без существенных нарушений их функции (нефропатия и гепатопатия I степени).
При тяжелых отравлениях в фазе наркотического действия яда наблюдается кома.
При крайне тяжелых интоксикациях кома сопровождается развитием острой сердечно-сосудистой недостаточности, параличом дыхательного центра. В отдельных случаях спустя 1-8 часов сознание постепенно проясняется, улучшается гемодинамика. Наступает период относительного благополучия (или временного улучшения). Однако уже к концу 1 суток состояние вновь ухудшается – появляются тошнота, рвота (нередко неукротимая и с кровью), понос, боли в животе, повышается температура. Сердечно-сосудистая недостаточность по существу является отражением интоксикационного шока, плохо поддается терапии и является главной причиной смертельного исхода в этом периоде.
При небольшой концентрации яда в воздухе и значительной экспозиции может развиться клиника тяжелой интоксикации без предшествующего наркотического эффекта. В этом случае диагноз интоксикации часто бывает ошибочным, т.к. не выявляются причинно-следственные связи (первые симптомы интоксикации наступают через 8-24 часа, а иногда и более после контакта с ядом).
Проявление отравления часто трактуется как пищевая токсикоинфекция, острый гастроэнтерит, почечная колика, аппендицит, грипп, холецистопанкреатит, внутреннее кровотечение и др. У некоторых больных на 2 или 3 сутки наряду с примесью крови в рвотных массах и стуле появляются симптомы поражения печени, боли в правом подреберье, иктеричность (могут встречаться и безжелтушные формы гепатита), обесцвечивание стула, увеличение размеров печени, поражение почек (жажда, боли в пояснице и животе, одутловатость лица, уменьшение или полное прекращение мочеотделения). Максимум проявлений почечно-печеночной недостаточности приходится на конец 1-й, начало 2-й недели отравления. При этом следует отметить определенную последовательность в развитии патологического процесса: сначала доминирует клиника печеночной, а затем почечной недостаточности. Почечно-печеночная недостаточность является главной причиной смертельного исхода в этом периоде. Стадия восстановления начинается после разрешения острой почечной недостаточности со 2-3 недели интоксикации. Еще длительное время сохраняются функциональная недостаточность печени и почек, астеническое состояние.
Еще нашла информацию, что сам дихлорэтан и его метаболиты повреждают эндотелий à падение ОЦЖ, сгущение крови à экзотоксический шок.
Основные методы лечения. Средства антидотной терапии для острых отравлений дихлорэтаном не созданы. В порядке оказания первой помощи необходимо вызвать рвоту. При возможности - промыть желудок сорбентом (активированным углем). По возможности в кратчайшие сроки для удаления всосавшегося яда произвести гемодиализ, форсированный диурез, перитонеальный диализ. Левомицетин 2-10мг\сут-ингибирует микросомальные ферменты печени.
Антидот (от anti dotum – «даваемое против») – применяемое при лечении острого отравления лекарственное средство, способное обезвреживать токсичное вещество, предупреждать или устранять вызываемый им токсический эффект.
Условия, необходимые для отнесения ЛВ к антидотам:
· терапевтическая эффективность ЛВ при лечении острого отравления
· наличие механизмов антидотного действия: 1) способность антидота «нейтрализовать» токсичное вещество, 2) способность антидота защищать структуру-мишень от действия токсиканта, 3) способность купировать/ снижать тяжесть последствий от повреждения структуры-мишени (обеспечивать более легкое течение интоксикации).
Антидотные препараты относятся к этиотропным средствам терапии (мы помним, что существуют еще патогенетические и симптоматические средства).
Механизмы действия антидотов:
1. Химический. Антидоты с данным типом действия способны непосредственно связываться с токсикантом и образовывать нетоксичные (или малотоксичные) соединения, которые быстро выводятся из организма. Могут связываться со свободными молекулами (циркулирующими в крови), с находящимися в депо, а также вытеснять молекулы токсиканта из связи со структурой-мишенью. Ex: комплексообразователи при отравлении солями тяжелых металлов, унитиол при отравлении люизитом или сердечными гликозидами.
2. Биохимический. Здесь несколько подтипов:
· Вытеснение токсиканта из его связи с биомолекулой-мишенью => восстановление поврежденных биохимических процессов (ex: реактиваторы холинэстеразы при острых отравлениях фосфорорганическими веществами)
· Поставка ложной мишени для токсиканта (ex: метгемоглобинообразователи при отравлении цианидами)
· Компенсация нарушенного токсикантом количества и качества биосубстрата
3. Физиологический. Способность антидота нормализовать функциональное состояние организма. Такие препараты не вступают с ядом в химическое взаимодействие!
· Стимуляция уравновешивающей функции (ех: холиномиметики при отравлении холинолитиками)
· Замещение утраченной функции (ех: проведение оксигенотерапии при отравлении угарным газом)
4. Модификаторы метаболизма.
· Препятствуют процессу токсификации ксенобиотика - превращению в организме индифферентного ксенобиотика в высокотоксичное соединение (ех: этанол при отравлении метанолом)
· Резко ускоряют биодетоксикацию вещества (ех: тиосульфат натрия при отравлении цианидами)
Помните: использование антидотов при отсутствии в организме специфического токсиканта может привести к отравлению антидотом. Поэтому! Использование антидота должно быть обоснованным и адекватным как по времени, так и по дозе.
Существуют:
· Антидоты первой помощи. Обладают высокой эффективностью и хорошей переносимостью, не вызывают тяжелой интоксикации при ошибочном использовании. Используются для максимально быстрого введения в условиях массового поражения. Ех: афин при отравлении фосфорорганическими средствами (фос).
· Врачебные антидоты. Более мощные ЛВ, требующие профессиональных знаний для их применения. Используются на этапах медицинской эвакуации. Ех: атропин при отравлении фос.
· Профилактические антидоты. Используются для заблаговременной защиты при высокой вероятности химического поражения. Ех: ингибиторы холинэстеразы при отравлении фос.
Далее очень важная таблица, которую вам нужно зазубрить (или вспомнить хорошо забытое). По слухам это любят спрашивать на экзамене, да и в жизни пригодится.
| Группа | Антидот |
| Фосфорорганические вещества: Инсектициды (дихлофос) БОВ (зарин) | Атропин + симптоматическая терапия Реактиваторы холинэстеразы (афин, будоксим) |
| Опиаты | Налоксон (нельзя при ацидозе, возможен отек мозга в результате гипоксии) |
| 1,4-бензодиазепины (феназепам) | Флумазенил (по словам Кузнецова мало эффективен, только в терапевтических дозах) |
| Холинолитики (атропин) Амитриптилин (трициклический а/д) Азалептин (атипичный нейролептик) | Ингибиторы холинэстеразы (прозерин, галантамин, аминостигмин) |
| Угарный газ | Гипербарическая оксигенация Ацизол (препятствует образованию карбоксигемоглобина) |
| Сердечные гликозиды (коргликон, строфантин) | Антитела к гликозидам Унитиол, тиосульфат натрия |
| Парацетамол | АЦЦ |
| Варфарин | Витамин К Свежезамороженная плазма |
| Метиловый спирт | Этанол |
| Тяжелые металлы | Берлинская лазурь (для таллия) Унитиол Тиосульфат натрия |
| Клофелин | Метоклопрамид (церукал) |
| Дихлорэтан | Левомицетин |
| Противотуберкулезные аб (изониазид) | Пиридоксин (вит В6) |
| Цианиды | Тиосульфат натрия Сахара Амилнитрит, нитроглицерин |
22. Общие принципы оказания неотложной помощи при острых интоксикациях. Основные принципы оказания первой, доврачебной и первой врачебной помощи при острых отравлениях
Пути поступления ядов (и идентичные им токсикокинетические виды отравлений)
Ø Алиментарный
Ø Ингаляционный
Ø Перкутанный
Ø Парентеральный (инъекционный: п/к, в/м, в/в)
Ø Интраназальный
Ø Сублингвальный
Кроме перечисленных «классических» путей поступления ядов в организм в современной клинической и судебной токсикологии существуют примеры менее традиционных путей поступления: ректального, вагинального, введения вещества в раневую поверхность, размещения имплантата под кожей, введения вещества в слуховой проход и др.
Токсичность, опасность. Определение токсичности. Основные регламенты (показатели) опасности. Пороговый и беспороговый принцип формирования токсического процесса.
Токсичность – свойство веществ, которое можно измерить
Измерение токсичности - определение КОЛИЧЕСТВА вещества, действуя в котором, оно вызывает различные формы токсического процесса. Чем в меньшем количестве вещество вызывает токсический процесс, тем оно токсичнее.
Опасность вещества – совокупность его свойств, определяющих вероятность вредного действия (вероятность попадания вещества в организм) в реальных условиях его производства и применения.
Токсикометрия - раздел токсикологии, в рамках которого количественно оценивается токсичность и опасность веществ.
1933 г. - Н.С.Правдин, термин «Токсометрия»
Определение токсичности веществ осуществляется в экспериментах на разных видах лабораторных животных, математически переносится для человека и уточняется в условиях клиники, в популяционных исследованиях.
Для обозначения количества вещества, действующего на биологический объект, используют понятие «доза».
Токсическая доза (D) – количество вещества, попавшее во внутренние среды организма (в/ж, ч/к, в/в, в/м) и вызвавшее токсический эффект.
Токсическая доза (D) выражается в единицах массы вещества на единицу массы организма :
мкг/кг; мг/кг; г/кг; Моль/кг; г/чел
Токсическая концентрация (С) – количество вещества, находящееся в единице объема (массы) некоего объекта окружающей среды (воздуха, воды, почвы), при контакте с которым развивается токсический эффект.
Токсическая концентрация (С) выражается в единицах массы или объема токсиканта на единицу объема среды (воздух, вода) - мг/л; г/м3; см3/м3; p. p. m. (части на миллион) или на единицу массы среды (почвы, продовольствия) – мг/кг; г/кг.
При расчете токсических доз веществ (W), действующих в виде пара, газа или аэрозоля учитывают не только токсическую концентрацию (С), но и время пребывания человека в зараженной атмосфере (t).
W = C . t ( мг . мин/м3 ), где W – токсодоза при ингаляции
Формула нобелевского лауреата Фрица Габера (1915г. Германия, ОВ)
При расчете токсодозы допускается, что одинаковый эффект наблюдается как при кратковременном действии токсиканта в высокой концентрации, так и при продолжительной аппликации малых концентраций вещества, то есть:
C.t=const (справедливо для веществ, обладающих способностью к кумуляции)
В токсикологии чрезвычайных ситуаций различают следующие токсические дозы (D) и концентрации (C) :
v эффективные
v смертельные
v выводящие из строя (непереносимые)
v пороговые
ED – эффективная доза (от англ. Effective Dose) – количество токсиканта, вызывающее при попадании в организм определенный токсический эффект (судороги, кардиотоксический, гепатотоксический, нефротоксический и пр. ).
ED50 – среднеэффективная доза (медианная)
EC50 – среднеэффективная концентрация (медианная)
Цифровой индекс – вероятность наблюдения эффекта в процентах, может иметь значение от 0 до 100.
LD – смертельная доза (от англ. Lethal Dose) – количество токсиканта, вызывающее при попадании в организм смертельный исход.
LD50 – среднесмертельная (медианная) доза
LС50 – среднесмертельная (медианная) концентрация
LС t50 – среднесмертельная (медианная) доза при ингаляции
ID – выводящая из строя доза (от англ. Incapacitating Dose) – количество токсиканта, вызывающее при попадании в организм выход из строя определенного процента пораженных как временно, так и со смертельным исходом.
ID50 – средняя выводящая из строя доза
IC50 – средняя выводящая из строя концентрация
pD – пороговая доза (от англ. Primary Dose) – количество токсиканта, вызывающее при попадании в организм начальные признаки действия вещества.
pD50 – средняя пороговая (медианная) доза
pC50 – средняя пороговая (медианная) концентрация
Lim D – пороговая доза (от лат. Limen – порог)
Lim C – пороговая концентрация
| Название дозы | Обозначение дозы при путях поступления | Эффект | |
| в/ж, ч/к, в/м, в/в | Ингаляционно | ||
| Среднеэффективная доза | ED50 | ECt50 | Токсический эффект у 50% пораженных |
| Среднесмертельная доза | LD50 | LCt50 | Гибель у 50% пораженных |
| Средняя выводящая из строя доза | ID50 | ICt50 | Выход из строя 50% пораженных |
| Пороговая доза | pD50 | pCt50 | Начальные симптомы у 50% пораженных |
| Предельно допустимая концентрация (количество) | ПДК | ПДК | Отсутствие эффектов поражения |
| Максимально допустимая концентрация (количество) | МДК | МДК | Отсутствие эффекта поражения при кратковременном воздействии (аварийный регламент) |
Токсический процесс на клеточном уровне проявляется:
-обратимыми структурно-функциональными изменениями клетки(изменение формы,
сродства к красителям, подвижности и т.д.);
-преждевременной гибелью клетки (некроз, апоптоз);
-мутациями (генотоксичность).
Токсический процесс со стороны органа или системы проявляется:
-функциональными реакциями (спазм гортани, кратковременное падение артериального давления, учащение дыхания, усиление диуреза, лейкоцитоз и т.д.);
-заболеваниями органа;
-неопластическими процессами.
Токсический процесс на уровне целостного организма проявляться:
- болезнями химической этиологии(интоксикации, отравления);
-транзиторными токсическими реакциями - быстро и самопроизвольно проходящими состояниями, сопровождающимися кратковременной утратой дееспособности (явление раздражение глаз, дыхательных путей;седативно-гипнотическиесостояния; психодислептические состояния и т.д.);
-аллобиозом - стойкими изменениями реактивности организма на воздействие физических, химических, биологических факторов окружающей среды, а также психические и физические нагрузки (аллергия, иммуносупрессия, повышенная утомляемость и т.д.);
-специальными токсическими процессами - развивающимися лишь у части популяции, как правило, в особых условиях (действие дополнительных веществ; в определенный период жизнедеятельности организма и т.д.) и характеризующимися продолжительным скрытым периодом (канцерогенез, эмбриотоксичность, нарушение репродуктивных функций и т.д.).-беспороговые эффекты
Экотоксический процесс на уровне популяции проявляется:
-ростом заболеваемости, смертности, числа врожденных дефектов развития, уменьшением рождаемости;
-нарушением демографических характеристик популяции (соотношение возрастов, полов и т.д.);
-падением средней продолжительности жизни членов популяции, их культурной деградацией.
Дата: 2019-03-06, просмотров: 354.