Реакция отщепления галогеноводорода от первичных галогеналканов протекает по бимолекулярному механизму Е2.
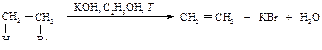
Механизм Е2. Основание НО– атакует водород (рис.15.6.а) при Сb, подает ему пару электронов и начинает образовывать с ним связь, связь Сb-Н ослабевает, пара электронов, связывавшая углерод и водород, освобождается и атакует атом галогена с тыла., одновременно растягивается связь Сa -Br (процесс согласованный). Возникает активированный комплекс: атомы углерода Сa и Сb переходят из sp3-гибридного состояния в состояние, близкое к sp2-состоянию, освобождающаяся пара электронов затрачивается на образование p-связи (рис.15.6.б) . Затем связи углерод- водород и углерод-галоген разрываются, атомы углерода переходят в sp2-состояние, образуется p-связь (рис.15.6.в).
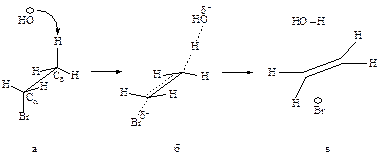
а – антикопланарное расположение связей Сa—Br и Сb—H, б – переходное состояние, в – конечные продукты.
Рис. 15.6. Механизм реакции бимолекулярного элиминирования.
Энергетическая диаграмма реакции изображена на следующем графике:
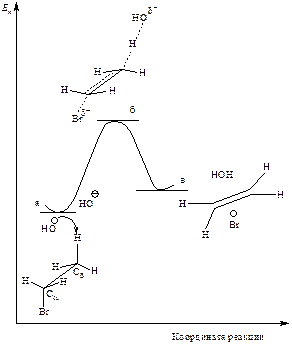
Рис.15.7. График изменения потенциальной энергии в ходе Е2.
Связи, разрывающиеся в активированном комплексе, должны быть в транс-положении друг к другу. Такая геометрия позволяет электронной паре, освобождающейся при связывании протона с основанием, атаковать с тыла атом углерода Сa и вытеснять галоген. Копланарность двух связей субстрата: Сa -Br и Сb -Н, которые разрываются в активированном комплексе, обеспечивает максимальное перекрывание р-орбиталей, то есть способствует процессу образования p-связи. Такая комбинация условий называется стереоэлектронным требованием.
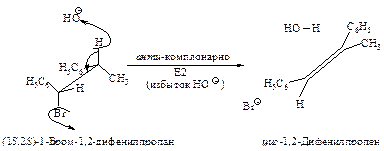
Ниже эта реакция изображена в проекциях Ньюмена.
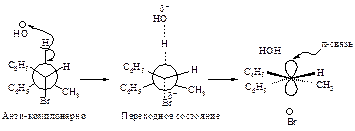
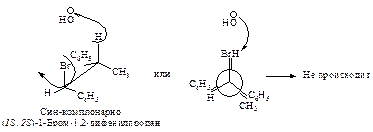
Реакция, в результате которой из данного стереоизомерного соединения получается в качестве продукта только один стереоизомер, называется стереоспецифической реакцией.
Cкорость реакции зависит от концентрации галогеналкана и основания и определяется по формуле V= K[R-Br] [O–].
Направление элиминирования - правило Зайцева: основным продуктом реакции отщепления от галогеналканов с двумя не эквивалентными Сb является наиболее устойчивый (наиболее алкилированный) алкен.
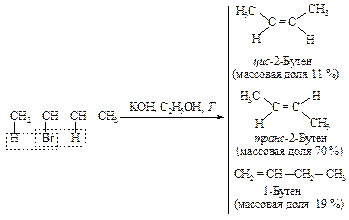
Основным продуктом реакции элиминирования 2-хлорбутана является транс-2-бутен (соотношение цис- и транс-изомеров 1:6). Активированный комплекс, возникающий при образовании транс-изомера, менее пространственно затруднен и более устойчив, и, следовательно, скорее образуется, чем активированный комплекс, ведущий к цис-изомеру.
Реакционная способность галогеналканов в реакциях Е2 изменяется в ряду:
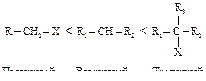
Такое увеличение реакционной способности галогеналканов при переходе от первичных к третичным обусловлено увеличением устойчивости образующихся алкенов.
15.2.2. Мономолекулярное отщепление Е1
Третичные галогеналканы реагируют по мономолекулярному механизму.
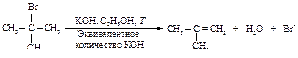
Механизм. Реакция протекает в две последовательные стадии. Первая стадия аналогична первой стадии мономолекулярного нуклеофильного замещения:
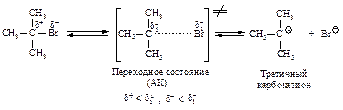
Во второй стадии основание атакует водород при Сb - атоме.
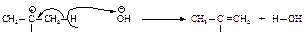
Реакционная способность галогеналканов увеличивается при переходе от первичных к третичным. Это обусловлено увеличением устойчивости карбокатионов, образующихся в медленной стадии.
Дата: 2018-12-21, просмотров: 445.