более 90 % профильтровавшегося натрия уже реабсорбировано в проксимальном канальце, восходящем колене петли Генле и дистальном извитом канальце.
Общее количество реабсорбируемого натрия, зависящего от действия альдо-стерона, составляет примерно 2 % всего профильтрованного натрия. Если учесть, что прочие факторы процесса постоянны, то при полном отсутствии альдостерона человек будет экскретировать эти 2 % профильтрованного натрия, а при максимальной концентрации альдостерона в плазме, натрий практически не будет экс-кретироваться. 2 % профильтрованного натрия, на первый взгляд, кажутся величиной незначительной, но на самом деле это количество очень большое, если учесть огромный объем клубочкового фильтрата.
общее количество профильтрованного Ка/сут = СКФ х Р№ =
= 180 л/сут х 145 ммоль/л = = 26 100 ммоль/сут.
Таким образом, альдостерон регулирует реабсорбцию 0,02 х 26 100 ммоль/сут = = 522 ммоль/сут.
Эта величина соответствует примерно 30 г КаС1 ежедневно, т. е. это больше того, что человек обычно потребляет в сутки с пищей. Вследствие рефлекторнрго изменения концентрации альдостерона в плазме от минимальной до максимальной, экскреция натрия может успешно регулировать его приемом рег оз, так что в результате общее количество натрия в организме и объем внеклеточной жидкости остаются постоянными.
(Интересно, что альдостерон также стимулирует транспорт натрия другими эпителиальными клетками организма, а именно клетками протоков потовых и слюнных желез, а также кишечника. В этих сегментах результирующий эффект тот же, что и в почке,— натрий переносится из просвета в кровь. Таким образом, альдостерон является многоцелевым стимулятором задержки натрия в организме.)
Альдостерон выполняет свою функцию после взаимодействия с внутриклеточными рецепторами, которые стимулирут в ядрах синтез РНК, которая затем становится медиатором трансляции специфических белков. Воздействие этих белков заключается в увеличении активности и/или числа натриевых каналов в люминальной мембране и Ма,К-АТФазных насосов в базолатеральной мембране3.
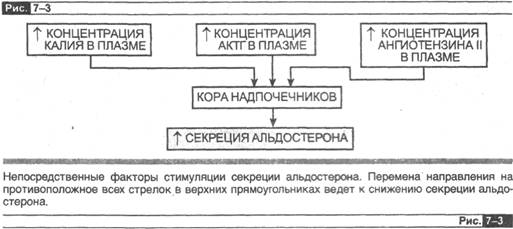
Регуляция секреции альдостерона. Существует прямые стимулы, действующие на надпочечники и стимулирующие секрецию альдостерона (рис. 7-3): (1) адренокортикотропный гормон (АКТГ), (2) увеличенная концентрация калия в плазме, (3) ангиотензин П. Кроме того, существует гормон, который угнетает секрецию альдостерона. Это — предсердный натрийуретический фактор, о котором речь пойдет позже4.
АКТЕ — это гормон, выделяемый передней долей гипофиза, который регулирует секрецию другого главного гормона надпочечников, кортизола. Нет сомнений, что при секреции АКТГ в очень больших количествах, например, вследствие механической травмы, секреция альдостерона тоже увеличивается. Более того, даже в небольшой концентрации, АКТГ является дополнительным стимулирующим фактором для других активаторов секреции альдостерона. Из сказанного следует, что АКТГ имеет важное значение для регуляции секреции альдостерона.
148
Регуляция экскреции натрия и воды : поддормциино постоянства объема плазмы .
Однако при всем том секреция АКТГ не является ключевым моментом в гомео-стазе натрия, т. е. он, как правило, не участвует в рефлекторной деятельности, которая специально «нацелена» на поддержание постоянного уровня натрия в организме.
Влияние концентрации калия в плазме на секрецию альдостерона будет описано в главе 8, когда речь пойдет об обработке калия почкой.
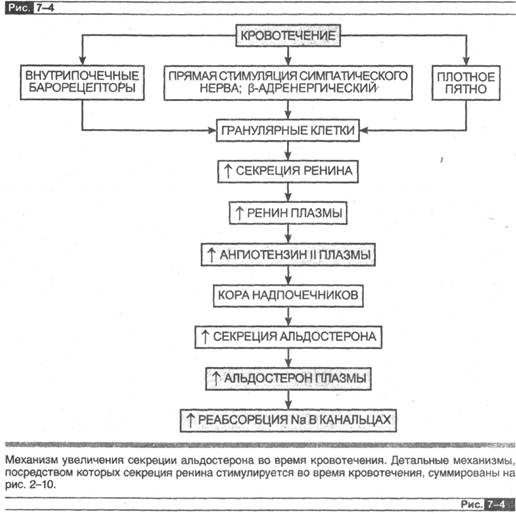
Теперь мы обратимся к третьему импульсу-фактору — ангиотензину II, который является самым сильным стимулятором секреции •альдостерона в рефлекторных дугах, регулирующих содержание натрия в организме. Как описано в главе 1, концентрация в плазме ангиотензина II определяется преимущественно концентрацией в плазме ренина. Соответственно регуляция секреции альдостерона в натрий регулирующих рефлексах зависит от состояния внутрипочечных барорецеп-торов, таси!а йенза, симпатических нервов почек, так как они регулируют секрецию ренина. (Более подробно этот вопрос освещен в разделе о регуляции секреции ренина в главе 2, рис. 2-8, 2-9 и 2-10.). В итоге, когда объем плазмы уменьшается в результате бессолевой диеты, кровотечения, диареи и т. д., интенсифицируется секреция ренина, которая, в свою очередь, через ангиотензин II приводит к увеличению секреции альдостерона, стимулирующего реабсорбцию натрия (рис. 7-4). Но когда человек находится на диете, богатой натрием, то секреция ренина снижена, а это обусловливает, через уменьшение в плазме ангиотензина И, снижение секреции альдостерона.

Для того чтобы не потерять из виду лес, увлекшись рассматриванием отдельных деревьев, давайте сформулируем сначала общие положения («лес»), а затем объясним каждое отдельно («деревья»). (1) Первичные изменения величины факторов Старлинга в перитубулярных капиллярах (гидростатическое и онкоти-ческое давление) оказывают влияние на почечное интерстициальное гидростатическое давление. (2) В результате вызванного таким воздействием увеличения
| 149 |
почечного интерстициального гидростатического давления уменьшается реаб-сорбция натрия и воды (одним словом, реабсорбция жидкости), преимущественг но в проксимальном канальце, снижение же почечного интерстициального гидростатического давления увеличивает реабсорбцию жидкости.
Прокомментируем два эти положения в обратном порядке. Вопрос первый: посредством каких механизмов почечное интерстициалыюе гидростатическое давление оказывает действие на реабсорбцию натрия и воды? Увеличенное ин-терстициальное гидростатическое давление вызывает обратную утечку реабсор-бированной жидкости из интерстициального объема через плотные соединения в каналец. Данное воздействие не изменяет работу клеточных транспортных механизмов для натрия и воды, но существенно снижает результирующую реабсорбцию, обусловленную действием этих механизмов, в особенности в «проницаемом» проксимальном канальце. Однако похоже, что увеличение почечного интерстициального гидростатического давления тормозит работу механизма
150 ______ Регуляция экскреции натрия и воды : поддержание постоянства объема плазмы
Ь V •
транспорта натрия рег зе, или за счет прямого воздействия на клетки канальца (возможно, за счет изменения их геометрии), или путем стимуляции освобождения паракринных агентов, которые, в свою очередь, оказывают влияние на клетки.
Вопрос второй: как силы Старлинга в перитубулярных капиллярах воздействуют на почечное интерстициальное гидростатическое давление? Как и для всех прочих капилляров организма, увеличение перитубулярно-капиллярного гидростатического давления СРрд) уменьшает силу, способствующую движению интерс-тициальной жидкости в капилляры; эта сила заставляет жидкость накапливаться в интерстициальном пространстве, что увеличивает почечное интерстициальное гидростатическое давление. Уменьшение онкотического давления (Прс) в перитубулярных капиллярах приводит к тому же. Таким образом, почечное интерстициальное гидростатическое давление пропорционально РРС и обратно пропорци онально прямо Прс5-
Данные объяснения подводят нас к вопросу о том, что же вызывает изменения ррс и про Ответ на это вопрос был дан в главе 2: РРС определяется (1) артериальным давлением и (2) комбинированным сосудистым сопротивлением афферентной и эфферентной артериол, которое определяет, насколько снижается артериальное давление, когда кровь достигает перитубулярных капилляров. прс определяется (1) артериальным онкотическим давлением и (2) фильтрационной фракцией (скорость клубочковой фильтрации/ППТ), которая определяет, насколько онкотическое давление увеличится после прохождения крови через клубочки.
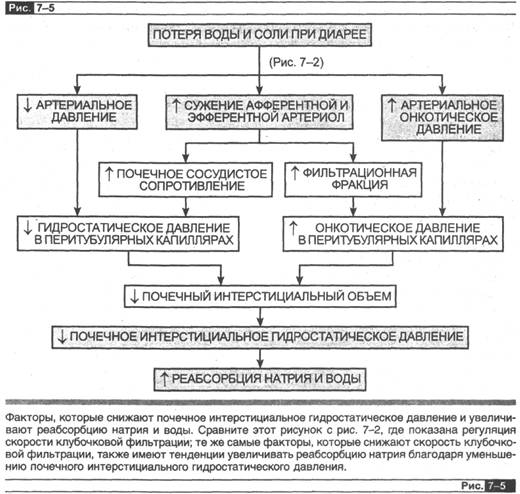
Телеологически здравый смысл подсказывает, что РРС и прс воздействуют на почечное интерстициальное гидростатическое давление и тем самым на реабсорбцию натрия, поскольку эти феномены являются просто логическим продолжением диаграммы потока. Их мы рассматривали ранее при обсуждении гомеостати-ческой регуляции скорости клубочковой фильтрации. Обратите внимание на рис. 7-2. Диаграмма потока, изображенная на нем, инициируется потерей жидкости и заканчивается тремя изменениями, которые затем приводят к снижению скорости клубочковой фильтрации: усилением спазма афферентной и эфферентной артериол (инициированным нервами почки и ангиотензином II), снижением артериального гидростатического давления и увеличением артериального онкотического давления.
На рис. 7-5 показано, как эти три фактора снижают почечное интерстициальное гидростатическое давление и тем самым увеличивают реабсорбцию натрия. Таким образом, гомеостатическая реакция, вызывающая уменьшение скорости клубочковой фильтрации в ответ на уменьшение количества натрия в организме, обычно усиливает реабсорбцию натрия, «ожидаемое» гомеостатическое явление, возникающее как реакция на уменьшение количества жидкости в организме.
Ту же логику мы применим при рассмотрении ситуации, когда «желаемые» гомеостатические реакции увеличивают скорость клубочковой фильтрации и уменьшают реабсорбцию натрия для того, чтобы удалить избыточное количество натрия из организма. Таким образом, если человек потребляет богатую солью диету или имеется увеличение внеклеточного объема в силу ряда физиологических причин, то происходит следующее: (1) снижается онкотическое давление плазмы (из-за разэедения белков плазмы); (2) повышается артериальное давление; (3) расширяются сосуды почки в результате снижения активности симпати-
| Регуляция канальцевой реабсорбциинатрия |
ческих нервов почки и снижения уровня ангиотензина II. (Как указывалось выше, данная вазодилатация может быть очень незначительной или вовсе отсутствовать, поскольку нервы почки столь слабо влияют на тонус стенки сосудов почки у здорового человека в покое, что этим можно пренебречь.) Затем скорость клубочковой фильтрации незначительно увеличивается, такая же динамика характерна и для почечного интерстициального гидростатического давления, что вызывает уменьшение реабсорбции жидкости6.
Дата: 2018-09-13, просмотров: 868.