1). Энтеротоксигенные кишечные палочки (ЭТКП, ETEC) являются возбудителями холероподобного заболевания у детей и взрослых, известного под названием «диарея путешественников». Заражение ЭТКП происходит водным и алиментарным путями.
Факторы патогенности: LT-, и ST-энтеротоксины, которые вызывают развитие секреторной диареи, а также пили IV типа, которые называются факторами колонизации CF. Благодаря CF ЭТКП прикрепляются и размножаются на поверхности эпителия тонкой кишки, внутрь энетроцитов они не проникают и не повреждают их. Колонизация поверхности тонкой кишки обеспечивает массивный выброс энтеротоксинов, которые нарушают водно-солевой обмен в кишечнике, приводя к развитию водянистой диареи. Механизм развития диареи связывают с активацией аденилатциклазы кишечника LT-токсином, а гуанилатциклазы - ST.
2). Энтероинвазивные кишечные палочки (ЭИКП, EIEC) способны внедряться и размножаться в колоноцитах толстой кишки, вызывая их деструкцию. Это обусловлено наличием плазмиды, идентичной плазмиде шигелл, которая кодирует синтез поверхностных белков, IPA-антигенов, опосредующих процесс инвазии в клетки слизистой оболочки толстой кишки. Результатом действия этих факторов патогенности является развитие дизентериеподобного заболевания. Заражение ЭИКП происходит водным и алиментарными путями, возможны вспышки внутрибольничных инфекций.
3). Энтеропатогенные кишечные палочки (ЭПКП, EPEC) вызывают диарею у детей первого года жизни. Заболевание может также протекать как внутрибольничная инфекция в отделениях для новорожденных и грудных детей, находящихся на искусственном вскармливании. Передается контактно-бытовом путем.
ЭПКП обладают способностью «прикрепления и сглаживания», т.е. способны к ограниченной инвазии. В результате этого процесса в участке прикрепления бактерий к эпителию тонкой кишки происходит дегенерация апикальной эпителиальной поверхности, сопровождающаяся потерей микроворсинок, следствием чего является уменьшение всасывающей поверхности кишечника. Этот процесс обеспечивается пилями IV типа, которые у ЭПКП называются пучокформирующими пилями, а также белком-интимином и эффекторными белками ТТСС, которые экспрессируются генами островка патогенности, известного как локус сглаживания энтероцитов, локализованного на хромосоме.
4). Энтерогеморрагические кишечные палочки (ЭГКП, EHEC) способны вызывать у людей кровавый понос (геморрагический колит) с последующим осложнением в виде гемолитического уремического синдрома и тромботической тромбоцитопенической пурпуры. Источником инфекции являются крупный рогатый скот и овцы. Основной путь передачи алиментарный, через мясо, не прошедшее достаточную термическую обработку. Поражаются слепая, восходящая и поперечная толстая кишки.
Механизм взаимодействия ЭГКП с колоноцитами происходит аналогично таковому у ЭПКП благодаря наличию на хромосоме островка патогенности LEE. Развитие гемолитического колита и уремического гемолитичского синдрома связано со способностью продуцировать шигаподобные токсины, синтез которых опосредуется конвертирующими бактериофагами, а также кодируемых плазмидой серинпротеазы и гемолизина, которые способствуют нарушению барьерной функции кишечника.
5). Энтероаггрегативные кишечные палочки (ЭАГКП, EAGGEC) являются преобладающим этиологическим агентом персистирующей диареи в развивающихся странах и медленно текущей диареи в индустриально развитых странах. Прикрепляясь к слизистой оболочке кишечника, они стимулируют продукцию слизи, приводя к образованию толстой слизистой биопленки. Образование биопленки усиливает персистенцию микроба и создает барьер, препятствующий проникновению антибиотиков и антибактериальных факторов хозяина. В развитии заболевания участвуют: фимбриальные адгезины (AAF), высокоиммуногенный белок дисперзин, который, связываясь с клеточной поверхностью, принимает участие в образовании биопленки, а также ST-токсин и токсины с цитотоксическим эффектом.
Иммунитет
При кишечных эшерихиозах вырабатывается местный иммунитет, опосредованный секреторными IgA. У детей первого года жизни пассивный трансплацентарный иммунитет к ЭПКП обеспечивается проходящими через плаценту IgG. Естественный иммунитет детей первого года жизни обеспечивают бифидобактерии, которые колонизируют кишечник к 5-му дню жизни, и антитела, находящиеся в материнском молоке. Надежный иммунитет к возбудителям парентеральных эшерихиозов не вырабатывается.
При колибактериозах в случае эндогенных инфекций имеет место гуморальный иммунный ответ. Однако образующиеся антитела не обладают протективными свойствами и не способствуют выздоровлению. Вместе с тем иммунодефицит, обуславливающий эндогенные инфекции, способствует угнетению фагоцитоза и других неспецифических факторов защиты, что способствует
нарушению естественных барьеров и распространению возбудителя.
Аналогичная ситуация имеет место и при гнойных раневых инфекциях экзогенной природы.
Лечение
Симптоматическое, этиотропное. Для лечения больных детей раннего возраста используют бифидобактерии, лактобактерин — препараты, содержащие молочно-кислые бактерии, являющиеся антагонистами Е. coli. Из антибиотиков используют все препараты, действующие на
грамотрицательные бактерии хлорамфеникол, пенициллин и цефалоспорины последних поколений, а также фторхинолон. Терапия этиотропная – антибиотики, колипротейный фаг.
Профилактика
Специфическая профилактика не разработана.
Неспецифическая профилактика сводится к соблюдению санитарно-гигиенических правил, санитарному контролю за источниками водоснабжения, пищевыми предприятиями, продуктами питания.
Диагностика
Осуществляется бактериологическим методом. Материал для исследования при кишечных эшерихиозах - испражнения, при парентеральных - материал из соответствующего инфекционного очага (моча, отделяемое раны, кровь, ликвор). Исследуемый материал (кроме крови и ликвора) засевается на дифференциальные лактозосодержащие среды, после инкубации при 37 ?С в течение 18 ч отбираются колонии, агглютинирующиеся поливалентной ОВ-агглютинирующей сывороткой, которые подвергаются идентификации до вида по биохимическим тестам с последующим определением их серовара.
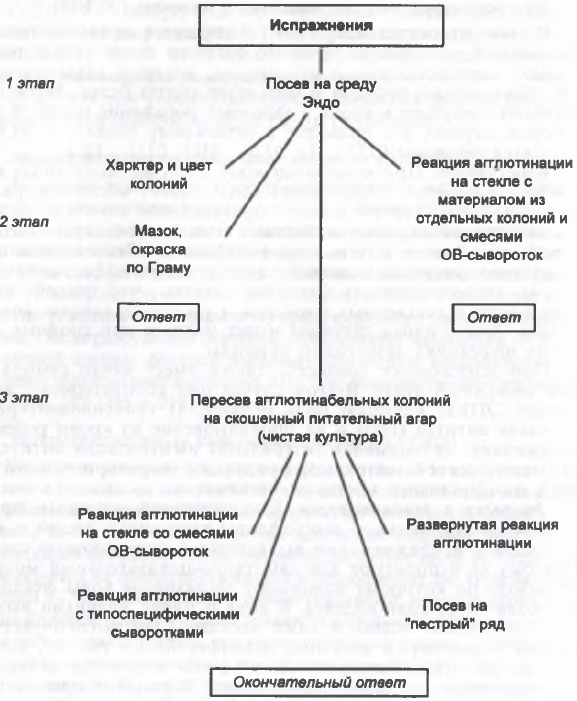 При кишечной коли-инфекции, а также при перитоните, септических и других состояниях
При кишечной коли-инфекции, а также при перитоните, септических и других состояниях
только на основании бактериологического исследования можно поставить окончательный диагноз заболевания. Идентификацию выделенной культуры проводят по морфологическим и биохимическим признакам и определению серовара возбудителя. Выделение чистой культуры сопряжено с определенными трудностями. Они связаны с наличием в исследуемом материале (фекалии) банальных эшерихий, представителей нормальной микрофлоры кишеника. Эти бактерии имеете с энтеропатогенными штаммами образуют однотипные колонии на дифференциально-диагностических средах. Идентификация выделенных эшерихий может быть произведена только на основании определения их принадлежности к определенной серогруппе, в реакциях агглютинации с диагностическими групповыми и типоспецифическими сыворотками.
Материалом для исследования при
-энтеральныхэшерихиозах являются фекалии,
-при парентеральных – гнойное отделяемое, при септических формах – кровь( в зависимости от локализации возбудителя.
Возможно использование методов иммуноиндикации и генной диагностики.
КАМПИЛОБАКТЕР
- Таксономия
Род Campylobacter (от греч. campylos — кривой, изогнутый). Известно около 18 видов возбудителя, из них наибольшее значение в патологии человека имеют С. jejuni, C. fetus, C. coli. Наибольшее значение в патологии человека имеет С. jejunii. Реже встречаются С. fetus и С. coli.
- Морфология
Кампилобактеры — грамотрицательные бактерии. Тонкие вибриоидные клетки, имеющие один или более витков спирали. Подвижные, совершают характерное винтовое движение с помощью одиночных жгутиков, расположенных на одном или обоих частях клетки. Капсулы и споры не образуют.
- Культуральные свойства
Микроаэро- и капнофилы. Растут на сложных питательных средах с добавлением крови, гемина, гидролизата белков, аминокислот, ростовых факторов и солей. Для подавления роста посторонней флоры в питательную среду добавляют антибиотики. Метаболизм дыхательного типа. Источником питания служат органические кислоты, в том числе аминокислоты. Хемоорганотрофы не требовательны к питательному субстрату.
В мазках из патологического материала часто располагаются попарно в виде ≪летящей чайки≫. При старении культуры переходят в кокковидную форму.
Кампилобактерии различаются по температуре культивирования: 37, 42 и, реже, 25 оС. Оптимальный для роста рН — 7,0.
Для культивирования используют сердечно-мозговой или шоколадный агар. Однако, даже на этих
высокопитательных средах видимый рост появляется на 6 сутки. Колонии круглые, мелкие, гладкие, выпуклые, блестящие.
- Биохимические свойства.
Не сбраживают углеводы. Оксидазоположительные и уреазоотрицательные. Пигментов не образуют.
Биохимические и ферментативные свойства выражены слабо. Проявляют оксидазную и каталазную активность, восстанавливают нитраты, образуют H2S.
- Резистентность
Резистентность кампилобактеров во внешней среде невысокая. Кампилобактерии чувствительны к действию высоких температур, однако достаточно долго сохраняются при низких температурах — из замороженного мяса их выделяют через несколько месяцев, на различных предметах при комнатной температуре они сохраняются до 2 нед. Невысокая. Чувствительны к факторам внешней среды,физическим и химическим факторам, в том числе к нагреванию и дезинфектантам. Устойчивы к целому ряду антибиотиков, но чувствительны к эритромицину и ципрофлоксацину.
- Антигенное строение.
Имеют О- и Н-антигены, по которым подразделяются на 60 сероваров. Облаают плазмидами, с которыми связана антибиотикоустойчивость. В настоящее время выделено свыше 50 О-серогрупп кампилобактеров.
- Факторы патогенности
Они обладают выраженной инвазивной активностью и способны к внутриклеточному размножению. Эндотоксин, связанный с ЛПС, а также продукция некоторыми штаммами холероподобного энтеротоксина и цитотоксина.
К факторам вирулентности относятся жгутики и муциназу, способствующие проникновению в слизистую оболочку тонкой кишки. Обладают умеренной пенетрационной активностью. Их токсичность связана с секрецией энтеротоксинов (функциональные блокаторы), нарушающими водно-солевой обмен через образование цАМФ, аналогично энтеротоксинам Е. coli и V. cholerae.
При разрушении кампилобактеров освобождается эндотоксин. Описаны цитотоксины, вызывающие гибель чувствительных клеток.
Основные факторы вирулентности:
- лейкоцидин, гемолизин, цитотоксины, тропизм к гепатоцитам.
- выраженная инвазивная активность,
-способность к внутриклеточному размножению;
-эндотоксин.
В зависимости от преобладания у данного штамма того или иного комплекса факторов вирулентности – будет наблюдаться та или иная форма клиники заболевания.
- Этиология.
Зооантропоноз. Источником инфекции являются сельско - хозяйственные животные и домашние птицы, редко человек., от которых кампилобактеры попадают в пищевые продукты (мясо, молоко) и воду.
В окружающей среде при 4°-10°С сохраняются около недели, (регистрированы пищевые, молочные и водные вспышки кампилобактериоза, чаще у детей). Естественная восприимчивость людей высокая. Кампилобактериоз распространен повсеместно и составляет 5–14% всех диарейных заболеваний. Механизм передачи — фекально-оральный
Пути передачи — пищевой, водный, контактно-бытовой или половой.
Случаи заболевания регистрируются в течение всего года, чаще в летне-осенние месяцы.
- Патогенез и клинические проявления
У человека кампилобактерии вызывают четыре группы заболеваний:
1) диарею (энтероколит), генерализованные поражения (сепсис);
2) локальные внекишечные инфекции (менингиты, энцефалиты, эндокардиты);
3) гнойно-воспалительные заболевания новорожденных;
4) заболевания ротовой полости - чаще всего вызывает C. Concаsus способствует возникновению гингивитов и стоматитов.
Гастроэнтерит возникает в результате действия энтеро- и цитотоксина, выделяемых некоторыми штаммами бактерий, размножающихся в ЖКТ.
Инкубационный период составляет, как правило, 2–3 дня. Болезнь начинается остро, с диспептических расстройств (диарея, рвота), интоксикации, повышения температуры; длится до 10 суток.
Наиболее частыми возбудителями диаррей являются C.coli, C.jejuni. Внекишечные формы кампилобактериозов обычно развиваются как осложнения кишечной, но могут возникать и как самостоятельное заболевание.
ЖКТ – форма;
1.Попав с пищей, водой, минует желудок и прикрепляется к эпителиальным клеткам тонкого кишечника.
2. Так как они способны к инвазии, проникают в эпителиальные клетки, способны к внутриклеточному паразитизму – вызывает let.клеток ( об этом косвенно говорит примесь слизи и свежей крови в испражнениях)
3. так как они ГРр (-), то выделяют эндотоксин, кроме того могут выделять экзо - эктеротоксигенные в 2-х субъединицах с холерогеном)
Инкубационный период длиться от 2-5 дней (иногда 10 дней).
Продромальный период – от нескольких часов до 2-3 суток; (в этот период на фоне общей интоксикации больные жалуются на миалгии и артралгии).
После этого наступает разгар заболевания, длится 3-10 дней
-появляется частый жидкий стул - слизеподобный с примесями свежей крови);
- реконвалесценция может продолжаться до 3-х недель. Долго держатся боли в брюшной полости;
- но если бактерии прорывает лимфатический барьер, то изгоняются в кровь вызывая различные внекишечные формы:
- менингит, перитонит,сепсис ,аппендицит
Иммунитет
При кампилобактериозе наблюдается гуморальный иммунный ответ. Однако образующиеся антитела не обладают выраженными протективными свойствами.
Лечение
Для лечения применяются фторхинолоны, аминогликозиды, хлорамфеникол (эритромицин или ципрофлоксацин).
Прифилактика
Вакцинопрофилактика не разработана. Проводятся противоэпидемические мероприятия, как при сальмонеллезах.
Лабораторная диагностика
Проводится бактериологическим методом с выделением чистой культуры возбудителя и ее идентификацией.
Основана на выделении чистой культуры возбудителя из испражнений, рвотных масс, промывных вод желудка посевом на кровяной или эритритный агар с железо-сульфитно-пируватными добавками. Для видовой дифференцировки культивируют при различных температурных режимах.
В мазках из фекалий определяют типичные по форме микробы в виде ≪летящей ласточки≫. Для серологической диагностики используют РИФ, РА, РПГА,РСК. Экспресс-диагностика — постановка РИФ со специфическими люминесцентными сыворотками.
ХОЛЕРА
Холера – антропонозная карантинная особо опасная инфекция с фекально-оральным механизмом передачи, характеризующаяся поражением тонкой кишки и нарушением водно-солевого и белкового обмена, обезвоживанием, токсикозом и гастроэнтеритом.
Таксономия
Возбудителем холеры являются бактерии семейства Vibrionaceae, рода Vibrio, вида Vibrio cholerae серогрупп О1 и О139.
Внутри вида Vibrio cholerae различают два основных биовара: биовар Сlassic и биовар El-Tor.
Этот вид включает многочисленных представителей, объединенных в один вид на основании морфологических, культуральных, биохимических свойств и данных геносистематики. Внутри вида они подразделяются по ферментативной активности, антигенному строению и патогенным возможностям. Возбудителями холеры являются патогенные представители данного вида (V.cholerae O1 и V.cholerae О139 Бенгал). Все другие холерные вибрионы являются условно-патогенными. Они могут вызывать у человека вибрионогенные диарреи.
Морфология
Холерный вибрион - грамотрицательная палочка в форме запятой, длиной 2-4 мкм, толщиной 0,5 мкм. Не образует спор и капсулы, монотрих, чрезвычайно подвижен.
Культуральные свойства
Аэроб или факультативный анаэроб. Является факультативным анаэробом, но предпочитает аэробные условия роста, поэтому на поверхности жидкой питательной среды образует пленку. Холерный вибрион неприхотлив в росте и может расти на простых средах. На плотных питательных средах образует мелкие, прозрачные, округлые колонии. Оптимальная температура роста 37 °С и рН 8,5-9,0, для оптимального роста требует присутствия в среде 0,5% натрия хлорида.
Средой накопления является 1% щелочная пептонная вода, на которой он образует пленку в течение 6-8 ч, и щелочной агар, на котором растут маслянистые голубоватые колонии.
Элективной средой является тиосульфат-цитратный сахарозо-желчесодержащий агар (TCBS-среда), на котором образует колонии желтого цвета.
Биохимические свойства
Биохимически активен:
1. Обладает протеолитическими и сахаролитическими свойствами: продуцирует индол и лизиндекарбоксилазу, разжижает в воронковидной форме желатин.
2. Ферментирует глюкозу, сахарозу, маннозу, крахмал, лактозу (медленно).
3. Не сбраживает рамнозу, арабинозу, дульцит, инозит, инулин.
4. Обладает нитратредуктазной активностью.
5. Продуцирует оксидазу.
Вибрионы относятся к хемоорганотрофам с окислительным и бродильным типами метаболизма.
Дифференциация среди биоваров возбудителей холеры проводится по биохимическим свойствам, а также по способности гемолизировать эритроциты барана, агглютинировать куриные эритроциты; чувствительности к полимиксину и чувствительности к бактериофагам. V. cholerae О139 по фенотипическим признакам относится к биовару El-Tor, который резистентен к полимиксину, агглютинирует куриные эритроциты и гемолизирует эритроциты барана, дает положительный результат в реакции Фогеса-Проскауэра и гексаминовом тесте.
Антигенная структура
Обладает термостабильным О- и Н-антигенами. В зависимости от строения О-антигена различают более 200 серогрупп, среди которых возбудителями холеры являются серогруппы О1 и О139. Внутри серогруппы О1 в зависимости от сочетания А-, В- и С-субъединиц происходит подразделение на серовары: Огава (АВ), Инаба (АС) и Гикошима (АВС). Н-антиген является общеродовым антигеном.
Холерные вибрионы имеют два антигена: О-антиген типоспецифический термолабильный и Н-антиген жгутиковый видоспецифический термостабильный. Возбудители холеры имеют 01-антиген Вибрионы, относящиеся к серогруппам 02, 03, 04 могут вызывать энтериты и гастроэнтериты. 01-антиген состоит из трех компонентов — А, В, С, разные сочетания которых образуют серовары Огава (АВ), Инаба (АС), Гикошима(АВС). Часто выделяются вибрионы, не агглютинирующиеся 01 антисывороткой. Их называют неагглютинирующимися НАГ-вибрионами.
Резистентность
Возбудители холеры чувствительны к УФ-лучам, высушиванию, дезинфектантам (за исключением четвертичных аминов), кислым значениям рН, нагреванию. Возбудитель холеры, особенно биовар Эль-Тор, способен к существованию в воде в симбиозе с гидробионтами, водорослями, в неблагоприятных условиях может переходить в некультивируемую форму. Эти свойства позволяют отнести холеру к антропонозно- сапронозным инфекциям.
Факторы патогенности
Факторы патогенности V. choleras:
1. Подвижность
2. Хемотаксис
3. Факторы адгезии и колонизации
4. Ферменты: муциназа, протеазы, нейроминидаза, лецитипеаза
5. Экзотоксин – холероген, который и обуславливает патогенез холеры
Молекула холерогена состоит из двух фрагментов – А и В. Фрагмент А состоит из двух петидов – А1 и А2, и обладает специфическим свойством холерного токсина. Фрагмент В состоит из пяти одинаковых субъединиц, и выполняет две функции:
1.Распознаёт рецептор энтероцита, и связывается с ним.
2.Формирует внутринемембранный гидрофобный канал для прохождения субъединицы А.
Пептид А2 служит для связи фрагментов А и В. Собственно токсическую функцию выполняет пептид А1. Он взаимодействует с НАД, вызывает его гидролиз, образующаяся при этом АДФ – рибоза связывается с аденилатциклазой. Это ведёт к угнетению гидролиза ГТФ. Возникший комплекс ГТФ+аденилатциклаза вызывает гидролиз АТФ с образованием цАМФ.
6.Помимо холерогена холерный вибрион синтезирует и выделяет фактор, повышающий проницаемость капилляров.
7.У холерных вибрионов обнаружены и другие экзотоксины (LT, ST, SLT).
Липополисарарид V. choleras обладает сильным эндотаксическим свойством.
Главными факторами патогенности являются токсинкорегулируемые пили (Тср), холерный энтеротоксин (СТ) и нейраминидаза, растворимая гемагглютининпротеаза.
1. Токсинкорегулируемые пили (являются пилями IV типа): обеспечивают колонизацию микроворсинок тонкой кишки, участвуют в образовании биопленок на поверхности панциря гидробионтов.
2. Холерный энтеротоксин - белок с молекулярной массой 84 000 Д, синтез которого осуществляется геном, локализованном на конвертирующем бактериофаге СТХ. Только серогруппы О1 и О139 лизогенизированы этим бактериофагом. Токсин состоит из 1 субъединицы А и 5 субъединиц В.
В-субъединицы связывают всю молекулу токсина с клеточным рецептором – моносиаловым ганглиозидом GM1, которым очень богаты эпителиальные клетки слизистой оболочки тонкой кишки. Для этого от него должна быть отщеплена сиаловая кислота, что осуществляется ферментом нейраминидазой (способствует реализации действия токсина). После прикрепления В-субъединицы, субъединица А проникает в клетку, где она активирует аденилатциклазу, переводя ее в постоянное активное состояние => усиление синтеза цАМФ => изменяется активный транспорт ионов: в области крипт эпителиоциты усиленно выделяют ионы Cl-, а в области ворсинок затрудняется всасывание Na и Cl, что составляет осмотическую основу для выделения в просвет кишечника воды.
3. Растворимая гемагглютининпротеаза способствует откреплению возбудителя от поверхности кишечника, давая возможность возбудителю инфицировать новые участки тонкой кишки.
4. Эндотоксин, активируя каскад арахидоновой кислоты, запускает синтез простагландинов, результатом действия которых являются сокращение гладкой мускулатуры кишечника и развитие тенезм
5. Добавочные белковые токсины, которые участвуют в увеличении проницаемости стенки кишечника.
Эпидемиология
Холера известна с древних времен. Но до начала XIX века она встречалась только в Индии, где расположен гиперэндемический очаг этого заболевания.
Место обитания - теплая вода. В воде у вибриона отсутствует О-АГ и имеется всего 1 копия гена, отвечающего за синтез токсина, поэтому в воде микроб авирулентен. При попадании в организм человека ( и повышении температуры) происходит амплификация генов и появляется О-АГ, т.е. микроб приобретает вирулентность.
Источники инфекции: больной человек, бактерионосители, а также водная среда и гидробионты.
Пути передачи: водный, алиментарный, контактно-бытовой.
Восприимчивый коллектив: лица с пониженной кслотностью желудочного сока, страдающие анацидным гастритом. Носительство вибриона Эль-Тор встречается чаще, чем классического вибриона (на 1 больного холерой приходится 10-1000 носителей). Больной наиболее опасен в первые дни болезни: в это время в испражнених и рвотных массах содержится наибольшее количество возбудителя.
Дата: 2019-07-30, просмотров: 423.