Ключевым понятием МФЗ является коэффициент наследуемости. Этот коэффициент выражает долю генетических факторов в развитии болезни в %% от совместного действия генетических и средовых факторов, принимаемых в сумме за 100%. При разных МФЗ этот коэффициент широко варьирует , но для группы в целом коэффициент наследуемости > 50%, но < 100%. Для некоторых наиболее распространенных МФЗ коэффициент наследуемости составляет: ИБС - 60%, аллергические заболевания - 50%, ревматизм при сочетанном митральном пороке - 78%, гломерулонефрит - 60%, холецистохолангит - 58%.
Риск возникновения МФЗ для родственников больного определяется эмпирически (экспериментально при обследовании и статистической обработке большого числа больных и их родственников). На основании фактических данных вычисляются значения риска для отдельных классов родственников. Если в литературе нет данных о семейной частоте, то ориентировочно её можно принять = 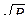 для родственников первой степени родства, где Р - частота заболевания в популяции.
для родственников первой степени родства, где Р - частота заболевания в популяции.
Риск для сибсов при некоторых распространенных МФЗ
( в некоторых случаях для потомства):
Умственная отсталость - 2,5-5%; эпилепсия - 3-12%; миопия высокой степени - 10-15%; косоглазие - 10-15%; язвенная болезнь двенадцатиперстной кишки - 3-9%; язвенная болезнь желудка - 7,5%; псориаз - 16%; бронхиальная астма - 8-9%; атопический дерматит - 16%; врожденные пороки сердца - 2-4%; диффузный токсический зоб - 10%.
Маркеры МФЗ
Маркеры (метки) МФЗ - признаки, указывающие на наличие генетической составляющей в возникновении болезни. Выделяют ассоциативные и патогенетические маркеры. К ассоциативным маркерам относятся группы крови (системы АВО), антигены главного комплекса гистосовместимости по системе HLA. Так, например язвенная болезнь чаще встречается у детей с 1 группой, ревматизм - со 2-й. Одно из наиболее обоснованных объяснений для механизма действия всех ассоциативных маркеров - плейотропное действие генов, т.е. одновременное воздействие генов и на маркер и на ряд биохимических, иммунологических и физиологических параметров, изменения которых оказываются характерными (маркерными) именно для этого заболевания. Возможно “сцепление” локусов генетического маркера и заболевания. Один и тот же ассоциативный маркер может быть для различных заболеваний.
С практических позиций более перспективен поиск биологических (патогенетических) маркеров предрасположения, т.е. маркеров, непосредственно отражающих патогенез болезни. Наличие взаимосвязи между клиникой заболевания и патогенетическим маркером означает, что определенная часть генных локусов, вовлеченных в генетическую систему заболевания, является общей и для какого-либо маркерного иммунологического или биохимического признака. Патогенетические маркеры делятся на одномерные - когда один какой-либо показатель указывает на болезнь и многомерными - когда о наличии патологии свидетельствует комплекс показателей. Например для атеросклероза биохимическими маркерами являются гиперхолестеринемия, гипертриглицеридемия.
Аллергические заболевания
Имеются многочисленные факты подтверждающие высокую степень генетического участия в возникновении аллергических заболеваний. Если аллергия имеется у обоих родителей то риск какого-либо аллергического заболевания составляет 40-60%; риск максимален (80%) если у обоих родителей поражен один и тот же орган мишень (например бронхиальная астма или атопический дерматит). В целом у детей первых трех лет жизни с отягощенной по аллергическим заболеваниям наследственностью частота таких болезней в 10 раз выше, чем у детей с благоприятной наследственностью. Симптомы аллергических болезней появляются тем раньше, чем сильнее отягощен анамнез. У членов одной семьи чаще поражается один и тот же орган.
Доказан генетический контроль за синтезом Ig E, играющего решающую роль в возникновении аллергических заболеваний. По крайней мере 2 гена конторолируют синтез Ig E: так называемый ген атопии и Ir - ген, который ответственен за продукцию Ig E и синтез других Ig. Склонность к гиперпродукции Ig E передается как полигенно, так и как аутосомно-рецессивный признак. Генетический контроль осуществляется и за другими звеньями аллергического процесса - за активностью макрофагов и мастоцитов, их способностью высвобождать медиаторы, за проницаемостью слизистых оболочек для различных АГ и др. В пределах мультифакториальной генетической системы существуют как факторы общего характера, т.е. усиливающую общую подверженность к атопическим заболеваниям, так и действующие совместно с ними другие факторы, влияющие на поражение конкретных органов. Для возникновения аллергической патологии одной лишь генетической предрасположенности недостаточно. Необходимо параллельное влияние разрешающих экзогенных факторов: попадание аллергена, мембрандестабилизирующих факторов и пр. Примером МФЗ аллергической природы может служить Бронхиальная астма. При которой генетически обусловлены: повышение общего и специфического IgE; низкий уровень гаптоглобина; имеется связь с группой крови А(П); часто выявляются у больных HLA- антигены A3; B7; DW2; С антигенами BW16 связаны наиболее тяжелые формы, с BW21, A9, B7- более легкие формы; гипореактивность бета-2 адренорецепторов; гиперреактивность холинорецепторов бронхов.
Во многом детерминированы генетически хронические и рецидивирующие пневмонии. При этом генетическая составляющая включает в себя нарушение иммунитета (дефицит синтеза Ig A , нарушение функции отдельных субпопуляций или клонов Т-лимфоцитов), нарушение мукоцилиарного транспорта.
Гипертоническая болезнь
Существует отчетливо выраженная генетическая предрасположенность к гипертонической болезни (ГБ). Популяционная вариабельность величины АД у детей примерно на 50% определяется генетическими и на 50% экзогенными факторами. При наличии артериальной гипертензии у обоих родителей вероятность возникновения ГБ у ребенка составляет 57%, если страдает только мать - 30%, только отец - 13%. Коэффициент наследуемости минимального АД = 85%, среднего - 78%.
Патогенез наследственных изменений при ГБ сложен и многоэтапен. Отмечается наследственная повышенная выработка инсулина в ответ на поступление в организм глюкозы, что стимулирует рост и миграцию сосудистых гладкомышечных клеток и приводит в итоге к увеличению периферического сопротивления сосудов и повышению АД. Кроме того, наследуется повышенная симпатоадреналовая активность, склонность к задержке натрия, повышения внутриклеточного кальция, что приводит к неадекватному спазму артерий в ответ даже на нормальный выброс адреналина; более быстрому развитию структурных изменений в стенке сосудов.
Наследуются и психологические особенности личности, способствующие возникновению ГБ - так называемое поведение типа” А” (сочетание сильного типа высшей нервной деятельности с повышенной агрессивностью и склонностью к межличностным конфликтам).
Дата: 2019-05-28, просмотров: 328.