Размер дендритной ячейки должен определять уровень ликвации элементов в отливках. Считается, что измельчение структуры должно приводить к снижению ликвации. Однако при исследовании отливок часто наблюдается повышение неоднородности структуры наряду с достигаемым ее измельчением. Для выяснения влияния различных технологических факторов изготовления отливок необходимо провести математический анализ процессов массопереноса, происходящих при росте частиц твердой фазы из легированного расплава [11].
Рассмотрим процесс образования новой фазы в двойной системе, образующей твердый раствор. Допустим, что сплав содержит C 0 добавки, тогда при кристаллизации сплава в интервале температур в общем случае состав жидкой фазы у поверхности растущего кристалла определяется диаграммой состояния. В изотермических условиях рост кристалла должен происходить до установления равновесного состава фаз и затем прекратиться. В реальном процессе теплоотвод является ведущей движущей силой и задает скорость роста кристалла. Перераспределение компонента является подчиненным процессом.
Для упрощения анализа распределения добавки обычно принимают, что линии являются прямыми; тогда соотношение w = C тв /СЖ, называемого коэффициентом распределения, является величиной постоянной для рассматриваемого угла диаграммы состояния. Процесс перераспределения второго компонента при кристаллизации сплава описывается дифференциальным уравнением диффузии следующего вида (рис. 4.12.):
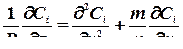 , (4.53)
, (4.53)
где i=1,2 относится соответственно к твердой и жидкой фазе;
D – коэффициент диффузии; m=0, 1, 2 определяют рост твердой фазы в виде пластинки, цилиндра или шара.
На границе раздела фаз (х = х m ) реализуется условие, определяемое диаграммой состояния, т.е.:
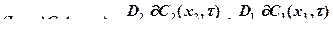 . 4. 54)
. 4. 54)
C 1 ( xm , t )= w C 2 ( xm , t ) . (4.55)
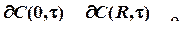 . (4.56)
. (4.56)
C ( x ,0)= С0 . (4.57)
Добавки и примеси, присутствующие в промышленных сплавах, имеют коэффициенты диффузии в области температур кристаллизации в твердой и жидкой фазах соответственно D 1 =10-12м2/ c и D 2 =10-9м2/ c, поэтому диффузией в твердой фазе на этом этапе можно пренебречь.
Аналитическое решение о распределении примеси в кристалле зонной плавки можно получить только для случая равномерного распределения примеси в исходном состоянии – начальное условие (4.57). При повторной кристаллизации в процессе получения монокристаллов, когда конечное распределение на предыдущем этапе является начальным для последующего, аналитическое решение получить невозможно. Поэтому в теории зонной очистки применяют приближенные решения, основанные на разбиении кристалла на элементарные объемы, с последующим расчетом в соответствии с дифференциальным уравнением (4.53) и с граничными условиями ( 4.54 ) – ( 4.57 ) на ЭВМ методом конечных разностей.
Процесс формирования структуры отливки отличается от зонной плавки и очистки наличием большого числа одновременно растущих центров твердой фазы. Это обусловливает криволинейную поверхность раздела твердой фазы и матричной жидкости, а также ограниченность объема, занимаемого одним кристаллом.
Предположение о полном выравнивании состава жидкой фазы является очень грубым приближением. Кроме того, такое предположение, по сути равносильно утверждению, что химическая неоднородность, возникающая в процессе кристаллизации, не зависит от скорости роста. Это опровергается экспериментальными данными, которые свидетельствуют, что химическая неоднородность сплавов существенно зависит от скорости теплоотвода. Таким образом, для анализа кинетики кристаллизации необходимо рассмотрение, как процесса теплообмена, так и процесса диффузии примеси. Причем рост кристаллов при затвердевании отливки сопровождается возникновением градиента температуры, не связанного с направлением теплоотвода. Анизотропия температурного поля в жидкой фазе усиливается также тем, что обогащение ее выделяющейся примесью снижает температуру ликвидус расплава и может прекратить рост кристалла. Этот эффект был назван Иванцовым концентрационным переохлаждением. Перераспределение примеси за счет диффузии в микрообъемах при кристаллизации сплавов, по-видимому, решающим образом влияет на кинетику роста ячеек первичной структуры. Аналитическое решение задачи о распределении примеси при кристаллизации в условиях ограниченного объема, занимаемого кристаллом, получить невозможно.
 |
Рассмотрим процесс дендритной кристаллизации, при котором рост дендритных ветвей происходит в толщину вокруг осей, т.е. фронтом кристаллизации является цилиндрическая поверхность (схема). Толщина ветви имеет конечное значение: например, для стали при скорости u =10-4м/ c значение R =2 · 10-4 м, D=5 · 10-9 м2/с, следовательно, u R / D = 4; таким образом, весь процесс укладывается в начальную стадию очистки монокристалла. Решение задачи для таких условий может быть получено методом конечных разностей.
Представим производные функции концентрации конечным соотношением:
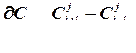 . (4.58)
. (4.58)
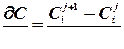 . (4.59)
. (4.59)
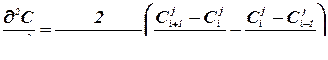 , (4.60)
, (4.60)
где i-относится к разбиениям по координате; j-по времени.
Анализ уравнения (4.53) и граничного условия (4.54) показывает, что распределение добавки определяется двумя процессами:
1) отвод добавки от границы раздела фаз, который характеризуется числом Фурье F 0 = D t / R 2;
2) выделение добавки на границе раздела фаз, которое определяется параметром v t (1- w )/ D 2.
Постановка конечных соотношений вместо частных производных в диффе-ренциальное уравнение диффузии приводит к явной схеме решения (рис 4.10).
Для i =1(х = х m ) уравнение (4.54)
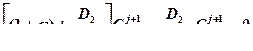 . (4.61)
. (4.61)
Для i = n (х = R ) уравнение (4.57)
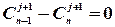 . (4.62)
. (4.62)
В расчетах обычно принимается uDt / D х <<1, т.е. скорость продвижения фронта много меньше, чем размер первого разбиения по координате, что повышает точность расчета; однако при этом увеличивается время счета, поэтому обычно выбирают соотношение 0,1> uDt / D х >0,01.
Начальное распределение задается условием (4.57) Ci 0 = C 0.Численное решение (рис. 4.12) позволяет определить концентрацию в каждой точке жидкости, которая, в свою очередь, является исходной для расчета концентрации в следующий момент времени. В последний момент (выбираемый в соответствии со значением uDt / D х) обогащенная жидкость переходит в кристалл того же состава без учета коэффициента распределения, поскольку добавке выделяться некуда.
Для условий изготовления стальных отливок представляет интерес рассмотреть ликвацию легирующих элементов и контролируемых примесей, которые определяют механические и технологические свойства стали. К ним относятся: легирующие элементы – углерод, хром, никель, марганец, кремний,
 |
молибден; примеси – фосфор и сера.
Рис 4.12. Схема разбиения расчетного объема конечноразностной сеткой
 Программная реализация модели дендритной ликвации
Программная реализация модели дендритной ликвации
Файл данных
0.0002 R толщина ветви дендрита, м
0.0001 Dtau шаг по времени, с
10 IMAX число элементов по горизонтали
0.00000001 d2 коэффициент диффузии в жидкости
0.001 v скорость кристаллизации, м/с
0.5 k коэффициент распределения
Файл программы
program likvazia; {программа расчета распределения ликвирующего компонента в твердой и жидкой фазе}
var C,ct,c1,t :array [1..20] of real;
A,dx,dxt,dxtt,dtau,R,tau,v,d2,k,ctt,x:real;
jj,j,i,imax,jmax,k1:integer;
f1,f2:text;
st:string[70];
begin
ASSIGN (F2,'e:/TP7/deendrit/likvazia.REZ'); REWRITE(F2);
ASSIGN (F1,'e:/TP7/deendrit/likvazia.DAT'); RESET(F1);
READ(F1,R);read (f1,st);WRITE (F2,R:5:3);WRITE (F2,st);READln(F1);
READ(F1,Dtau);read (f1,st);WRITEln(F2);WRITE(F2,Dtau:9:6);WRITE(F2,st);
READln(F1);READ(F1,IMAX);read(f1,st);WRITEln(F2);
WRITE(F2,IMAX:2);WRITE(F2,st);
READln(F1);
READ(F1,d2);read(f1,st);WRITEln(F2);WRITE(F2,d2:11:9);WRITE(F2,st);
READln(F1);READ(F1,v);read(f1,st);WRITEln(F2);WRITE(F2,v:6:4);WRITE(F2,st);
READln(F1);READ(F1,k);read(f1,st);WRITEln(F2);WRITE(F2,k:6:2);WRITE(F2,st);
WRITEln(F2);
FOR I:=1 TO IMAX DO BEGIN; c[i]:=1.0; end;
FOR j:=1 TO 30 DO BEGIN; ct[j]:=0.0; end;
j:=1; jmax:=1; dxtt:=0.0; jj:=1;
dxt:=0.00001; {шаг увеличения твердого слоя в м}
ctt:=k*c[1];{начальная концентрация в твердом слое}
WRITEln(F2);
FOR k1:=1 TO 10 DO BEGIN; {начало цикла продвижения твердой фазы}
dxtt:=dxtt+dxt; {общая толщина твердого слоя}
A:= d2/(v*dxt);
c[1]:=((1.0+k+A)*ctt)/A; { концентрация в жидком слое}
c1[1]:=c[1];
ctt:=A*c[1]/(1.5+A);{ концентрация в твердом слое}
ctt:=k*c[1];{ концентрация в твердом слое}
ct[jj]:=ctt;
t[jj]:=dxtt; {концентрация элемента в жидкости на границе с кристаллом }
dx:=(R-dxtt)/imax;{величина шага в жидкой фазе}
FOR I:=2 TO IMAX-1 DO BEGIN; {концентрация в следующий момент времени}
c1[i]:=((d2*dtau)/(2*dx)*(c[i+1]-2*c[i+1]+c[i-1])/(2*dx))+c[i]; end;
{концентрация в граничной точке}
c1[imax]:=c1[imax-1];
FOR I:=1 TO IMAX DO BEGIN; c[i]:=c1[i]; end;
WRITEln(F2,'концентрация элемента в твердой фазе в % и толщина в м');
FOR j:=1 TO jMAX DO BEGIN; WRITE(F2,' ct[',j:2,']=',ct[j]:5:3);
WRITE(F2,' t[j]=',t[j]:9:6); WRITEln(F2); end;
WRITEln(F2,'толщина ветви дендрита в м',R:9:6);
x:=(R-dxtt);
WRITEln(F2,'длина жидкой части в м',x:9:6);
WRITEln(F2,'концентрация элемента в жидкости');
FOR I:=1 TO IMAX DO BEGIN;
WRITEln(F2,' c[',i:2,']=',c[i]:5:3); end;
tau:=tau+dtau; jMAX:=jMAX+1; JJ:=JJ+1; end;
WRITEln(F2,'tau=',tau:9:6);
CLOSE(F1);CLOSE(F2);
END.
Файл результатов
0.0002 R толщина ветви дендрита, м
0.0001 Dtau шаг по времени, с
10 IMAX число элементов по горизонтали
0.000000010 d2 коэффициент диффузии в жидкости
0.0010 v скорость кристаллизации, м/с
0.50 k коэффициент распределения
концентрация элемента в твердой фазе (%) и толщина, м
ct[ 1]=0.625, t[j]= 0.000010
толщина ветви дендрита, м 0.000200
длина жидкой части, м 0.000190
концентрация элемента в жидкости
c[1]=1.250
c[2]=1.000
c[3]=1.000
c[4]=1.000
c[5]=1.000
c[6]=1.000
c[7]=1.000
c[8]=1.000
c[9]=1.000
c[10]=1.000
концентрация элемента в твердой фазе (%) и толщина, м
ct[1]=0.625, t[j]= 0.000010
ct[2]=0.781, t[j]= 0.000020
толщина ветви дендрита, м 0.000200
длина жидкой части, м 0.000180
концентрация элемента в жидкости
| c[1]=1.563 c[2]=1.001 | c[3]=1.000 c[4]=1.000 | c[5]=1.000 c[6]=1.000 | c[7]=1.000 c[8]=1.000 | c[9]=1.000 c[10]=1.000 |
концентрация элемента в твердой фазе (%) и толщина, м
| ct[1]=0.625, t[j]= 0.000010 ct[2]=0.781, t[j]= 0.000020 ct[3]=0.977, t[j]= 0.000030 ct[4]=1.221, t[j]= 0.000040 ct[5]=1.526, t[j]= 0.000050 | Ct[6]=1.907, t[j]= 0.000060 Ct[7]=2.384, t[j]= 0.000070 Ct[8]=2.980, t[j]= 0.000080 Ct[9]=3.725, t[j]= 0.000090 Ct[10]=4.657, t[j]= 0.000100 |
толщина ветви дендрита, м 0.000200
длина жидкой части, м 0.000100
концентрация элемента в жидкости
| c[1]=9.313 c[2]=1.057 | c[3]=1.000 c[4]=1.000 | c[5]=1.000 c[6]=1.000 | c[7]=1.000 c[8]=1.000 | c[9]=1.000 c[10]=1.000 |
tau= 0.001000.
Таблица 4.6
Коэффициенты распределения легирующих и примесных элементов в железе
| Элемент | Тип диаграммы | Концентрация элемента (массовое содержание), % | Коэффициент распределения |
| Углерод | Перитектика | До 0,5 | 0,20 |
| До 0,3 | 0,26 | ||
| Марганец | До 13 | 0,74 | |
| Кремний | Твердый раствор | 1,0 | 0,7 |
| Хром | Твердый раствор | До 5 | 0,6 |
| 10–13 | 0,9 | ||
| 15–20 | 1,0 | ||
| Никель | Перитектика | До 5,2 | 0,66 |
| Молибден | Твердый раствор | До 2,0 | 0,50 |
| Медь | Перитектика | До 1,0 | 0,50 |
| До 2,0 | 0,62 | ||
| Фосфор | Эвтектика | До 0,2 | 0,08 |
| Сера | До 0,2 | 0,11 | |
| Алюминий | Твердый раствор | До 1,0 | 0,30 |
| Ванадий | Твердый раствор | До 10 | 0,50 |
| Титан | Эвтектика | До 15 | 0,83 |
| Цирконий | До 7 | 0,61 |
Степень обогащения зависит¸ кроме коэффициента распределения¸ от скорости роста (охлаждения) и размера дендритной ячейки¸ которые
 |
Рис. 4.13. Зависимость состава границ между ветвями дендритов
от скорости роста (u)¸ размера ветви (r) и коэффициента диффузии (D)
в жидкости для углерода (K = 0.26)
можно объединить в критерий Sm = u r / D¸ это отражено на рис. 4.13.В крупных заготовках степень обогащения границ дендритов выше, чем в мелких, однако последующая переработка крупных заготовок экономически более целесообразна.
Следует отметить, что полиморфные превращения по математическому описанию ничем не отличаются от кристаллизации скорость роста новой фазы в них определяется соотношением теплоты фазового превращения и теплоотводом¸ имеются аналогичные коэффициенты распределения между старой и новой фазой. Однако теплота перехода и коэффициенты диффузии при этом значительно меньше и образующаяся фаза имеет значительно меньшие размеры.
Неметаллические включения
Неметаллические включения в отливках представляют собой твердые частицы соединений компонентов сплавов с неметаллическими примесями. Их размеры колеблются от долей микрона до десятков микрон. Основная масса неметаллических включений в литейных сплавах делится по составу на окислы и сульфиды. По видам источников неметаллические включения де
|
|
а) _ б)
Рис. 10.1. Формы неметаллических включений: а — сферические; б.— кристаллические; в — дендритные; г — пленочные
лятся на попадающие в сплав вместе с шихтой, продукты взаимодействия компонентов сплава с примесями или добавками, продукты взаимодействия компонентов сплава с атмосферой. По формам неметаллические включения делятся на круглые, кристаллические, дендритные и пленочные (рис. 10.1).
Методы определения неметаллических включений в сплавах бывают химические и металлографические.
При химическом методе образцы сплава растворяются в слабых кислотах, часто с наложением постоянного тока, а включения остаются в растворе в виде осадка и отделяются от него фильтрацией. Они изучаются под микроскопом, а их состав определяется методами микрохимического анализа. К сожалению, при выделении часть включений, в особенности сульфидных, разрушается.
При металлографическом методе неметаллические включения изучаются на шлифах. Оценка количества производится либо при просмотре определенного числа полей и их сравнении с эталонами, либо сплошным обмером всех включений, находящихся на определенной площади. При обмере определяются диаметр каждого включения и их число. Эти величины позволяют вычислить средний процент площади, занятой включениями на шлифе.
Неметаллические включения делятся на растворимые в основе сплава в жидком состоянии и мало- или почти нерастворимые. Первая группа формируется в качестве самостоятельной фазы только при кристаллизации; вторая может существовать в жидком металле в виде мелких частиц.
Соединения, входящие в состав неметаллических включений, наиболее часто встречающиеся в литейных сплавах, указаны в табл. 10.1.
Таблица 10. 1.
Соединения, входящие в состав неметаллических включений различных сплавов
| Основа сплава | Окислы | Сульфиды | Нитриды нерастворимые | ||
| нерастворимые | растворимые | нерастворимые | растворимые | ||
| Fe | Si02 А1А МпО Сг03 ТЮ2. | FeO | — | FeS MnS | TiN |
| Си | SnO2 А1 | CuO Cu20 | — | Cu2S CuS | — |
| А1 | А1203 MgO | — | MgS | — | — |
| Mg | MgO А1А | MgS | — | — | |
Массовая доля кислорода в %, а следовательно, и окисных включений в важнейших литейных сплавах характеризуется следующими цифрами:
Сталь ................ 0,01—0,03
Чугун ................ 0,002-0,006
Бронза ................ 0,08—0,15
Объемная доля сульфидных включений в железных сплавах равна или больше объемной доли окислов.
Неметаллическая фаза в сплавах на основе алюминия и магния представлена в основном окислами, имеющими форму плен. В сталях плены встречаются в больших количествах только в тех случаях, когда она содержит легирующие добавки элементов, образующих устойчивые окислы — хром, алюминий, титан.
Малорастворимые включения (например, окислы в стали) при увеличении скорости кристаллизации в широком диапазоне не изменяют своих размеров. Только при затвердевании очень крупных слитков наблюдается тенденция к их укрупнению. По-видимому, это связано с коагуляцией включений при длительных выдержках в жидком состоянии. На объемную долю этих включений скорость кристаллизации не оказывает никакого влияния.
Неметаллические включения, относящиеся к этим двум группам, образуются элементами, дающими с основой сплава диаграммы состояния различного типа. Железо и медь происходит накопление примеси, достигающее эвтектической концентрации у границ зерен, даже если исходного содержания примеси в жидком металле было мало.
Для предотвращения образования или уменьшения количества неметаллических включений в сплавах необходимо проведение следующих мероприятий:
А. Борьба с нерастворимыми включениями.
1. Отстаивание жидкого металла. Способ действенен только по отношению к крупным включениям.
2. Продувка сплавов инертными газами, пузырьки которых увлекают за собой и флотируют включения.
3. Обработка цветных сплавов флюсами, растворяющими окисные включения и переносящими их в слой шлака.
4. Фильтрация через огнеупорные фильтры легких цветных сплавов.
Б. Борьба с растворимыми включениями.
I - Переведение растворимых включений в нерастворимые, способные легко удаляться из соединения, например раскисление.
2. Ускорение затвердевания.
Газы
Под газами в металлах понимаются такие простые тела или соединения, которые при нормальных условиях в свободном состоянии находятся в газообразном виде.
При выделении из раствора в процессе кристаллизации газы могут образовывать пустоты, которые разделяются на скопление мелких пузырьков, называемых газовой по р и с т о с т ь ю, и отдельные крупные пузыри, называемые газовыми р а ковинами. Их выделение из раствора в твердом металле может вызывать значительные местные давления, внутренние напряжения и надрывы, которые проявляются в виде флокенов в стали или вспучивания на листах из цветных сплавов.
Некоторые газы, в частности водород, оставаясь в растворенном состоянии в твердых сплавах, понижают их механические свойства.
Источниками газов в отливках являются:
1) шихтовые материалы, содержащие их в растворенном состоянии или в виде окисленных поверхностей;
2) атмосфера печи при плавке, которая содержит основные компоненты воздуха — азот и кислород; водяные пары и водород, образующийся при их разложении; окислы углерода и серы, образующиеся при сгорании топлива;
3) атмосфера формы при разливке.
Методы определения газов в сплавах делятся на следующие.
Химический анализ. В этом случае образец из сплава нагревается (желательно до расплавления) в высоком вакууме. При этом газы из него выделяются, а затем определяется их количество и состав обычными методами газового анализа.
Технологические пробы. В этом случае о содержании газов судят по их выделению в пробе сплава, затвердевающей в определенных условиях. Например, в алюминиевых сплавах тигель с расплавом охлаждают при давлении 0,1 мм рт. ст. В этих условиях выделение газов происходит весьма интенсивно и довольно полно с образованием пористости. После охлаждения пробу разрезают и подсчитывают количество газовых пузырьков на 1 см2 поверхности продольного разреза. Развитие пористости, пропорциональное содержанию газа, можно определять по эталонам и выражать в баллах.
Кроме того, за последнее время получают распространение различные физико-химические методы определения газов, например метод спектрального анализа.
Количество газов выражается либо в процентах, либо в кубических сантиметрах (при нормальных условиях) на 100 г сплава.
Зависимость растворимости газа в жидком металле S от давления определяется по формуле, впервые предложенной А. Сивертсом в 1912 г.,
где р — парциальное давление газа в кгс/сма; А — постоянная для данного металла и газа величина.
S= 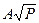
Одним из эффективных средств удаления газов из металла является вакуумирование, т. е. выдерживание или переливание его в расправленном состоянии в вакууме.
Зависимость растворимости газа в жидком металле от температуры в ряде случаев может выражаться формулой
S=B e- 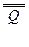 (11.1)
(11.1)
где В — постоянная для данного газа и металла величина; Q теплота растворения газа; Т — абсолютная температура.
|
|
Рис. 11.1 Схема растворимости газа от температуры.
При переходе из жидкого состояния в твердое и при аллотропических превращениях растворимость газов изменяется скачкообразно. Общая схема зависимости растворимости газа S от температуры металла представлена на рис. 11.1 При температуре кипения растворимость всех газов падает до нуля. У некоторых металлов, например цинка, растворимость газов падает, начиная с точки кристаллизации.
С алюминием и магнием азот образует нитриды. Однако в реальных сплавах они не имеют значения. С медью азот практически не взаимодействует. Кислород со всеми металлами образует окислы, которые являются неметаллическими включениями. Его растворимость в твердых чистых металах очень мала.
Хлор является инертным газом по отношению к алюминию и магнию; в других металлах он не встречается.
Аргон и гелий инертны по отношению ко всем металлам. Реальные содержания газов в литейных сплавах всегда существенно меньше, чем их растворимость в твердом состоянии при температуре кристаллизации.
В условиях кристаллизации при малых коэффициентах распределения концентрации растворенных газов около границы зерен возрастают. Однако газы, в особенности водород, обладают в металлах высокой скоростью диффузии, и это снижает вероятность их выделения. Кроме изменения растворимости, образование газовых пузырей возможно за счет протекания реакций с получением газообразных продуктов. Например, при недостаточно раскисленной стали в результате увеличения концентрации углерода и кислорода вблизи границы твердой фазы при кристаллизации, протекает реакция FеО + С = Fe + CO .
Для образования самостоятельной фазы в жидком металле газовый пузырек должен преодолеть давление атмосферы рв, гидростатический напор рH и поверхностное натяжение металла σ. Для того чтобы пузырек мог расти, давление р в нем должно отвечать следующему неравенству:
р>Ра + ρн + 2σ/r (11.1)
Если радиус пузырька r равен нулю, то давление, необходимое для его возникновения, становится бесконечным. Следовательно, его возникновение в непрозрачной жидкости весьма затруднено.
Возникновение пузырьков, как и кристаллов в жидкости, происходит несравненно более легко на твердых поверхностях в виде гетерогенных зародышей из флюктуации растворенных атомов газа.
Если в жидкий металл вводятся пузырьки нейтральных газов, то парциальное давление в них будет равно нулю, и растворенные газы легко проникают в пузырек.
Пузыри, формирующиеся в зоне ориентированных кристаллов, растут между ними и имеют вытянутую форму. При большом развитии, например, в слитках кипящей стали, их называют сотовыми пузырями. По границе зоны столбчатых кристаллов наблюдается усиленное образование пузырей, связанное с изменением режима кристаллизации. В средней части отливки образуются так называемые ликвационные пузыри, не имеющие определенной ориентации, как и окружающие их кристаллы. Для уменьшения содержания газов в литом металле проводятся следующие основные мероприятия.
1) Пересечение всех путей попадания газов в жидкий металл: применение незагрязненной шихты; защита металла при плавке шлаками и флюсами; плавка и разливка в атмосфере инертных газов или вакууме.
2) Продувка жидкого металла инертными газами; введение в сплавы соединений, образующих при взаимодействии с металлом инертные газообразные вещества; перелив и выдерживание металла в вакууме (вакуумирование).
3) Обработка металла веществами, связывающими газы в устойчивые соединения; раскисление металла.
4) Применение некоторых специальных мероприятий: нагрев легкоплавких металлов до температуры кипения; вымораживание, заключающееся в предварительной разливке в чушки для удаления избытков газов, с последующей переплавкой; вибрационная обработка, способствующая дегазации и др.
Дата: 2019-04-23, просмотров: 393.

