1,2-Гликоли при каталитическом действии кислот могут перегруппировываться в кетоны. Реакции этого типа аналогичны перегруппировкам карбониевых ионов, которые образуются при действии кислот на одноатомные спирты. Так, при действии кислот, например, на 2,3-диметилбутандиол-2,3 (пинаколин) он перегруппировывается в кетон – 3,3-диметилбутанон-2 (пинаколин). Такая перегруппировка называется пинакон-пинаколиновой. Пинакон-пинаколиновая перегруппировка осуществляется в несколько стадий. Сначала протон кислоты присоединяется к одному из гидроксилов двухатомного спирта и образует оксониевое соединение (1). Этим самым протон активирует данный гидроксил к реакции отщепления. На следующей стадии от оксониевого соединения (1) отщепляется за счет активированного гидроксила вода и образуется карбониевый ион (II), который затем перегруппировывается путем перемещения соседней метильной группы (1,2-замещение) в оксониевый катион (III).Катион (III) на заключительной стадии депротонизируется и превращается в конечный продукт реакции – кетон:
|
|
| |||||||||
|
| ||||||||||
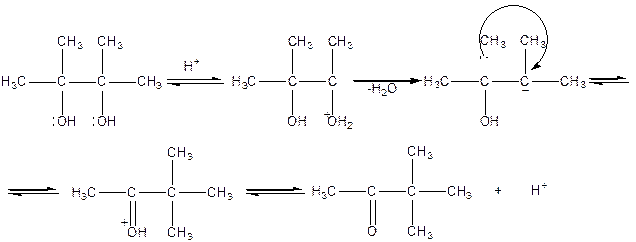
ТРЕХАТОМНЫЕ СПИРТЫ (ГЛИЦЕРИН)
Трехатомные спирты имеют три гидроксильные группы, их хмимческий состав описывается общей формулой CnH2n-1(OH)3. Устойчивыми являются такие трехатомные спирты, в молекулах которых гидроксильные группы расположены у разных углеродных атомов. Если три гидроксильные группы находятся у одного углеродного атома, то такие спирты неустойчивы, легко распадаются, отщепляя воду за счет гидроксильных групп, и превращаются в карбоновые кислоты:

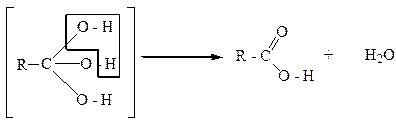
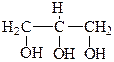 Первым и наиболее важным представителем трехатомных спиртов является глицерин (Tкип.=290оC), который открыл К. Шееле в 1779 г.
Первым и наиболее важным представителем трехатомных спиртов является глицерин (Tкип.=290оC), который открыл К. Шееле в 1779 г.
По систематической номенклатуре название трехатомного спирта образуют от названия соответствующего углеводорода, к которому добавляют суффикс – триол, указывая номера атомов углерода, возле которых находятся гидроксильные группы. Так, глицерин по этой номенклатуре называется пропантриол-1,2,3.
МЕТОДЫ ПОЛУЧЕНИЯ
1. Глицерин получают гидролизом (омылением жиров), который осуществляется в присутствии воды под влиянием кислот, щелочей или ферментов (например, липазы). В результате гидролиза жиры расщепляются на глицерин и соответствующие высшие карбоновые кислоты:
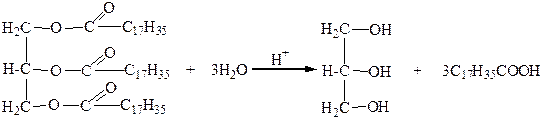
2. Синтезом из пропилена, который включает несколько стадий:
Аллиловый спирт
Хлористый аллил
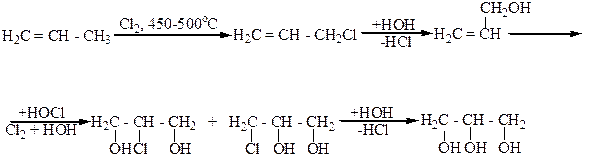
Монохлоргидрины глицерина
ХИМИЧЕСКИЕ СВОЙСТВА
Химические свойства глицерина аналогичны свойствам этиленгликоля и обусловлены присутствием в его молекуле трех гидроксильных групп. Благодаря взаимному влиянию гидроксильных групп кислотные свойства выражены более сильно по сравнению с одноатомными спиртами. Степень диссоциации глицерина приблизительно в 10 раз больше, чем у метилового спирта. Вследствие этого глицерин легко образует глицераты (алкоголяты) не только со щелочными металлами, но и со щелочами, и с гидроксидами железа, меди, кальция, бария и др. металлов. При этом нерастворимые в воде гидроксиды, например гидроксид меди, растворяются. Растворение Cu(OH)2 осуществляется с образованием комплексного соединения (глицерата меди) характерного синего цвета:
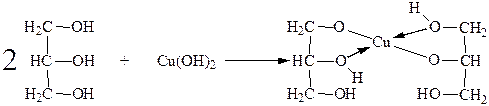
Глицерат меди
Эта реакция является качественной на глицерин и другие многоатомные спирты, с помощью этой реакции можно отличить от одноатомных. Поскольку одноатомные спирты с Cu(OH)2 не взаимодействуют.
Следует отметить, что способность этиленгликоля, глицерина и других многоатомных спиртов растворять Cu(OH)2 связана не только с повышением их кислотности, но также со способностью этих спиртов образовывать внутрикомплексные высокоустойчивые соединения.
Глицерин может вступать в реакцию с галогеноводородами (HCl, HBr). При этом в его молекуле одна или две гидроксильные группы замещается на галоген и образуются галогеноспирты, которые называют галогеногидринами глицерина:
Дихлоргидрины глицерина
Монохлоргидрины глицерина
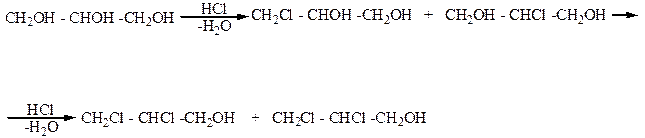
ДИХЛОРГИДРИНЫ ГЛИЦЕРИНА
Органические и минеральные кислоты образуют с глицерином сложные эфиры. В зависимости от количества введенной в реакцию кислоты образуются полные или неполные сложные эфиры. Например, при достаточном колическтве HNO3 образуется полный эфир азотной кислоты – тринитрат глицерина, который часто не совсем верно называют нитроглицерином:
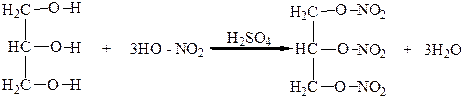
Тринитрат глицерина – взрывчатое вещество и используется для приготовления динамита. Тринитрат глицерина ядовит, однако в небольших количествах он расширяет кровеносные сосуды сердца. Поэтому его используют в медицине для лечения стенокардии.
Глицерин может образовывать полные и неполные сложные эфиры и с органическими кислотами, например с уксусной:
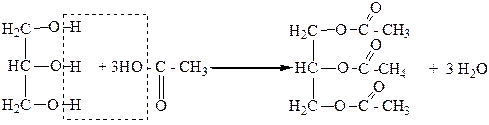
Глицеринтриацетат
Взаимодействие глицерина с высшими карбоновыми кислотами приводит к образованию сложных эфиров, которые называют жирами:
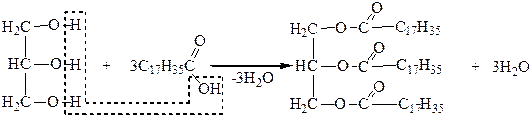
|
|
Глицерин, как и другие спирты, легко окисляется. Причем окислению могут подвергаться одна, две или все три гидроксильные группы. Первичные гидроксильные группы окисляются в альдегидные, а потом в карбоксильные группы. Вторичная ОН-группа окисляется в кетонную. Состав продуктов окисления зависит от природы окислителя.
При окислении глицерина можно получить такие вещества:
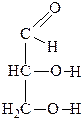
| 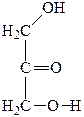
| 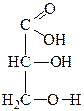
| 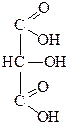
| 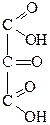
|
| Глицериновый альдегид | Диоксиацетон | Глицериновая кислота | Тартроновая кислота | Мезоксалевая кислота |
ФЕНОЛЫ
Фенолами называются гидроксильные производные ароматических углеводородов, у которых один или более атомов водорода бензольного кольца замещены гидроксильной группой.
В зависимости от количества гидроксильных групп фенолы делятся на одно-, двух- и трехатомные.
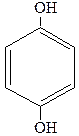
Простейшим фенолом является одноатомный фенол, или как его принято называть „карболовая кислота” C6H5OH. Из двух атомных фенолов или дигидроксибензолов большое значение имеют следующие:
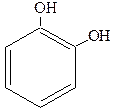
| 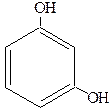
| 
|
| Пирокатехин Орто-дигидроксибензол (1,2-дигидроксибензол) | Резорцин Мета-дигидроксибензол (1,3-дигидроксибензол) | Гидроксихинон Пара-дигидроксибензол (1,4-дигидроксибензол) |
Существуют и трехатомные фенолы, как, например, порогаллол, флоро-глюцин и гидроксигидрохинон:
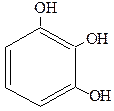
| 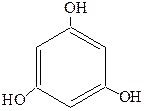
| 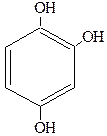
|
| Пирогаллол (1,2,3-тригидроксибензол) рядовой изомер | Флороглюцин (1,3,5-тригидроксибензол) симметричный изомер | Гидроксигидрохинон (1,2,4-тригидроксибензол) несимметричный изомер |
Дата: 2019-04-23, просмотров: 424.