Отек легких вследствие повышенной проницаемости (ОЛГТП) вызывается острым обширным повреждением эндотелия легочных микрососудов. Анатомическая основа такого отека легких была изучена при электронномикроскопических исследованиях легких после острого повреждения. Вода и белок выходят из легочного микроциркуляторного русла в прилегающие интерстициальные и альвеолярные пространства сквозь появившиеся щели между поврежденными клетками эндотелия и эпителия. Возможно, такие щели образуются в результате разрушения и слущива-ния некротизированных клеток.
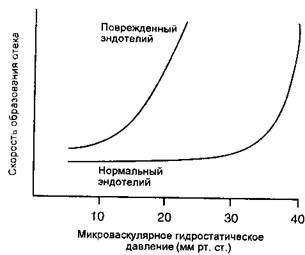
Рис. 14-8 иллюстрирует главные физиологические различия между ОЛПП и гемодинамическим отеком. В первом случае острое повреждение легочной микроциркуляции повышает коэффициент фильтрации (Kf) и снижает коэффициент осмотического отражения (а) эндотелия настолько, что жидкость проникает в легкие с непропорционально высокой скоростью относительно системного движущего давления. Когда проницаемость альвеолярно-капиллярной мембраны повышается, отек развивается даже при нормальных величинах микрососудистого гидростатического давления (8-12 мм рт. ст ). При более высоких величинах давления наблюдается
тяжелый отек.
Помимо изменения величины этих двух констант уравнения Старлинга острое повреждение микроциркуляции ослабляет или подавляет факторы защиты от отека, связанные с просеивающим эффектом. Поскольку поврежденные стенки микрососудов плохо задерживают белки плазмы, их содержание в фильтрате не уменьшается с ростом скорости фильтрации (рис. 14-9). Следовательно, онкотическая сила абсорбции [а (П)т, - П,)] не растет при повышенных скоростях фильтрации. В результате, нет противодействия дальнейшей фильтрации жидкости, как это происходит в здоровых легких.
ОЛПП и гемодинамический отек отличаются также по своему течению. Гемо-динамический отек часто проявляется в первые минуты после внезапного повыше-
Рис. 14-7. Двустороннее1 "затуманивание", вызванное тяжелым it мод и нами-ческим отеком легких
Рис. 14-8. Отношение между микрососудистым гидрос гаги'к чжим давлением и скорость ю раз! жтия отека у пациента с и лрмалг пым эпителием легких и у пацисьта е острым повреждением: элдотс кия
мня легочного капиллярного гидростатического давления, подобно острому инфаркту миокарда. В противоположность этому ОЛПП клинически не п роявляется в течение 6-48 ч с момента острого повреждения легких. Этот временной интервал, возможно, отражает постепенню усиливающееся воздействие на прон ицаемо^сть капилляров воспалительной реакции, вызванной первичным поврежде нием легких.
Оба типа отека имеют и разные скорости восстановления функции легки х. Гемодинамический отек заметно уменьшается в течение нескольких часов после4 восстановления нормального легочного микрососудистого давления. Вода активно всасывается из альвеолярных воздушных пространств через неповрежденный эгг.ите-лий с помощью АТФ-зависимых ионных каналов. Даже тяжелый гемодинами1 чес-кий отек может разрешиться полностью всего за 2-4 дня. Срок разрешения ОЛ1Ш, как правило, больше. Репарация остро поврежденных альвеолярно^-капиллярн ых мембран требует времени. Кроме того, высокое содержание белка в отечной жид! со-сти снижает скорость разрешения отека, поскольку белок "возвращается" в инте р-стиций через эпителий гораздо медленнее, чем вода и соли.
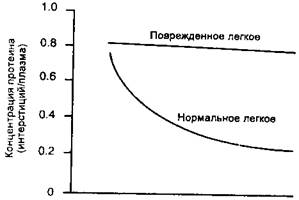
Рис. 14-9. Утрата просеивающего эффекта при остром повреждении легких. Отношение концентрации протеина в иптерстиции к таковой в плазме в поврежденных легких не понижается с увеличением мик-роваскулярного гидростатического давления, поскольку поврежденный эндотелий слабо ограничивает проход протеинов плазмы

Дата: 2019-03-05, просмотров: 346.