Продукты, получаемые на установках по разделению изотопов урана: 1) гексафторид урана, обогащенный легким изотопом уран-235 до 2,5, 5, 10, 40, 60, 90 и даже 95—98% его содержания. Понятно, что процентный выход такой обогащенной фракций всецело зависит от степени обогащения: он мал при высокой степени обогащения и намного больше при низкой. Но даже для сравнительно низкой степени обогащения (например, 2%) он не превышает 20—25%; 2) гексафторид урана, обедненный легким изотопом уран-235 до его содержания 0,2— 0,4%. Выход этой фракции близок к исходному количеству гексафторида урана и колеблется в пределах 75—99% от него. Это так называемый отвальный гексафторид урана.
Для практического использования в качестве ядерного топлива требуется обогащенный уран в виде металла, двуокиси, тетрафторида или некоторых других соединений (карбиды, нитриды и т. п.). Поэтому гексафторид урана приходится перерабатывать снова в окислы, тетрафторид и металл с использованием описанных ниже химико-технологических методов.
Гидролиз UF6 в водной среде. В основе этого метода лежит реакция
UF6 + 2Н2О ® UО2F2 + 4НF + 50,5 ккал/моль.
Эту реакцию практически можно осуществить по-разному, например с помощью барботажа газообразного UF6 через воду или смешением твердого UF6 с водой.
В обоих случаях существенно обеспечить надлежащий отвод тепла, поэтому процесс проводят в охлаждаемых агитаторах, выполненных из платины, серебра, иногда свинца (или футерованных этими материалами), с мешалками. Из полученного раствора UO2F2 + НF осаждают диуранат аммония, который отфильтровывают и прокаливают до закиси-окиси урана (рис. 109). Далее следует восстановление до UO2. Главная задача при этих операциях—наиболее полное удаление F-, для чего используют высокую температуру (~900° С), длительное время и воздействие паров воды (пирогидролиз). Полученная двуокись урана может идти непосредственно на приготовление керамических твэлов. Надо подчеркнуть, что за последнее время твэлы на основе обогащенной двуокиси урана получают все большее распространение.
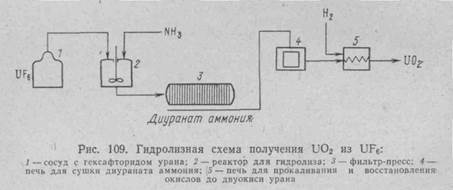
Если же предполагается получить металлический уран, то двуокись подвергают гидрофторированию по рассмотренному нами ранее методу с получением тетрафторида урана, который поступает на металлотермическое восстановление до металла. Несмотря на то, что несколько лет тому назад описанный гидролитический метод был распространен повсеместно, в настоящее время он признан устаревшим и заменяется другими методами. Основные недостатки гидролитического метода: громоздкость и многостадийность технологии: повышенные потери дорогостоящего обогащенного урана, связанные с громоздкостью и многостадийностью схемы; полная потеря всего фтора гексафторида урана.
Восстановление гексафторида урана водородом. В основе метода лежит реакция, осуществляемая в газовой фазе:
UF6газ + Н2 газ ® UF4 тв + 2HF газ. (DН0298 == — 68,8 ккал/моль).
Процесс протекает со значительной убылью энергии Гиббса, но энергия активации реакции восстановления UF6 водородом очень велика и для ее осуществления требуется подвод тепла. Экспериментально показано, что при 100° С между UF6 и Н2 никакого взаимодействия не происходит. Оно начинается с очень малой скоростью лишь при 225—250° С. Однако и при 350° С процесс протекает только наполовину, даже если содержание Н2 в пять раз больше стехиометрического количества.
Исследования, проведенные за последнее время, показали, что трудности, обусловленные высокой энергией активации, можно успешно преодолеть и обеспечить эффективное осуществление данного процесса в аппарате типа пламенного реактора. Для этого тепло, необходимое для начала и поддержания реакции, подводят к системе извне через стенки реактора (метод горячестеночного реактора). Общая высота реактора производительностью 45 кг/ч по гексафториду урана составляет 4,3 м при диаметре трубы 152 м.м. Температуру стенок реактора поддерживают в пределах 430—540° С. Подачу водорода производят в двойном против требуемого по реакции количестве.
Описанный процесс позволяет получать тетрафторид урана очень хорошего качества с высокой насыпной массой (3,4—5 г/см3). Серьезный недостаток горячестеночного реактора - перегрев стенок, особенно в верхней зоне аппарата, оплавление и налипание материала на стенках, частые перебои в работе и необходимость остановки аппарата для его чистки. Продолжительность непрерывной работы не выше 8 ч.
Недостатки горячестеночных реакторов потребовали направления усилий исследователей на поиск других инженерных технологических решений процесса восстановления гексафторида урана водородом. Такое значительно более эффективное решение представляет собой совместная подача в реактор смеси UF6 + F2.
За счет энергии реакции Н2+F2 = 2НР (DН°=—128 ккал/моль) в факеле фторводородного пламени возбуждается и реакция восстановления UF6 до UF4. Применяемый аппарат аналогичен описанному выше, однако его стенки охлаждают до 95—205° С. Аппаратурная схема восстановления гексафторида урана водородом в холодностеночном реакторе показана на рис. 110.
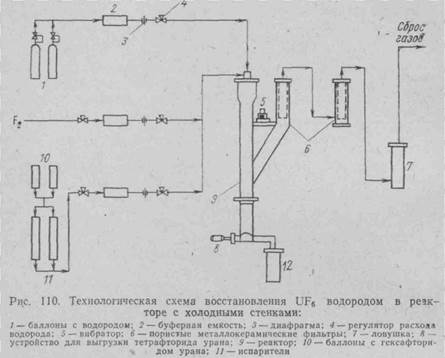
Процесс позволяет получать прекрасный продукт с весьма малым содержанием примесей (0,002%) и высокой насыпной массой. Содержание UF6 в отходящих тазах ничтожно мало (0,0002%), что свидетельствует о полноте протекания реакции.
Вибраторы, установленные на реакторе, препятствуют накоплению порошка UF4 на стенках аппарата. Весь UF4 собирается в нижней части, откуда его непрерывно выгружают с помощью шнека. В некоторых случаях целесообразно осуществлять процесс в вакууме, что также возможно в аппаратах данного типа.
Превращение гексафторида урана в двуокись в пламенном реакторе. Поскольку двуокись урана в настоящее время продолжает оставаться одним из наиболее распространенных химических соединений, применяемых для непосредственного изготовления твэлов, представляет большой интерес организация производства этого продукта из гексафторида урана, обогащенного изотопом уран-235.
Этот процесс можно осуществить в пламенном реакторе с использованием кислородо-водородного пламени. Общая реакция может быть описана уравнением
UF6 + 3H2 + O2 ® UO2 + 6HF.
При этом возможны промежуточные стадии:
2Н2 + О2 ® 2Н2О;
UF6 + Н2 ® UF4 + 2HF;
UF4 + 2Н2О ® UO2 + 4HF;
или UF6 + 2H2O ® UO2F2 + 4НF;
UO2F2 + 2Н2 ® 2HF + UO2
или UO2F2 + Н2O ® 2HF + UO3;
UO3 + Н2 ® H2O + UO2.
В продуктах реакции пламенного реактора (температура около 1300° О обнаружены UO2, UO3, UF4, U(ОН)4, Н2O, UO2F2. Основным элементом, загрязняющим конечный продукт, был фтор, содержание которого составляло 4—8%. Содержание фтора в продукте, полученном пламенным пирогидролнзом, значительно снижалось при термической обработке его в водороде при 1000° С и достигало значения менее 3.10-3%, что вполне удовлетворительно.
Известно, что уранил-фторид восстанавливается водородом до UF4 при 600—1000° С, а получаемый тетрафторид при этом далее не восстанавливается и не улетучивается. Поэтому возможный механизм глубокого обесфторирования продукта состоит в том, что UF4 гидролизуется парами воды, источником которой является адсорбированная влага, продукт восстановления UО3 и продукт разложения U(ОН)4.
Как показывает практика некоторых заводов, этот процесс непосредственного получения обесфторенной двуокиси урана можно осуществлять в холодностеночном пламенном реакторе непрерывно и без вынужденных остановок и перебоев в работе.
 Подача исходных продуктов организована так. Три газа (UF6, O2 и F2) поступают по центральной трубке, а Н2 — по кольцевому зазору. F2 подают только в самом начале для инициирования процесса взаимодействия UF6 с водородом.
Подача исходных продуктов организована так. Три газа (UF6, O2 и F2) поступают по центральной трубке, а Н2 — по кольцевому зазору. F2 подают только в самом начале для инициирования процесса взаимодействия UF6 с водородом.
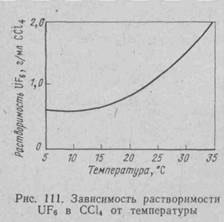
Восстановление UF6 четыреххлористым углеродом. Этот метод технологически также очень интересен и имеет практическое применение в технологии ядерного топлива. Как уже указывалось, UF6 легко растворим в ССl4, причем получаемые растворы вполне устойчивы. Характер зависимости растворимости UF6 в ССl4 от температуры иллюстрирует рис. 111.
Однако при более высоких температурах, например ³150° С, характер взаимодействия совершенно меняется. Происходит бурная реакция, причем Сl2 и ССl2F являются легколетучими веществами:
UF6 + 2ССl4 ® UF4 + Сl2 + ССl2F (DH0298 == — 53 ккал/моль),
Исходные материалы загружают в нагреваемый автоклав. При температуре »150°С в автоклаве быстро возрастает давление, по которому и судят о ходе реакции. Дозируемое количество ССl4 вдвое больше, чем требуется по реакции. Выход UF4 достигает 99,7%. Насыпная масса получаемого тетрафторида »2 г/см3. Продукт очень чистый, потери урана незначительны. Как правило, в отходящих газах уран не обнаруживают.
Применение автоклавного способа восстановления гексафторида ССl4 эффективно для фракций UF6 высоких степеней обогащения, так как именно в этом случае необходимо контролировать габариты и критическую массу вещества. Для многотоннажного производства тетрафторида из продукта низких степеней обогащения возможна организация процесса непрерывного восстановления с помощью ССl4. Его осуществляют в трубчатой вращающейся печи при температуре 200—300° С (а еще лучше 400—450° С), получаемой предварительным нагреванием подаваемых газов UF6 и ССl4 до 300° С и использованием теплоты реакции. Для завершения реакции в газовой фазе достаточно пребывания материалов в печи в течение 10 мин. Схема процесса восстановления гексафторида урана с помощью ССl4 в трубчатой печи показана на рис. 112.
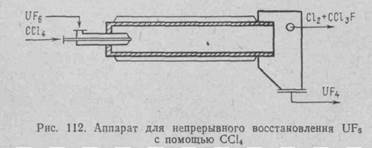
Описанные методы переработки гексафторида урана наиболее распространены на практике. Среди других предложенных, но еще не внедренных в производство методов внимания заслуживает непосредственное восстановление газообразного гексафторида урана до металла, парами натрия по реакции и UF6 + 6Nа ® U + 6NaF, протекающей со значительным уменьшением энергии Гиббса (DG01250K =—200 ккал/моль). К преимуществам этого процесса помимо его простоты и малого количества необходимых операций можно отнести возможность создания высокопроизводительных установок непрерывного действия, низкое давление в реакторе, более низкую стоимость реагентов, невысокие капитальные и эксплуатационные затраты и другие потенциальные преимущества. Однако основной проблемой, осложняющей реализацию данного способа, остается подбор достаточно стойких конструкционных материалов, которые можно было бы использовать при высокой температуре в среде UF6.
Из других методов стоит упомянуть о предложении восстанавливать ирб газообразным хлористым водородом при 200—400o С или о возможной замене ССl4 другими органическими восстановителями, например трихлорэтиленом СНСl-CCl2.
Однако эти способы не имеют особенных преимуществ перед ранее описанными и иногда вносят дополнительные трудности.
Хорошим восстановителем UF6 является аммиак, действующий уже на холоду и очень энергично при 100—200° С.
Повышенное содержание легкого изотопа уран-235 па химию процессов переработки гексафторида урана не влияет, однако оно обусловливает ограничения и специфические требования к аппаратурному оформлению с точки зрения ядерной безопасности.
При всех операциях с обогащенным ураном, чтобы избежать возникновения цепной реакции, необходимо строжайшим образом учитывать критические массы и факторы, влияющие на их значение. К ним прежде всего относятся: количество присутствующего изотопа уран-235; степень обогащения ураном-235, выраженная массовым процентом урана-235, геометрия объема, отношение поверхности к объему; концентрация делящегося изотопа в растворе или в твердом веществе; отражение нейтронов от окружающих предметов; замедление нейтронов; поглощение нейтронов; степень гомогенности распределения делящегося изотопа по объему и некоторые другие факторы.
Относительно меньший масштаб работ с ураном высоких степеней обогащения несколько облегчает реализацию мероприятий по специальной технике безопасности. Тем не менее, строжайшее соблюдение правил ядерной безопасности является законом.
Требования к качеству обогащенной двуокиси урана. Основными объектами применения урана со степенями обогащения от 1 до 5% урана-235 являются атомные электростанции и двигатели кораблей торгового флота, ледоколов и некоторых других транспортных средств.
Уран, содержащий более 5% урана-235, применяют, когда возникает необходимость иметь мощные источники энергии при их малой массе. Сюда, например, относятся малогабаритные транспортабельные военные реакторы американской армии, работающие на обогащенном уране с содержанием урана-235- более 90%, реакторы для подводных лодок (военно-морской флот США, Англии и Франции) и небольших кораблей. Хорошо известно использование высокообогащенного урана для военных целей, а также при осуществлении подземных ядерных взрывов в мирных целях.
При этом в большинстве случаев используют или металлический уран (чаще в виде сплавов), или, особенно в связи с бурным развитием ядерной энергетики в последние годы, в виде двуокиси урана. Положительные свойства двуокиси урана — ее стойкость в условиях длительного облучения, термостойкость, отсутствие аллотропических модификаций и анизотропности, а также хорошая совместимость с большинством жидких и газообразных теплоносителей. Относительно пониженное содержание урана в двуокиси по сравнению с металлическим ураном может быть компенсировано некоторым дополнительным количеством ядерного топлива (урана-235).
К двуокиси урана как к одному из основных видов конечной товарной продукции предъявляют чрезвычайно жесткие и строгие технические требования по чистоте и некоторым другим параметрам.
В качестве примера рассмотрим требования Государственного стандарта США (АSТМ Standart) к порошкообразной спекаемой двуокиси урана ядерной чистоты. Содержание урана — не менее 87,7% массы сухого вещества. Содержание влаги—не более 0,40% массы урана. Содержание примесей не должно превышать следующих количеств, млн"': Тh 10; Аl, С, Со 100; Са, Мg, Cr, Ni, N, Si 200; Сu, Fe, Pb, Mg, Mo, P, Ta, Sb, Ti, V, Zn 250; Сl 350. Однако суммарное содержание перечисленных элементов не должно превышать 1500 млн-1. Помимо требований по химическому составу к товарной двуокиси урана предъявляют и другие требования (ядерные, физические, по изотопному составу урана и т. п.). Также строго оговорены методы пробоотбора, комплектации партий, анализа, других измерений, упаковки, маркировки и транспортировки. Из регламентированных физических свойств наиболее важны нормы на размер частиц двуокиси урана, насыпная масса, спекаемость, определяемые с помощью специальных методик.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какие соединения в системе уран-фтор вам известны? Укажите их основные свойства.
2. Охарактеризуйте кристаллогидраты тетрафторида урана, условия их образования и разрушения.
3. Укажите особенности и условия осуществления процесса гидрофторирования двуокиси урана.
4. Сколько гексафторида урана можно получить в год, если предприятие располагает 25 электролитными ваннами для получения фтора, работающими при силе тока 7кА?
5. Поясните взаимодействие гексафторида урана с водой. Приведите примеры.
6. Перечислите методы восстановления, шестивалентного урана до четырехвалентного в водной среде.
7. Какие промышленные методы переработки гексафторида урана вы знаете?
8. Охарактеризуйте различные способы конденсации гексафторида урана из газовой фазы.
9. Опишите основные тенденции, характеризующие равновесие в системе UO2 + 4HF « UF4+ 2Н2O.
10. Обоснуйте основные процессы, используемые в технологии гексафторида урана на основе диаграммы состояния Р—Т для гексафторида урана.
11. Укажите, как, по вашему мнению, можно использовать основные выводы диффузионно-кинетической теории гетерогенного реагирования для интенсификации процессов получения гексафторида урана?
12. Охарактеризуйте физико-химические основы улавливания гексафторида урана и фтора из отходящих газов.
13. Какие вам известны методы переработки гексафторида урана? Наиболее рациональные случаи их применения в конкретных случаях.
14. В чем заключается специфичность требований к качеству двуокиси урана, получаемой после переработки гексафторида урана?
Дата: 2019-02-25, просмотров: 363.