Процесс гидрофторирования двуокиси урана газообразным фтористым водородом описывается реакцией
UO2 + 4HF « UF4 + 2H2O
DHo298 =DH298 (UF4)+2DH298 (H2O)-DH298 (UO2)-4DH298 (HF) =-443–2. 68,3+259,2+4.64,2 = -63,6 ккал
Возможность прохождения того или иного процесса, при температуре, отличной от 298 К, определяют значения DGoT и константы равновесия К, которая зависит от температуры. Обе эти величины связывает уравнение изотермы реакции DGoT = -4,576 lg K, откуда lg K = DGoT /4,576 T. Изменение энергии Гиббса DGoT реакции для различных температур определяется решением уравнения Гиббса-Гельмгольца. При этом используются данные, имеющиеся в справочниках по термодинамике:
1) уравнения зависимости Ср от температуры для всех продуктов реакции;
2) теплоты образования DНo298 продуктов реакции при 298 К;
3) абсолютные значения энтропии, выраженные в единицах калория на моль.градус [кал/(моль.град] при 298 К.
Учитывая теплоту превращения воды в пар при 100оС и соответствующее изменение энтропии, получаем:
DGoT = -42 540 + 56,46Т (для 373 –1309 К)
Это уравнение позволяет вычислить значения DGoT и констант равновесия для некоторых температур, представляющих интерес для практики (табл. 41).
Таблица 41
Значение изменений энергии Гиббса DGoT и констант равновесия К реакции взаимодействия двуокиси урана и фтористого водорода
| Температура, оС | DGoT, ккал/моль | К |
| 100 | -21,48 | 3,9.1012 |
| 300 | -9,96 | 6,3.103 |
| 500 | +1,44 | 3,9.10-1 |
| 700 | +12,67 | 1,4.10-4 |
| 900 | +23,69 | 3,9.10-5 |
Зависимость DGoT от температуры изображена на рис. 95.
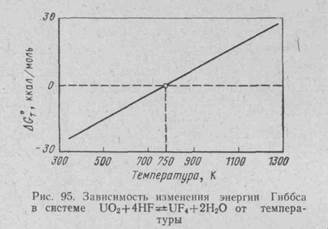
Таким образом, мы имеем дело с типичной обратимой реакцией с достаточно большим тепловым эффектом. Чем выше температура, тем «обратимее» реакция, тем больше ее стремление протекать справа налево. Каждой температуре отвечает определенное равновесное парциальное давление паров НF и Н2О. По закону действующих масс
K = [PHF]4/[PH2O]2.
Если PHF + PH2O =1, PHF / PH2O = K’, K = [K’/(K’+1)]2, т. е. константа равновесия реакции гидрофторирования двуокиси урана сильно зависит от относительной концентрации НF.
В табл. 42 приводится равновесное давление паров НF и Н2O в этой реакции при различных температурах.
Таблица 42
Равновесное парциальное давление паров HF и Н2О в реакции гидрофторирования
| Температура, оС | Равновесное парциальное давление | |
| HF | H2O | |
| 200 | 0,014 | 0,984 |
| 300 | 0,036 | 0,964 |
| 500 | 0,160 | 0,840 |
| 600 | 0,574 | 0,426 |
| 700 | 0,823 | 0,177 |
Мы видим, что тетрафторид урана должен чрезвычайно легко разлагаться водяным паром при повышенной температуре, так как вероятность обратной реакции увеличивается с температурой. Очевидно, что для обеспечения полноты реакции гидрофторирования двуокиси урана нужен избыток НF в газовой фазе. Когда же в газовой фазе преобладает Н2О, реакция протекает слева направо только при относительно низкой температуре.
Как показывает термодинамический анализ реакции, рационально организовать технологический процесс гидрофторирования двуокиси в несколько стадий. Однако закономерности кинетики значительно усложняют практическое решение задачи, так как скорость реакции при низкой температуре весьма мала. Скорость взаимодействия UО2 с НF определяется прежде всего температурой, затем концентрацией НF и Н2О. Причем последний фактор влияет отрицательно.
 Следует подчеркнуть огромное значение для практического осуществления гидрофторирования двуокиси урана ее физических и физико-химических характеристик. Поведение двуокиси урана в процессе гидрофторирования существенно зависит от ее «истории» и «происхождения», т. е. от метода и условий ее получения, исходных продуктов, температурных условий, крупности частиц и т. п.
Следует подчеркнуть огромное значение для практического осуществления гидрофторирования двуокиси урана ее физических и физико-химических характеристик. Поведение двуокиси урана в процессе гидрофторирования существенно зависит от ее «истории» и «происхождения», т. е. от метода и условий ее получения, исходных продуктов, температурных условий, крупности частиц и т. п.
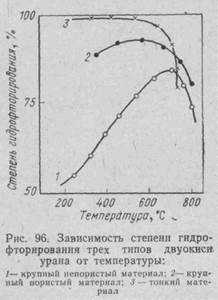
Все многообразие образцов двуокиси урана можно условно разделить на три типа: крупный непористый материал; крупный пористый материал; тонкий продукт.
На рис. 96 показана степень превращения трех типов двуокиси урана в процессе гидрофторирования при различных температурах.
Хотя и с термодинамической, и с кинетической точек зрения эффективнее использовать большой избыток НF в газовой фазе, на практике с учетом экономики все же стараются применять минимально необходимый избыток НF. Кроме того, для уменьшения времени гидрофторирования выгодно увеличить поверхность соприкосновения фаз в этой гетерогенной реакции. Примером практического осуществления гидрофторирования, где сделана попытка учесть оба этих обстоятельства, служит технология получения тетрафторида урана на заводах США в Падьюке и Уэлдон-Спринге. По существу аналогичные процессы применяют и на многих других установках (в США их 20) по получению тетрафторида за рубежом.
Гидрофторирование в шнековых реакторах. На заводах в Падьюке и Уэлдон-Спринге гидрофторирование осуществляют в трех горизонтальных шнековых реакторах, расположенных один над другим (рис. 97).
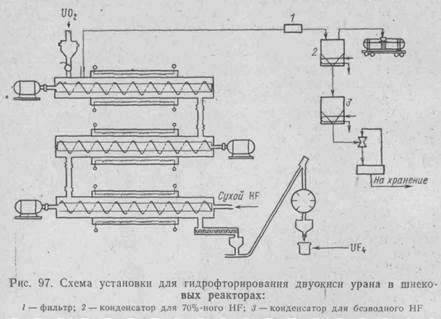
Шнек предназначен для транспортировки материала по длине реактора и для его перемешивания. В целях подавления обратной реакции, вызываемой накоплением водяных паров в результате прямой реакции, применяют противоток твердой фазы относительно газовой и соблюдение особого температурного режима, при котором температура входящего газа составляет 500—600° С, а выходящего 300—400° С. На заводе в Уэлдон-Спринге применяют более высокие температуры в указанных пределах, на заводе в Падьюке – более низкие.
Процесс характеризуется следующими показателями: производительность установки 660 кг/ч при времени пребывания материала в зоне реакции 5—6ч. Питание производится газообразным НF с чистотой 99,95%, подогретым до 100—120° С, в количестве 220 % стехиометрического. Непрореагировавший избыток НF конденсируют после аппарата в виде 70%-ного продукта и продают другим предприятиям с некоторым убытком вследствие некондиционности продукта.
Состав получаемого на этих заводах тетрафторида урана характеризуется следующими данными, %: UF4 95—96,2%; UO2F2 2,5—2,0; UO2 2,5—1,8; Fe 5,5. 10-3; Ni 3,5.10-3, Сг 9.10-4; Мn, Cd, Mo 1. 10-3. .
Гидрофторирование в «кипящем слое». На некоторых заводах США и Канады, а также в Англии на заводе в Спрингфилде гидрофторирование осуществляют в «кипящем» (псевдоожиженном) слое. Этой операции предшествуют: экстракционный аффинаж с применением ТБФ, термическое разложение уранил-нитрата в аппаратах кипящего слоя, восстановление трехокиси урана до двуокиси также в кипящем слое. Таким образом, для трех основных технологических операций используют унифицированную аппаратуру -печи кипящего слоя.
Отметим достоинства и преимущества применения кипящего слоя для гидрофторирования двуокиси урана: интенсивность газового контакта; непрерывность процесса; хорошая теплопередача и перемешивание псевдоожиженной фазы; хорошая регулируемость процесса и возможность его полной автоматизации; отсутствие движущихся частей, сальниковых уплотнений и т. п. в зоне реакции; более простое решение вопросов предотвращения коррозии.
В процессе организации производства тетрафторида урана с применением кипящего слоя были испытаны три варианта аппаратурного оформления (табл.43).
Таблица 43
Некоторые характеристики аппаратов кипящего слоя для гидрофторирования двуокиси урана
| Аппарат | Температура реакции, оС | Продолжительность обработки, ч | Содержание UO2 в готовом продукте, % |
| Одноступенчатый | 450 | 16 | 1,4 |
| Трехступенчатый без температурного градиента | 450 | 8 | 1,8 |
| Трехступенчатый с температурным градиентом | 400 |
4 |
0,9 |
| 500 | |||
| 600 |
Питающая газовая фаза содержала 60% HF и 40% N2, причем общий расход НF удавалось снизить до 150-% стехиометрического. Основные недостатки таких аппаратов: большой пылеунос и трудности утилизации отхода разбавленной плавиковой кислоты.
Применение для гидрофторирования виброреакторов. Для снижения расхода НF при гидрофторировании UO2, что существенно с экономической точки зрения, на заводе в Ок-Ридже предложены реакторы с вибрирующим лотком. В реакторах такого типа твердый продукт перемещается по лотку непрерывными толчками, создаваемыми с помощью вибраторов. При этом значительно улучшается контакт частиц твердого продукта с газообразным НF.
Гидрофторирование двуокиси урана плавиковой кислотой. Этот процесс осуществляется в пульпе, состоящей из двуокиси урана и 40%-ной плавиковой кислоты, с использованием реактора с мешалкой или каскада таких реакторов. Образующийся UF4.0,75Н2O в виде густой пульпы направляют на фильтрацию, промывку, сушку и прокаливание до безводной соли. Серьезные недостатки данного метода — необходимость обезвоживания соли и переработки маточника.
Применение фтористых солей аммония. При получении тетрафторида урана в качестве фторирующих агентов можно использовать фторид и бифторид аммония, взаимодействующие с UO2 по реакции
2UO2 + 5NH4HF2 ® 2NH4UF5 + 3NH3 + 4Н2О
Последовательность операций: замес исходных материалов, сушка при 150-200°С, прокаливание получаемого аммонийуранпентафторида до тетрафторида урана при 550°С.
Если использовать не двуокись урана, а его высшие окислы, то получение четырехвалентного соединения обеспечивается восстановлением в процессе фторирования. Ход процесса может быть представлен следующей реакцией:
3UO3 + 6NH4HF2 ® 3UF4 + N2 + 4NH3 + 9Н2О
Предложены и другие варианты применения фторидов аммония для получения тетрафторида урана, например обработка ими уранилфторида. Ценным для технологического применения фторида и бифторида аммония является то, что они, будучи: перспективным сырьевым источником фтора, в некоторых случаях могут оказаться дешевле НF. Фториды аммония относительно легче регенерируются по сравнению с НF и меньше корродируют аппаратуру. Несмотря на то, что до настоящего времени использование фторидов аммония в производстве тетрафторида урана не вышло из стадии опытных работ, оно является перспективным.
Применение фреонов. Фреоны, например ССl3F (фреон-11), ССlF2 (фреон - 12), С2Сl3F (фреон-13), С2Сl2F4 (фреон-14), могут эффективно фторировать окислы урана с получением безводного тетрафторида урана, например, по реакции
UO3 + 2CCl2F2 ® 3UF4 + CO2 + Cl2 + COCl2 (фосген)
Процесс можно осуществить в барабанной вращающейся печи при небольшом избытке (%г10%-ном) фреона. Достоинство процесса в отсутствии паров воды, но фреоны дороги, что препятствует их практическому использованию.
Конструкционные материалы. При производстве тетрафторида урана «сухими» методами приходится сталкиваться со специфическими трудностями подбора коррозионно-стойких материалов, которые были бы достаточно пригодны для работы в условиях сложной системы агрессивных газов, содержащих фтористый водород, пары плавиковой кислоты, воды, часто аммиак, углекислый газ, окись углерода, азот, кислород, водород и т. п. Заранее исключаются все стали и чугуны, в том числе и все «нержавеющие» как абсолютно нестойкие в данных условиях. Из других материалов заслуживает внимания никель, хотя он стоек только до 600° С. Кроме того, сварка никеля сложна, несмотря на то что за последнее время она вполне освоена на наших предприятиях.
Магний и его сплавы с небольшим количеством алюминия также стойки, но только до 300°С, кроме того, они дороги и подвержены сильной электрохимической коррозии в контакте с Сu, Ni, Fe, нержавеющей сталью. В большинстве случаев с успехом применяют монель-металл. Этот сплав (на основе никеля с 27-29% меди, 1,8% марганца и 2,3% железа) прекрасно стоит до 550°С в атмосфере, содержащей HF, а также в 50%-ных растворах плавиковой кислоты. Монель-металл отлично обрабатывается, сваривается, обладает хорошими литейными качествами, вследствие чего его довольно широко используют на практике.
Медь стойка в отсутствие паров воды к НF, но сильно корродирует в среде Н2 и особенно аммиака даже при умеренной температуре. Алюминий характеризуется стойкостью в сухом HF до 500° С. Инконель - сравнительно новый сплав, впервые примененный в английской практике, устойчив до 600° С, т. е. несколько лучше монель-металла. Его состав, %: Ni 75—78; Сr 12—15; Fе 6—9; Мn 1; Si 0,5; Сu 0,5; С 0,15.
В некоторых случаях оправдано применение специальных сплавов типа хастеллой А, В, С, D, представляющих собой тройные сплавы никеля, молибдена, железа, иногда с добавкой меди. Также применяют пятикомпонентный сплав иллиум-К, в составе которого 67% Ni, 21% Сr, 8% Fе, 5%Мо и 3% Сu. Эти достаточно хорошие с технологической и металлургической точек зрения сплавы удовлетворительно стоят в атмосфере газов, содержащих НF, при довольно высокой температуре. Неметаллические материалы—графит, угли, керамические изделия из СаF2—используют также довольно часто, хотя их применение сильно ограничено присущими им нетеплопроводностью, хрупкостью, другими неудовлетворительными физическими свойствами.
В некоторых случаях успешно применяют фторопласты, в частности тефлон (тетрафторэтилен). Тефлон обладает идеальной химической стойкостью, великолепно обрабатывается и вообще это прекрасный конструкционный материал, но, к сожалению, термически стойкий только до 325° С.
Как видно из приведенных данных, выбор конструкционных материалов для процессов, где применяют НF, довольно ограничен, что создаст серьезные трудности при практическом осуществлении не только получения тетрафторида урана с помощью «сухих» методов, но и всех процессов фторидной технологии.
Дата: 2019-02-25, просмотров: 461.