| Показатели | Возраст | |||||
| 15 лет | 16 лет | 17 лет | 18 лет | 19 лет | 20 лет | |
| Грудной индекс | 70 ± 0,5 | 71 ± 0,5 | 71 ±0,5 | 73 ±1 | 74 ±1 | 75±1 |
| Длина пениса в покое (см)* | 7±2 | 8±2 | 9±2 | 9 + 2 | 10±2 | 10±2 |
| Длина пениса в эрекции (см) | 11 ±3 | 12 ± 3 | 13±3 | 14±4 | 15±4 | 16±4 |
| Окружность яичка (см)** | 11 ±4 | 12±3 | 13±3 | 15 + 6 | 15±6 | 15±5 |
*Длина пениса измеряется от корня до конца головки без учета крайней плоти. **Окружность яичка измеряется специальными тестомером или орхиметром.
346
 ложения менархе начинаются гораздо позже. Эти девочки обычно имеют рост ниже среднего.
ложения менархе начинаются гораздо позже. Эти девочки обычно имеют рост ниже среднего.
Среди причин задержки полового развития у девочек на первое место следует поставить семейно-кон-ституциональные особенности созревания, которые могут касаться не только половой системы, но и физического статуса в целом. Дисбаланс эстрогенов и андрогенов, который может возникать у подростков в периоде пубертата, большинство исследователей связывают с аналогичными отклонениями, которые нередко наблюдаются в юности у родителей таких подростков.
Конституциональная задержка развития — крайний физиологический вариант между хронологическим возрастом и возрастом, который можно дать, судя по степени развития ребенка. Эту задержку развития вначале относили к патологическим состояниям, однако низкий рост и задержка полового созревания могут настолько отрицательно влиять на поведение юного пациента, что в ряде случаев требуется терапевтическое вмешательство. У подростков с «физиологическим вариантом» недостаточности полового развития показатели евнухоидности и инфантильности скелета в возрасте 14-16 лет соответственно в 4,5 и 2,4 раза выше, чем у здоровых подростков того же возраста, при этом обычно развиваются элементы гиноидности.
Задержка полового развития часто имеет место у одного или обоих родителей и у братьев и сестер пациента.
Задержка полового развития — частый симптом многих хромосомных аномалий (например, синдрома Шерешевского-Тернера).
Возникающие в результате тяжелых инфекций, черепно-мозговых и психических травм (особенно — военного времени), первичные нарушения на уровне гипоталамуса, которые нарушают нормальную функцию гипоталамо-гипофизарного нейросекреторного комплекса с гипосекрецией гонадотропин-рилизинг факторов, с развитием гипотироза, гипофизарного нанизма, ожирения с розовыми стриями, нервной анорексии нередко сопровождаются задержкой полового развития.
Токсикозы первой половины беременности у матери, повреждающее действие на плод различных препаратов {аминазин, резерпин, атропин, этимизол), асфиксия в родах, эпидемический паротит, осложненный орхитом, могут формировать задержку полового развития в будущем (Холодова Е.А., 1996).
Определенную роль играют различные соматические заболевания, в частности, болезни органов пищеварения с синдромом мальабсорбции (хронический панкреатит, хронический энтерит, дисбактериоз, глютеновая болезнь —целиакия, спру), хроническая патология лег-
ких и сердца (бронхиальная астма, врожденные пороки сердца), хроническая почечная недостаточность (хронический пиелонефрит, хронический нефрит), длительное неполноценное питание с развитием трофологичес-кой недостаточности, гипо- и авитаминозы. Такие тяжелые истощающие заболевания в детском или пре-пубертатном периодах, как туберкулез (в частности, туберкулез придатков, яичек), сахарный диабет нередко сопровождаются задержкой полового развития.
Задержку полового развития следует отличать от гипогонадизма (см. соответствующий раздел выше).
Гипогонадизм — это синдром с выраженными нарушениями функций всей репродуктивной системы подростка, требующий иногда пожизненной заместительной терапии половыми гормонами. Напротив, задержка полового развития считается пограничным состоянием, которое может постепенно исчезать по мере взросления подростка.
В каждом конкретном случае задержка полового развития имеет различный генез. В основе каждой разновидности лежат особые нарушения гипота-ламо-гипофизарно-гонадных взаимосвязей, которые определяют многообразие форм задержки полового развития.
У юношей можно говорить о трех основных механизмах задержки:
— позднее созревание гонадостата;
— позднее созревание рецепторов интерстициаль-ных клеток, взаимодействующих с гонадотро-пинами, главным образом — с лютеинизирую-щим гормоном;
— низкая чувствительность тканей наружных половых органов к тестостерону.
Первый механизм — наиболее типичен для задержки полового развития типа ложной адипозо-гениталь-ной дистрофии, третий — для подростков с микропенисом.
Задержка полового развития полиэтиологична. Так, наряду с ярко выраженной дисфункцией гонадостата, которая приводит к нарушению последовательного включения различных гонадотропных гормонов в процесс регуляции развития гонад, отмечено значительное снижение чувствительности клеток яичек к лю- теинизирующему гормону.
Непоследовательность этапов полового развития при синдроме его задержки вызывается дисфункцией коры надпочечников. Слабые андрогены надпочечников не только оказывают стимулирующее действие на структурные образования гипоталамуса, секретирующие гонадолиберин, но и способны вли-
347
ять на процесс созревания рецепторов яичка, взаимодействующих с гонадотропинами. В зависимости от количества секретируемых андрогенов это влияние разнонаправленно.
Существенное значение для нормального полового развития имеет гормон роста. Недостаточная секреция гормона роста играет существенную роль в происхождении задержки пубертата. Известна первичная роль гормона роста в недоразвитии полового члена у юношей (микропенис).
У юношей с задержкой полового развития существенно повышен уровень пролактина в крови, особенно при тех формах, патогенез которых связан с недостаточной чувствительностью гонад или андрогенозависимых тканей. Гиперпролактинемия (особенно у мальчиков с микропенисом) участвует в патогенезе задержки по лового развития. Генез этого варианта связан с недостаточной чувствительностью ткани кавернозных тел пениса к тестостерону. Можно полагать, что физиологическое значение пролактина заключается не только в ускорении созревания рецепторов семенников, но и в регуляции гормонорецепторного взаимодействия непосредственно на уровне тканей. Функция пролактина в процессе пубертата заключается в обеспечении рациональных взаимоотношений между степенью зрелости гонад и реализацией их центральной и периферической функциональной активности.
Таким образом, задержка полового развития тесно связана с изменениями всех механизмов, обеспечивающих регуляцию полового созревания.
Установлено, что эпифизарные мелатонин и серо- тонин в большинстве случаев оказывают ингибиру-ющее воздействие на гипофизарно-половую систему. Таким образом тормозится секреция лютеинизирую- щего и фолликулостимулирующего гормонов. Это отрицательно отражается на секреции гонадотроп-ных гормонов гипофиза. Мелатонин тормозит синтез мужских половых гормонов и активирует их разрушение. Следовательно, он может затормозить половое созревание. Уровень мелатонина также связан с формой заболевания и со степенью выраженности патологического процесса. Подтверждена роль мелатонина в формировании задержки полового развития у подростков. Обнаруживается отрицательная корреляционная связь его секреции с уровнем фолликулостимулирующего гормона. У девушек при задержке полового развития обнаруживается повышение секреции мелато нина.
У юношей с задержкой полового развития отмечается наиболее характерное отклонение в обмене моноаминов — умеренное или значительное снижение
348
уровня норадреналина, а также ванилилминдальной кислоты. Характер этих изменений определяется не возрастом, а степенью проявления патологического процесса.
Вещества, ингибирующие моноаминооксидазу, оказывают выраженное угнетающее влияние на половое развитие экспериментальных животных. Таким же действием обладает и резерпин, повышающий, как и мелатонин, продукцию серотонина, который, как известно, оказывает через гипоталамус тормозящее влияние на половое развитие и участвует в процессах половой дифференцировки.
Клиника. При задержке полового развития чувство физической неполноценности может стать причиной душевных переживаний и своеобразных поведенческих реакций таких подростков. Им свойственны ребячество, хвастовство, неадекватное поведение в школе. Они не принимают участия в мальчишеских играх, избегают физических нагрузок, не ходят на физкультуру, легко поддаются чужому влиянию, почему нередко становятся жертвами сомнительных компаний. При этом наблюдается снижение школьной успеваемости за счет ослабления памяти и затруднения восприятия. Могут не посещать школу. Часто наблюдается ночное недержание мочи, что еще больше травмирует подростков. Они становятся замкнутыми, друзей практически не имеют. Характерно грызение ногтей (кстати, эта дурная привычка, за редким исключением, передается по наследству).
При внешнем осмотре—лицо подростков глуповатое. Они обычно невысокого роста. Нейроэндокринное развитие соответствует развитию ребенка того же костного возраста. Так, юноша 16 лет может выглядеть как 12-летний мальчик. Окончательный рост таких подростков — в среднем 166,7 см. Обычно у таких подростков родители также низкорослые (Блунк В., 1981). Л.М. Скородок и О.Н. Савченко (1984) выделяют у подростков мужского пола четыре формы задержки полового развития.
Первую форму называют конституционально-соматогенной. Такие подростки сложены пропорционально. Темпы роста обычно замедленные. Имеют небольшую длину тела и конечностей. Костный возраст отстает от фактического. Евнухоидных и гиноидных черт нет. Мышечная масса недостаточная. Сила мышц снижена. Мутация голоса и половые признаки запаздывают. Пубертатное увеличение тестикул, полового члена и мошонки фактически отсутствует. Поллюций у таких подростков не бывает. Часто обнаруживаются ложный или истинный крипторхизм. Даже в 14-летнем возрасте отсутствует возрастная динамика разме-
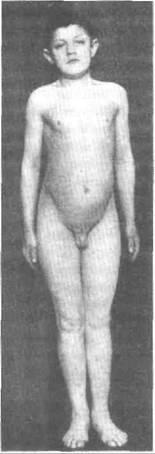
Рис. 97. Задержка полового развития у юноши по типу ложной адипозогенитальной дистрофии (по В. Фальта, 1913)
ров наружных половых органов. Эти признаки слабо выражены даже в 15-летнем возрасте. Эрекции редкие и вялые. Выявляются гипофункция тестикул или выработка неактивных андрогенов. Аденогипофиз обычно не страдает, а его резервы соответствуют III-IV стадиям пубертата. Секреция лютеинизирующего гормона повышена, а фолликулостимулирующего — нормальная. Низкая секреторная активность яичек в сочетании с высоким уровнем лютеинизирующего гормона может быть связана только с первичной относительной недостаточностью гонад. Половое созревание у подростков этой группы наступает в более позднем возрасте. Следовательно, органического поражения тестикул нет. По-видимому, у них замедлено созревание рецепторов яичка, что снижает взаимодействие в системе «лютеинизирующий гормон — клетки Лейдига».
При второй форме имеется недоразвитие наружных половых органов и отсутствие вторичных половых признаков на фоне выраженного ожирения, что напоминает адипозогенитальную дистрофию (рис. 97). Задержки роста, несахарного диабета, изменений глазного
дна и полей зрения, а также других симптомов поражения структур мозга при этой форме, однако, не бывает. Эта форма получила название ложной адипозогени-тальная дистрофии {функциональный адипозоге-нитальный синдром, псевдофрелих).
У подростков преобладает гипоталамическое ожирение в области живота и бедер, создающее впечатление микропениса, ложная гинекомастия. Нередко наблюдается семейная предрасположенность к ожирению. Ожирение прогрессирует. Иногда наблюдаются розовые стрии, различные варианты нейроцирку-ляторной дистонии, гиперостоз внутренней пластинки лобной кости. Становится шире таз. Формируется ев-нухоидное диспропорциональное телосложение с длинными нижними конечностями. Мышечная сила сохраняется.
Ведущий фактор — преходящее снижение функции гипоталамо-гипофизарной системы в начале пубертата. Восстановление активности гипофиза происходит позже, чем в популяции. Размеры гениталий явно отстают от нормы. Имеются признаки феминизации. Вторичные половые признаки даже в 15-летнем возрасте отсутствуют, может быть слабое оволосение лобка. Юношеских угрей, мутации голоса, увеличения щитовидного хряща — не бывает. Эрекции редкие, слабые. Поллюций нет. Половое созревание может начинаться без стимуляторов, но с опозданием. Из-за дефицита тестостерона вначале нормальный рост к 15-16 годам замедляется. Обнаруживается недостаточная секреция тестостерона в надпочечниках, продуцируется избыточное количество эстрогенов и малоактивных андро- генов — в гонадах. В ночное время наблюдаются подъемы секреции лютеинизирующего гормона. При пробе с хорионическим гонадотропином выявляются достаточные гормональные резервы гонад: повышаются уровни тестостерона в крови и 17-КС— в моче. Может быть диабетический тип гликемической кривой, повышается холестерин крови.
При третьей форме задержки полового развития вторичные половые признаки появляются своевременно, размеры яичек удовлетворительные, но пенис недоразвит за счет недостаточного развития кавернозных тел (микропенис или микрогенитализм). Патология вызвана генетически детерминированным неполноценным гормонорецепторным взаимодействием для тестостерона на уровне кавернозных тел, то есть низкой их чувствительностью к андрогенам.
Иногда видны только крайняя плоть или отверстие уретры. Это требует корригирующих мероприятий. Пубертатный рост яичек может задерживаться. Других проявлений гипогонадизма нет. Часто имеет мес-
349
то ожирение при нормальной длине тела и конечностей. Гонадотропная функция аденогипофиза сохранена. Продукция тестотерона — нормальная или даже повышенная. Экскреция 17-КС также нормальная.
Четвертая форма характеризуется нормальным оволосением лобка и подмышек (обычно в 11-12 лет) при отсутствии пубертатных изменений пениса, яичек и мошонки, которые остаются инфантильными, в то время как в норме вначале увеличиваются размеры яичек и пениса, а оволосение начинается позже. Размеры яичек и пениса сохраняются маленькими, меньше, чем у сверстников до пубертата. У 1/3 подростков наблюдается ложная ретенция яичек. Это дало повод называть такую форму задержки полового развития синдромом неправильного пубертата {иррегулярным пубертатом, непоследовательным пубертатом), О ней говорят, если после оволосения лобка (в норме — до 14-15-летнего возраста) отсутствуют другие признаки полового развития. Причина этой формы задержки полового развития — повышенная продук ция надпочечниковых андрогенов. Внегонадное их происхождение подтверждает нормальный или даже повышенный уровень 17-КС в моче. Поэтому экскреция 17-ОКС также повышена, но подавляется декса- метазоном. Обнаруживается высокая продукция в ГГНСК лютеинизирующего гормона, секреция которого происходит пиками (Сильницкий П.А. с со-авт.,1987).
Такие нарушения возникают в результате смешанной дисфункции гипоталамо-гипофизарно-гонадной системы и повышенной продукции слабых андрогенов коры надпочечников. При этом наблюдается недостаточная чувствительность яичек к эндогенному гона-дотропину из-за позднего созревания рецепторов ин-терстициальных клеток для лютеинизирующего гормона. Избыток андрогенов надпочечника воздействует на клетки Лейдига патологически. Это вызывает гипофункцию яичек, как при первичной недостаточности интерстициальных клеток при неправильном пубертате. В результате в яичках значительно падает продукция тестостерона.
Рост при этом обычно нормальный, но чаще избыточная масса тела с ожирением по женскому типу. Таз — широкий, пропорции тела— гиноидные, но не ев-нухоидные, так как длина тела и ног нормальная. Ожирение изредка отсутствует. Возникает чаще ложная гинекомастия. Костный возраст опережает нормальный примерно на 1 год. Нередки булимия, артериальная ги-пертензия, розовые стрии на коже.
Осложнения. Задержка полового развития у юношей, по наблюдениям психиатров и сексопатологов, неблагоприятно влияет на формирование их полового
350
поведения. Формируются неправильная психофизиологическая ориентация и, соответственно, различные специфические сексуальные извращения, которые могут возникать достаточно поздно.
Так, характерные сексуальные отклонения, которые практически совершенно не обращали на себя внимание в пубертате, в третьем десятилетии жизни неожиданно выходят на первый план, а профилактикой сексуальных извращений может стать своевременная коррекция полового развития.
Имеются данные о том, что у мужчин, развивавшихся замедленно, в будущем возможны расстройства сперматогенеза.
Классификация. Различают первичные (тестику-лярные), вторичные (церебро-питуитарные) и коррелятивные (при сопутствующей патологии) формы задержки полового развития подростков. По Л.М. Ско-родку и О.Н. Савченко (1984), выделяют 4 варианта задержки полового развития (см. выше—Клиника).
Л. Лоу и К. Вонг ( 2001) приводят более подробную современную классификацию форм этого расстройства.
1. Конституциональная задержка роста и полового развития.
2. Первичный (гипергонадотропный) гипогонадизм:
— синдром Кляйнфельтера;
— синдром Нунан;
— вирусный орхит (паротит, корь, вирусы Кок-саки В и ECHO);
— противоопухолевые средства (метилгидрази-ны, алкилирующие вещества, циклофосфан);
— облучение яичек.
3. Вторичный (гипогонадотропный) гипогонадизм:
— изолированный дефицит гонадотропных гормонов (синдром Кальмана);
— синдром Паскуалини (синдром фертильного евнуха);
— идиопатический гипопитуитаризм;
— синдром Прадера-Вилли;
— синдром Лоуренса-Муна-Барде-Бидля;
— талассемия (средиземноморская анемия);
— облучение головного мозга при лейкозах и опухолях;
— поражения головного мозга (опухоли, инфек
ции — менингит или энцефалит, аплазии и ги
поплазии гипофиза, «пустое» турецкое седло, гид
роцефалия, септооптическая дисплазия).
4. Задержка полового развития при хронических си
стемных заболеваниях.
По тяжести задержка полового развития делится на легкую (задержка на 1 год), среднюю (задержка на 2
 года) и тяжелую степень (задержка на 3 года и более) степени.
года) и тяжелую степень (задержка на 3 года и более) степени.
Оценка полового развития проводится по Дж. М. Тан- неру (1979) и по половой формуле (см. Приложение 4).
Диагностика. Отсутствие увеличения яичек у подростка старше 13,5 лет и отсутствие оволосения лобка у подростка старше 14,5 лет уже может служить поводом для диагностики задержки полового развития. Увеличение грудного индекса—соотношения между глубиной и шириной грудной клетки на уровне пятых ребер в % (табл. 17) —на 5 % и более относительно нормы позволяет заподозрить нарушение половой дифферен-цировки (Демченко А.Н., Черкасов И.А., 1978).
В сыворотке крови таких подростков необходимо обязательно определить уровни фолликулостимулирую- щего и лютеинизирующего гормонов, тестостерона, кортизола, пролактина, гормонов щитовидной железы, тиротропина, антитироидных аутоанти-тел. Необходимо установить костный возраст подростка с помощью рентгенограмм левых кисти и запястья (см. Приложение 10). Проводят рентгенографию черепа.
При определении функционального состоянии го-надостата полезна проба с верошпироном. Для этого в течение 5 дней подростку дают верошпирон по 150 мг/м2 поверхности тела, что приводит к нарастанию лютеинизирующего, но к снижению фолликуло- стимулирующего гормонов в сыворотке крови, чего не происходит при гипогонадотропном гипогонадизме и в препубертате.
Важной в диагностике синдрома неправильного пубертата является типичная клиническая картина: выраженный микрогенитализм (иногда с псевдоретенцией тестикул), наличие лобкового и / или подмышечного оволосения 11-111 стадий по Таннеру, ожирение (в ряде случаев — с розовыми стриями), гиноидная диспропорциональность телосложения, ускорение роста и диф-ференцировки скелета. Клиническая картина у 1/3 подростков напоминает гипоталамический синдром пубертатного периода (см. выше). У большинства таких подростков анамнестически можно установить наследственный характер ожирения и полового развития. Уровень лютеинизирующего гормона в крови повышается, а содержание тестостерона и фолликулос-тимулирующего гормона значительно снижается. У таких подростков может быть плоская гликемичес-кая кривая при ГТТ, что свидетельствует о функциональном гиперинсулинизме. Изредка тест на толерантность к глюкозе протекает по сомнительному типу, что требует уточнения диагноза с помощью глюкозо- кортизонового теста по Конну.
Критерии диагноза. Снижение уровней лютеини- зирующего и фолликулостимулирующего гормонов в сыворотке крови свидетельствует в пользу вторичного гипогонадизма, что связано с первичным заболеванием гипоталамо-гипофизарной области и требует соответствующего обследования подростка.
Повышение в сыворотке крови концентрации люте- инизирующего и фолликулостимулирующего гормо нов, напротив, указывают на первичный гипогонадизм, то есть на первичную тестикулярную недостаточность (ЛоуЛ.,ВонгК.,2001).
Типичная внешность больных при ряде эндокринологических синдромов, сопровождающихся задержкой полового развития (например, синдром Кляйнфельте- ра и др.) помогает установить причину задержки полового развития.
Дифференциальный диагноз.
Дифференциальная диагностика конституциональной задержки полового развития и гипогонадизма достаточно трудная ввиду большого сходства клинических проявлений. Ведущими признаками являются низкорослость при конституциональной задержке полового развития и нормальный рост — при изолированном дефиците гонадотропинов. Для обоих состояний характерно снижение базальной продукции как лютеинизирующего, так и фолликулостимулирующего гормонов. Но уровень пролактина в сыворотке крови при конституциональной задержке полового развития нормальный или слегка снижен, в то время как при гипогонадизме его секреция низкая, и она не нарастает или незначительно нарастает после пробы с тиролиберином (см. выше).
Синдром Кальмана характеризуется отсутствием ночных выбросов лютеинизирующего и фолликулостимулирующего гормонов.
В отличие от физиологического варианта задержки полового развития, при первичном гипогонадизме гиноидность выражена существенно выше, и она не исчезает, а прогрессирует. У подростков с конституциональной задержкой полового развития при уменьшении относительной андрогенизации (падает соотношение уровня андрогенов и эстрадиола) наблюдаются некоторая задержка обратного развития ев-нухоидности и умеренное повышение инфантилизации скелета. Для гипогонадизма характерно отсутствие пубертатной динамики продукции тестостерона и нормального соотношения уровней тестостерона и эстрадиола. Наряду с прогрессированием евнухо-идности у подростков при гипогонадизме возникают признаки нарушения полового диморфизма скелета.
351
Исходы заболевания и прогноз. Эволюция задержки полового развития у подростков благоприятная. Иногда наступает спонтанное излечение. Если к возрасту 17-19 лет происходит нормализация андрогенной и гаметогенной функций гонад, и появляется фертиль-ность, то в таких случаях у большинства больных прогноз благоприятный. Если нет динамики после 18-20 лет, то достижение спонтанного полового развития, за редким исключением, практически невозможно.
В дальнейшем задержка полового развития может трансформироваться не только в половой, но и в общий инфантилизм.
У некоторых больных подростков с нарушениями полового развития возможны суицидальные попытки.
Возникающий евнухоидизм является необратимым. Такие подростки мужского пола нуждаются в пожиз ненной терапии тестостероном или его аналогами (метилтестостерон, сустанон-250, станозолол).
Лечение. Так как задержка полового развития подростков часто сочетается с тучностью, то оптимальным методом ее лечения является комбинированная терапия, включающая мероприятия по лечению ожирения (см. Гипоталамический синдром пубертатного периода) и гипогонадизма. Назначается диета, богатая белками и витаминами, но с ограничением углеводов. Тучным подросткам необходимо похудеть, а тощим — необходимо обязательно прибавить массу тела (см. Нейрогенные анорексия и булимия). Использование щадящей патогенетической терапии — необходимое условие успешного лечения этой патологии.
Целесообразно начинать коррекцию задержки полового развития у мальчиков уже в возрасте 11-13 лет, так как она наблагоприятно влияет на физическое и психическое здоровье подростков и способствует нарушениям репродуктивной функции в будущем.
При конституциональной задержке физического и полового развития подростки нуждаются в основном в психотерапии. Медикаментозная терапия используется в крайних случаях, когда подростки тягостно переживают свою неполноценность и в состоянии депресии готовы на угрожающие их жизни поступки. Если ведущей причиной депрессивного состояния подростка является задержка полового развития, то ему в течение 3 месяцев назначают внутримышечные инъ екции 5 % тестостерона пропионата {по 1 мл 1 раз в неделю) или тестостерона энантата (по 100 мг 1 раз в месяц). Такая терапия способствует увеличению размеров пениса и лобковому оволосению. Через 3-4 месяца курс лечения можно повторить, но короткий. Иногда такая терапия быстро устраняет задержку полового развития.
352
Следует помнить о том, что тестостерон способствует преждевременному закрытию зон роста костей, и если у подростка имеется одновременно и патологическая задержка роста, то такое лечение может привести к плачевным результатам. Поэтому при сочетании задержки полового развития с низкорослостью нужно начинать лечение с низкорослости, то есть задержки физического развития. В таких случаях подросткам сначала проводят заместительную терапию гормоном роста (см. Гипофизарный нанизм), а по достижении ими 12-летнего костного возраста к лечению добавляют те стостерон. При невозможности лечения гормоном роста можно в течение 3-4 месяцев применять анабо лические стероиды (ретаболил, метандростенолон, оксандролон) или хорионический гонадотропин, обладающий ростостимулирующим действием.
Если к 13 годам у подростков выявляются другие выраженные формы задержки полового развития, то используют чередующиеся курсы хорионического гона- дотропина и спиронолактона (верошпирона) или курсы хронического и менопаузалъного (менотро- пин) гонадотропинов. По-видимому, спиронолакто- ны повышают чувствительность гонад к воздействию как эндогенного так и экзогенного лютеинизирующе- го гормона.
Иногда к хорионическому гонадотропину у лечащихся им подростков могут появиться антитела, что вызывает резистентность к такой терапии.
При синдроме неправильного пубертата, для которого характерен дефицит фолликулостимулирующего гормона, патогентически обосновано использование менопаузалъного гонадотропина, который обладает преимущественно фолликулостимулирующей активностью.
При выраженном первичном гипогонадизме в целях стимуляции полового развития подростков Л.Лоу и К. Вонг (2001) с 12-14 лет рекомендуют заместительную терапию тестостероном. Назначают тестосте рон энантат внутримышечно по 50 мг 1 раз в месяц, затем дозу повышают на 50 мг каждые 6 месяцев до 200 мг 1 раз в 2-3 недели. После введения тестосте рона его уровень в крови нарастает выше нормального, но через 2-3 недели падает до минимального. За рубежом выпускается тестостерон в виде пластырей (в комбинации с циклодекстрином).
При вторичном гипогонадизме для профилактики и лечения бесплодия в будущем подросткам старше 14 лет вместо тестостерона назначают хорионический гонадотропин, менотропин (менопаузалъный гона дотропин) или — в импульсном режиме — гонадоре- лин (см. ниже). Хорионический гонадотропин назначают по 1000 ME внутримышечно 2 раза в неделю, затем


 дозу постепенно увеличивают до 2000-3000 ME 2 раза в неделю в течение 2-3 лет. Даже лечение одним хори- оническим гонадотропином вызывает увеличение тестикул. В дальнейшем, на втором-третьем году лечения, для стимуляции сперматогенеза и роста тестикул используют менопаузальный гонадотропин, который содержит лютеинизирующий и фолликулостимули-рующий гормоны.
дозу постепенно увеличивают до 2000-3000 ME 2 раза в неделю в течение 2-3 лет. Даже лечение одним хори- оническим гонадотропином вызывает увеличение тестикул. В дальнейшем, на втором-третьем году лечения, для стимуляции сперматогенеза и роста тестикул используют менопаузальный гонадотропин, который содержит лютеинизирующий и фолликулостимули-рующий гормоны.
Лечение гонадорелином ацетатом используется редко ввиду его очень высокой стоимости и технической сложности. Препарат вводят подкожно или внутривенно с помощью специально программируемых носимых пациентом дозаторов, которые импульсно, каждые 90 минут, выбрасывает в организм 5 мкг гонадорели- на на протяжении 7 суток. Интервал между курсами — 3 недели. Этот метод лечения вторичного гипогонадиз-ма считается самым физиологичным.
Ввиду накапливающихся данных о важной роли леп-тина, критический уровень которого достигается при определенной массе тела и участвует в запуске механизмов пубертата, делаются попытки лечить некоторые формы задержки полового созревания этим гормоном (Матарезе Дж., 2003).
Ворохобина Н.В. с соавт. (2000) рекомендуют использовать у мужчин аналог гонадолиберина — бусерелин (2 % раствор бусерелина ацетата) фирмы «Фарм Синтез» не только для диагностики различных форм мужского гипогонадизма, но и для лечения третичного гипогонадотропного (гипоталами-ческого) гипогонадизма.
Подростки с задержкой полового развития нуж даются в витаминах. В возрасте 14-15 лет им показано лечение Аевитом, 5 % раствором витамина В1 [через день по 1 мл внутримышечно, чередуя, в течение 1 месяца). Витаминотерапия способствует андрогенизации, так как витамин Е является си-нергистом андрогенов, витамин А — ингибитором эстрогенов, а витамин B 1 переводит активные эстрогены в менее активные формы.
Имеются сведения о выраженном стимулирующем влиянии сульфата цинка на рост подростков с задержкой полового развития. Доза составляет до 220 мг в сутки. Показаны порошки в составе—сульфат цинка (0,005) с глицерофосфатом кальция (0,2)—по 1 порошку 3 раза в день в течение 2 месяцев. Цинк стимулирует биосинтетические процессы в семенниках. Если нет должного эффекта, то через 1 месяц проводят второй курс такой терапии. Назначают АТФ по 1 мл внутримышечно через день в течение 1 месяца, 5 % раствор вита мина В6 по 1 мл внутримышечно через день в течение 1 месяца. Показана глютаминовая кислота по 0,25 г 2
раза в день в течение 1 месяца, которая через ц-АМФ усиливает эффект эндогенных гонадотропинов.
После этого лечения обыкновенно наступает явное улучшение. Если эффекта от такой терапии нет, то вероятнее всего имеется патологическая форма задержки полового развития. В таких случаях проводят дополнительное обследование и при исключении опухолевой патологии лечат внутримышечными инъекциями тесто стерона.
В начале лечения тестостероном в течение нескольких месяцев могут наблюдаться угри и гинекомастия, в дальнейшем они ликвидируются. При оральном введении тестостерона и его препаратов возможны нарушения функции печени. Изредка наблюдается умеренная полицитемия и заметное увеличение гематокрита, что может вызывать у подростов апноэ во время сна. У мальчиков быстрое увеличение уровня тестостерона после лечения может приводить к психологическим трудностям (Мак-Дермотт М.Т., 2001).
Лечение задержки полового развития у девочек также должно быть комплексным и проводиться совместно с гинекологом и невропатологом.
Если гипофункция яичников - следствие гипопитуи-таризма и не сопровождается задержкой роста, то больным назначают циклы витаминотерапии, рекомендуют соблюдать режим труда и отдыха, заниматься физкультурой на воздухе, сбалансировано питаться. Показаны глютаминовая кислота по 0,25 г 3 раза в день, вита мин Е, аскорбиновая кислота, витамины группы В. Желательно использовать эндоназальный ионофорез кальция, вибромассаж. Применяется дифенин.
При терапии гипоталамических форм задержки полового развития у девочек используют гонадолиберин, вводимый в пульсирующем режиме, каждые 90 мин. подкожно или внутривенно. Хорошие результаты дает подобное введение гонадолиберина по 2 мкг препарата с 23.30 до 7.30 утра (по 12 мкг в сутки) - 3 ночи в неделю, на протяжении 6 недель. При этом отмечается ускорение роста и развития молочных желез. Девочкам, у которых гонадотропная недостаточность сочетается с задержкой роста и дефицитом СТГ, назначается терапия препаратами гормона роста, а также гонадотропинов (префизоном или пергонадом) в сочетании с общеукрепляющим лечением и предшественниками нуклеоти-дов (инозин, оротат калия). Применяется витамино терапия и ферментотерапия панзинормом и абомином. При задержке полового развития вследствие дефицита массы тела терапия вышеуказанными гормонами противопоказана (Гуркин Ю.А., 1993).
Профилактика. Нельзя оставлять без внимания подростков, у которых отсутствуют признаки пубертата
353
спустя 2 года и более после средних сроков появления этих признаков в популяции.
Профилактикой задержки полового развития у будущих мальчиков является ограничение приема гормональных контрацептивов будущей матерью. Высокой степенью риска задержки полового развития характеризуются токсикозы беременности.
Пассивность педиатров, школьных, подростковых врачей и детских эндокринологов, а также поздняя обращаемость подростков с задержкой полового развития являются основными причинами поздней ее выявляемости.
У подростков на ежегодных профилактических осмотрах в школах и других учебных заведениях необходимо присутствие эндокринолога и подросткового врача с определением индекса массы тела, измерением размеров таза, яичек и пениса, вычислением грудного индекса.
Диспансеризация. Диспансерная группа — Д-2.
Подростки с задержкой полового развития нуждаются в наблюдении эндокринологом и подростковым врачом, а по показаниям — психотерапевтом и психологом. Особого внимания требуют подростки, у которых задержка полового развития сочетается с патологической пробой на толерантность к глюкозе.
В диспансеризации нуждаются все подростки с задержкой полового развития. Выделяются группы с физиологическим и патологическим пубертатом.
Диспансеризацию осуществляют эндокринологи и врачи подростковых кабинетов. В каждом областном центре должны быть эндокринолог—специалист по воп-росам пубертата, для девочек—гинеколог-эндокринолог, а для подростков мужского пола— андролог. На всех подростков должен заполняться контрольный лист, куда вносятся данные осмотров, сведения об эффективности лечения, рекомендации по профилактическим мероприятиям. Не менее двух раз в год у подростков оценивается состояние гениталий и вторичных половых признаков, а также производится измерение параметров тела, пениса и тестикул, коррегируется гормональное лечение. При необходимости подростков направляют к андрологу (Демченко А.Н., Черкасов И.А., 1978).
Подростки с задержкой полового развития нуждаются в длительном диспансерном наблюдении. Снятие с учета—только при полной компенсации заболевания.
Девушки с гипоменструальным синдромом и вторичной аменореей должны находиться под наблюдением эндокринолога и эндокринолога-гинеколога на протяжении 2 лет с момента восстановления менструального цикла, после чего они переводятся под наблюдение женской консультации. При задержке полового развития И-Ш степени (до 3-4 лет и более) девочки находятся под не-
354
прерывным наблюдением эндокринологом до перехода в женскую консультацию. .
Вопросы экспертизы. В клинической эндокринологии постоянный контроль за состоянием подростков с задержкой полового развития занимает особое место, так как речь идет о полноценности генофонда страны и о здоровье будущих ее поколений. У подростков с задержкой полового развития и ожирением П-Ш степени без осложнений группа здоровья-2. При ожирении II-IV степени с осложнениями группа здоровья - 3.
Подростки с выраженными признаками задержки полового развития относятся в 3 группу здоровья.
Юноши с явными внешними признаками гипогонадиз-ма и при отсутствии положительного эффекта от лечения на военный учет не ставятся и службе в армии не подлежат. При полной компенсации заболевания вопрос о призыве на военную службу решается индивидуально.
В военные учебные заведения они не принимаются.
ЮНОШЕСКАЯ ГИНЕКОМАСТИЯ
Определение. Юношеская гинекомастия — любое видимое или пальпируемое одно- или двустороннее увеличение молочной железы у мальчиков и у подростков мужского пола.
Синоним: пубертатная гинекомастия, транзиторная гинекомастия.
Распространение. У 75 % мальчиков-подростков бывает преходящая гинекомастия (МакДермотт М.Т., 2001). Частота ювенильной гинекомастии на протяжении всего пубертата достигает 15-50 %. Чаще всего она наблюдается в возрасте 13-14 лет.
Этиология. У девочек может наблюдаться в пубертатном периоде бурный рост молочных желез. Каких-либо гормональных нарушений при этом выявить не удается. Иногда гигантское увеличение молочных желез требует оперативного вмешательства. В одном случае за 1,5 года молочные железы достигли колоссальных размеров, общая масса удаленных молочных желез достигала 20 кг.
Ювенильная гинекомастия у мальчиков и подростков развивается в результате гиперплазии эпителия и соединительной ткани молочных железистых ходов.
У подростков размеры при гинекомастии могут ва-риировать от маленького комочка, который можно определить только путем пальпации, до железы взрослой женщины.
Истинная юношеская гинекомастия — это увеличение молочной железы у подростка, связанное с периодом полового созревания. Юношеская гинекомастия в типичных случаях встречается в стадиях И-Ш пубертата по Таннеру.
Вообще ее рассматривают как физиологический фе номен, не требующий врачебного вмешательства.
При этом увеличение может сопровождаться нагру-банием и болезненностью. Оно, как правило, двустороннее, но не обязательно увеличение обеих желез наступает одновременно.
Гинекомастия может возникать после голодания, после хронического гемодиализа. Изредка это может быть проявлением системного заболевания крови — односторонняя псевдогинекомастия (см. ниже) может быть при лимфолейкозе (экстрамедуллярный очаг кроветворения), при первичной опухоли.
Гинекомастия может возникать в связи с травмой или механическим раздражением железы, а также в результате лечения эстрогенами, гонадотропинами, хориогонином.
Опухоли печени, легких, средостения могут давать паранеопластическую гинекомастию. Нередко имеется ложная гинекомастия при гипоталамическом синдроме пубертатного периода.
Семейная гинекомастия — с развитием по мужской линии в нескольких поколениях—наследуется как доминантный признак, появляется рано, еще в детстве.
Симптоматическая гинекомастия часто встречается при ряде эндокринных и соматических заболеваний (при хронических гепатитах и циррозах печени, при туберкулезе ), при генетических аномалиях (синдром Кляйнфельтера, синдром Прадера-Вилли), гипер-пролактинемии, гипертирозе у подростков, при феминизирующей опухоли яичка, при синдроме Кушинга. Гинекомастия при гиперпролактинемии у подростков— позднее проявление пролактиномы.
Гинекомастия наблюдается при синдроме Рейфен- штейна (см. выше), который характеризуется дефектом биосинтеза тестостерона. Это семейное заболевание с мужским кариотипом, когда имеется вирилизация половых органов, явная с самого рождения, но сопровождаемая гипоспадией с относительно малым половым членом, часто — крипторхизмом, а к периоду полового созревания появляется выраженная гинекомастия при скудном оволосении тела.
При феминизирующих опухолях коры надпочечников, и яичек, при различных формах интерсексуализма, при истинном гермафродитизме — также отмечают гинекомастию.
Гинекомастия может быть при лечении преждевременного полового созревания. Часто это — семейное проявление резко выраженной пубертатной гинекомастии.
За рубежом гинекомастия нередко выявляется при употреблении в пищу молока от коров, получающих
эстрогены, а также мяса птиц, получавших на птицефабриках корм с добавлением в целях эффективной прибавки веса анаболических стероидов.
Так, в 1972 г. в Мариинской больнице нами наблю дался молодой пациент Л-нов с обострением язвенной болезни двенадцатиперстной кишки — кок тор гового судна дальнего плавания. Он поведал полуюмористическую историю о том, как после очередного кругосветного плавания практически у всей судовой команды возникла выраженная гинекомастия, появление которой было необъяснимым. Команда серьезно забеспокоилась. Позже выяснилось, что по пути следования судна из ленинградского порта в Сингапур во Франции была закуплена большая партия куриного мяса для команды. По тем непростым для России временам с бесконечными коммунистическими «продовольственными программами» такая «деликатесная пища» могла присниться морякам разве только во сне. Поэтому вся команда в течение всего рейса налегала на куриное мясо. У судового врача возникло предположение, что в матросской гинекомастии виновата курятина. Когда капитан судна обратился с претензиями к французским поставщикам курятины, он получил ответ, что французские куры на птицефабриках действительно получают анаболические гормоны, но во Франции их не употребляют в пищу ежедневно и в таких гро-
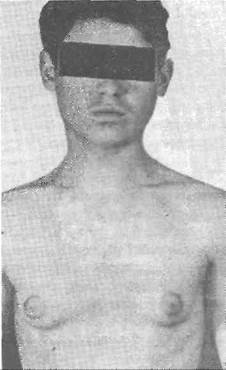
Рис. 98. Гинекомастия (по М. Юлесу и И. Холло, 1967)
355
мадных количествах... Иск был, таким образом, от клонен.
У девочек изолированное телархе — гетерогенная по клиническим и лабораторным показателям группа. Прогностически благоприятными при телархе являются нормальные показатели пролактина (Лисе В.Л., Цыбулькина Е.Э., 2000).
Возможны гинекомастии невыясненной этиологии (рис. 98). Когда причина неясная, то говорят об идио-патической гинекомастии.
Гинекомастия остается загадочным синдромом с точки зрения патофизиологии. Ее патогенез до сих пор детально не изучен. До настоящего времени известны лишь некоторые гормональные факторы регуляции роста молочной железы (эпидермальный фактор роста, ИФР-1, прогестины и эстрогены). Повышенной продукции эстрогенов при юношеской гинекомастии не наблюдается.
По-видимому, это местная эндокринопатия с повышенной чувствительностью клеток органа-мишени (молочных желез) к ростовым факторам—цитокинам.
Считают, что дело в андроген-эстрогенном дисбалансе, смещенном в сторону эстрогенов. Роль играют гонадотропные гормоны гипофиза, так как при гинекомастии нередко обнаруживается фоллитропинемия.
По современным представлениям, в патогенезе истинной пубертатной гинекомастии определенную роль играет гиперпролактинемия (Матковская А.Н. с со-авт., 1980).
Половой диморфизм в развитии зачатка молочных желез прямо не зависит от набора половых хромосом в клетках железы, он является следствием различной чувствительности к гормональным влияниям.
Различают две различные гистологические формы гинекомастии: пролиферация молочных протоков с образованием долек (паренхиматозная трансформация) и пролиферация интерлобулярной и парадуктальной ткани с разрастанием соединительной ткани и отложением жира (интерстициальная трансформация). По-видимому, первая является следствием воздействием эстрогенов, а также тестостерона и прогестерона. Пролактин играет при этом лишь пермессивную роль. Интерстициальная трансформация, напротив, связывается с избыточным воздействием пролактина, а также наблюдается при гинекомастии неясного генеза.
Клиника. Для юношей гинекомастия — это источник беспокойства и большая психическая травма: вместо возмужания, он феминизируется. Ассиметрия увеличения может оказаться косметически весьма резкой. Кроме того, зачатки грудных желез иногда становятся довольно-таки болезненными.
356
Подростки скрывает гинекомастию всеми способами, уклоняются от занятий спортом, плаванием, не играют со сверстниками. Так как это преходящее явление, то его нередко удается скрыть от окружающих.
Кожа в области молочных желез обычно нормальная. Сосок почти всегда увеличен, ареола пигментирована и расширена. Может быть небольшое втяжение соска. Вес молочной железы может достигать 160 г.
Эпителий протоков находится в состоянии гиперплазии. В соске обнаруживается большое количество гладкомышечных волокон.
У юношей могут наблюдаться и другие признаки феминизации: гермафродитизм, недоразвитие гонад, крип-торхизм, гипоспадия, атрофия яичек.
Классификация. Гинекомастия может быть физиологической и патологической. Этиологически различают истинную юношескую, идиопатическую, лекарственную, семейную, симптоматическую и ложную гинекомастию. Ложной или псевдогинекомастией называют увеличение молочных желез вследствие разрастания в них жировой клетчатки или вследствие опухоли.
Различают также двустороннюю (симметричную или асимметричную) и одностороннюю гинекомастию.
Прогноз. При одновременном развитии ожирения распределение жира может быть таким, что в дальнейшем остается выраженная «жировая молочная железа».
При гинекомастии обычно наблюдается весьма бурное созревание подростков.
Пубертатная гинекомастия — явление преходящее, повергается обратному развитию в течение 6-12 месяцев, длится не более 2 лет, но может задержаться на годы. Так, у 27 % подростков гинекомастия сохраняется на протяжении 2 лет, а у 7,7 % подростков — на протяжении 3 лет.
Операцию с учетом большой психической травмы подростка не следует откладывать надолго.
Следует обратить внимание на узловую форму гинекомастии, на фоне которой чаще возникают опухоли, хотя вопрос о том, является ли гинекомастия предраковым состоянием — спорен.
Дифференциальная диагностика. Гинекомастию необходимо отличать от рака, аденофибром, аденом, кистозной мастопатии.
Мастит юношей тесно связан с ранней стадией гинекомастии, которая в большинстве случаев проходит при наступлении полового созревания.
Идиопатическая гинекомастия встречается у детей и в допубертаном периоде без признаков соматических и эндокринных отклонений. Но она бывает редко.
Лекарственная гинекомастия может развиться у подростков, занимающихся бодибилдингом, наращива-
 нием мышечной массы и злоупотребляющих анаболиками (ретаболил).
нием мышечной массы и злоупотребляющих анаболиками (ретаболил).
Может возникать ятрогенная гинекомастия. Так, увеличение молочных желез могут вызвать экзогенные половые гормоны как мужские, так и женские, препараты наперстянки, фенотиазиды, метилдопа, резерпин и другие алкалоиды раувольфии, противотуберкулезные производные ГИНК (при длительных курсах терапии), спиронолактон и др. У девушек гинекомастию могут вызвать противозачаточные средства (нагрубание молочных желез).
Ложная гинекомастия (псевдогинекомастия) — часто сводится к увеличению количества жировой клетчатки при очень умеренной или отсутствующей железистой гиперплазии. Она устанавливается при пальпации: жировая ткань мягче железистой.
Диагностика. Если гинекомастия с возрастом не уменьшается, а увеличивается, то требуется специальное обследование.
Подростки с гинекомастией должны быть проконсультированы у специалиста-маммолога с подробным специальным обследованием при наличии показаний. В сомнительных случаях используют маммографию. Вопрос о биопсии подозрительных участков ткани молочной железы у мальчиков решается проще, чем у девушек.
Если у подростка одновременно есть признаки неполной маскулинизации, то необходимо заподозрить либо нарушение продукции тестостерона, либо резистентность к андрогенам. Если обнаруживается увеличение одного яичка, то необходимо исключить тес-тикулярное новообразование (Лоу Л., Вонг К., 1999).
Лечение. Особенно успокаивает подростка с юве-нильной гинекомастией сообщение отца о том, что у него «тоже было такое, но вскоре прошло». При пубертатной транзиторной гинекомастии медикаментозное лечение проводить не следует.
Если юношеская гинекомастия длится дольше, чем 2 года, то может понадобиться хирургическое лечение (МакДермотт М.Т., 2001). Если размеры молочных желез более 3,5 см в диаметре, то также требуется лечение. В таких случаях можно попытаться лечить гинекомастию парлоделом. Можно также лечить кломи- феном, кломифенцитратом. Используют в лечении такие препараты, как даназол (данатрол). Появились сообщения о положительном эффекте дигидротесто- стерона (андростанолона) в виде накожных апплика-
ции, в том числе — в опытах на животных, но пока как лекарство он труднодоступен.
Если же увеличение молочных желез создает выраженный косметический дефект и приносит подростку большие переживания, насмешки сверстников, то можно прибегнуть к косметическим операциям.
При патологической гинекомастии лечение—эти-отропное.
Мужские половые гормоны сейчас не употребляются, так как они сами могут вызывать гинекомастию. Однако уменьшать размеры молочных желез способно внутримышечное введение тестостерона, хотя эффект непредсказуем, так как тестостерон повышает активность ароматазы и усиливает его конверсию в женский половой гормон —эстрадиол.
Положительный эффект может дать ношение тугой лифообразной повязки.
Диспансеризация. Больной гинекомастией нуждается в диспансерном наблюдении и даже в обследовании в условиях стационара.
Повторная консультация специалиста должна быть через 2 года. Больные с узловой формой гинекомастии должны находиться под диспансерным наблюдением.
Важным является снижение массы тела подростков (МакДермотт М.Т., 2001), так как уменьшение жировой ткани сопровождается и уменьшением железистой ткани молочных желез.
Вопросы экспертизы. При пубертатной гинекомастии экспертные вопросы возникают, как правило, у юношей. Юноши с пубертатной гинекомастией относятся во 2-ю группу здоровья.
Юношам с косметически выраженной пубертатной гинекомастией и в случаях задержки ее обратного развития дается отсрочка от призыва на военную службу, но только после тщательного клинического обследования в эндокринологическом стационаре.
Подростки с гинекомастией, вызванной феминизирующими опухолями различной локализации, даже при успешном оперативном лечении нуждаются в постоянном диспансерном наблюдении, призыву в армию не подлежат, с военного учета снимаются и в военные учебные заведения не принимаются.
При идиопатической и при ложной гинекомастиях в случаях успешных косметических операций юноши могут призываться на военную службу на общих основаниях. Вопрос о приеме таких подростков в военные учебные заведения решается индивидуально.
357
ПРИЛОЖЕНИЯ
1. Нормальные концентрации гормонов , их метаболитов и некоторых биохимических показателей в крови и в моче здоровых лиц ( Тиц Н . У ., 1997; Лавин И ., 1999)
Возраст
Показатель
Лет
Взрослые
КРОВЬ :
Адреналин
Дата: 2019-02-02, просмотров: 1295.