КРАТКАЯ ХАРАКТЕРИСТИКА И ОТЛИЧИЯ ЦЕПНОГО И
СТУПЕНЧАТОГО ПРОЦЕССОВ ПОЛИМЕРИЗАЦИИ
Цепная полимеризация – это полимеризация, в ходе которой многократно повторяется процесс присоединения молекул мономера к активному центру растущей макромолекулы.
В цепной полимеризации могут участвовать те мономеры, которые содержат в своей структуре ненасыщенные связи или неустойчивые циклы. В таблице мономеров (таблице 3) -это соединения, приведенные в колонке 1 и 2 (знать представителей таких мономеров!).
Мономеры должны быть химически чистыми, не должны содержать примеси, которые могут дезактивировать инициатор или катализатор. Кроме этого мономеры должны обладать необходимой реакционной способностью, быть нетоксичными, пожаро-, взрывобезопасными и, что немаловажно, должны быть дешевыми.
В общем виде этот цепной процесс идет в три стадии. Его можно изобразить так:
 М М* 1. Образование активного центра
М М* 1. Образование активного центра
М* + М М - М*
М - М* + М М - М - М* 2. Рост цепи
М - М - М* + М М - М - М - М* и т. д.
М - М - М - М* М - М - М – М 3. Обрыв цепи
Для цепной (аддиционной) полимеризации (ЦП) характерны следующие признаки и отличительные особенности:
1. Цепной характер роста цепи. Он заключается в том, что возникающий в начале процесса активный центр М* сразу же (моментально) вызывает цепь последовательных реакций присоединения молекул мономера. Молекулярная масса макромолекул полимера в этом случае нарастает быстро. За каждый акт присоединения она нарастает на величину молекулярной массы присоединившегося мономера.
2. За счет быстрого (бурного) цепного характера макромолекулы полимеров с высокой молекулярной массой образуются сразу же в первые моменты реакции.
Элементный состав структурного звена (СЗ) полимера идентичен элементному составу молекул исходных мономеров
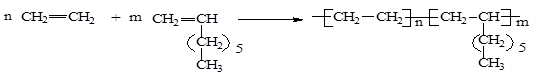
КРАТКАЯ ХАРАКТЕРИСТИКА МЕТОДА ПОЛИМЕРАНАЛОГИЧНЫХ
ПРЕВРАЩЕНИЙ (ПАП)
Значительную группу искусственных полимеров получают не методом полимеризации из мономеров, а путем модификации уже готовых природных полимеров.
Метод модификации уже имеющихся полимеров используют также для расширения ассортимента выпускаемых синтетических полимеров и получения полимеров с новым комплексом свойств. Такой метод модификации исходных готовых полимеров называется полимераналогичные превращения (ПАП).
ПАП – это процесс взаимодействия функциональных групп макромолекул полимеров с низкомолекулярными веществами, который сопровождается изменением природы функциональных групп полимера без изменения средней степени полимеризации и без изменения структуры скелета основной цепи.
Схематично этот процесс ПАП можно представить так:
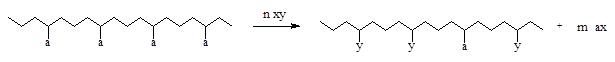
где  - основная цепь (скелет) макромолекулы;
- основная цепь (скелет) макромолекулы;
а – боковые функциональные группы исходного полимера;
ху - низкомолекулярное вещество, используемое для химической модификации:
у – новые функциональные группы полимера, образовавшиеся при модификации.
Конкретным примером ПАП является получение поливинилового спирта ПВС из готового полимера – поливинилацетата ПВА.
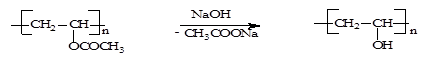
ПВС невозможно получать из мономера винилового спирта путем полимеризации, т.к. мономер неустойчив и изомеризуется в ацетальдегид 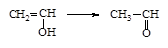 .
.
Две трети всех полимеров, производимых в мире, получают методом цепной полимеризации.
ПОЛИМЕРИЗАЦИИ
Скорость ЦП сильно зависит от типа заместителя в молекулах мономеров. Влияние заместителей в мономерах винилового ряда (1 колонка в таблице мономеров) на кинетику полимеризации обусловлено их полярностью и интенсивностью индуктивного, мезомерного (резонансного) и стерического эффектов.
В частности это влияние сказывается следующим образом:
1. Электронодонорные заместители Х виниловых мономеров*, такие как алкил (-R), алкокси (-ОR), алкенил (иначе винил – СН=СН2), фенил (-С6Н5) обладают положительным индуктивным эффектом +J , смещают электронное облако двойной связи в мономере от себя и повышают плотность на b-атоме углерода.
 |
| Пропилен * | Винил н-бутиловый эфир | Стирол | Бутадиен | Изобутилен |
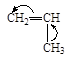
| 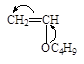
| 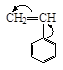
| 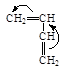
| 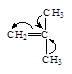
|
*- виниловые мономеры содержат ненасыщенную группу (винил) вида – СН=СН2
Благодаря этому эффекту облегчается и ускоряется присоединение катионов к b-атому углерода.
Следовательно, электронодонорные заместители способствуют протеканию катионной полимеризации с большей скоростью.
2. 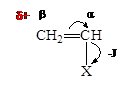 Электроноакцепторные заместители Х виниловых мономеров, такие как нитрильная группа (-CºN), карбонильная группа (-С=О), нитрогруппа обладают отрицательным индуктивным эффектом - J , оттягивают плотность электронного облака на себя, понижают электронную плотность на b-атоме углерода и облегчают протекание анионной полимеризации с большей скоростью.
Электроноакцепторные заместители Х виниловых мономеров, такие как нитрильная группа (-CºN), карбонильная группа (-С=О), нитрогруппа обладают отрицательным индуктивным эффектом - J , оттягивают плотность электронного облака на себя, понижают электронную плотность на b-атоме углерода и облегчают протекание анионной полимеризации с большей скоростью.
| Акрилонитрил | Метилакрилат | Метилметакрилат | Акриламид | Стирол | Бутадиен |

| 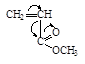
| 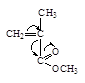
| 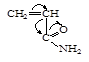
| 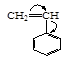
| 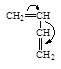
|
У таких мономеров, как стирол и бутадиен в зависимости от природы катализатора и внешней среды, заместители могут проявлять положительный и отрицательный индуктивные эффекты, поэтому эти мономеры могут участвовать и в катионной и в анионной полимеризации.
3. Заместители - атомы галогенов обладают слабым индуктивным эффектом, поэтому полимеризация винил - галогенидов преимущественно протекает по радикальному механизму.
4. Если в мономере два одинаковых заместителя расположены симметрично у a и b-атомов углерода винильной группы, то в этом случае проявляется их экранирующий эффект, и гомополимеризация вообще не протекает.
5. Это характерно для 1.2 –дихлорэтилена 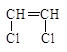 и малеинового ангидрида
и малеинового ангидрида 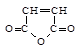 .
.
Совокупное влияние индуктивного, резонансного и стерического эффектов приводит к тому, что каждый тип мономеров может участвовать только в характерном для него виде полимеризации (смотри таблицу 9).
Таковы основные закономерности любого вида цепной полимеризации ЦП.
Мы начнем более подробное знакомство с основной разновидностью ЦП – с радикальной полимеризацией РП.
Таблица 9 - Способность ряда ненасыщенных полимеров к цепной полимеризации
| Тип инициирования | ||||
| МОНОМЕР | радикальный | катионный | анионный | ионно-кординационный |
| Этилен a- олефины 1,1-диалкилолефины Диены-1,3 Стирол и его замещенные Галогенированные олефины Сложные виниловые эфиры Акрилаты, метакрилаты Акрилонитрил, акриамид Простые виниловые эфиры Альдегиды, кетоны Изоцианаты Нитрилы Ацетиленовые соединения | + - - + + + + + + - - - - - | + - + + + - - - - + + - - - | + - - + + - - + + - + + + + | + + + + + + - - - + - - - - |
РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯ
Радикальная полимеризация (РП) – это вид цепной полимеризации, т.е. это многократно повторяющийся процесс последовательного присоединения молекул мономера к растущему активному центру.
 РП протекает за счет раскрытия ненасыщенных (двойной, тройной, сопряженной двойной) p -связей в мономерах и дальнейшего последовательного присоединения молекул мономера к растущему активному центру с образованием химической связи между концевым звеном растущего активного центра и молекулой мономера.
РП протекает за счет раскрытия ненасыщенных (двойной, тройной, сопряженной двойной) p -связей в мономерах и дальнейшего последовательного присоединения молекул мономера к растущему активному центру с образованием химической связи между концевым звеном растущего активного центра и молекулой мономера.
Роль активного центра в радикальной полимеризации играет свободный радикал, т.е. частица, имеющая неспаренный электрон на внешней орбитали.
Радикал при РП обладает электрофильными (электрофильный – это любящий электроны) свойствами. Он стремится завершить заполнение внешней орбитали и поэтому атакует электроны p-связи ненасыщенного мономера, оттягивает электронное облако на себя и раскрывает p-связь. Молекула мономера за счет электрона своей раскрытой p-связи и электрона радикала присоединяется к радикалу:

|
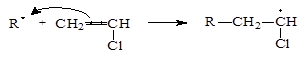
В результате генерируется (образуется) новый радикал, который называют радикал роста.
В радикальной полимеризации участвуют виниловые и диеновые мономеры (смотри в таблице 3 колонки 1, и таблицу 9):
Как любой цепной процесс радикальная полимеризация протекает в 3 стадии:
1. Образование активного центра. На этом этапе происходит образование свободного радикала роста (инициирование). Чаще всего свободный радикал получают благодаря распаду специально вводимых веществ – инициаторов J .
этап а) Распад инициатора на радикалы 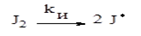
этап б) присоединение к радикалу инициатора молекулы мономера и обрахование радикала роста 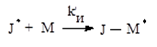
2. Рост цепи. На данной стадии наблюдается постоянное многократное раскрытие p-связи молекул мономера, присоединение их к растущему радикалу с образованием химической связи между концевым звеном растущего радикала и молекулой мономера. Молекулярная масса и размеры макромолекул увеличиваются.
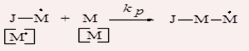
3.
 |
Обрыв цепи. На третьем этапе происходит либо исчезновение активных радикальных центров и прекращение роста макромолекул или передача активных радикальных центров на другие молекулы с прекращением роста одних макромолекул и началом роста других.
Энергия активации всего процесса Еарп включает в себя энергии активации всех трех стадий: инициирования Еаи, роста цепи Еар, обрыва цепи Еао.
Она вычисляется по формуле:
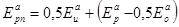
Наибольшая энергия активации Еаи, равная 112÷170 кДж/моль, требуется на 1 стадии – стадии инициирования. Итоговая величина энергии активации всех стадий РП Еарп составляет ~ 83÷90 кДж/моль.
Для виниловых мономеров, у которых в процессе полимеризации двойная p -связь с энергией связи 605,3 кДж/моль раскрывается и превращается в две простые s -связи с энергией 349,5 кДж/моль, можно рассчитать величину теплового эффекта DН:
DН = 2Еs - Е p = 2*349,5 – 605,3 = 93,7 кДж/моль
Реальный тепловой эффект при радикальной полимеризации ниже из-за стерических и кинетических факторов. Обычно тепловой эффект составляет 56-88 кДж/моль
Между величинами теплового эффекта и энергии активации радикальной полимеризации учеными Эвансом и Поляни установлена взаимосвязь:


где А-const, а a - число в пределах от 0 до 1 (0<a<1).
Из данного уравнения следует, что в ряду однотипных реакций полимеризации с ростом теплового эффекта D Н требуется меньшая величина энергии активации Еарп.
На первой стадии инициирования энергия активации Еаи необходима для распада молекул инициатора J на радикалы J × Молекулы инициаторов при распаде могут давать первичные, вторичные или третичные радикалы.
Для образования третичных и вторичных радикалов требуется меньше энергии активации, чем для образования первичных радикалов. Третичные и вторичные радикалы стабильнее (устойчивее) за счет делокализации (распределения, «размазывания») электронного облака между заместителями, по сравнению с первичными, у которых электронное облако локализовано (например, на атоме углерода) (смотри ниже).

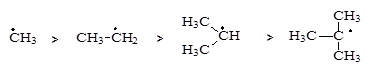
Энергия активации Еаи снижается от первичного к третичному радикалу,
стабильность радикалов растет, скорость реакции РП w р уменьшается,
регулярность присоединения звеньев повышается
В связи с этим на вторичных и третичных радикалах последующая скорость реакции роста цепи будет ниже, чем на первичных. В итоге уменьшается вероятность побочных реакций и увеличивается регулярность присоединения звеньев по типу «голова к хвосту».
Рассмотрим подробнее каждую стадию радикальной полимеризации.
Б) При диспропорционировании радикал атома водорода, слабо связанный с b -атомом углерода концевого звена одного радикала мигрирует (перескакивает) на a -атом углерода в концевом звене другого радикала.

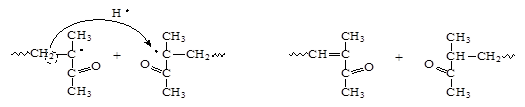
[M·] [M·]
В ходе диспропорционирования молекулярная масса макромолекул не изменяется. Однако на конце одной из макромолекул появляется ненасыщенная связь ~CH=С(R)2. Скорость реакции обрыва цепи методом диспропорционирования описывается формулой, аналогичной для случая рекомбинации 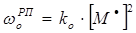 . Обрыв реакции полимеризации путем диспропорционирования характерен для третичных радикалов и для вторичных радикалов с громоздкими объемными заместителями, в частности, при полимеризации метилметакрилата (смотри выше рассмотренный пример).
. Обрыв реакции полимеризации путем диспропорционирования характерен для третичных радикалов и для вторичных радикалов с громоздкими объемными заместителями, в частности, при полимеризации метилметакрилата (смотри выше рассмотренный пример).
Энергия активации процесса обрыва цепи Еао мала и составляет от 8,0 до 20,0 кДж/моль. Это значит, что теоретически обрыв цепи может протекать самопроизвольно и с высокой скоростью. И действительно, значение константы скорости химической реакции обрыва цепи велико и лежит в пределах k о » 106 ÷ 108л/(моль × с), что на 3÷4 порядка выше, чем значение константы скорости стадии роста цепи при РП (k Р » 102 ÷104л/(моль × с)). Казалось бы, когда k о >> k Р и обрыв цепи идет быстрее роста, то наращивание макромолекул вообще невозможно.
Однако рост макромолекул все-таки идет, так как к моменту наступления стадии обрыва цепи размер макромолекул очень велик и вязкость реакционной смеси сильно возрастает. На этой стадии прекращение роста макромолекул обеспечивается не химической реакцией обрыва, а скоростью диффузии и сближения растущих макрорадикалов в высоковязкой среде образовавшегося полимера.
Установлено, что при конверсии ~20÷25 % мономера в полимер, вязкость среды увеличивается на 4÷5 порядков. В такой вязкой среде скорость диффузии макрорадикалов приближается к нулю, т.е. w оÞ 0, а скорость роста макромолекул остается высокой w р >> w о. Следовательно, при отсутствии обрыва, общая скорость полимеризации молниеносно возрастает и резко, скачкообразно увеличивается молекулярная масса макромолекул.
Эффект значительного нарастания скорости полимеризации и молекулярной массы полимера на глубоких стадиях превращения мономера в полимер называется «гель-эффект». Например, в ходе радикальной полимеризации метилметакрилата в массе (без растворителя) при степени конверсии мономера в полимер 10% скорость роста меньше скорости обрыва цепи, а при конверсии в 60% скорость роста уже превышает скорость обрыва в 11 раз (смотри ниже).
| Степень конверсии мономера метилметакрилата (ММА) в полимер, % | 10 | 60 |
| ( k Р / k о ) | 0,21 | 11,02 |
При полимеризации в отсутствие растворителей (такой способ называется полимеризацией «в блоке» или «в массе») «гель-эффект» проявляется сильнее, чем при полимеризации в разбавленных растворах или при полимеризации в дисперсионной среде (смотри рисунок 2)
 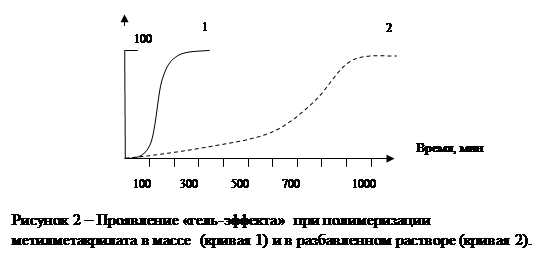 |
В) Передача цепи – это реакция радикала с неактивной (нейтральной) молекулой, при которой неактивное вещество обрывает растущую материальную цепь, само становится новым радикалом, начинает новую материальную цепь и продолжает кинетическую цепь (продолжает процесс).
Энергия активации реакций передачи цепи Еапер невелика и колеблется в пределах 20÷32 кДж/моль, поэтому эти реакции протекают самопроизвольно, если в реакционной среде имеются вещества, на которые возможна передача цепи.
Чем выше активность радикалов ~ М ·, т.е. чем правее стоит мономер в ряду активности (смотри выше ряд активности мономеров и радикалов), тем выше вероятность и скорость реакций передачи цепи. Например, у радикала винилацетата, стоящего последним в ряду активности мономеров, константа скорости передачи цепи на молекулы растворителя в 300 раз выше, чем у радикала стирола.
| Получаемый полимер | Полистирол ПС | Поливинилацетат ПВА |
| Константа скорости передачи цепи на растворитель ССl4 при 600С, kR , л/(моль×с) | 0,5×10-4 | 150 ×10-4 |
Реакции передачи цепи протекают тогда, когда в нейтральных молекулах реагентов - объектах передачи цепи, имеются слабо связанные, легко подвижные атомы водорода или галогенов. Эти атомы с неспаренным электроном легко отщепляются в виде радикалов Н· или На l · и присоединяются к растущему макрорадикалу. Новые радикалы, образовавшиеся из нейтральных молекул реагентов после отщепления водорода или галогена, инициируют далее процесс полимеризации.
В результате этого рост одних макромолекул прекращается, но процесс полимеризации как бы и не заканчивается, а продолжается. Общая скорость полимеризации практически не изменяется, но молекулярная масса полимера снижается. Поэтому реакции передачи цепи специально часто используют для регулирования и достижения требуемой величины молекулярной массы полимера.
Легче всего отщепляются атомы водорода или галогенов у соединений с третичным атомом углерода 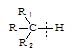 . Когда в реакционной среде при радикальной полимеризации присутствуют молекулы таких веществ (веществ - примесей, растворителей, специально вводимых регуляторов и др.), тогда вероятность реакций передачи цепи на эти молекулы возрастает.
. Когда в реакционной среде при радикальной полимеризации присутствуют молекулы таких веществ (веществ - примесей, растворителей, специально вводимых регуляторов и др.), тогда вероятность реакций передачи цепи на эти молекулы возрастает.

Механизм реакций передачи цепи идентичен в перечисленных случаях и имеет следующий вид:
|
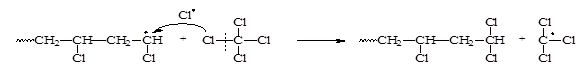 [ M · ] [ R ]
[ M · ] [ R ]
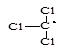
Вновь образовавшийся радикал инициирует далее процесс полимеризации.

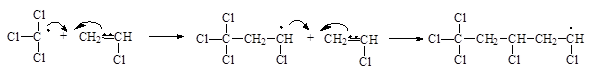
Скорость реакции передачи цепи на растворитель R описывается уравнением:
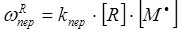
Скорости реакций передачи цепи на другие реагенты аналогичны:
· на инициатор J 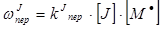
· на примесь, замедлитель S 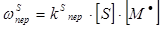
· на мономер М 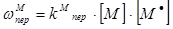
Передача цепи на полимер протекает только на очень глубоких степенях конверсии мономера в полимер. Вероятность этой реакции не велика, но, если она протекает, то образуются разветвленные макромолекулы:


Например, при радикальной полимеризации этилена при температуре Т»1800С и давлении Р »300 МПа число боковых ответвлений достигает 40 штук (ветвей) на каждые 500 составных повторяющихся звеньев.
КРАТКАЯ ХАРАКТЕРИСТИКА И ОТЛИЧИЯ ЦЕПНОГО И
Дата: 2019-02-02, просмотров: 402.