Содержание
Ревматизм (ревматическая лихорадка)......................................... .... 105
Инфекционный эндокардит............................................................... .... 116
Миокардит............................................................................................. .... 128
Перикардит............................................................................................ 136
Нарушения сердечного ритма и проводимости. —
Проф. А.В. Недоступ, канд. мед. наук О.В. Благова 146
Экстрасистолия.......................................................................... .... 148
Пароксизмальная тахикардия................................................ .... 154
Мерцательная аритмия............................................................ 159
Атриовентрикулярная блокада.............................................. 166
Синдром слабости синусового узла..................................... .... 170
Приобретенные пороки сердца........................................................ .... 174
Пороки митрального клапана................................................ .... 175
Пороки аортального клапана................................................. 187
Пороки трехстворчатого клапана......................................... 198
Кардиомиопатии.................................................................................. ... 203
Дилатационная кардиомиопатия.......................................... ... 203
Гипертрофическая кардиомиопатия.................................... ... 206
Рестриктивная кардиомиопатия............................................ ... 211
Нейроциркуляторная дистония....................................................... 213
Гипертоническая болезнь.................................................................. 222
Симптоматическая артериальная гипертония . . . 241
Ишемическая болезнь сердца........................................................... ... 250
Стенокардия................................................................................ ... 251
Острый коронарный синдром................................................. 262
Инфаркт миокарда. — Проф. В.А. Сулимое . . 265
Сердечная недостаточность............................................................. 276
Контрольные вопросы и задачи............................................ 287
положенных к нему лиц, главным образом молодого возраста, в связи с инфекцией (3-гемолитическим стрептококком группы А.
Это определение болезни [Насонова В.А., 1989] подчеркивает:
• преимущественное поражение сердечно-сосудистой системы;
• роль патологической наследственности;
• значение стрептококковой инфекции.
Сущность болезни заключается в поражении всех оболочек сердца, но главным образом миокарда и эндокарда с возникновением деформации клапанного аппарата — порока сердца и последующим развитием сердечной недостаточности. Поражение других органов и систем при ревматизме имеет второстепенное значение и не определяет его тяжести и прогноза.
Пик заболеваемости приходится на детский и юношеский возраст (5—15 лет) и не зависит от пола. Первичная атака ревматизма может быть у лиц в возрасте 20—30 лет, однако после 30 лет первичный ревматизм практически не встречается. После 40 лет ревматизмом не заболевают. Тем не менее можно встретить больного и старше 60 лет, страдающего ревматическим пороком сердца, однако из этого не следует, что он заболел впервые в этом возрасте; ревматическая атака у него была в молодом возрасте.
Этиология. Отмечено, что заболевшие ревматизмом незадолго до начала болезни перенесли ангину, обострение хронического тонзиллита, а в крови у них определялось повышенное количество стрептококкового антигена и противострептококковых антител. Такая связь с предшествующей стрептококковой инфекцией особенно выражена при остром течении ревматизма, сопровождающемся полиартритом.
В развитии ревматизма имеют значение социальные факторы (неблагоприятные бытовые условия, недостаточное питание), а также генетическая предрасположенность (хорошо известно существование «ревматических» семей), которая заключается в гипериммунном ответе на антигены стрептококка, склонности заболевших к аутоиммунным и иммунокомплексным процессам.
Патогенез. В ответ на попадание в организм стрептококковой инфекции вырабатываются противострептококковые антитела и образуются иммунные комплексы (антигены стрептококка + антитела к ним + комплемент), циркулирующие в крови и оседающие в микроциркуляторном русле. Повреждающее действие на миокард и соединительную ткань оказывают также токсины и ферменты стрептококка (схема 8).
Вследствие генетически обусловленного дефекта иммунной системы из организма больных недостаточно полно и быстро элиминируются стрептококковые антигены и иммунные комплексы. Ткани таких больных обладают повышенной склонностью фиксировать эти иммунные комплексы. Кроме того, важны перекрестно реагирующие антитела, которые, появляясь в ответ на присутствие антигенов стрептококка, способны реагировать с тканевыми, в том числе кардиальными антигенами организма. В ответ развивается воспаление на иммунной основе (по типу гиперчувствительности немедленного типа — ГНТ), при этом факторами, реализующими воспалительный процесс, являются лизосомные ферменты нейтрофилов, фагоцитирующих иммунные комплексы и разрушающихся при этом. Этот воспалительный процесс локализуется в соединительной ткани преимущественно сердечно-сосудистой системы и изменяет антигенные свойства ее и миокарда. В результате развиваются аутоиммунные процессы по типу гиперчувствительности замедленного типа (ГЗТ), и в крови больных обнаруживаются лимфоциты, реагирующие с миоцитами. Этим клеткам придают 106
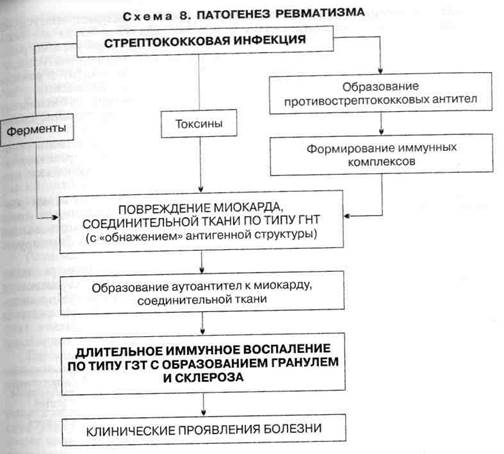
большое значение в происхождении органных поражений (прежде всего сердца). В крови выявляются также противомиокардиальные антитела, но они имеют меньшее значение в развитии поражения сердца.
Системный воспалительный процесс при ревматизме проявляется характерными фазовыми изменениями соединительной ткани (мукоидное набухание — фибриноидные изменения — фибриноидный некроз) и клеточных реакциях (инфильтрация лимфоцитами и плазмоцитами, образование ревматической, или ашофф-талалаевской, гранулемы). Эти клеточные Реакции являются морфологическим выражением иммунных нарушений. Патологический процесс завершается склерозированием.
Другим морфологическим субстратом поражения сердца при ревмокардите является неспецифическая воспалительная реакция, по существу аналогичная таковой в суставах и серозных оболочках. Она выражается в отеке межмышечной соединительной ткани, выпотевании фибрина, инфильтрации клеточными элементами, преимущественно нейтрофилами и лимфоцитами.
Так как патологический процесс имеет аутоиммунный характер, то и заболевание течет волнообразно, обостряясь под влиянием инфекции или Неспецифических факторов (переохлаждение, физическое напряжение, эмоциональный стресс и пр.).
107
При поражении сердца воспалительный процесс распространяется на эндокард и миокард (эндомиокардит или ревмокардит) либо на все оболочки сердца (панкардит) или поражает только миокард (при первой, реже при второй атаке). Морфологические изменения при ревматизме обнаруживаются прежде всего в миокарде, поэтому именно миокардит в ранние сроки определяет клиническую картину. Воспалительные изменения в эндокарде (вальвулит, бородавчатый эндокардит), поражение сухожильных нитей и фиброзного кольца клинически выявляются в более поздние сроки атаки ревматизма — спустя 6—8 нед.
Наблюдается определенная закономерность поражения клапанов сердца: чаще всего поражается митральный, затем аортальный и трехстворчатый клапаны. Клапан легочной артерии при ревматизме практически никогда не поражается.
Различные пороки сердца возникают в разные сроки после атаки ревматизма: недостаточность митрального клапана — спустя 6 мес после начала атаки (недостаточность клапана аорты немного раньше), митральный стеноз — через 2 года после атаки; в еще более поздние сроки формируется стеноз устья аорты.
Классификация. В настоящее время приняты классификация ревматической лихорадки (Ассоциация ревматологов России, 2003), отражающая клинические варианты, основные и дополнительные клинические проявления, исходы и функциональное состояние сердечно-сосудистой системы (табл. 8).
Таблица 8. Классификация ревматической лихорадки
| Клинические варианты | Клинические проявления | Исход | Недостаточность кровообращения, | |
| основные | дополнительные | Выздоровление Хроническая ревматическая болезнь сердца: без пороков сердца; с пороком сердца | Отсутствует I II III | |
| Острая ревматическая лихорадка Повторная ревматическая лихорадка | Кардит Артрит Хорея Кольцевидная эритема Ревматические узелки | Лихорадка Артралгии Абдоминальный синдром Серозиты | ||
Клиническая картина. Как известно, при ревматизме преимущественно страдает сердечно-сосудистая система. Поэтому целесообразно все проявления болезни разделить на сердечные и внесердечные и описывать клиническую картину болезни с этих позиций.
Следует иметь в виду, что клиническая картина собственно ревматизма более отчетлива при первой его атаке, пока порок еще не сформирован. При рецидивах ревматизма, когда уже сформировался порок сердца, а тем более при наличии сердечной недостаточности клиническую симптоматику активного ревматического процесса выявить труднее, так как она обусловливается сочетанием порока сердца и нарушением кровообращения. В связи с этим ниже рассматривается клиническая картина первичной атаки ревматизма.
На I этапе диагностического поиска выявляется связь болезни с перенесенной инфекцией. В типичных случаях, спустя 1—2 нед после ангины 108
илИ острого респираторного заболевания, повышается температура тела (Ъ 90 % случаев), иногда до 38—40 °С, с суточными колебаниями 1—2 °С и сильным потом (как правило, без озноба). При повторных атаках ревматизма рецидив болезни часто развивается вне связи с перенесенной инфекцией (имеют значение неспецифические факторы: переохлаждение, физическая перегрузка, оперативное вмешательство).
В настоящее время наиболее частым, а у большинства больных единственным проявлением ревматизма является поражение сердца — ревмокардит. Под ревмокардитом понимают одновременное поражение миокарда и эндокарда. Попытки дифференцировать миокардит от эндокардита не увенчались успехом.
У взрослых ревмокардит протекает легко. Больные предъявляют жалобы на слабые боли или неприятные ощущения в области сердца, легкую одышку при нагрузке, значительно реже отмечают перебои или сердцебиения. Эти симптомы не являются специфичными для ревматического поражения сердца и могут наблюдаться при других заболеваниях. Природа таких жалоб уточняется на последующих этапах диагностического поиска.
Ревмокардит у некоторых больных молодого возраста (чаще у детей) может протекать тяжело: с самого начала болезни возникают сердцебиения, сильная одышка при нагрузке и в покое, постоянные боли в области сердца. Могут появляться симптомы недостаточности кровообращения в большом круге в виде отеков и тяжести в области правого подреберья (за счет увеличения печени). Все эти симптомы указывают на диффузный миокардит тяжелого течения.
Перикардит, так же как внесердечные проявления ревматизма, в настоящее время встречается редко, обычно при остром течении у детей и лиц молодого возраста.
При развитии сухого перикардита больные отмечают лишь постоянные боли в области сердца. Экссудативный перикардит, который характеризуется накоплением в сердечной сумке серозно-фибринозного экссудата, имеет свою клиническую картину: боли исчезают в связи с разъединением воспаленных листков перикарда накапливающимся экссудатом. Появляется одышка, которая усиливается при горизонтальном положении больного. Вследствие затруднения притока крови к правым отделам сердца появляются застойные явления в большом круге кровообращения (отеки, тяжесть в правом подреберье вследствие увеличения печени).
Изменения опорно-двигательного аппарата проявляются в виде ревматического полиартрита. Больные отмечают быстро нарастающую боль в крупных суставах (коленных, локтевых, плечевых, голеностопных, лучеза-пястных), невозможность активных движений, увеличение суставов в объеме.
Особенностью ревматического полиартрита является быстрое и полное обратное его развитие при назначении противоревматических препаратов. Иногда поражение суставов проявляется лишь полиартралгией — болями в суставах без развития артрита (в 10 % случаев).
Ревматические поражения легких в виде пневмонии или плеврита наблюдаются крайне редко, их субъективные симптомы такие же, как и при ооычных поражениях (см. «Острая пневмония», «Плеврит»).
Ревматические поражения почек также крайне редки, выявляются лишь а III этапе диагностического поиска (при исследовании мочи).
Ревматические поражения нервной системы встречаются исключительно urtf°' пРеимУЩественно У детей. Жалобы не отличаются от жалоб при энцефалите, менингоэнцефалите, церебральном васкулите иной этиологии.
 Заслуживает внимания лишь «малая хорея», встречающаяся у детей (преимущественно у девочек) и проявляющаяся сочетанием эмоциональной лабильности и насильственных гиперкинезов верхней части туловища, верхних конечностей и мимической мускулатуры.
Заслуживает внимания лишь «малая хорея», встречающаяся у детей (преимущественно у девочек) и проявляющаяся сочетанием эмоциональной лабильности и насильственных гиперкинезов верхней части туловища, верхних конечностей и мимической мускулатуры.
Абдоминальный синдром (перитонит) возникает почти исключительно у детей и подростков с острым первичным ревматизмом, характеризуется внезапным появлением наряду с лихорадкой диффузных или локализованных схваткообразных болей, сопровождающихся тошнотой, реже рвотой, задержкой или учащением стула. Ревматический перитонит не оставляет стойких изменений и не рецидивирует.
Таким образом, на I этапе диагностического поиска при первичном ревматизме наиболее часты жалобы, связанные с поражением сердца, реже с вовлечением в патологический процесс суставов, а также жалобы общего порядка (утомляемость, потливость, повышение температуры тела).
На II этапе диагностического поиска наибольшее значение имеет обнаружение признаков поражения сердца.
При первичном ревмокардите сердце обычно не увеличено (лишь изредка отмечается умеренное его увеличение), при аускультации выявляются приглушенный I тон, иногда III тон, мягкий систолический шум над верхушкой. Эта симптоматика — не проявление поражения клапанного аппарата; она обусловлена изменениями миокарда (ревматический миокардит). Однако нарастание интенсивности шума, большая продолжительность его и стойкость могут указывать на формирование недостаточности митрального клапана. Уверенно судить о формировании порока можно спустя 6 мес после начала атаки при сохранении приведенной аускультативной картины.
В случае поражения клапана аорты может выслушиваться и в дальнейшем нарастать по интенсивности и продолжительности протодиастоличе-ский шум в точке Боткина, при этом звучность II тона может сохраняться. Лишь спустя много лет, после формирования выраженной недостаточности клапана аорты, вместе с протодиастолическим шумом определяется ослабление (или отсутствие) II тона во втором межреберье справа.
При более редко встречающемся сухом перикардите появляются характерные симптомы (подробно см. «Перикардит») в виде шума трения перикарда, а при наличии выпота в полости перикарда — глухость тонов в сочетании со значительным расширением границ сердца во все стороны и симптомами недостаточности кровообращения в большом круге.
У больных полиартритом отмечаются деформация суставов за счет воспаления синовиальной оболочки и околосуставных тканей, болезненность при пальпации сустава. Все эти изменения после проведения противоревматической терапии бесследно исчезают.
Поражение периартикулярных тканей проявляется в виде ревматических узелков, которые располагаются в области пораженных суставов, на предплечьях и голенях, над костными выступами. Это мелкие (величиной с горошину), плотные безболезненные образования, исчезающие под влиянием лечения. В настоящее время эти образования почти не встречаются.
Кольцевидная эритема — признак, практически патогномоничный для ревматизма, представляет собой розовые кольцевидные элементы, не зудящие, располагающиеся преимущественно на коже внутренней поверхности рук и ног, живота, шеи и туловища. Этот признак встречается исключительно редко (1—2 % больных). Иногда наблюдается также узловатая эри тема.
Ревматические пневмонии и плевриты имеют те же физикальные признаки, что и аналогичные заболевания банальной этиологии. ПО
В целом внесердечные поражения в настоящее время наблюдаются айне редко, у лиц молодого возраста при остром течении ревматизма /уши наличии высокой активности — III степени). Они нерезко выражены, быстро поддаются обратному развитию при проведении противоревматической терапии.
На III этапе диагностического поиска данные лабораторно-инструмен-ального исследования позволяют установить активность патологического процесса и уточнить поражение сердца и других органов. При активном ревматическом процессе лабораторные исследования выявляют неспецифические острофазовые и измененные иммунологические показатели.
К «острофазовым» показателям относятся нейтрофилез со сдвигом лейкоцитарной формулы крови влево (лейкоцитоз до 12—15 109/л отмечается лишь при III степени активности процесса, что обычно сочетается с ревматическим полиартритом); увеличение содержания (32-глобулинов, сменяющееся повышением уровня у-глобулинов; повышение содержания фибриногена; появление С-реактивного белка; возрастает СОЭ. В большинстве случаев биохимические показатели параллельны величинам СОЭ, которая остается основным лабораторным признаком активности ревматизма.
Что касается иммунологических показателей, то повышаются титры противострептококковых антител (антигиалуронидазы и антистрептокина-зы более 1:300, анти-О-стрептолизина более 1:250). Повышение уровня этих антител отражает реакцию организма на воздействие стрептококка и поэтому часто наблюдается при любой стрептококковой инфекции. Диагностическое значение имеют значительно повышенные титры антител.
Все лабораторные показатели у больных с активным ревматическим процессом и с наличием сердечной недостаточности вследствие порока сердца изменены нерезко или соответствуют норме. Однако при уменьшении явлений сердечной недостаточности после применения мочегонных средств и сердечных гликозидов лабораторные признаки активности начинают определяться.
При электрокардиографическом исследовании иногда выявляются нарушения ритма и проводимости, преходящая атриовентрикулярная блокада (чаще I степени — удлинение интервала P—Q, реже II степени), экстрасис-толия, атриовентрикулярный ритм. У ряда больных регистрируются изменения зубца Т в виде снижения его амплитуды вплоть до появления негативных зубцов (преимущественно в грудных отведениях).
Указанные нарушения ритма и проводимости нестойкие, в процессе противоревматической терапии быстро исчезают. Иногда они исчезают самостоятельно. В подобных случаях ЭКГ отражает не столько поражение миокарда, сколько изменение функционального состояния его нервного аппарата в связи с повышением тонуса блуждающего нерва. После назначения атропина изменения на ЭКГ исчезают. Если изменения на ЭКГ стойкие и остаются после ликвидации ревматической атаки, то следует думать об органическом поражении миокарда. При развитии ревмокардита на фоне уже имеющегося порока сердца на ЭКГ отражаются изменения, свойственные данному клапанному поражению (синдромы гипертрофии Миокарда предсердий и желудочков, выраженные в различной степени).
При фонокардиографическом исследовании уточняются данные аускуль-ации: ослабление I тона, появление III тона, систолический шум. В слу-ае формирования порока сердца на ЦКГ появляются изменения, соответствующие характеру клапанного поражения. Развитие ревмокардита на фоне порока сердца на ЦКГ проявляется характерными признаками это-10 порока.
111
Рентгенологически при первой атаке ревматизма каких-либо изменений выявить не удается. Лишь при тяжелом ревмокардите у детей и лиц молодого возраста можно обнаружить увеличение сердца за счет дилатации левого желудочка.
При развитии ревмокардита на фоне уже имеющегося порока сердца рентгенологическая картина будет соответствовать конкретному пороку.
Эхокардиографическое исследование при первичном ревмокардите каких-либо характерных изменений не выявляет. Лишь при тяжелом течении ревмокардита с признаками сердечной недостаточности на эхокардиограм-ме (ЭхоКГ) обнаруживают признаки, указывающие на снижение сократительной функции миокарда и расширение полостей сердца. Если ревмокардит развивается на фоне порока сердца, то выявляются признаки, свойственные этому поражению.
Данные, полученные на всех трех этапах диагностического поиска, лежат в основе определения степени активности ревматического процесса (табл. 9).
Таблица 9. Клинико-лабораторная характеристика активности ревматического процесса
| Степень активности | Клинические признаки | ЭКГ-ФКГ и рентгенологические признаки | Лабораторные признаки |
| III (максимальная) II (умеренная) I (минимальная) | Яркие общие и местные проявления с наличием лихорадки, экс-судагивного компонента в пораженных органах Умеренные клинические проявления и лихорадка (или без нее), без выраженного экс-судативного компонента в пораженных органах, меньшая тенденция к множественному вовлечению органов в патологический процесс Клинические симптомы выражены слабо, иногда едва выявляются. Преимущественно мо-носиндромный характер воспалительных поражений | В зависимости от преимущественной локализации ревматического процесса могут выявляться ярко. Умеренно или слабо-выраженные признаки поражения сердца, легких, плевры Признаки кардита выражены умеренно Выражены слабо | Нейтрофильный лейкоцитоз, СОЭ 40 мм/ч и выше. Резкое увеличение содержания фибриногена, а2-глобули-нов. Высокие титры противостреп-тококковых антител СОЭ 20-40 мм/ч, умеренное повышение титров про-тивострептококко-вых антител Не изменены или минимально повышены |
Диагностика. Распознавание первичного ревматизма представляет большие трудности, так как наиболее частые его проявления, такие как полиартрит и поражение сердца, неспецифичны. В настоящее время во всем мире наибольшее распространение получили большие и малые критерий
112
Таблица 10. Большие и малые критерии ревматизма
| Кардит Полиартрит Хорея Кольцевидная эритема Подкожные ревматические | узелки | Клинические: артралгии лихорадка Лабораторные: острофазовые показатели (СОЭ, СРБ, лейкоцитоз) Инструментальные: удлинение интервала P—Q на ЭКГ признаки митральной или аортальной ре-гургитации при допплер-ЭхоКГ |
ревматизма Американской ассоциации кардиологов, пересмотр которых производился в 1992 г. (табл. 10).
Свидетельства связи со стрептококковой инфекцией:
повышенный титр противострептококковых антител (АСЛ-О, АГ и др.),
недавно перенесенная скарлатина.
Сочетание двух больших или одного большого и двух малых критериев указывает на большую вероятность ревматизма лишь в случаях тщательно документированной предшествующей стрептококковой инфекции (недавно перенесенная скарлатина, высевание из носоглотки стрептококков группы А, повышенные титры противострептококковых антител — АСЛ-О, АГ,
АСК).
При постепенном начале ревматизма имеет значение предложенная А.И. Нестеровым (1973) синдромная диагностика: клинико-эпидемио-логический синдром (связь со стрептококковой инфекцией); клинико-иммунологический синдром (признаки неполной реконвалесценции, артралгии, повышение титров противострептококковых антител, а также обнаружение диспротеинемии и острофазовых показателей); кардиоваску-лярный синдром (обнаружение кардита, а также экстракардиальных поражений).
Дифференциальная диагностика. Распознавание активного ревматического процесса у больных с ранее сформировавшимся пороком сердца не представляет особенных трудностей. Первичный ревматизм, протекающий без ярких клинических проявлений, весьма сходен с другими заболеваниями, что заставляет проводить дифференциальную диагностику, в первую очередь с инфекционно-аллергическим миокардитом.
Для первичного ревмокардита в отличие от инфекционно-аллергиче-ского миокардита характерны:
а) связь заболевания с носоглоточной стрептококковой инфекцией;
б) латентный период в 1—3 нед от окончания предшествующей инфек
ции до первых клинических проявлений ревматизма;
в) преимущественное возникновение болезни в детском и юношеском
возрасте;
г) обнаружение полиартрита или острых артралгии как начальных про
шений болезни;
Д) отсутствие «кардиальных» жалоб или их констатация лишь при целе-
Направленном сборе анамнеза;
е) частое выявление объективных симптомов поражения сердца;
| 113 |
ж) четкая корреляция выраженности клинических проявлений ревматиз-
а с лабораторными показателями активности ревматического процесса.
При ревмокардите отсутствует хронологическая связь с нестрептокок-ковыми инфекциями, стрессовыми воздействиями; латентный период всегда присутствует и не укорочен. Инфекционно-аллергический миокардит отмечается у лиц молодого, среднего, пожилого возраста; характеризуется постепенным началом, отсутствием суставного синдрома в начале болезни-лабораторные признаки активности могут отсутствовать при наличии выраженных признаков кардита; отмечаются астенизация и вегетативная дисфункция.
Первичный ревмокардит следует дифференцировать от так называемых функциональных заболеваний сердца (см. «Нейроциркуляторная дистония»). Общими для обоих заболеваний являются «кардиальные» жалобы, связь ухудшения состояния с перенесенной инфекцией, субфебрилитет, молодой возраст.
Углубленный анализ симптомов показывает, что при первичном ревмокардите в отличие от нейроциркуляторной дистонии нет связи начала болезни с разнообразными стрессорными воздействиями, отсутствуют ас-теноневротические «кардиальные» жалобы (ощущение остановки, замирания сердца), так называемый респираторный синдром (чувство нехватки воздуха, неудовлетворенность вдохом) и вегетативно-сосудистые кризы. В то же время при нейроциркуляторной дистонии отмечается длительный анамнез, и больные попадают в поле зрения врача во время очередного обострения болезни, при этом не выявляется признаков поражения миокарда (увеличение размеров, глухость I тона, систолический шум, трехчленный ритм в сочетании с тахикардией), нет и лабораторных острофазовых показателей, а также измененных иммунологических показателей. Эффект седативной терапии и применения (3-адреноблокаторов отчетливо выражен.
Если в клинической картине первичного ревматизма доминирует поражение суставов (выраженный полиартрит), то дифференциальную диагностику необходимо проводить с реактивными артритами (развивающимися в ответ на кишечную или урогенитальную неспецифическую инфекцию), а также с системной красной волчанкой. Основу отличия ревматизма от этих заболеваний составляют такие признаки, как эпидемиологический анамнез, частое сочетание полиартрита с поражением сердца, быстрая динамика клинической симптоматики под влиянием противоревматической терапии.
Распознавание активного ревматического процесса у больных с наличием сформированного порока сердца (возвратного ревмокардита) основывается на тех же диагностических критериях, однако данные физикального исследования сердца, инструментальные и рентгенологические показатели в гораздо большей степени будут обусловлены существующим пороком сердца, а не активным ревматическим процессом. Поэтому при диагностике рецидива ревматизма следует ориентироваться на связь ухудшения состояния больного (проявляется появлением или нарастанием симптомов сердечной недостаточности) с перенесенной инфекцией, наличием артрал-гий, субфебрильной температуры, лабораторных показателей активности ревматического процесса (острофазовых и иммунологических).
Возвратный (рецидивирующий) ревмокардит на фоне того или иного порока сердца при наличии недостаточности кровообращения следует дифференцировать от инфекционно-аллергического (неспецифиче ского) миокардита тяжелого течения. Основным при этом является отсутствие «ревматического» анамнеза, признаков клапанного порока сердца и лабораторных показателей активности при миокардите.
114
формулировка развернутого клинического диагноза осуществляется в со-
етствии с классификацией и номенклатурой ревматизма и включает педуюшие пункты: 1) наличие активности процесса (степень активности) ли ремиссии; 2) характер поражения сердца; 3) наличие (отсутствие) потения других органов и систем; 4) характер течения; 5) состояние кровообращения.
Лечение. В настоящее время при ревматизме лечение проводится в 3 этапа: 1) лечение в активной фазе в стационаре; 2) продолжение лечения больного после выписки в кардиоревматологических кабинетах поликлиники; 3) последующее многолетнее диспансерное наблюдение и профилактическое лечение в поликлинике.
Лечебные мероприятия включают: а) борьбу со стрептококковой инфекцией; б) подавление активного ревматического процесса (воспаление на иммунной основе); в) коррекцию иммунологических нарушений.
На I этапе (стационарном) показано соблюдение постельного режима в течение 2—3 нед, питание с ограничением хлорида натрия (поваренной соли) и достаточным количеством полноценных белков (не менее 1—1,5 г на 1 кг массы тела).
Этиотропная терапия осуществляется пенициллином, оказывающим бактерицидное действие на гемолитические стрептококки группы А. Пенициллин назначают в дозе 1,5—4 млн ЕД в течение 10 дней. Вместо пенициллина можно использовать полисинтетические пенициллины (ампициллин, оксациллин и пр.). При индивидуальной непереносимости пеницил-линов применяют макролиды: спирамицин по 6 млн ME в два приема в течение 10 дней; азитромицин по 0,5 г 1 раз в течение 3 дней; рокситроми-цин по 0,3 г 2 раза в день в течение 10 дней.
Активный ревматический процесс купируют различными нестероидными противовоспалительными препаратами (НПВП). Преимущество отдается индометацину и диклофенаку — наиболее эффективным средствам, оказывающим наименее выраженное побочное действие. Суточная доза этих препаратов составляет 100 мг. Вместо них можно назначать ацетилсалициловую кислоту по 4—5 г/сут. Эти препараты следует принимать до полной ликвидации активности ревматического процесса.
При высокой активности (III степень), тяжелом первичном ревмокардите с признаками сердечной недостаточности (чаще встречается у лиц молодого возраста) или признаками полисерозита показаны глюкокортико-стероидные препараты (преднизолон 1—1,5 мг/кг). По достижении клинического эффекта (обычно через 2 нед) дозу постепенно снижают с последующим назначением НПВП.
При вяло текущем процессе больший эффект достигается от проведения иммуносупрессивной терапии (коррекция иммунного гомеостаза) с помощью аминохинолиновых производных гидроксихлорохина (плаквени-ла), хингамина (делагила). Эти препараты назначают по 0,2 и 0,25 г соответственно 1—2 раза в сутки в течение длительного времени (не менее 1 года). Спустя год доза может быть уменьшена вполовину.
На II этапе (поликлиническом) лекарственная терапия должна продолжаться в дозах, с которыми больные были выписаны из стационара. Длительность приема противовоспалительных препаратов при остром течении 'оьгчно 1 мес, при подостром — 2 мес; как уже упоминалось выше, амино-Хинолиновые препараты принимают длительно (1—2 года).
Поликлинический этап предусматривает также обязательную бицилли-Нопрофилактику в течение 5 лет после перенесенной атаки ревматизма в 4°зах 1 500 000 ЕД бициллина-5 каждые 3 нед.
115
В задачу III этапа входит пребывание детей и подростков в местно^ ревматологическом санатории, а у взрослых — направление на реабилита. цию в кардиологический санаторий.
При хроническом тонзиллите хирургическое лечение должно прово. диться только при неэффективности консервативного, а также в случаях если обострение тонзиллита приводит к рецидиву ревматизма.
Больным с сердечной недостаточностью проводится соответствующая терапия ингибиторами ангиотензинпревращающего фермента (ИАПФ) сердечными гликозидами, мочегонными средствами (см. «Сердечная не. достаточность»).
Больных ревматизмом ставят на диспансерный учет не только с целью проведения противорецидивной терапии, но и для своевременного обнару. жения рецидива, а при прогрессировании клапанного порока — для своевременного направления в кардиохирургическое учреждение.
Прогноз. Непосредственная угроза для жизни при ревматизме наблюда-ется крайне редко. Прогноз в основном определяется выраженностью порока сердца и состоянием сократительной функции миокарда.
Профилактика. Первичная профилактика состоит из комплекса общественных и индивидуальных мер, направленных на предупреждение первичной заболеваемости (повышение жизненного уровня, пропаганда здорового образа жизни, в частности закаливания, улучшение жилищных условий, борьба со скученностью в детских садах, школах, общественных учреждениях).
Важным является раннее и эффективное лечение ангин и других острых стрептококковых заболеваний верхних дыхательных путей. Это достигается назначением пенициллина в течение первых 2 сут по 1 500 000 ЕД, на 2-е сутки вводят бициллин-5 по 1 500 000 ЕД. При непереносимости пе- [ нициллина можно назначать эритромицин в течение 10 дней. Любое лечение ангины должно продолжаться не менее 10 дней, что приводит к полному излечению стрептококковой инфекции.
Профилактика рецидива ревматической лихорадки (вторичная профилактика) проводится в стационаре сразу после окончания 10-дневного лечения пенициллинами (макролидами). Классический парентеральный режим — это бензатина бензилпенициллин (ретарпен, экстенциллин) по 1,2—2,4 млн ЕД внутримышечно 1 раз в течение 3—4 нед. Чем меньше возраст больного при первой атаке, тем больше вероятность рецидива. После пятилетнего наблюдения частота рецидивов, как правило, снижается с возрастом. Больные без ревмокардита в период первых атак должны получать противорецидивную пофилактику минимум 5 лет после последней атаки, по крайней мере до 21 года. Больным, имевшим поражение сердца в период предыдущей атаки, профилактику проводят минимум до 40 лет и более. Больным, перенесшим операцию на сердце по поводу ревматического порока сердца, вторичная профилактика проводится пожизненно.
Инфекционный эндокардит
ИНФЕКЦИОННЫЙ ЭНДОКАРДИТ (ИЭ) - полипозно-язвенное поражение клапанного аппарата сердца или пристеночного эндокарда (реже эндотелия аорты или крупной артерии), вызванное различными патогенными микроорганизмами или грибами и сопровождающееся тромбоэмбо-лиями, а также системным поражением сосудов и внутренних органов на фоне измененной реактивности организма. па
Термин «инфекционный эндокардит» в настоящее время вытеснил page использовавшиеся термины «бактериальный эндокардит», «затяжной Оптический эндокардит», так как лучше отражает причину заболевания, зываемого самыми разными микроорганизмами — бактериальными Рентами, риккетсиями, вирусами и грибами.
3 Наиболее часто заболевают ИЭ лица в возрасте 20—50 лет, несколько аще мужчины, чем женщины. Однако особенностью «современного» ИЭ ^пляется высокая частота заболевания в пожилом и старческом возрасте ?более 20 % всех случаев). Другая особенность ИЭ в настоящее время — увеличение числа больных с первичной формой болезни (более 50 %), появление новых клинических вариантов течения, значительное изменение характера возбудителя.
Этиология. Среди вызывающих ИЭ возбудителей наиболее часто встречайся кокковая флора — стрептококки (зеленящий стрептококк ранее встречался в 90 % случаев), а также стафилококки (золотистый, белый), энтерококк. Значительно реже причиной болезни является грамотрицательная флора _ кишечная палочка, синегнойная палочка, протей, клебсиелла. В последние годы важную роль стали играть патогенные грибы, протей, сарцины, бруцеллы, вирусы. У ряда больных истинный возбудитель заболевания не обнаруживается (частота отрицательного результата посева крови колеблется в пределах 20—50 %). Обнаружение возбудителя зависит от многих факторов: качества бактериологического исследования, длительности предшествующей антибактериальной терапии, характера возбудителя.
Источники инфекции и бактериемии при ИЭ самые разные:
• Операции в полости рта.
• Операции и диагностические процедуры в мочеполовой сфере.
• «Малые» кожные инфекции.
• Оперативное вмешательство на сердечно-сосудистой системе (в том числе протезирование клапанов).
• Длительное пребывание катетера в вене.
• Частые внутривенные вливания и эндоскопические методы исследования.
• Хронический гемодиализ (артериовенозный шунт).
• Наркомания (внутривенное введение наркотиков).
ИЭ может развиться на интактных клапанах — так называемый первичный эндокардит, а также на фоне предсуществующих (врожденных и приобретенных) изменений сердца и его клапанного аппарата — так называемый вторичный ИЭ. К числу этих изменений можно отнести пороки сердца (врожденные и приобретенные), пролапс митрального клапана, арте-риовенозные аневризмы, постинфарктные аневризмы, шунты при хроническом гемодиализе, состояние после операции на сердце и крупных сосудах (включая протезирование клапанов, комиссуротомию, искусственные сосудистые шунты).
Имеет значение в развитии ИЭ и ряд медицинских манипуляций (оперативные вмешательства в полости рта, катетеризация мочевого пузыря, Ректороманоскопия, установка внутривенного катетера. Наконец, имеет Так>ке значение ряд состояний, сопровождающихся снижением иммунитета: сахарный диабет, токсикомания, в том числе алкоголизм), ВИЧ-инфек-^ия, лечение мощными иммунодепрессантами. В настоящее время приобрел большое значение «ИЭ наркоманов».
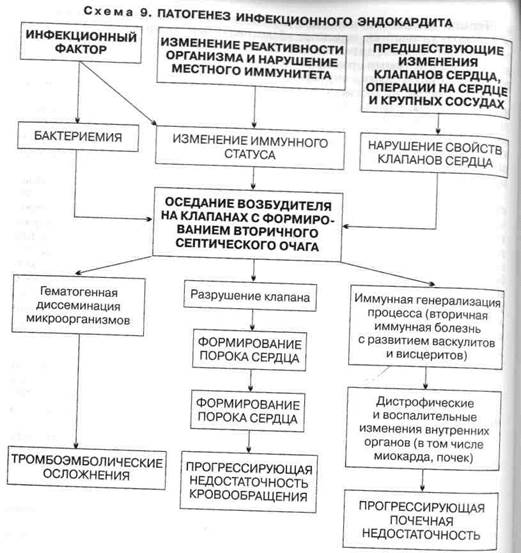
Патогенез. Механизм развития заболевания сложен и изучен недоста-
°чно, однако основные моменты развития ИЭ не вызывают сомнения
^схема 9). При наличии в организме очага инфекции под влиянием различ-
|
|
ных эндогенных и экзогенных факторов, изменяющих реактивность и имунный статус организма, развивается бактериемия.
Микроорганизмы из крови попадают на клапаны сердца, где создают в дальнейшем «вторичный» очаг инфекции. Фиксации и размножению микроорганизмов на эндокарде с формированием вторичного септического очага способствуют дополнительные факторы. По-видимому, имеют значение предшествующее изменение ткани и поверхности клапана, наличие на нем тромботических масс (часто с развитием абактериального эндокардита), возникающих под влиянием прямого повреждающего действия струи крови, движущейся с большой скоростью или под большим давлением (при имеющемся пороке сердца). Деформация клапанов вследствие возникновения большого градиента давления, узости отверстия и изменения скорости кровотока создает условия, способствующие
118
еДрению инфекционных агентов в эндокард с образованием инфекционного очага.
При поражении ранее интактного клапана происходят изменения, настающие нормальные свойства отдельных участков этого клапана в виде течности, экссудативных или пролиферативных процессов («интерстици-° ный вальвулит» — доклиническая фаза). Подобная ситуация возможна я при повреждении интимы крупных сосудов.
Происходит снижение иммунитета (в основном клеточного) с развитием вторичных иммунных нарушений (наряду с бактериальными антигена-мИ существуют и антигены тканевого происхождения, что приводит к образованию иммунных комплексов, которые циркуляруют в крови и оседают на различные органы и ткани).
В клинической картине заболевания принято выделять группы симптомов, обусловленных различными патогенетическими механизмами.
Симптомы, обусловленные инфекционно-токсическим воздействием, протекают с интоксикацией различной степени выраженности и с повышением температуры. Рост бактерий сопровождается формированием вегетации с разрушением клапанов (развитие порока сердца). Происходит также генерализация процесса за счет гематогенного распространения инфекции. Отрыв фрагментов клапанных микробных вегетации способствует заносу инфицированных эмболов в различные участки сосудистого русла и усугубляет септические проявления. Одновременно эмболы, попадая с током крови в различные органы, вызывают развитие тромбоэмболических осложнений, проявляющихся симптомами инфаркта почки, миокарда, селезенки, сосудов глаз, кожи и т.п.
Симптомы, обусловленные иммуновоспалительными механизмами, связаны с иммунной генерализацией процесса. Микроорганизмы, фиксированные на клапанах, вызывают длительную аутосенсибилизацию и гиперергиче-ское повреждение органов и тканей организма. В этой стадии выявляются циркулирующие в крови и фиксированные в тканях (сердце, почки, печень, сосуды) иммунные комплексы. Иммунные и аутоиммунные нарушения обусловливают развитие васкулитов и висцеритов (иммунокомплекс-ный нефрит, миокардит, гепатит, капиллярит и т.д.). В ряде случаев иммунные нарушения, называемые вторичными, могут развиваться с самого начала болезни, по существу в продромальном периоде.
При дальнейшем прогрессировании болезни могут развиваться дистрофические изменения органов с их функциональной недостаточностью (наибольшее значение имеют сердечная и почечная недостаточность, часто приводящая к смерти больных).
Классификация. В настоящее время отсутствует общепринятая классификация болезни. Тем не менее следует выделять клинико-морфологиче-ские формы (первичный — развивающийся на интактных клапанах, при этом выделяется ИЭ у наркоманов; вторичный с указанием фона, на котором развился ИЭ), варианты течения (острый, подострый, затяжной), Функциональное состояние органов и систем.
Острый ИЭ (быстропрогрессируюший) развивается, как правило, у лиц, Ранее не имевших поражения сердца, и клинически проявляется картиной общего сепсиса. Острый вариант ИЭ отличается очень высокой летальностью и длится не более 2 мес; однако при современных методах лечения иногда удается перевести его в подострый.
Подострый ИЭ обычно длится более 2 мес; после проведения достаточно упорной терапии может наступить ремиссия. В последующем возможны Рецидивы болезни. Это наиболее частый вариант болезни.
119
Затяжной ИЭ длится многие месяцы с периодами обострения и ремиссий. При благоприятном течении клинические проявления неяркие, лабораторные показатели и нарушения общего состояния незначительные. Заболевание обычно вызывают маловирулентные возбудители (чаще стрептококк); оно хорошо поддается лечению. Неблагоприятный вариант характеризуется вялым течением без ярких клинических проявлений, но с тяжелыми осложнениями и плохим прогнозом (больные погибают от прогрессирующей сердечной недостаточности, нарастающей септической интоксикации).
Клиническая картина. Проявления ИЭ весьма разнообразны и могут быть представлены в виде ряда синдромов.
• Синдром воспалительных изменений и септицемии (лихорадка, озноб, геморрагические высыпания, изменение острофазовых показателей крови: лейкоцитоз со сдвигом влево, увеличение СОЭ, появление СРБ, повышение содержания фибриногена, а2-глобулинов, положительная гемо-культура).
• Интоксикационный синдром (общая слабость, выраженная потливость, головные боли, миалгии и артралгии, снижение аппетита, бледность кожных покровов с желтушным оттенком).
• Синдром клапанных поражений (формирование порока сердца, чаще аортального или митрального прежде не измененных клапанов или присоединение новых поражений клапанов к ранее существовавшим).
• Синдром «лабораторных» иммунных нарушений (наличие циркулирующих в крови иммунных комплексов, фиксированных иммунокомплекс-ных депозитов в почках, миокарде, сосудах; гипергаммаглобулинемия; появление ревматоидного фактора; выявление противотканевых антител).
• Синдром тромбоэмболических осложнений (очаговый нефрит, инфаркт миокарда, селезенки, кишечника, тромбоэмболии в мозг, сетчатку глаза, сосуды нижних конечностей и т.д.).
• Синдром иммунных поражений органов и систем (диффузный гло-мерулонефрит, миокардит, гепатит, васкулит и т.д.).
Степень выраженности указанных синдромов различна. Она определяется не только периодом болезни, но и характером течения ИЭ, на который влияет вид возбудителя. Стафилококковый эндокардит характеризуется высокой активностью процесса, тяжелым общим состоянием, гектиче-ской лихорадкой, развитием гнойных осложнений. Грибковые эндокардиты, как правило, сопровождаются эмболической окклюзией крупных артерий, особенно нижних конечностей. «Классическая» картина заболевания характерна для ИЭ, вызванного зеленящим стрептококком.
На I этапе диагностического поиска обращают внимание на жалобы, обусловленные инфекцией и интоксикацией, тромбоэмболическими осложнениями, поражением сердца, вовлечением в патологический процесс других органов и систем.
Наиболее существенным для последующего диагноза следует считать одновременное появление жалоб, указывающих на инфекционный процесс и поражение сердца.
В анамнезе обычно выявляются указания на перенесенный в прошлом ревматизм, приобретенный или врожденный порок сердца, а также эпизоды «немотивированной» длительной лихорадки или субфебрилитета. Начало заболевания часто связано с острой инфекцией или обострением хронической инфекции, а также с рядом врачебных манипуляций (экстракция зубов, аборты, тонзиллэктомия, катетеризация мочевого пузыря, сосудов, операции на сердце и т.д.). Особенно характерно сочетание повышения
120
| те |
■мпературы тела с ознобами и потливостью. Степень повышения темперами тела может быть различной: при остром течении отмечается повыше-
ие ДО 39 "С, тогда как при подостром и затяжном течении температура иожет быть субфебрильной. Вместе с тем у больных, длительно болеющих
имеющих сердечную или почечную недостаточность, при рецидивах болезни и несомненной активности процесса температура тела может быть
нормальной.
Кроме того, можно выявить жалобы, обусловленные и сердечной недостаточностью (на фоне длительно существовавшего порока сердца), а также жалобы, связанные с тромбоэмболическими осложнениями (в особенности тромбоэмболии мелких мезентериальных сосудов, почечных артерий и селезенки).
В анамнезе больных могут быть эпизоды длительного лечения антибиотиками (это бывает при рецидиве ИЭ у больных, ранее уже подвергавшихся лечению).
В случае типичного течения болезни уже на этом этапе можно заподозрить ИЭ. У ряда больных на I этапе характер заболевания (ИЭ или какое-то иное заболевание) остается неясным и может быть установлен в дальнейшем лишь с учетом результатов последующих этапов диагностического поиска.
На II этапе диагностического поиска наибольшее значение для постановки правильного диагноза имеет обнаружение:
1) поражения клапанов сердца (появление патогномоничных для ИЭ симптомов аортальной или митральной недостаточности; изменение ау-скультативной картины ранее существовавших пороков сердца; появление «дополнительных» шумов);
2) поражения кожи и слизистых оболочек: цвет кожных покровов, напоминающий «кофе с молоком», геморрагии, положительные симптомы Гехта (щипка) и Кончаловского—Румпеля—Лееде (жгута), а также узелки Ослера — болезненные гиперемированные плотные узелки на ладонной поверхности и кончиках пальцев, признак Лукина—Либмана (пятна Лукина) — геморрагия на переходной складке конъюнктивы. Весьма типичным симптомом ИЭ является снижение массы тела, иногда значительное (на 15-20 кг);
3) увеличения селезенки и печени (спленомегалия часто наблюдается при ИЭ и почти никогда при ревматизме).
Пальцы в виде барабанных палочек — симптом, не имеющий в настоящее время большого диагностического значения, так как он встречается чрезвычайно редко (ранее этот симптом наблюдался в 30—50 % случаев). Тем не менее наличие его — лишний довод в пользу постановки Диагноза ИЭ.
При пороке сердца (особенно при «вторичных» ИЭ) можно обнаружить признаки хронической сердечной недостаточности. Другая причина их появления — развитие миокардита, что проявляется глухостью сердечных тонов, систолическим шумом, относительной недостаточностью митрального Клапана и дилатацией полостей сердца.
В редких случаях развивается перикардит (нерезкий шум трения периода, обусловленный фибринозными наложениями на перикарде).
При физикальном обследовании можно выявить повышение АД, вызы-
ающее подозрение на развитие диффузного гломерулонефрита. У части
гиЛЬНЫХ опРеДеляются нарушения центральной нервной системы (парезы,
перкинезы, патологические рефлексы и т.д.) как проявление васкулитов
^ли эмболии в мозговые сосуды. При исследовании органов дыхания мож-
выявить инфарктную пневмонию.
С учетом выявленных симптомов на этом этапе диагностического поиска диагноз ИЭ представляется весьма вероятным, особенно при характерном анамнезе. У лиц, не имеющих характерного анамнеза, выявленных симптомов также бывает достаточно, чтобы заподозрить ИЭ.
На II этапе наиболее частой диагностической ошибкой является оценка того или иного синдрома в качестве проявлений самостоятельного заболевания: например, при выраженных изменениях в анализе мочи ставят диагноз гломерулонефрита (как самостоятельного заболевания) и пр. Естественно, это возможно при недостаточном учете всей клинической картины и отсутствии связи ведущего синдрома с другими проявлениями болезни.
На III этапе диагностического поиска проводят исследования, подтверждающие предварительный диагноз ИЭ и позволяющие сформулировать окончательный развернутый диагноз.
Лабораторно-инструменталъные исследования предусматривают: 1) повторные попытки обнаружения возбудителя болезни при многократных посевах крови; 2) подтверждение и/или выявление воспалительного характера патологического процесса (выявление острофазовых показателей крови); 3) выявление иммунных сдвигов; 4) уточнение (или выявление) характера поражений различных органов и систем; 5) получение прямых диагностических признаков инфекционного поражения эндокарда.
• Получение положительной гемокультуры — наиболее важный диагностический признак ИЭ. Для подтверждения диагноза требуется не менее 2—3 анализов. Единичная положительная гемокультура должна интерпретироваться с большой осторожностью вследствие возможности случайного загрязнения. Большое значение имеют техника забора и посева крови, время посева (желательно на высоте лихорадки), использование обогащенных сред. Отрицательная гемокультура не исключает ИЭ. Переоценивать роль посевов крови нельзя, так как имеет значение только положительный результат в сопоставлении с клинической картиной.
• В клиническом анализе крови наиболее важным для диагностики является повышение СОЭ до 50 мм/ч и более. В начале ИЭ выявляется лейкоцитоз со сдвигом лейкоцитарной формулы влево; далее могут обнаруживаться лейкопения и гипохромная анемия.
Диагностическое значение придают обнаружению гистиоцитов в крови, взятой из мочки уха. Содержание их более шести в поле зрения может свидетельствовать в пользу ИЭ.
При биохимическом анализе крови выявляется увеличение содержания фибриногена, а2-глобулинов и резкое увеличение уровня гамма-глобулинов — до 30—40 относительных процентов. Как правило, оказываются положительными осадочные пробы (формоловая и тимоловая).
• Кроме гипергаммаглобулинемии, показателями иммунных сдвигов являются обнаружение циркулирующих иммунных комплексов, снижение титра комплемента, появление ревматоидного (антиглобулинового) фактора, усиление реакции бластной трансформации лимфоцитов с ФГА (фито-гемагглютинин) и бактериальными антигенами, выявление противоткане-вых антител. Как правило, при ИЭ в отличие от ревматизма титры анти-О-стрептолизина и антигиалуронидазы нормальные.
• Анализ мочи позволяет выявить гломерулонефрит, проявляющийся протеинурией, цилиндрурией и гематурией. При высоких показателях про-теинурии можно предположить развитие амилоидоза (редко встречающееся осложнение ИЭ). Повышение содержания билирубина, трансаминаз указывает на поражение печени.
рентгенологическое, электро- и фонокардиографическое исследования помогают уточнить характер клапанного поражения сердца.
• Прямой диагностический признак ИЭ — вегетацию на клапанах
дца _ можно обнаружить при эхокардиографии (ЭхоКГ), особенно если применяется чреспищеводная регистрация с помощью специального датчика.
Таким образом, на заключительном этапе диагностического поиска диагноз ИЭ можно поставить с уверенностью у большинства больных. В некоторых случаях для постановки окончательного диагноза необходимо динамическое наблюдение.
Диагностика. Распознавание ИЭ при развитой клинической картине заболевания не представляет существенных трудностей. В современной клинической практике применяют критерии, разработанные в 1994 г.
D. Durack.
Большие критерии:
1. Положительная гемокультура: типичные для ИЭ возбудители, выделенные их двух раздельно взятых проб крови, взятых с интервалом 12 ч, или во всех трех (или в большинстве проб из четырех и более посевов крови), взятых с более чем часовым интервалом.
2. Эхокардиографические признаки ИЭ: вегетации на клапанах сердца или подклапанных структурах, впервые возникшая клапанная недостаточность, абсцесс или дисфункция протезированного клапана.
Малые критерии:
1. Предшествующее поражение клапанов или частые внутривенные введения лекарств (в том числе и наркомания).
2. Лихорадка более 38 "С.
3. Сосудистые симптомы: артериальные эмболии, инфаркты легких, микотические аневризмы, внутричерепные кровоизлияния, пятна Лукина.
4. Иммунные проявления: гломерулонефрит, узелки Ослера, пятна Рота (овальные с бледным центром геморрагические высыпания на глазном дне), ревматоидный фактор.
5. Положительная гемокультура, не соответствующая требованиям
больших критериев, или серологические признаки активной инфекции
всевозможных возбудителей ИЭ.
6. Эхокардиографические признаки, согласующиеся с ИЭ, но не удовлетворяющие «большому» критерию («старые» вегетации, утолщение клапанных створок).
7. «Острофазовые» показатели, анемия, тромбоцитопения, гипергамма-
глобулинемия, протеинурия, гематурия.
ИЭ считается достоверным, если представлены:
• два больших критерия;
• один большой + три малых критерия;
• пять малых критериев.
ИЭ считается возможным, если нет полного набора признаков (как при достоверном диагнозе ИЭ), но есть признаки, не исключающие заболевание.
ИЭ исключается, если:
• доказан альтернативный диагноз, объясняющий проявления, типич-
ные для ИЭ;
• симптомы, напоминающие эндокардит, исчезли через 4 дня (или
менее) антибиотической терапии;
• отсутствовали морфологические признаки ИЭ на операции или
101
Укрытии.
Трудности диагностики обусловлены стертым и атипичным течение^ ИЭ. Если вторичный септический очаг локализуется не в сердце, а в интиме крупных артерий, то исчезает такой важный диагностический признак, как формирование порока сердца. С учетом этого необходимо оценивать комплекс других диагностически значимых симптомов ИЭ.
Определенные сложности возникают в диагностике на ранних этапах болезни, особенно при первичном ИЭ, начало которого очень напоминает другие заболевания.
Следует помнить о разнообразных вариантах начала ИЭ.
• «Типичное» постепенное начало заболевания (субфебрильная темпе
ратура тела, слабость, недомогание, головная боль, артралгии). В таких
случаях ИЭ следует дифференцировать от ревматизма; при развитии аор
тальной недостаточности — от висцерального сифилиса.
• Начало болезни по типу «острого инфекционного заболевания»: высокая температура тела с проливным потом и ознобом. Следует проводить дифференциальную диагностику с гриппом, брюшным тифом, малярией и другими инфекциями.
• Болезнь начинается с развития тромбоэмболии (наиболее часто в мозг, селезенку, почки). ИЭ необходимо дифференцировать от инсульта. Наиболее часто ИЭ проявляется тромбоэмболиями в мозг у пожилых людей. Дифференциальная диагностика проводится с почечной коликой при эмболии в почки.
• При появлении симптомов острого гломерулонефрита в начале болезни (гематурия, протеинурия, отеки, гипертония) необходим учет диагностически значимых проявлений ИЭ (шум регургитации, данные ЭхоКГ, положительная гемокультура и пр.).
• «Гематологическая маска» ИЭ, проявляющаяся анемией, увеличением селезенки, требует дифференциальной диагностики с целым рядом болезней системы крови.
Формулировка развернутого клинического диагноза включает: 1) клини-ко-морфологическую форму ИЭ (первичный или вторичный); 2) этиологию (если удается повторно получить положительную гемокультуру); 3) характер клапанного поражения; 4) наиболее важные органные поражения с указанием выраженности функциональных расстройств (сердечная, почечная недостаточность, анемия и пр.); 5) осложнения (тромбоэмболии и пр.).
Лечение. При лечении больных ИЭ следует руководствоваться рядом правил: 1) использовать антибиотики, активные в отношении потенциальных и установленных возбудителей; 2) применять бактерицидные антибиотики, так как в вегетациях микроорганизмы находятся в низкой метаболической активности; 3) использовать антибиотики, обладающие синергизмом; 4) вводить антибиотики парентерально для получения более высоких и предсказуемых сывороточных концентраций; 4) антимикробная терапия должна быть длительной для обеспечения стерилизации вегетации клапанов; 5) антибиотическую терапию следует начинать как можно раньше.
Следует различать эмпирическую антибиотикотерапию ИЭ и анти-биотикотерапию ИЭ установленной этиологии (известна бактериальная флора).
Эмпирическая антибиотическая терапия ИЭ при подостром течении:
• пенициллин 12—24 млн ЕД/сут в равных дозах каждые 4 ч (4 нед)
или
• ампициллин 175 мг/(кгсут) внутривенно в равных дозах каждые
4 ч (4 нед) и гентамицин 3 мг/(кгсут) внутривенно или внутримышечно в
2—3 дозах (2 нед)
или
• ванкомицин 15 мг/кг внутривенно каждые 12 ч (4—6 нед) и гента-мииин 3 мг/кг внутривенно или внутримышечно в 2—3 дозах (2 нед).
При ИЭ установленной этиологии (зеленящий стрептококк с различной ируЛентностью) используют также пенициллин в высоких дозах в сочетании с гентамицином или антибиотики группы цефалоспоринов III поколения (цефриаксон), аминогликозидов (тобрамицин); препараты вводят, как правило, внутривенно или внутримышечно (не менее 4 нед).
При ИЭ нестрептококковой этиологии целесообразно применять комбинированную терапию: пенициллин чаще всего комбинируют с аминоглико-зидами (гентамицином). Гентамицин применяют в дозах 240—320 мг/сут И—5 мг/кг) в виде курсового лечения: препарат вводят в течение 8 дней, затем 5—7 дней перерыв, повторное введение препарата в течение 8 дней, снова перерыв, при необходимости проводят третий курс. Цель прерывистого лечения — предупреждение нефротоксического, гепатотоксического действия препарата. У больных пожилого и старческого возраста суточная доза не должна превышать 240 мг. Вместо гентамицина может быть применен препарат этой же группы — сизомицин (2 мг/кг). Все препараты этой группы противопоказаны при почечной недостаточности и заболеваниях слухового нерва. Тем не менее комбинация пенициллина с аминогликозидами является одной из наиболее эффективных при лечении ИЭ.
При ИЭ стафилококковой этиологии весьма эффективны полусинтетические пенициллины, устойчивые к ферменту пенициллиназе, продуцируемой стафилококком. Наиболее часто используют оксациллин (10—20 г/сут), а также ампициллин, ампиокс (10—16 г/сут). Эти препараты сочетают с гентамицином. При отсутствии эффекта от лечения следует назначать антибиотики цефалоспоринового ряда: клафоран 6—8 г внутривенно или внутримышечно равными дозами каждые 6—8 ч (6 нед) в сочетании с сульфатом ами-кацина (1—1,5 г внутримышечно равными дозами каждые 8—12 ч в течение 14 дней с интервалом 14 дней); цефалотин (цефалотина натриевая соль) 8—12 г внутривенно или внутримышечно равными дозами каждые 6 ч (6 нед).
При энтерококковой инфекции — пенициллин 20 000 000 — 30 000 000 ЕД внутривенно или внутримышечно каждые 4 ч (6 нед) в сочетании со стрептомицином по 1 г внутримышечно равными дозами каждые 12 ч (4 нед). При недостаточном эффекте от данной комбинации препаратов назначают ампициллин по 8—12 г внутримышечно равными дозами каждые 6 ч (6 нед) с гентамицином в обычных дозах.
Лечение грибкового ИЭ проводится амфотерицином (30—55 мг/сут); курс — не менее 40—50 дней. Используют также дифлюкан.
В качестве антибиотиков резерва назначают вибрамицин, рондомицин, ФУзидин (2—3 г/сут).
К основным антибиотикам, применяемым при ИЭ, относится также
РИфампицин (в дозе 600—1200 мг в капсулах и внутривенно), действующий
на стафилококки и стрептококки. Препарат оказывает сенсибилизирующее
Действие, поэтому лучше проводить один длительный курс лечения, чем
повторные короткие курсы, чаще применяется как резервный препарат
Ри неэффективности других антибиотиков. Отмена антибиотиков произ-
одится сразу, без постепенного уменьшения дозы. После отмены антибак-
ериальных средств при хорошем самочувствии и благополучных лабора-
орных показателях больной наблюдается в стационаре еще 7—10 дней для
Рофилактики ранних рецидивов. Если в процессе лечения развивается ре-
зистентность микроорганизмов к проводимой терапии (что проявляется возвратом симптомов: вновь повышается температура тела, возникают озноб, слабость, увеличивается СОЭ), то необходимо резко повысить дозу применяемых антибиотиков либо сменить препарат.
Следует отметить, что факторами, обусловливающими резистентность к проводимой антибиотикотерапии, являются позднее начало лечения (в связи с трудностями диагностики); особая вирулентность микрофлоры; наличие микробных ассоциаций (патологический процесс вызывается не одним микроорганизмом); пожилой возраст больных; поражение нескольких клапанов одновременно; эндокардит трехстворчатого клапана; ИЭ, развивающийся у больных, имеющих протезы клапанов или подвергающихся гемодиализу.
Глюкокортикостероиды (ГКС) применяют в настоящее время для лечения ИЭ нечасто. Следует отметить, что при лечении ИЭ ГКС показаны при резко выраженных иммунных сдвигах: высоком уровне циркулирующих иммунных комплексов в крови, концентрации иммуноглобулинов М и А, васкулите, артрите, миокардите, а также в случае высокой аллергической чувствительности к антибиотикам. Назначают обычно небольшие дозы (15—20 мг преднизолона в сутки). Лечение кортикостероидами необходимо проводить обязательно в сочетании с антибиотиками и заканчивать его за 1 нед до отмены антибиотиков.
У больных с клиническими признаками миокардита на фоне антибактериальной терапии можно применять нестероидные противовоспалительные средства — индометацин (75—100 мг/сут). Эффективность их ниже, чем кортикостероидов, но применение при ИЭ менее опасно в отношении развития нагноительных осложнений, поэтому у некоторых больных назначение этих средств предпочтительнее.
Из препаратов иммунотерапии применяют антистафилококковую плазму в сочетании с антибактериальной терапией (5 вливаний на курс), что может обеспечить при стафилококковом ИЭ наступление стойкой ремиссии, которую иногда не удается получить при применении одних антибиотиков. В ряде случаев эффективны сеансы плазмафереза, во время которых удаляются из крови различные иммунные комплексы.
В случае необходимости назначают симптоматическое лечение: при сердечной недостаточности — мочегонные средства и ингибиторы АПФ; при тромбоэмболии — фибринолитики и антикоагулянты, хирургическое удаление эмбола; при анемии — препараты железа, при кахексии — анаболические стероиды; при повышении артериального давления (АД) — анти-гипертензивные препараты и т.д.
В последние годы проводится хирургическое лечение ИЭ, показаниями к которому являются:
• рефрактерная сердечная недостаточность в сочетании с ИЭ, устойчивым к антибиотикотерапии;
• инфицирование протезов клапанов;
• большие вегетации на клапанах;
• полная резистентность к терапии;
• абсцессы миокарда;
• разрыв хорд или папиллярных мышц.
Операция заключается в замене пораженного клапана протезом (при
непрерывной антибиотикотерапии). Летальность при неотложной замене аортального клапана довольно высока (около 30 %), тогда как при плановой операции она значительно ниже (9 %).
ПС
Исходы и эволюция ИЭ. Ближайшие исходы: 1) полное выздоровление (с формированием порока сердца или, что более редко, без него); 7) смерть на ранних этапах болезни от прогрессирования инфекции (10 %); х) летальные эмболии (10—20 %); 4) переход в хроническое течение, возможны рецидивы болезни. При этом различают ранние и поздние рецидивы Наиболее опасны ранние рецидивы, возникающие в течение первых ?Z-3 мес (отмечаются в 10—15 % случаев); поздние рецидивы возникают в более продолжительные сроки, обычно после ремиссии патологического
процесса.
Отдаленные исходы: 1) смерть при прогрессировании сердечной недостаточности (60—65 %); 2) формирование хронического нефрита и смерть от прогрессирующей почечной недостаточности (10—15 %).
Прогноз. Раннее начало лечения антибиотиками в адекватных дозах может полностью подавить воспалительный процесс. Так, выздоровление от ИЭ, вызванного зеленящим стрептококком, отмечается у 80—90 % больных. Однако при других возбудителях прогноз хуже. Так, при стафилококковом и особенно грибковом ИЭ летальность достигает 70—90 %, поэтому, если говорить об отдаленных результатах лечения, то полное выздоровление отмечается лишь у '/з больных. Прогноз при аортальной локализации ИЭ хуже, нежели при митральной. Ближайший и отдаленный прогноз при врожденных пороках лучше, чем при приобретенных.
Профилактика. У больных с пороками сердца и другими заболеваниями, которые могут осложняться ИЭ, необходима тщательная санация инфекционных очагов, раннее и энергичное лечение любой интеркуррент-ной инфекции. Следует профилактически использовать лечение антибиотиками короткими курсами у лиц с повышенным риском развития ИЭ (экстракция зубов, снятие зубных камней, тонзиллэктомия, удаление ка-
| » |
тетера после урологических операций, фиброгастроскопия, колоноскопия и пр.). Согласно международным рекомендациям (2004 г.), ниже приводится схема профилактических мер при разного рода инвазивных вмешательствах.
При манипуляциях в полости рта (зубы, миндалины, придаточные пазухи носа), фибробронхоскопии, эзофагоскопии, отсутствии аллергических реакций к пенициллину назначают внутрь амоксициллин 2 г за 1 ч до предполагаемого вмешательства; если прием внутрь по каким-либо причинам невозможен, то амоксициллин или ампициллин вводят внутривенно в Дозе 2 г за 0,5—1 ч до предполагаемого вмешательства.
При наличии аллергических реакций к пенициллину за 1 ч до инвазив-ного вмешательства назначают внутрь клиндамицин (600 мг) или азитро-мицин/кларитромицин (500 мг).
При манипуляциях в урогенитальной области или фиброгастроскопии (колоноскопии) и отсутствии аллергических реакций к пенициллину в группе больных высокого риска — ампициллин или амоксициллин 2 г внутривенно + гентамицин 1,5 мг/кг внутривенно за 0,5—1 ч до исследования или инвазивной манипуляции и через 1 ч после исследования — ампициллин или амоксициллин 2 г внутрь; в группе больных умеренного риска — ампициллин или амоксициллин 2 г внутривенно за 0,5—1 ч до исследования или инвазивного вмешательства (или амоксициллин 2 г внутрь).
При аллергических реакциях к пенициллину в группе больных высоко-
0 риска — ванкомицин 1 г более чем за 1—2 ч до процедуры + гентами-
ЦИн 1,5 мг/кг внутримышечно, а в группе больных умеренного риска —
анкомицин 1 г более чем за 1—2 ч до процедуры (без гентамицина).
1
Миокардит
МИОКАРДИТ — воспалительное поражение миокарда, вызванное инфекционными, токсическими или аллергическими воздействиями. Миокард повреждается при прямом воздействии инфекционного или токсического агента либо косвенным путем — опосредованным по механизму предварительной аллергизации или аутоиммунизации сердечной мышцы. В данном разделе рассматривается неревматический миокардит (о ревматическом миокардите см. «Ревматизм»).
Неревматический миокардит, как правило, встречается у людей молодого возраста (чаще женщин), но может поражать лиц любого возраста.
Миокардит может быть самостоятельным заболеванием или составной частью другого заболевания (например, системной склеродермии, системной красной волчанки, инфекционного эндокардита и др.).
Классификация. Классификация миокардитов, предложенная в 1982 г. Н.Р. Палеевым и соавт., представлена в несколько сокращенном и упрощенном виде.
Инфекционные, инфекционно-токсические миокардиты.
1. Вирусные.
2. Бактериальные.
3. Спирохетозные.
4. Риккетсиозные.
5. Паразитарные.
6. Грибковые. Аллергические миокардиты.
1. Инфекционно-аллергический.
2. Идиопатический (Абрамова—Фидлера).
3. Лекарственный.
4. Нутритивный.
5. При аллергозах.
6. Ожоговый.
7. Сывороточный.
8. Трансплантационный.
По течению принято выделять три варианта миокардита.
• Острый: острое начало, выраженные клинические проявления, повышение температуры тела, выраженные изменения лабораторных (острофазовых) показателей.
• Подострый: постепенное начало, затяжное течение, меньшая степень выраженности острофазовых показателей.
• Хронический: длительное течение, чередование обострений и ремиссий.
По тяжести течения выделяют три варианта.
• Легкий (слабо выраженный, протекающий с минимальными симптомами).
• Средней тяжести (умеренно выраженный, симптоматика более отчетливая, возможны нерезко выраженные признаки сердечной недостаточности).
• Тяжелый (ярко выраженный с признаками сердечной недостаточности).
Этиология. Из представленной классификации вытекает чрезвычайное разнообразие факторов, приводящих к развитию миокардита. Наиболее часто причиной миокардита является инфекция, в особенности вирусы (до 50 %).
1
Патогенез. Различные этиологические факторы вызывают повреждение миокарда и высвобождение («демаскирование» или обнажение) его антигенов. Иммунокомпетентная система обусловливает выработку противомио-рДИальных антител, которые участвуют в образовании иммунных комплексов, что способствует дальнейшему повреждению миокарда. Наряду с этим развивается иммунная реакция замедленного типа, в результате которой Т-лимфоциты становятся «агрессивными» в отношении миокардиаль-ной ткани. Миокард, таким образом, повреждается несколькими путями.
1. Прямое миокардиоцитолитическое действие вследствие миокарди-альной инвазии и репликации возбудителя.
2. Клеточное повреждение циркулирующими токсинами.
3. Неспецифическое клеточное повреждение вследствие генерализованного воспаления.
4. Клеточное повреждение вследствие продукции специфическими
клетками или гуморальной иммунной системой факторов в ответ на воз
действующий агент.
Эти пути находят свое отражение в сроках развития миокардита — в раннем или же в более отдаленном периоде инфекционного заболевания
(схема 10).
Клиническая картина. Проявления миокардита определяются следующими факторами: 1) временной связью симптомов болезни с воздействием этиологических факторов; 2) выраженностью морфологических изменений (степень распространенности повреждения миокарда воспалительным процессом).
Дата: 2018-12-28, просмотров: 373.