Течении
| Симптомы | Бронхитическая форма | Эмфизематозная форма |
| Соотношение основных симптомов Обструкция бронхов Гиперинфляция* легких Цвет кожи и видимых слизистых оболочек Кашель Изменения на рентгенограмме Легочное сердце Полицитемия, эритроци- тоз Кахексия Масса тела больного Функциональные нарушения Нарушения газообмена Смерть | Кашель > одышки Выражена Слабо выражена Диффузный синий С гиперсекрецией мокроты Диффузный пневмоскле-роз В среднем и пожилом возрасте; более ранняя декомпенсация Часто выражена, вязкость крови повышена Нехарактерна Тучные больные Признаки прогрессирующей ДН и ЗСН РаО2<60, РаС02>45 В среднем возрасте | Одышка > кашля Выражена Сильно выражена Розово-серый Малопродуктивный Эмфизема легких В пожилом возрасте, более поздняя декомпенсация Нехарактерны Часто имеется Снижение Уменьшение DLCO. Преобладание ДН РаО2<60, РаС02<45 В пожилом возрасте |
* Гиперинфляция — повышенная воздушность, выявляемая при рентгенографии.
Примечание. ДН — дыхательная недостаточность; ЗСН — застойная сердечная недостаточность; DLCO — диффузионная способность легких по СО; Ра02 и Расо2 — парциальное напряжение газа в артериальной крови.
Оценивают следующие основные показатели: форсированный выдох за первую секунду (ОФВ,); форсированную жизненную емкость легких (ФЖЕЛ); отношение ОФВ,/ФЖЕЛ (модифицированный индекс Тиффно).
Наиболее важным параметром в диагностике ограничения воздушного потока является отношение ОФВ,/ФЖЕЛ. Этот показатель является определяющим, и его значение при всех степенях тяжести ХОБЛ всегда ниже 70 %, даже при сохранении ОФВ] > 80 % от должной величины (легкое течение ХОБЛ). Величина ОФВ, в постбронходилатационной пробе отражает степень тяжести заболевания.
Обструкция считается хронической, если она регистрируется как минимум 3 раза в течение одного года, несмотря на проводимую терапию.
Пикфлоуметрия [определение объема пиковой скорости выдоха (ПСВ)] — самый простой и быстровыполнимый метод оценки состояния бронхиальной проходимости, но имеющий низкую чувствительность и специфичность при ХОБЛ. Пикфлоуметрия может быть использована для оценки эффективности проводимой терапии. Ее проведение также показано для исключения бронхиальной астмы, при которой отмечается высокая вариабельность значений ПСВ: более 20 %, в случае если диагноз остается до конца не ясным. Кроме того, пикфлоуметрию можно использовать как скри-нинговый метод для выявления группы риска развития ХОБЛ и установле-
£1
ния негативного влияния различных поллютантов. При ХОБЛ определение ПСВ является методом контроля в период обострения заболевания.
Бронходилатационный тест проводится при первичном обследовании, а также при динамическом наблюдении. Тест проводится с короткодействующими ингаляционными бронхолитиками: (32-агонистами и М-холино-литиками. После назначения этих препаратов оценивается изменение величины ОФВ,. Бронхиальная обструкция считается обратимой, если прирост ОФВ, > 15 % от должного.
Рентгенологическое исследование органов грудной клетки. При легкой степени ХОБЛ существенные рентгенологические изменения, как правило, не обнаруживаются.
Первичное рентгенологическое обследование органов грудной клетки помогает исключить другие заболевания (рак легких, туберкулез и др.), сопровождающиеся аналогичными с ХОБЛ клиническими симптомами. При установленном диагнозе ХОБЛ в период обострения заболевания рентгенография органов грудной клетки позволяет исключить пневмонию, спонтанный пневмоторакс, плевральный выпот и др. При развитии легочного сердца выявляются «выбухание» ствола легочной артерии на левом контуре тени сердца, расширение прикорневых артерий с последующим конусообразным их сужением и уменьшением диаметра периферических разветвлений. Рентгенография органов грудной клетки помогает выявить эмфизему, однако более уточненную ее характеристику может дать только компьютерная томография, особенно высокого разрешения, которая имеет более высокую чувствительность и специфичность для диагностики эмфиземы. Компьютерная томография может идентифицировать специфический анатомический тип эмфиземы (панацинарный, центриацинарный или пара-септальный) и выявить ее в тех случаях, когда при обычном рентгенологическом обследовании она не выявляется.
При бронхитическом варианте ХОБЛ благодаря компьютерной томографии можно диагностировать бронхоэктазы и четко установить их локализацию.
Бронхоскопия позволяет оценить состояние слизистой оболочки бронхов, а также помогает в дифференциальной диагностике ХОБЛ с другими брон-хообструктивными заболеваниями, в первую очередь — с раком бронхов.
Электрокардиография обнаруживает признаки гипертрофии правых отделов сердца, выявляет нарушения ритма и проводимости; при появлении иных изменений позволяет выявить кардиальный генез респираторной симптоматики.
Эхокардиография помогает оценить и выявить признаки легочной ги-пертензии, дисфункции правых (а при наличии изменений — и левых) отделов сердца и определить степень выраженности легочной гипертензии.
Особое место в диагностических исследованиях у больных с ХОБЛ отводится пробе с физической нагрузкой. Она проводится в следующих случаях: когда выраженность одышки не соответствует снижению значений ОФВ,, для контроля за эффективностью проводимой терапии и для отбора больных на реабилитационные программы. Предпочтение отдается выполнению теста с шестиминутной ходьбой. Этот метод является наиболее простым средством для индивидуального наблюдения и мониторирования течения заболевания и может быть выполнен в условиях амбулаторной практики.
Лабораторные исследования помогают оценить активность воспалительного процесса и уточнить степень дыхательной недостаточности.
В клиническом анализе крови при обострении заболевания обычно выявляют нейтрофильный лейкоцитоз с палочкоядерным сдвигом и увеличение
£0
9 q развитием гипоксемии формируется полицитемический синдром: ^и тщается число эритроцитов, растет уровень НЬ, снижается СОЭ, повы-П°Бтся гематокрит > 47 % у женщин и > 52 % у мужчин, повышается вяз-шае крови. Обнаруженная анемия может быть причиной одышки на ран-К° х стадиях ХОБЛ или фактором, усиливающим ее на более поздних ста-
пиях заболевания.
У больных с дефицитом 0ц -антитрипсина обнаруживается отсутствие -глобулинового пика при электрофорезе белков сыворотки крови. а'~ Исследование мокроты (цитологический анализ) дает информацию о характере воспалительного процесса и его выраженности, а также позволяет выявить атипичные клетки (учитывая пожилой возраст большинства больных ХОБЛ, всегда должна быть онкологическая настороженность). Окраска по Граму дает возможность для ориентировочного выявления групповой принадлежности (грамположительной, грамотрицательной) возбудителя. Более детальную информацию о характере возбудителя получают по результатам посева мокроты.
Пулъс-оксиметрия позволяет измерить и мониторировать насыщение крови кислородом (Sa02), однако дает возможность регистрировать лишь уровень оксигенации и не позволяет следить за изменениями РаС02. Если показатель Sa02 составляет менее 94 %, необходимо исследование газов крови. Оно проводится пациентам при нарастании одышки, снижении значений ОФВ, менее 50 % от должного или появлении клинических признаков дыхательной недостаточности или недостаточности правых отделов сердца. Ра02 < 8 кПа (60 мм рт. ст.) или Sat02 менее 90 % в сочетании (или без) РаС02 > 6 кПа (45 мм рт. ст.) является объективным критерием дыхательной недостаточности.
Осложнения: острая или хроническая дыхательная недостаточность, вторичная полицитемия, хроническое легочное сердце, застойная сердечная недостаточность, пневмония, спонтанный пневмоторакс, пневмоме-диастинум.
Диагностика. ХОБЛ можно предполагать у каждого человека, у которого имеются кашель, избыточная продукция мокроты и/или одышка при условии существования в анамнезе факторов риска развития болезни (курение и табачный дым, промышленная пыль и химикаты, дым домашних отопительных приборов и гарь от приготовления пищи). При клиническом обследовании определяются удлиненная фаза выдоха в дыхательном цикле, при перкуссии над легкими — легочный звук с коробочным оттенком, при аускультации легких — ослабленное везикулярное дыхание или жесткое, рассеянные сухие хрипы. Приведенные признаки не являются диагностически значимыми в отдельности, но наличие нескольких из них повышает вероятность заболевания.
В установлении диагноза ХОБЛ наиболее важными и определяю-ОсТшИ являются результаты ФВД. Обязательный признак — снижение иФВ,/ФЖЕЛ < 70 %. Этот показатель постоянен для всех стадий заболевания и служит наиболее ранним признаком ограничения скорости воздушного потока даже при сохранении ОФВ! > 80 %. В процессе обследования ольного необходимо исключить другие заболевания — бронхиальную аст-Щ, недостаточность левого желудочка (отек легкого), ТЭЛА, обструкцию рхних дыхательных путей, рак легкого, туберкулез, пневмоторакс, прояв-J ЯЮшиеся бронхообструктивным синдромом.
д 1аким образом, диагностика ХОБЛ осуществляется на основании слегла11111* данных: 1) наличия факторов риска; 2) клинических признаков,
вными из которых являются кашель и экспираторная одышка; 3) неук-
63
лонно прогрессирующего нарушения бронхиальной проходимости по данным ФВД; 4) исключения других заболеваний, которые могут привести к появлению аналогичных ХОБЛ симптомов.
Формулировка развернутого клинического диагноза ХОБЛ включает тя жесть течения заболевания: легкое (I стадия), среднетяжелое (II стадия), тяжелое (III стадия) и крайне тяжелое (IV стадия); фазу процесса — обострение или ремиссия; наличие осложнений (дыхательная недостаточность, легочное сердце, недостаточность кровообращения). При тяжелом течении заболевания рекомендуется указывать клиническую форму ХОБЛ (эмфизематозная, бронхитическая, смешанная).
Лечение. Направлено на предупреждение прогрессирования болезни, повышение толерантности к физическим нагрузкам, уменьшение симптоматики, улучшение качества жизни, профилактику и лечение обострений и осложнений.
Первый и самый важный шаг в программе лечения ХОБЛ — снижение влияния факторов риска и в первую очередь — прекращение курения. Это единственный и пока наиболее эффективный метод, позволяющий уменьшить риск развития и прогрессирования ХОБЛ. Разработаны специальные программы лечения табачной зависимости.
Выбор терапии зависит от степени тяжести (стадии) заболевания и его фазы (стабильное состояние или обострение), а также наличия или отсутствия осложнений.
Главное место в комплексной терапии больных ХОБЛ занимают брон-холитические препараты. Показано, что все виды бронхолитиков повышают толерантность к физической нагрузке даже при отсутствии изменений ОФВ,. Предпочтение отдается ингаляционной терапии.
Лечение ХОБЛ при стабильном состоянии. При легком течении ХОБЛ применяют ингаляционные бронходилататоры короткого действия «по требованию» (р2-агонисты и м-холинолитики). Ипратропия бромид (атровент) назначают по 40 мкг (2 дозы) 4 раза в день, сальбутамол (вентолин) по 100—200 мкг до 4 раз в сутки, фенотерол (беротек) по 100—200 мкг до 4 раз в сутки. При применении короткодействующих бронходилататоров предпочтение отдается их бесфреоновой форме. М-холинолитические препараты являются препаратами первого ряда в лечении ХОБЛ, их назначение обязательно при всех степенях тяжести болезни. При среднетяжелом, тяжелом и крайне тяжелом течении приоритетным является длительное и регулярное лечение бронхолитиками. Преимущество отдается бронхолити-кам длительного действия: тиотропия бромид (спирива) 1 раз в сутки по 18 мкг через хендихалер, сальмотерол по 25—50 мкг 2 раза в сутки, формо-терол (оксис) по 4,5—9 мкг 2 раза в сутки, формотерол (форадил) по 12 мкг 2 раза в сутки.
У больных с тяжелым и крайне тяжелым течением ХОБЛ бронходила-тационная терапия осуществляется специальными растворами (атровент, беротек, беродуал) через небулайзер. Небулайзерная терапия предпочтительнее, как и применение дозированного аэрозоля со спейсером у пожилых людей и больных с ментальными нарушениями.
Из препаратов ксантинового ряда применяют только пролонгированные теофиллины (теопек, теотард и т.п.), но с учетом их потенциальной токсичности они могут быть только препаратами «второй линии».
У пациентов с ОФВ, < 50 % от должной величины (тяжелая и крайне тяжелая стадии ХОБЛ) и повторяющимися обострениями (3 раза и более за последние 3 года) наряду с бронходилатационной терапией применяют ингаляционные глюкокортикостероиды (ИГКС) [производные беклометазо-
64
м — беклазон (так называемое легкое дыхание), производные (pn7in>»»-на — фликсотид, производные будесонида — пульмикорт, бенакорт]. Наиболее эффективна комбинация ИГКС с (32-агонистами длительного действия (сальметерол/флутиказон — серетид и формотерол/будесонид — симбикорт).
Муколитики (мукорегуляторы, мукокинетики) показаны очень ограниченному контингенту больных стабильной ХОБЛ и применяются при наличии вязкой мокроты; они существенно не влияют на течение заболевания.
Для профилактики обострения ХОБЛ перспективно длительное применение муколитика N-ацетилцистеина (флуимуцила), обладающего одновременно и антиоксидантной активностью.
Антибактериальные препараты для профилактики обострения ХОБЛ использовать не рекомендуется. С этой целью показана ежегодная вакцинация во время эпидемических вспышек гриппа (однократно в октябре _ первой половине ноября).
Помимо лекарственных средств, при стабильном течении ХОБЛ применяется немедикаментозное лечение. Больным с хронической дыхательной недостаточностью проводят постоянную многочасовую малопоточную (> 15 ч в сутки) кислородотерапию, которая пока остается единственным методом, способным снизить летальность при крайне тяжелой стадии ХОБЛ. На всех стадиях течения процесса высокой эффективностью обладают физические тренирующие программы, повышающие толерантность к физической нагрузке и уменьшающие одышку и усталость.
В последние годы стали применяться хирургические методы лечения, в первую очередь — буллэктомия, которая приводит к снижению одышки и улучшению легочной функции. Однако оперативная коррекция легочного объема, достигаемая буллэктомией, считается паллиативной хирургической
процедурой.
Лечение обострения заболевания. В связи с тем что все обострения ХОБЛ следует рассматривать как фактор прогрессирования, терапия должна быть более интенсивной. В первую очередь это относится к бронхоли-тической терапии. При лечении обострения увеличивают дозы препаратов и модифицируют способы их применения. Предпочтение отдают небулай-зерной терапии. В зависимости от тяжести течения и тяжести обострения ХОБЛ лечение можно проводить как в амбулаторных условиях (легкое или среднетяжелое обострение у больных с легким течением ХОБЛ) или в стационарных условиях.
Для купирования обострения наряду с бронхолитической терапией применяют антибиотики, глюкокортикостероиды (ГКС), а в условиях стационара — контролируемую оксигенотерапию и неинвазивную вентиляцию
легких.
При обострении ХОБЛ, сопровождающемся снижением ОФВ, < 50 % должного, отдают предпочтение системным ГКС: по 30—40 мг преднизоло-на на протяжении 10—14 дней. В дальнейшем при достижении клинического эффекта переводят больных на ингаляционное введение ГКС.
При усилении одышки, увеличении количества мокроты и ее гнойном характере назначают антибактериальную терапию. В большинстве случаев обострения ХОБЛ антибиотики можно назначать внутрь. Продолжительность антибактериальной терапии — от 7 до 14 дней. При неосложненном обострении препаратом выбора является амоксициллин (в качестве альтернативы можно использовать респираторные фторхинолоны или амокси-Циллин/клавуланат, а также «новые» макролиды — азитромицин, кларитро-мицин). При осложненных обострениях препаратами выбора являются респираторные фторхинолоны (левофлоксацин, моксифлоксацин) или це-
65
фалоспорины II—III поколения, в том числе с антисинегнойной активностью.
Показанием для парентерального введения антибиотиков являются тяжелое обострение; нахождение больного на ИВЛ; отсутствие формы антибиотика для приема внутрь; нарушения со стороны желудочно-кишечного тракта.
Для лечения тяжелого инфекционного обострения ХОБЛ показано применение через небулайзер раствора, содержащего муколитик (N-аце-тилцистеин) и антибиотик (тиамфеникол глицинат) — препарат флуиму-цил — антибиотик ИТ.
Обязательным методом лечения ХОБЛ при обострении является окси-генотерапия. При неосложненных обострениях быстро достигается адекватный уровень оксигенации — Ра02 > 8 кПа (> 60 мм рт. ст.) или С02 > 90 %. После начала оксигенотерапии через назальные катетеры (скорость потока — от 1 до 2 л/мин) или маску Вентури (содержание кислорода во вдыхаемой кислородно-воздушной смеси — от 24 до 28 %) газовый состав крови должен контролироваться через 30—45 мин (адекватность оксигенации, исключение ацидоза, гиперкапнии).
При отсутствии эффекта после 30—45 мин ингаляции кислорода необходимо решать вопрос о применении неинвазивной вентиляции легких с положительным давлением. Если у больного с тяжелым обострением ХОБЛ неинвазивная вентиляция легких оказывается неэффективной (или недоступной), проводят инвазивную вентиляцию легких.
Прогноз. Прогноз в отношении выздоровления неблагоприятен. Болезнь характеризуется неуклонно прогрессирующим течением, приводящим к инвалидизации. Для оценки прогноза определяющую роль играют следующие параметры: возможность устранения провоцирующих факторов, приверженность больного к лечению, социально-экономические условия. Неблагоприятные прогностические признаки: тяжелые сопутствующие заболевания, сердечная и дыхательная недостаточность, пожилой возраст больных.
Применение длительно действующего холинолитика (тиотропия бромида) и комбинации ИГКС с длительно действующими (32-агонистами открывает перспективу для улучшения прогноза заболевания.
Профилактика. Главное условие для профилактики — ранняя диагностика заболевания, а также устранение факторов риска. Особое место занимают отказ от курения и профилактика инфекционных заболеваний дыхательных путей.
Бронхиальная астма
БРОНХИАЛЬНАЯ АСТМА (БА) — «хроническое заболевание, основой которого является воспалительный процесс в дыхательных путях с участием разнообразных клеточных элементов, включая тучные клетки, эозинофилы и Т-лимфоциты. У предрасположенных лиц этот процесс приводит к развитию генерализованной бронхиальной обструкции разной степени выраженности, полностью или частично обратимой спонтанно или под влиянием лечения. Воспалительный процесс вызывает также содружественное усиление ответа дыхательных путей в виде бронхиальной обструкции на различные внешние и внутренние стимулы» (определение экспертов ВОЗ, 1993).
Данное определения БА (в отличие от предшествующих) стало возможным в связи с тем, что за последние 10 лет существенно изменилось пред-
ставление о существе БА, ее этиологии, патогенезе, клинике, лечении и
профилактике.
В основе БА (независимо от степени ее тяжести) лежит хронический неинфекционный воспалительный процесс в дыхательных путях. Гиперактивность бронхов, изменяющаяся со временем бронхиальная обструкция и связанные с ними клинические симптомы болезни являются следствием персистирующего воспаления в бронхах.
Этиология. БА является часто встречающимся заболеванием (распространенность БА колеблется от 3 до 8 %).
В возникновении БА имеет значение наследственная предрасположенность. Выявлена связь некоторых антигенов гистосовместимости (HLA) с тяжестью течения БА; нарастание тяжести заболевания особенно часто отмечается у носителей антигенов А2, В7, В12, В13, В27, В35, DR2, DR5 и их
комбинации.
В развитии болезни играют роль внутренние и внешние факторы. Внутренние факторы —это биологические дефекты иммунной, эндокринной систем, вегетативной нервной системы, чувствительности и реактивности бронхов, мукоцилиарного клиренса, эндотелия сосудов легких, «системы быстрого реагирования» (тучные клетки и др.), метаболизма арахидоновой кислоты и т.д.
Внешние факторы, способствующие клинической реализации биологических дефектов, включают: 1) аллергены (пыльцевые, пылевые, пищевые, лекарственные, производственные, аллергены клещей, насекомых, животных и пр.); 2) инфекцию (вирусы, грибы; некоторые виды бактерий); 3) механические и химические раздражители (металлическая, древесная, силикатная, хлопковая пыль; пары кислот, щелочей; дымы и пр.); 4) метеорологические и физико-химические факторы (изменение температуры и влажности воздуха, колебания барометрического давления, магнитного поля земли, физические усилия и пр.); 5) стрессовые нервно-психические воздействия и физическую нагрузку; 6) фармакологические воздействия ф-адре-ноблокаторы, нестероидные противовоспалительные препараты и т.д.).
Инфекционные агенты, помимо их аллергизирующего действия, могут также: а) снижать порог чувствительности организма к неинфекционным (атопическим) аллергенам, повышать проницаемость для них слизистой оболочки дыхательных путей; б) формировать неиммунологическим путем изменение реактивности клеток-мишеней (тучные клетки, базофилы, моноциты и др.) и эффекторных систем. Известно, что некоторые вирусы и бактерии оказывают р-адреноблокирующее действие и способны воздействовать на эфферентные зоны вагусного бронхоконстриктивного механизма. Как правило, при БА у одного и того же больного можно заподозрить или выявить сочетание нескольких этиологических факторов. Вместе с тем важнейшим идентифицируемым предрасполагающим фактором развития БА является атопия, т.е. выработка избыточного количества антител IgE как реакция на воздействие аллергенов окружающей среды.
При продолжительном течении болезни большее значение приобретают различные неспецифические раздражения и психогенные факторы. Первоначально вызвавший БА аллерген может со временем утратить свое значение, исчезнув из зоны окружения больного, сами же обострения болезни обусловливаются иными причинами.
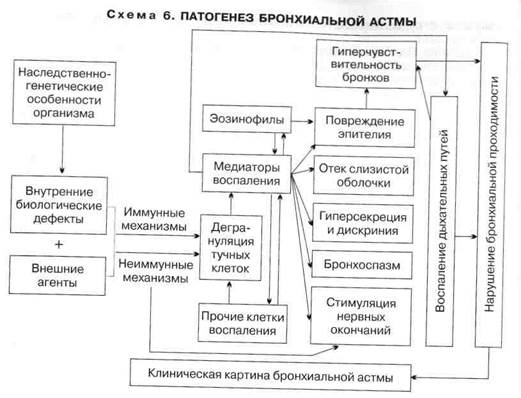
Патогенез. Центральным звеном патогенеза БА является неинфекционный воспалительный процесс в бронхах, который вызывается воздействием различных воспалительных клеток и выделяемых ими биологически активных веществ — медиаторов. В свою очередь воспаление бронхов ведет к
67
|
|
развитию их гиперчувствительности и гиперреактивности, предрасполагая таким образом бронхиальное дерево к сужению в ответ на различные стимулы (схема 6).
Иммунные механизмы. В подавляющем большинстве случаев БА является аллергической болезнью, поэтому главным механизмом формирования патологического процесса является иммунный. У значительной части больных БА нарушения иммунокомпетентной системы протекают по I, III и IV типам реакций гиперчувствительности (согласно классификации R. Coombs и P.Gell). Развитие реакций II типа (цитотоксического) при БА пока не описано.
Чаще других главную роль играют механизмы гиперчувствительности I типа (анафилактического, или атопического). К этому типу аллергии относят немедленные реакции, развивающиеся вследствие взаимодействия аллергена (антигена) со специфическим IgE. Реакция антигена с IgE происходит преимущественно на поверхности субмукозных тучных клеток дыхательных путей и циркулирующих в крови базофилов. В результате наблюдается их дегрануляция с высвобождением биологически активных молекул, среди которых преобладают медиаторы воспаления. Уже через несколько секунд после реакции дегрануляции клетки секретируют ранее синтезированные вазоактивные амины: гистамин, серотонин. Более отдаленным последствием активизации тучных клеток является запуск продукции метаболитов арахидоновой кислоты (простагландинов, лейкотриенов), тромбоксанов и цитокинов, которые участвуют в поддержании воспалительной реакции в тканях (интерлейкины 3, 4, 5, 8; нейтрофильный хемо-68
таксический фактор, фактор агрегации тромбоцитов, гранулоцитарно-мак-рофагальный колониестимулируюший фактор и др.).
Секретируемые тучными клетками медиаторы и цитокины вызывают интенсивный приток эозинофилов и других клеток воспаления (грануло-цитов, моноцитов, Т-лимфоцитов) к месту проникновения аллергена. Через 6—12 ч развивается поздняя стадия аллергической реакции, при которой доминирует клеточная инфильтрация. Эозинофил рассматривается как «ключевая» клетка в повреждении эпителия дыхательных путей вследствие продукции и секреции им эозинофильного катионного белка, а также выделения фактора активации тромбоцитов и так называемого большого основного протеина. В свою очередь повреждение эпителия бронхов эозино-фильным «большим основным протеином» приводит к развитию неспецифической гиперреактивности и гиперчувствительности.
Медиаторы тучных клеток привлекают в зону воспаления нейтрофилы и способствуют выделению ими активных форм кислорода. Активированные нейтрофилы в свою очередь стимулируют дегрануляцию тучных клеток, что замыкает «порочный круг».
В развитии хронического воспаления в бронхах велика роль лимфоцитов, выделяющих интерлейкины с последующей активацией тучных клеток и эозинофилов. Кроме того, вещества, обладающие мощным бронхоспа-стическим действием и потенцирующие воспаление, вырабатываются макрофагами и моноцитами.
Под влиянием всех вышеописанных изменений повышается проницаемость микроциркуляторного русла, развиваются отек, гипер- и дискриния, бронхоспазм и прочие проявления неинфекционного воспаления дыхательных путей. Клинически это выражается острым нарушением проходимости бронхов и развитием приступа БА.
В возникновении реакции I типа большая роль отводится избыточному синтезу реагинов, дефициту секреторного IgA и, главное, снижению Т-су-прессорной функции лимфоцитов.
Реакция III типа (иммунокомплексный тип, или феномен Артюса) происходит в зоне избытка антигена с участием преципитирующих антител. Реакция развивается под воздействием экзоаллергенов (микроорганизмы, ферменты, пыль, антибиотики и др.) и эндоаллергенов (инфекционное и/или аллергическое воспаление, различные раздражители и другие факторы могут приводить к денатурации белков бронхиол и альвеол с последующим формированием эндоаллергенов — аутоаллергенов).
При иммунокомплексных реакциях III типа образуются антитела, принадлежащие преимущественно к иммуноглобулинам классов G и М. Повреждающее действие образованного комплекса антиген—антитело реализуется главным образом через активацию комплемента, освобождение ли-зосомных ферментов. Происходят повреждение базальных мембран, спазм гладких мышц бронхов, расширение сосудов, повышается проницаемость микроциркуляторного русла.
Тип IV (клеточный), при котором повреждающее действие оказывают сенсибилизированные лимфоциты, относится к гиперчувствительности замедленного типа (ГЗТ).
Основными медиаторами аллергической реакции IV типа являются интерлейкины — лимфокины (действующие на макрофаги, эпителиальные клетки) и лизосомные ферменты; не исключена роль активации кинино-вой системы. Под влиянием этих веществ происходят развитие отека, набухание слизистой оболочки, бронхоспазм, гиперпродукция вязкого бронхиального секрета. Выделяющиеся лимфоцитами интерлейкины спо-
собствуют также привлечению к месту аллергической реакции других клеток воспаления с развитием персистирующей воспалительной реакции. Все это приводит к длительному нарушению бронхиальной проходимости.
В патогенезе БА определенная роль принадлежит местной «поломке» иммунной защиты: отмечается уменьшение секреторного IgA, нарушается система фагоцитоза, которая в органах дыхания обеспечивается в основном альвеолярными макрофагами. При нарушении их функции (воздействие лимфокинов и др.) резко снижается противовирусная защита организма (вследствие снижения продукции интерферона). Воспаление приобретает персистирующий характер.
В целом основные этапы развития аллергической реакции включают:
• нарушение соотношения субпопуляций лимфоцитов (Th,—ТЬ2-кле-ток), приводящее к поляризации ТЪ2-клеток;
• синтез Th-клетками цитокинов (интерлейкины IL-4, IL-5, IL-10);
• стимулирование интерлейкинами внутриклеточной продукции IgE, индукция под их влиянием активности и пролиферации эозинофилов и созревания тучных клеток;
• вовлечение в аллергическую реакцию других клеток (базофилы, макрофаги, эпителиальные клетки, фибробласты);
• высвобождение активированными клетками провоспалительных медиаторов: гистамина, цистеиниловых лейкотриенов, эйкозаноидов, активных форм кислорода и др.;
• высвобождение нейротрансмиттеров и активация афферентных нервов.
Воспалительный процесс, возникший в результате аллергической реакции, приводит к целому ряду патоморфологических изменений:
• спазму гладких мышц (острая бронхоконстрикция);
• гипертрофии слизистых желез, гиперсекреции слизи и образованию слизистых пробок в просвете бронхов;
• отеку слизистой оболочки, ее инфильтрации активированными клетками;
• дилатации и пролиферации сосудов, повышению их проницаемости;
• перестройке (ремоделированию) морфологических структур легочной ткани: гибели эпителиального покрова, утолщению стенок бронхов, изменению размеров базальной мембраны, васкуляризации слизистых оболочек дыхательных путей.
Неиммунные механизмы. Известно, что, помимо антигензави-симой дегрануляции тучных клеток, существует большое количество неспецифических факторов (токсины, ферменты, лекарства, различные макромолекулы и др.), вызывающих дегрануляцию тучных клеток неиммунным путем. Различные физические, механические и химические раздражители (например, дым, двуокись серы, пыль, холодный воздух и др.), инфекционные агенты (без сенсибилизации и аллергизации) провоцируют рефлекторный бронхоспазм путем стимуляции рецепторов в дыхательных путях. Ранее считалось, что такая реакция осуществляется путем повышенной активности парасимпатической нервной системы. Однако в настоящее время этот механизм не считается основным. Обнаружена распространенная сеть нервных волокон неадренергической нехолинергической регуляции бронхов, содержащих мощные нейропептиды (нейрокин А и В, субстанцию Р, вазоактивный интестинальный пептид и др.), которые имеют отношение к развитию большинства признаков обострения бронхиальной астмы.
Предполагают участие глюкокортикостероидной (ГКС) недостаточности, дизовариальных расстройств (гиперэстрогенемия и гипопрогестероне-
мия) и нервно-психических нарушений в формировании «нестабильного метаболизма» тучных клеток.
Недостаточность ГКС способствует развитию гиперреактивности тучных клеток, снижению синтеза катехоламинов, активации простагландинов F2 и др., а также нарушению иммунокомпетентной системы (комплексное участие в патогенезе БА и иммунологических и неиммунологических механизмов).
Гиперэстрогенемия и гипопрогестеронемия воздействуют главным образом на а- и р-адренорецепторы, повышая активность а-рецепторов и снижая активность р-рецепторов.
При нарушении бронхиальной проходимости, обусловленной любыми другими механизмами, также отмечается адренергический дисбаланс, выражающийся в преобладании системы гуанилатциклазы над системой аде-нилатциклазы. Кроме того, изменяется содержание внутриклеточного фермента фосфодиэстеразы, усиливается поступление ионов кальция в клетку, нарушается обмен простагландинов.
Преобладание того или иного механизма в патогенезе БА позволяет выделить ее различные патогенетические варианты [Федосеев Г.Б., 1982; Чу-чалин А.Г., 1985].
Классификация. Единой классификации БА до настоящего времени не существует. В 1982 г. Г.Б. Федосеев предложил классификацию, подчеркивающую многообразие патогенетических механизмов в развитии БА. Она не отменяет классификацию, разработанную А.Д. Адо и П.К. Булатовым (1969), но развивает ее с учетом результатов новых исследований.
Классификация бронхиальной астмы [по Федосееву Г.Б., 1982]:
• Этапы развития БА: 1) состояние предастмы, 2) клинически оформ
ленная БА.
К предастме относят все состояния, представляющие угрозу возникновения БА (острый и хронический бронхит, а также пневмония с элементами бронхоспазма в сочетании с вазомоторным ринитом, крапивницей и другими состояниями, при которых выявляются эозинофилия крови и увеличенное содержание эозинофилов в мокроте). После первого приступа или сразу возникшего астматического статуса БА считается клинически оформленной.
• Формы БА: 1) иммунологическая; 2) неиммунологическая (в формулировку клинического диагноза не включается).
• Патогенетические механизмы (клинико-патогенетические варианты) БА: 1) атопический; 2) инфекционно-зависимый; 3) аутоиммунный; 4) дис-гормональный; 5) нервно-психический дисбаланс; 6) адренергический дисбаланс; 7) первично измененная реактивность бронхов.
Разделение БА по патогенетическим механизмам и выделение основного из них представляют трудную и часто неразрешимую задачу, особенно Для врачей поликлиник. Однако во всех случаях такая попытка оправдана, так как каждый из патогенетических механизмов предполагает определенный, свойственный только ему характер лекарственной терапии.
У одного больного возможно сочетание нескольких клинико-патогене-тических вариантов. В такой ситуации необходимо на момент обследования выделить основной для данного больного, так как это важно для проведения адекватной терапии. В процессе длительного течения БА возможна смена патогенетического механизма.
• Тяжесть течения БА: 1) легкое течение; 2) течение средней тя
жести; 3) тяжелое течение.
При легком течении БА обострения не длительные, возникают 2—3 раза в год. Приступы удушья купируются, как правило, приемом различных
Классификация бронхиальной астмы по тяжести течения
бронхолитических препаратов внутрь. В межприступный период признаки бронхоспазма, как правило, не выявляются.
Среднетяжелое течение характеризуется более частыми обострениями 3—4 раза в год. Приступы удушья протекают тяжелее и купируются инъекциями лекарственных препаратов.
При тяжелом течении БА обострения возникают часто (5 раз в год и более), отличаются длительностью. Приступы тяжелые, нередко переходят в астматическое состояние.
В ряде случаев деление БА по тяжести течения бывает условным. Так, при легком течении БА больной может погибнуть от внезапно развившегося астматического статуса. В то же время возможна «спонтанная» ремиссия при довольно тяжелом течении болезни.
• Фазы течения БА: 1) обострение; 2) стихающее обострение;
3) ремиссия.
Фаза обострения характеризуется выраженными признаками заболевания, прежде всего повторно возникающими приступами БА или астматического состояния.
В фазе стихающего обострения приступы становятся более редкими и нетяжелыми. Физикальные и функциональные признаки заболевания выражены меньше, чем в фазу обострения.
В фазе ремиссии исчезают типичные проявления БА: приступы удушья не возникают; полностью или частично восстанавливается проходимость бронхов.
• Осложнения: 1) легочные: эмфизема легких, дыхательная недо
статочность, ателектаз, пневмоторакс, астматический статус и пр.; 2) вне-
легочные: легочное сердце (компенсированное и декомпенсированное с раз
витием правожелудочковой недостаточности), дистрофия миокарда и др.
Примечания к классификации:
1. Первично измененная реактивность бронхов может быть врожденной и приобретенной, проявляется приступами удушья при физической нагрузке, воздействии холодного воздуха, лекарств, инфекции и др.
2. При инфекционно-зависимом варианте БА необходимо указывать характер этой зависимости: стимуляция атопической реакции; инфекционная аллергия; формирование первично измененной реактивности бронхов. В тех случаях, когда инфекция является аллергеном, БА определяется как инфекционно-аллергическая.
Предлагаемая классификация, как и все остальные, не лишена недостатков, но более прогрессивна по сравнению с существующей. Приведенная классификация хотя и не является утвержденной, однако она позволяет более эффективно проводить патогенетическую терапию больных БА.
Экспертами ВОЗ (1993) даны новые критерии тяжести БА, определяемой выраженностью клинических симптомов, объемом форсированного выдоха за первую секунду (ОФВ,) и пиковой скоростью выдоха (ПСВ, л/мин) — наиболее значимыми показателями выраженности обструкции дыхательных путей. Оценка по этим степеням тяжести БА позволяет осуществить так называемый ступенчатый подход к лечению больных: объем терапии должен повышаться при увеличении степени тяжести болезни.
Классификация БА, основанная на степени тяжести, наиболее важна, когда нужно принять решение о выборе терапии. Кроме того, предложение экспертов ВОЗ классифицировать БА по степени тяжести базируется на том, что нередко другие рубрики приведенной выше классификации невозможно с достоверностью определить у всех больных.
• Легкая интермиттирующая (эпизодическая).
Кратковременные симптомы реже 1 раза в неделю.
Короткие обострения (от нескольких часов до нескольких дней). Ночные симптомы < 2 раз в месяц.
Отсутствие симптомов и нормальная функция внешнего дыхания между обострениями. ПСВ и ОФВ,: > 80 % от должных.
Вариабельность (суточный разброс) показателей ПСВ или ОФВ! < 20 %. . Легкая персистирующая.
Симптомы от 1 раза в неделю до 1 раза в день.
Обострения могут снижать физическую активность и нарушать сон.
Ночные симптомы > 2 раз в месяц.
ПСВ и ОФВ,: > 80 % от должных.
Вариабельность (суточный разброс) показателей ПСВ или
ОФВ! = 20-30 %.
• Среднетяжелая персистирующая.
Ежедневные симптомы.
Обострения могут приводить к ограничению физической активности
и сна.
Ночные симптомы > 1 раза в неделю.
ПСВ и ОФВ,: 60-80 % от должных.
Вариабельность (суточный разброс) показателей ПСВ или
ОФВ, > 30 %.
• Тяжелая персистирующая.
Постоянное наличие симптомов.
Частые ночные симптомы.
Ограничение физической активности из-за симптомов астмы.
ПСВ и ОФВ,: < 60 % от должных.
Вариабельность (суточный разброс) показателей ПСВ или
ОФВ, > 30 %. Клиническая картина. Наиболее характерный признак БА — приступы удушья. Однако клинический диагноз БА можно поставить с учетом оценки результатов всех трех этапов диагностического поиска, так как удушье возникает как симптом и при других заболеваниях. Кроме того, у ряда больных вместо приступа удушья БА может проявляться его эквивалентом — приступообразным надсадным кашлем, сопровождающимся острым нарушением бронхиальной проходимости. В связи с этим возникает необходимость на каждом из трех этапов диагностического поиска дифференциации БА от заболеваний, составной частью которых является бронхоспа-стический синдром с развитием приступов удушья или их эквивалентов. На I этапе диагностического поиска устанавливают: а) наличие приступов удушья (их эквивалентов), особенности и связь с определенными факторами; б) аллергический анамнез (наследственную предрасположенность, непереносимость пищевых и лекарственных веществ); в) предшествующие заболевания легких; г) влияние метеорологических факторов, физических Усилий, дизовариальных расстройств и других причин на возникновение приступов удушья; д) эффективность проводимой ранее терапии; е) течение болезни, появление осложнений.
Больные жалуются на приступы удушья (затрудненное дыхание, преимущественно на выдохе), одышку и кашель. Характер кашля может
73
быть разнообразным: чаще кашель сухой, надсадный, приступообразный или с выделением вязкой, трудноотделяемой мокроты. При развитии легочной недостаточности одышка беспокоит и в межприступный период. Повышение температуры тела может свидетельствовать об активности бронхолегочной инфекции. Затрудненное носовое дыхание, как правило, служит проявлением аллергической риносинусопатии (вазомоторный ринит, полипоз) — частого спутника или предшественника БА. При расспросе больного необходимо уточнить частоту возникновения симптомов БА в неделю, обратив особое внимание на ночные симптомы. Эти данные особенно важны для оценки тяжести течения болезни на момент обследования больного.
Данные анамнеза помогают установить связь развития приступов с воздействием определенных аллергенов и других факторов. Наиболее частой причиной развития БА является инфекция дыхательных путей, особенно при обострении болезни. Из анамнеза узнают о влиянии физического усилия (быстрая ходьба, смех и пр.), изменений метеорологических факторов (холод, повышенная влажность и др.), дизовариальных расстройств на возникновение приступов удушья. Знакомство с условиями труда помогает обнаружить профессиональную БА.
Изучение аллергологического анамнеза способствует диагностике ато-пического варианта БА. В подобных случаях можно получить сведения о поллинозе: обострения болезни имеют сезонный характер (чаще весной и летом), сопровождаются ринитом, конъюнктивитом. У таких больных бывают крапивница, отек Квинке, выявляется непереносимость пищевых продуктов, ряда лекарственных веществ, отмечается наследственная предрасположенность к аллергическим заболеваниям.
Ориентируясь на данные анамнеза, можно предположительно, а в ряде случаев и с уверенностью высказаться о так называемой аспириновой астме. Эти больные не страдают наследственной формой аллергических заболеваний. Их беспокоит нарушенное носовое дыхание (полипозные разрастания). Наиболее характерный симптом у таких больных — непереносимость нестероидных противовоспалительных препаратов (ацетилсалициловая кислота, индометацин и пр.), вызывающих астматические приступы. На этом этапе уже можно предположить простагландиновый механизм БА. Указание в анамнезе на прием ГКС свидетельствует о тяжести болезни, а эффективность приема — об иммунной форме БА или кортикостероидо-зависимом ее варианте. Отсутствие эффекта от приема ГКС, особенно у больных с тяжелым течением БА, делает предположение об аллергическом генезе БА менее достоверным и практически исключает наличие у больного глюкокортикостероидной недостаточности. ГКС неэффективны также при астме физического усилия.
Данные о развитии в прошлом астматического статуса свидетельствуют о тяжести течения заболевания и указывают на необходимость проведения терапии ГКС. Наличие предшествующих заболеваний органов дыхания (ХБ, ХП) обычно предопределяет тяжесть течения БА, отсутствие «светлых» промежутков.
БА может протекать монотонно, с постоянно нарушенным дыханием и потребностью принимать ежедневно противоастматические средства.
Другой тип течения БА характеризуется периодическими обострениями с заметно усиливающимися признаками бронхиальной обструкции и ремиссиями, когда нарушения бронхиальной проходимости резко уменьшаются или исчезают. Такое течение БА наиболее характерно для атопиче-ского варианта заболевания.
74
Значение I этапа диагностического поиска особенно велико для диагностики БА в начальном периоде заболевания, когда все проявления астмы имеют эпизодический характер, а физикальное исследование не дает достаточной информации для постановки диагноза.
На II этапе диагностического поиска в развернутой стадии болезни выявляют: а) внелегочные проявления аллергии; б) признаки бронхообструк-тивного синдрома; в) осложнения БА; г) другие заболевания, сопровождающиеся приступами бронхоспазма.
При обследовании кожных покровов иногда можно выявить изменения, характерные для аллергических проявлений: крапивницу, папулезные и эритематозные высыпания. Эти изменения могут свидетельствовать об иммунологическом варианте БА. При аллергических формах БА могут быть конъюнктивиты (особенно часто у больных поллинозами). Сочетание БА с экземой, нейродермитом, псориазом предрасполагает к тяжелому течению астмы. Грибковое поражение кожи, ногтевых лож может сопровождаться гиперчувствительностью к грибковым аллергенам.
Часто можно выявить нарушение носового дыхания. Риниты и полипоз рассматриваются как предастма. Гаймориты и другие синуситы служат очагом инфекции, который может провоцировать удушье. При физикальном обследовании легких могут быть выявлены признаки эмфиземы.
Аускультация легких помогает обнаружить признаки бронхиальной обструкции, для которой характерны удлиненный выдох и сухие, преимущественно свистящие, хрипы. Иногда при обследовании вне приступа удушья сухих хрипов может быть немного или они не прослушиваются. Форсированный выдох позволяет выявить скрытый бронхоспазм (появление или нарастание сухих хрипов).
При аускультации легких в положении больного лежа количество сухих хрипов увеличивается (при «вагусном» их механизме).
Постоянно выслушиваемые на определенном участке влажные звонкие («трескучие») мелкопузырчатые хрипы могут свидетельствовать о развившемся пневмосклерозе.
В случае астматического статуса отмечается уменьшение количества сухих хрипов при аускультации вплоть до развития «немого» легкого, несмотря на резкое нарастание удушья и одышки.
Объективное обследование больного помогает выявить симптомы других заболеваний («бабочка» на коже лица, лимфаденопатия в сочетании с увеличением печени и селезенки, стойкое повышение артериального давления, упорная лихорадка и пр.), при которых возникают приступы бронхоспазма, проявляющиеся удушьем (системная красная волчанка, узелковый периарте-риит, реже другие диффузные заболевания соединительной ткани). В таких случаях предполагаемый диагноз БА становится маловероятным. На III этапе диагностического поиска выявляют:
а) нарушение бронхиальной проходимости;
б) измененную реактивность бронхов;
в) характерные изменения при проведении аллергологического обсле
дования;
г) очаги инфекции и признаки воспаления;
д) осложнения БА.
Спирография выявляет снижение объема форсированного выдоха за первую секунду (ОФВ,), уменьшение коэффициента Тиффно (соотношения ОФВ, к ЖЕЛ в процентах) и процентного соотношения ОФВ, к ФЖЕЛ (модифицированный коэффициент Тиффно) — характерные признаки нарушения бронхиальной проходимости по обструктивному типу.
75
При обострении БА значительно возрастают (на 100 % и более превышают исходный уровень) остаточный объем легких (ООЛ) и функциональная остаточная емкость (ФОБ). Анализ спирограммы позволяет обнаружить признаки трахеобронхиальной дискинезии по наличию зазубрины в верхней части нисходящего колена спирограммы (симптом Колбета—Висса).
Пикфлоуметрия — определение пиковой объемной скорости выдоха — является непременным условием контроля за состоянием больного. Ее проводят утром (до приема лекарств) и вечером с помощью индивидуального карманного прибора — пикфлоуметра. Желательно, чтобы разброс утренних и вечерних значений ПСВ не превышал 20 %.
Пневмотахография с построением кривой «поток—объем» позволяет диагностировать нарушение бронхиальной проходимости раздельно на уровне крупных, средних и мелких бронхов по данным экспираторного потока при легочном объеме, равном 75, 50, 35 % ФЖЕЛ. Для периферической обструкции характерно значительное снижение кривой «поток—объем» на участке 50-75 % ФЖЕЛ (МОС50, МОС75).
По увеличению мощности выдоха и приросту показателей МОС75, МОС50, МОС25 по данным пневмотахометрии, проводимой после предварительного вдыхания больным бронхолитических (симпатомиметических и/или холинолитических) веществ, определяют роль бронхоспазма в нарушении бронхиальной проходимости и степень его выраженности.
С помощью этих же методов подбирают наиболее активный для данного больного ингаляционный бронхолитический (симпатомиметический или холинолитический) препарат.
Появление повышенного бронхиального сопротивления (зарегистрированного с помощью спирографии, пневмотахометрии и пневмотахографии) в ответ на физическую нагрузку, вдыхание холодного воздуха, раздражающих газов, пылей и ацетилхолина, свидетельствует об измененной реактивности бронхов.
Аллергологическое тестирование осуществляется только вне обострения заболевания и проводится с помощью набора разнообразных неинфекционных и инфекционных аллергенов.
Проводят кожные аллергические пробы (аппликационный, скарифика-ционный и внутрикожный способы нанесения аллергена). Выявленный аллерген можно наносить на конъюнктиву глаза, слизистую оболочку носа для оценки его провоцирующего действия. Наиболее достоверным методом специфической диагностики БА считают выявление специфической гиперреактивности бронхов с помощью ингаляционных провокационных тестов. Ингаляционно аллерген вводят с большой осторожностью, так как такой путь введения может спровоцировать тяжелый приступ БА или развитие астматического статуса. Установление аллергена и уточнение его провоцирующего действия — прямое доказательство аллергической природы БА.
Для специфической диагностики БА применяют также радиоиммуносор-бентный тест, позволяющий количественно оценить уровень IgE-антител. Повышение уровня общего IgE подтверждает при соответствующих данных анамнеза атопический механизм развития БА (этот тест применяют при невозможности проведения аллергологического тестирования).
Лабораторные исследования помогают подтвердить предполагаемый диагноз, оценить эволюцию заболевания и эффективность проводимого лечения.
Наличие эозинофилов в мокроте является одним из основных диагностических критериев БА. Кроме того, диагностическое значение имеет обнаружение в мокроте спиралей Куршмана и кристаллов Шарко—Лейдена.
76
Эозинофильный лейкоцитоз представляет собой неспецифический признак Л может служить проявлением общей аллергической реакции организма.
Лабораторные исследования помогают решать вопрос о наличии активного воспалительного процесса и степени его выраженности (увеличение острофазовых показателей).
При обострении БА и астматическом статусе особое значение имеет исследование кислотно-основного состояния и газового состава крови (изменяющихся при увеличении дыхательной недостаточности).
Рентгенологическое исследование помогает выявить очаги инфекции (в придаточных пазухах, зубах, желчном пузыре) и установить наличие острого (пневмония) или обострения хронического воспалительного процесса в легких, эмфиземы легких и пневмосклероза.
По данным ЭКГ обнаруживают признаки развития компенсированного легочного сердца — гипертрофию правых отделов сердца (подробнее см. «Легочное сердце»). При подозрении на симптоматический характер бронхоспазма проводят дополнительное обследование по программе, определяемой предполагаемым заболеванием.
Астматический статус. Факторы, предрасполагающие к его развитию, почти всегда являются результатом неадекватной терапии. Чаще всего причинами его служат:
1) бесконтрольный прием симпатомиметических и ГКС;
2) резкое прерывание длительно проводимой глюкокортикостероидной терапии;
3) обострение хронического или возникновение неэффективно леченного острого воспалительного процесса в бронхолегочном аппарате;
4) неудачно проведенная специфическая гипосенсибилизация;
5) злоупотребление снотворными и седативными средствами.
Критерии астматического («метаболического») статуса:
1) прогрессирующее нарушение дренажной функции бронхов;
2) развернутая клиническая картина удушья, которая может осложняться легочной обструкцией, гипоксемической комой, острым легочным сердцем;
3) резистентность к симпатомиметическим и бронхолитическим препаратам;
4) гиперкапния;
5) гипоксия тканей.
Классификация астматического статуса: I стадия — затянувшийся приступ удушья, сформировавшаяся резистентность к симпатомиметикам; О стадия — нарастание дыхательной недостаточности по обструктивному типу; Ш стадия — гипоксемическая, гиперкапническая кома.
Стадия I клинически характеризуется затянувшимся приступом удушья, вынужденным положением больного, учащенным дыханием, приступообразным кашлем со скудной, трудноотделяемой мокротой, тахикардией, повышением АД.
Из физикальных симптомов отмечают несоответствие между интенсивностью дыхательных шумов, выслушиваемых на расстоянии, и данными непосредственной аускультации легких (скудность хрипов, участки ослабленного дыхания).
Стадия I характеризуется умеренной артериальной гипоксемией (Ра02 составляет 60—70 мм рт. ст.) и нормо- или гипокапнией (показатели Рас0, нормальные или уменьшены в результате гипервентиляции и составляют менее 35 мм рт. ст.).
Для II стадии характерно очень тяжелое состояние больного: бледно-серые влажные кожные покровы, учащенное поверхностное дыхание, при
77
аускультации — «немое легкое» (хрипы почти не слышны), частый пульс малого наполнения, аритмия, снижение АД. Периоды безразличия у больного сменяются возбуждением.
Стадия II характеризуется более выраженной гипоксемией (Ра0, 50— 60 мм рт. ст.) и нарастающей гиперкапнией вследствие снижения эффективной (альвеолярной) вентиляции (Расо, 50—70 мм рт. ст. и даже несколько выше).
В стадии III сознание отсутствует, тахипноэ, часто разлитой «красный» цианоз, нередко коллапс. Летальность на высоте астматического статуса достигает 5—20 %. Наиболее частые причины смерти — асфиксия вследствие позднего проведения реанимационных мероприятий, невозможность восстановления эффективной вентиляции легких.
Стадия III характеризуется тяжелой артериальной гипоксемией (Ра02 40—55 мм рт. ст.) и резко выраженной гиперкапнией (Рас02 на уровне 80—90 мм рт. ст. и выше) с некомпенсированным респираторным ацидозом.
При своевременно начатой интенсивной терапии прогноз астматического статуса может быть благоприятным.
Все изложенное выше касалось так называемого метаболического (медленно развивающегося) астматического статуса. Кроме того, существует немедленно развивающийся (анафилактический) астматический статус, обусловленный гиперергической анафилактической реакцией немедленного типа с мгновенным высвобождением медиаторов аллергии и воспаления, что приводит к тотальному бронхоспазму и асфиксии в момент контакта с аллергеном.
Диагностика БА осуществляется на основании выявления определенных признаков.
Основные признаки: 1) наличие приступа удушья или его эквивалентов; 2) генерализованная обратимая бронхиальная обструкция; 3) эози-нофилия в мокроте; 4) отсутствие заболеваний, сопровождающихся брон-хоспастическим или бронхообструктивным синдромом (данный синдром — одно из проявлений болезни).
Дополнительные признаки: 1) клинико-аллергологический анамнез; 2) результаты аллергологического тестирования: а) для выявления аллергена — кожные пробы (аппликационные, внутрикожные, скарифика-ционные); б) для уточнения специфичности аллергена — назальные, ингаляционные, конъюнктивальные (проводятся в стадии стойкой ремиссии); радиоаллергосорбентный тест; в) провокационные пробы (с ацетилхоли-ном, гистамином) — при сомнительном диагнозе; 3) повышение содержания IgE в сыворотке крови; 4) эозинофилия крови.
Формулировка развернутого клинического диагноза БА учитывает:
1) основной клинико-патогенетический вариант БА (наиболее часто встречаются инфекционно-зависимый и атопический);
2) тяжесть течения (легкое, среднетяжелое, тяжелое);
3) фазу течения (обострение, стихающее обострение, ремиссия);
4) осложнения: а) дыхательная недостаточность (степень); б) легочно-сердечная недостаточность (степень); в) астматический статус (стадия); г) другие осложнения.
Примечание. При инфекционной зависимости Б А рекомендуется указывать: 1) характер хронического поражения легких, на фоне которого развилась БА или которое сопутствует БА; 2) характер инфекционной зависимости — инфекция, играющая роль аллергена, способствующая проявлению атопических реакций или же формирующая первично измененную реактивность бронхов.
78
Лечение. 1. Неотложная терапия приступа БА; интенсивная терапия при развитии астматического статуса.
2. Лечение в фазе обострения.
3. Лечение в фазе ремиссии.
Лечение приступа БА проводят с учетом возраста пациента и тяжести приступа.
Легкий приступ больные, как правило, купируют самостоятельно. Используются лекарственные вещества в таблетках (эуфиллин) или в ингаляторах (сальбутамол, вентолин, беротек — р2-адреностимуляторы; беродуал, сочетающий р2-адреностимулирующий эффект с холинолитическим). При отсутствии ингаляторов приступ купируют подкожными инъекциями эфедрина (0,5 мл 5 % раствора) в сочетании с папаверином (1 мл 2 % раствора) и антигистаминным препаратом (1 мл димедрола или супрастина).
Приступы средней тяжести у молодых пациентов с немедленным анамнезом купируют ингаляциями симпатомиметических средств; при отсутствии эффекта внутривенно вводят эуфиллин. Возможно введение растворов бронхолитических средств через небулайзер. Иногда приступ купируется только после внутривенного введения преднизолона (60 мг).
Пожилым больным при сред нетяжелом и тяжелом приступе, особенно при длительном анамнезе, приступ купируют с помощью введения бронхолитических средств через небулайзер (прибор, позволяющий рапылять лекарственные вещества до мельчайших частиц — 1—5 мкм, проникающих в дыхательные пути), а при отсутствии эффекта внутривенно вводят предни-золон.
При тяжелых приступах, помимо внутривенного введения преднизолона и назначения его внутрь (40—50 мг), существенное значение имеет выравнивание измененного кислотно-основного состояния, в связи с чем проводится инфузионная терапия натрия гидрокарбонатом, изотоническим раствором хлорида натрия (особенно в тех случаях, когда приступ затягивается и очень плохо отходит мокрота). При тяжелом приступе показана бронхолитическая терапия в сочетании с мукорегуляторами (лазолван, флуимуцил) и введением ГКС (суспензия пульмикорта 1 —2 мг) через небулайзер. При отсутствии небулайзера прибегают к повторному введению преднизолона. Больного обязательно госпитализируют.
При затянувшихся тяжелых приступах БА резко возрастает угроза развития астматического статуса.
Лечение астматического статуса заключается в проведении интенсивной терапии, которую необходимо начинать в максимально ранние сроки. Она включает:
а) оксигенотерапию, терапию в виде непрерывной подачи кислородно-
воздушной смеси с относительно небольшим содержанием 02 (35—40 %);
б) инфузионную терапию, при которой внутривенно вводят декстраны,
глюкозу, инсулин, 20 000 ЕД гепарина, натрия гидрокарбонат (под контро
лем показателей КОС) в общем количестве не менее 3—3,5 л в первые су
тки с целью восполнения дефицита жидкости, устранения гемоконцентра-
Ции, разжижения бронхиального содержимого;
в) небулайзерную терапию бронходилататорами и ГКС (суспензия
пульмикорта);
В качестве бронхорасширяющих средств используют небулайзерную терапию р2-агонистами или беродуалом, несмотря на то, что до этого боль-Ной мог использовать р2-агонисты (беротек, сальбутамол, вентолин) в больших количествах через дозированный аэрозольный ингалятор без выраженного эффекта;
7Q
г) при отсутствии небулайзера дают внутрь преднизолон по 40—60 мг 1 раз в сутки в сочетании с внутривенным введением гидрокортизона по 1 мг/кг, преднизолона по 60—90 мг каждые 2—4 ч в I стадии; в стадии Ц суточную дозу преднизолона доводят до 1000—1500 мг. После выведения из астматического статуса дозу ГКС ежесуточно уменьшают на 25 % до минимальной.
Для разжижения мокроты используют щелочное питье, парокислород-ные ингаляции. Мочегонные средства показаны лишь при возрастании центрального венозного давления до 150 мм вод. ст. и выше.
Активно используют перкуссионный и вибрационный массаж грудной клетки для улучшения выделения содержимого бронхов.
Прогрессирующее нарушение легочной вентиляции, не поддающееся консервативной терапии, является показанием для применения неинвазив-ной или искусственной вентиляции легких, лечебной бронхоскопии и проведения бронхоальвеолярного лаважа с «отмыванием» и удалением бронхиального содержимого.
Лечение анафилактического варианта астматического статуса требует проведения немедленной парентеральной лекарственной терапии: внутривенного введения 0,3—0,5 мл 0,1 % раствора адреналина на 20 мл изотонического раствора хлорида натрия и струйно внутривенно 120 мг преднизолона (200—400 мг гидрокортизона) с последующим переходом на внутривенное капельное введение этих же препаратов. Одновременно можно добавить 0,5—1 мл 0,1 % раствора атропина, вводя его струйно на 10 мл изотонического раствора хлорида натрия.
При отсутствии эффекта от перечисленных мероприятий проводят фто-ротановый наркоз и переводят больного на искусственную вентиляцию легких (ИВЛ).
После купирования приступа БА проводят плановую терапию, основные направления которой сформулированы ниже.
• Обучение пациента для создания более тесного сотрудничества с врачом при лечении БА.
• Повторный контроль за функциональным состоянием органов дыхания и оценка в динамике полученных данных.
• Выявление и устранение причинно-значимых факторов внешней среды.
• Разработка плана долгосрочного лечения больного с учетом его индивидуальных особенностей.
• Разработка плана лечения обострений БА.
• Обеспечение систематического наблюдения за состоянием больного с корректировкой при необходимости плана лечения.
Лечебные мероприятия, осуществляемые в период обострения заболевания и в период ремиссии, имеют свои особенности.
Лечение больного БА в период обострения, помимо купирования приступа, включает ряд различных мероприятий.
> Устранение контакта с выявленным аллергеном.
> Лекарственная противовоспалительная терапия.
ГКС в настоящее время являются наиболее эффективными противовоспалительными средствами при лечении БА. Их можно применять местно (ингаляционно) или при тяжелом течении БА системно (внутрь или парентерально).
Ингаляционное введение ГКС является предпочтительным, оказывает местный эффект и дает минимум побочных эффектов. К числу короткодействующих препаратов относятся беклазон «легкое дыхание», бекотид и
80
йекломет (беклометазон дипропионат); их следует применять 4 раза в день. Тякие препараты, как фликсотид (флютиказон пропионат) и пульмикорт •пюбухалер (будезонид), бенакорт (будезонид) характеризуются большей подолжительностью действия, что позволяет использовать их для надеж-пго контроля за течением БА 2 раза в сутки. В настоящее время считается Желательным применение всех дозированных ингаляторов вместе со специальной пространственной насадкой (спейсером), что облегчает больному пользование аэрозолем, увеличивает его поступление в нижние дыхательные пути, а также дополнительно снижает риск местных и системных побочных эффектов.
При тяжелом обострении ингаляционное введение ГКС следует осуществлять через небулайзер.
Если высокие дозы ингалируемых ГКС (более 1000 мкг/сут) не обеспечивают надежный контроль за течением БА, добавляют ГКС внутрь. При выраженной эозинофилии крови местное введение ГКС сочетается с приемом этих препаратов внутрь в виде так называемых толчков: 3 дня по 20—25 мг преднизолона (или другого ГКС в адекватной дозе). Большую часть суточной дозы рекомендуется принимать в утренние часы, заканчивать прием не позднее 5—6 ч вечера.
Противовоспалительным эффектом обладает также натрия хромогликат (интал, ломудал, кромолин), который показан больным преимущественно при лечении большинства больных атопической (аллергической) БА легкого течения и, кроме того, иногда дает положительный эффект у больных «аспириновой» астмой и астмой физического усилия. Препарат вводят ингаляционно в виде сухого порошка (с использованием спинхайлера) или распыляемого раствора (с помощью дозированного ингалятора). Лечение следует начинать с двух ингаляций препарата 4 раза в сутки; при достижении эффекта переходят на поддерживающую терапию. Противовоспалительным эффектом обладает также вводимый ингаляционно тайлед (натрия недокромил), назначаемый по 2—4 ингаляции в сутки; он дает возможность контролировать легкое персистирующее течение БА. У части больных со среднетяжелым течением БА его назначение позволяет уменьшить дозу применяемых ГКС.
При затрудненном дыхании за 15 мин до ингаляции противовоспалительного препарата больной должен сделать 1—2 вдоха бронхолитика.
А Бронхолитическая терапия: симпатомиметические и/или холиноли-тические препараты короткого действия назначают в дозированном аэрозоле, как правило, при появлении предвестников приступа удушья. Постоянное применение этих препаратов в ингаляторах не рекомендуется чаще 4 раз в сутки во избежание развития побочных эффектов (тахикардия, повышение АД, нарушения ритма сердца); руадреностимуляторы эффективны при БА, вызываемой физической нагрузкой, точно так же как и блока-торы медленных кальциевых каналов [Чучалин А.Г., 1985]. При тяжелом обострении БА эти препараты (специальные растворы беротека, атровента или беродуала) можно вводить при помощи небулайзера.
u В настоящее время наряду с ингаляционными (32-агонистами короткого Действия — фенотеролом (беротек), сальбутамолом (вентолин), тербутали-ном (бриканил) и др., длительность бронхолитического действия которых составляет 4—6 ч, применяют пролонгированные руагонисты с продолжительностью действия более 12 ч, в частности сальмотерол [серевент, фор-мотерол(оксис, форадил)].
Симпатомиметики длительного действия применяют также в форме таблеток (вольмакс и др.). Они показаны для приема внутрь на ночь при
HI
ночных приступах БА у лиц молодого возраста (у пожилых больных их применение нежелательно).
В настоящее время внутривенное введение эуфиллина не рекомендуется. Из препаратов теофиллина используют его пролонгированные формы (теопек, теотард, теобилонг).
Ингаляционные холинолитики — ипратропиум бромид (атровент) — имеют определенные преимущества перед р*2-агонистами У ЛИП пожилого возраста. Атровент применяют также в комбинации с фенотеролом (беро-теком) под названием беродуал.
С учетом тяжести течения БА предлагается ступенчатая схема лечения заболевания с применением описанных выше средств (табл. 6).
*• Дополнительная патогенетическая терапия: 1) новое направление в лечении БА — применение антагонистов лейкотриеновых рецепторов — препарата аколата (зафирулакст) по 20 мг внутрь 2 раза в день, мон-телукаста по 10 мг 1 раз в день. Эти препараты особенно эффективны при «аспириновой астме» и «астме физического усилия»;
2) муколитические препараты в виде ингаляции (лазолван, флуимуцил) или таблеток (лазолван, флуимуцил, халиксол, мукалтин), назначают при вязкой, трудноотделяемой мокроте. .Хорошее секретолитическое действие оказывает горячее щелочное питье. Йодистые препараты (3 % раствор йо-дида калия по 1 столовой ложке 3—4 раза в день) следует назначать с осторожностью и помнить о возможной непереносимости препарата: слезотечение, ринорея, усиление бронхоспазма. Прием настоев и отваров трав в качестве муколитической терапии не рекоменуется;
3) антибактериальную терапию проводят при обострении воспалительного процесса в бронхолегочной системе у больных с инфекционно-зави-симой БА;
4) лечебная бронхоскопия под наркозом проводится в случае отсутствия эффекта от лекарственной терапии у больных при сопутствующем ка-тарально-гнойном и гнойном эндобронхите (местно вводят антибактериальные средства, предпочтение оказывают 1 % раствору диоксидина). При необходимости эндобронхиально вводят гидрокортизон;
5) антагонисты кальция (верапамил) ингибируют трансмембранный поток кальция, что ведет к уменьшению выхода медиаторных веществ из тучных клеток. Препараты показаны больным при сочетании БА с ишемиче-ской болезнью сердца и при астме «физического усилия»;
6) антимедиаторы имеют небольшое значение в лечении БА: а) анти-гистаминные препараты блокируют Н,-рецепторы, уменьшая действие гис-тамина на гладкую мускулатуру бронхов; б) антисеротониновые препараты (циннаризин) применяют лишь при лечении больных БА с четкими клиническими признаками гиперсеротонинемии (тахикардия, наклонность к поносам, гиперемия лица); в) ингибиторы калликреина — трасилол, кон-трикал (по 10 000 ЕД) — вводят внутривенно капельно при затянувшихся приступах БА. Используют также гепарин, улучшающий микроциркуляцию. В настоящее время применяют две генерации антагонистов Н,-рецеп-торов. Препараты первого поколения (димедрол, тавегил, супрастин, пи-польфен, диазолин) оказывают ряд нежелательных воздействий (сонливость, сухость во рту, тахикардия, задержка мочи и т.д.), что резко ограничивает их применение. Препараты второго поколения — астемизол, лоратадин (эролин, кларитин), дезлоратадин (эриус), эбастин (кестин), фексофенадин (телфаст) и др. — лишены этих недостатков. Кроме того, эти препараты, помимо блокады Н,-рецепторов, в высоких дозах уменьшают выделение медиаторов из тучных клеток и базофилов. Комбинацию со-
блица 6. Ступенчатый подход к лечению бронхиальной астмы GINA 2002*
Тля всех ступеней: помимо ежедневного приема препаратов для контроля заболевания, для купирования острой симптоматики следует применять ингаляционный ру'агонист быстрого действия по потребности, однако не чаще 3—4 раз в день
| Степень тяжести | Ежедневный прием препаратов для контроля заболевания | Другие варианты лечения |
| Ступень 1 Интермиттируюшая | Нет необходимости | — |
| БА** | ||
| Ступень 2 | ||
| Легкая персистирую- | Ингаляционный ГКС | Теофиллин замедленного |
| щая БА | (< 500 мкг БДП или эквива- | высвобождения, или |
| лент) | Кромон, или Антилейкотриеновый препарат | |
| Ступень 3 | ||
| Персистирующая БА | Ингаляционный ГКС | Ингаляционный ГКС |
| средней степени тя- | (200-1000 мкг БДП или эк- | (500-1000 мкг БДП или |
| жести | вивалент) плюс ингаляцион- | эквивалент) плюс теофил- |
| ный р2-агонист длительного | лин замедленного высво- | |
| действия | бождения, или Ингаляционный ГКС (500-1000 мкг БДП или эквивалент) плюс пероральный р2-агонист длительного действия, или Ингаляционный ГКС (>1000 мкг БДП или эквивалента), или Ингаляционный ГКС (500-1000 мкг БДП или эквивалент) плюс антилейкотриеновый препарат | |
| Ступень 4 | ||
| Тяжелая персисти- | Ингаляционный ГКС (>1000 | — |
| рующая БА | мкг БДП или эквивалент) плюс ингаляционный (32-аго-нист длительного действия плюс один или более из следующих препаратов, если это необходимо: Теофиллин замедленного высвобождения Антилейкотриеновый препарат Пероральный (32-агонист длительного действия Пероральный ГКС |
в т 'Зля всех ступеней: после достижения контроля за лечением БА и его сохранения бы vrHHe Mec следУет попытаться постепенно уменьшать поддерживающую терапию, что-Роля новить минимальный объем лечения, требующегося для поддержания этого конт-
лечен циенты с интермиттирующей БА, но с тяжелыми обострениями должны получать Но"и^ соответственно персистирующей БА средней степени тяжести (уровень доказатель-
82
Я-\
судосуживающего средства с лоратадином (псевдоэфедрина сульфат 120 мг и лоратадин 5 мг) — клариназе с успехом применяют (по 1 таблетке 2 раза в день) для лечения аллергических ринитов;
7) физиотерапевтические методы воздействия (массаж грудной клетки, специальный комплекс дыхательной гимнастики). Иглорефлексотерапия оказывает благоприятный эффект в комплексной терапии БА.
а Симптоматическая терапия. При лечении БА применяют: 1) корректоры иммунных нарушений — тималин, рибомунил, бронхомунал — назначают больным со склонностью к рецидивирующим инфекционным процессам органов дыхания, трудно поддающимся антибактериальной терапии; 2) экстракорпоральные методы — плазмаферез и гемосорбция, эффективные у больных атопической формой БА с широким спектром аллергенов при аутоиммунной БА; 3) психотропные средства (тианептин, рела-ниум и пр.); психотерапия — при выраженных невротических реакциях и гипервентиляционных расстройствах у больных БА; 4) противокашлевые препараты (тусупрекс, бромгексин, либексин) — при упорном кашле; при сухом надсадном кашле рекомендуются кодеин, дионин, стоптуссин.
Лечение больного БА в фазе ремиссии включает:
• устранение контакта с аллергеном, исключение воздействия раздражителей слизистой оболочки бронхов;
• специфическую гипосенсибилизацию (проводится при установленном аллергене);
• неспецифическую гипосенсибилизацию (лечение гистоглобулином);
• санацию очагов инфекции (как правило, оперативную);
• ингаляционные ГКС в подобранных дозах;
• бронхолитические препараты в подобранных ранее дозах, желательно длительного действия;
• поддерживающие дозы интала (при его эффективности) или кетоти-фена;
• иглорефлексотерапию;
• постоянные занятия ЛФК и другие физиотерапевтические процедуры;
• при наличии у больного аллергического риносинусита — эндона-зально ИГКС (назонекс, фликсоназа, альдецин, насобек);
• санаторно-курортное лечение (Южный берег Крыма, курорты с горным морским воздухом).
Обучение пациентов в программе лечения БА является одной из главных задач. Цель его — научить больного «жить с бронхиальной астмой», широко используя «партнерство» врача и больного в лечении заболевания. Пациенты, проходя занятия в «астмашколе», увеличивают объем знаний о сущности патологии, принципах лечения и самоконтроля. Знания закрепляются в процессе индивидуального общения врача и больного.
Прогноз. Прогноз при БА различный в зависимости от клинико-патоге-нетического варианта (при атопической БА он более благоприятный, чем при инфекционно-зависимой), тяжести и характера течения, эффективности терапии.
Отсутствие успеха от лечения обычно отмечается среди молодых пациентов. Это может происходить из-за небрежного отношения к приему противовоспалительных препаратов, невысокой степенью содружества с врачом или неадекватной оценкой БА как пациентами, так и медицинскими работниками.
Все больные БА должны постоянно находиться под наблюдением как терапевта, так и врача-аллерголога.
84
Профилактика. Первичная профилактика БА состоит как в лечении
больных в состоянии предастмы, так и в выявлении у практически здоро-
ых лиц с отягощенной наследственностью биологических дефектов, пред-
втавЛЯЮЩих угрозу возникновения БА (повышенная чувствительность к
яиетилхолину и др.).
Методы первичной профилактики должны включать устранение из окружающей больных среды потенциально опасных аллергенов, ирритантов и ггоугих факторов, которые могут привести к развитию болезни (гипоаллер-генная диета, запрещение курения, прекращение контакта с производственными вредностями, занятия физкультурой и пр.).
При лечении больных в состоянии предастмы необходимо санировать очаги инфекции, проводить терапию аллергической риносинусопатии, применять различные методы немедикаментозного лечения, включая игло-и психотерапию, ЛФК, баротерапию, санаторно-курортное лечение. Показано проведение специфической (при выявлении аллергена) и неспецифической гипосенсибилизации.
Плеврит
ПЛЕВРИТ — термин, которым обозначают воспаление листков плевры с образованием на их поверхности фибрина или скоплением в плевральной полости экссудата того или иного характера. Этим же термином называют процессы в плевральной полости, сопровождающиеся скоплением патологического выпота, когда воспалительная природа плевральных изменений не представляется бесспорной (карциноматозный плеврит).
Помимо плевритов, выпот встречается при гидротораксе (транссудат), хилотораксе (скопление лимфы). Эти понятия не следует подменять термином «плеврит», как неверно и употребление названия «адгезивный плеврит», включающий в себя необратимые (спаечные, рубцовые) изменения плевры — исход закончившегося воспаления.
Плеврит, как правило, не является самостоятельным заболеванием. Он представляет собой патологическое состояние, осложняющее течение различных процессов как в легких, так и, значительно реже, в прилежащих к плевре структурах (грудная стенка, средостение, диафрагма, поддиафраг-мальное пространство). Иногда плеврит может быть проявлением общих (системных) заболеваний, протекающих без отчетливого поражения соприкасающихся с плеврой тканей. В связи с этим достоверных сведений о частоте плевритов и смертности от них не существует, так как плевриты в большинстве случаев регистрируются под рубриками основного заболевания (туберкулез, пневмония, рак).
Этиология. Причины, ведущие к развитию болезни, разнообразны. Все плевриты по этиологии можно разделить на две большие группы: инфекционные, т.е. вызванные воздействием на плевру того или иного возбудителя, и неинфекционные (асептические), при которых воспалительный процесс в плевре возникает без прямого участия патогенных микроорганизмов.
Причинами, приводящими к развитию плевритов инфекционной этиологи, являются:
1) бактериальная инфекция (пневмококк, стафилококк, грамотрица-тельные палочки и т.д.);
2) вирусные, риккетсиозные и микоплазменные возбудители;
3) грибковые (кокцидиоидоз, бластомикоз), протозойные (амебиаз) и паразитарные (эхинококкоз) вобудители;
rs
4) туберкулез (у 20 % больных плевритом);
5) сифилис, бруцеллез, брюшной и сыпной тиф, туляремия (крайне редко, но сопровождаются выпотом в плевральную полость).
Основными причинами плевритов неинфекционной этиологии служат: I. Опухоли (40 % всех плевритов): 1) первичные опухоли плевры (доброкачественные — локализованная мезотелиома и злокачественные — диффузная мезотелиома); 2) метастазы злокачественных опухолей в плевру; 3) лимфогранулематоз, лимфосаркома и другие лимфомы; 4) синдром Мейгса (плеврит и асцит при опухолях яичников).
П. Системные заболевания соединительной ткани (системная красная волчанка, ревматоидный артрит, узелковый периартериит, склеродермия, дерматомиозит, ревматизм — крайне редко).
III. Травма и операционные вмешательства.
IV. Тромбоэмболия легочной артерии, инфаркт легкого.
V. Другие причины: панкреатит (так называемый ферментный плеврит), острые лейкозы, геморрагические диатезы (геморрагический плеврит), постинфарктный синдром Дресслера, периодическая болезнь и др.
Патогенез. Механизм воздействия микроорганизмов на плевру отличается разнообразием.
• Непосредственное инфицирование плевры из субплеврально расположенных очагов (пневмония, абсцесс, бронхоэктазы, нагноившаяся киста, туберкулез) — контактный путь повреждения.
• Лимфогенное инфицирование плевральной полости — ретроградный ток тканевой жидкости.
• Гематогенное распространение микроорганизмов (имеет небольшое значение).
• Прямое инфицирование плевры из внешней среды (травмы, ранения, оперативные вмешательства) — нарушение целостности плевральной полости.
Помимо микроорганизмов, на плевру оказывает воздействие и ряд других повреждающих факторов, приводящих к плевральной экссудации.
1. Токсичные продукты (эндотоксины, опухолевый процесс) и протео-литические ферменты (при острых панкреатитах) повышают проницаемость кровеносных и лимфатических сосудов.
2. Поражение сосудов плевры (как проявление системного васкулита) повышает проницаемость капилляров.
3. Нарушение циркуляции лимфы в результате блокады путей ее оттока.
4. Местные и общие аллергические процессы, изменение общей реактивности организма.
Характер экссудата определяется не только разнообразием этиологических факторов, но и соотношением накопления и резорбции выпота, длительностью его существования:
> умеренный выпот и сохранившаяся способность к его резорбции — фибринозный, или сухой, плеврит;
> скорость экссудации превышает возможности всасывания экссудата — серозный или серозно-фибринозный плеврит;
> инфицирование экссудата гноеродной микрофлорой — серозно-гнойный или гнойный (эмпиема плевры);
> скорость резорбции превышает скорость экссудации — образование шварт при рассасывании;
> карциноматоз и туберкулез плевры, инфаркт легкого и травма, панкреатит и цирроз печени, болезнь Верльгофа и передозировка антикоагулянтов — геморрагический выпот;
86
*. преобладание аллергических процессов — эозинофильный выпот; >. хроническое многолетнее наличие экссудата — холестериновый
^Классификация. Общепринятой классификации плевритов не существу-
В различных классификациях учитываются этиология, характер патоло-
емческого процесса (сухие, экссудативные), выпота (серозный, серозно-
лмбоинозный, гнойный, гнилостный, геморрагический, эозинофильный,
илезный, холестериновый, смешанный; локализация (диффузные и осум-
^ованные), острота течения (острый, подострый, хронический).
Клиническая картина. Проявление плеврита характеризуют:
1) форма (сухой или экссудативный);
2) характер воспалительной реакции плевры (вид экссудата);
3) локализация и распространенность экссудата (диффузный или осум-кованный);
4) характер течения (острый или хронический).
Среди клинических проявлений плеврита можно выделить три основных синдрома. Основной синдром, определяющийся особенностями патологического процесса, дает название различным клиническим формам плеврита: сухой (фибринозный) плеврит; негнойный (выпотной) экссудативный плеврит; гнойный выпотной плеврит (эмпиема плевры). Эти формы плевритов наблюдаются изолированно или сменяют одна другую в динамике заболевания.
Второй синдром отражает воспалительную реакцию организма — это синдром острофазовых показателей. Наконец, в клинической картине могут наблюдаться симптомы (признаки) того заболевания, которое послужило причиной возникновения плеврита, — это третий синдром.
Кроме трех основных, при выпотных плевритах могут встречаться дополнительные синдромы: а) компенсированного ателектаза легкого; б) смещения средостения; в) сдавления верхней полой вены.
Довольно часто плевральная экссудация является первым, а иногда и единственным проявлением болезни в течение некоторого времени, маскирующим основное заболевание. При обследовании больного следует прежде всего определить характер поражения плевры, а затем установить этиологию болезни. Иногда это не удается даже при самом тщательном анализе клинической картины; в таких случаях говорят об идиопатическом плеврите. При отсутствии патологических процессов в легких и органах брюшной полости плеврит рекомендуется расценивать как туберкулезный.
Сухой плеврит. На I этапе диагностического поиска выявляют жалобы больного на боль в груди при дыхании, повышение температуры тела, слабость, одышку. Обычно заболевание начинается остро (на фоне видимого благополучия), и главной жалобой является боль при дыхании.
Боль при сухом плеврите, локализуясь в основном в зоне фибринозных наложений, имеет ряд особенностей:
а) при диафрагмальном плеврите боль нередко иррадиирует по ходу
диафрагмального нерва — в область шеи, по нижним межреберным нер
вам — на переднюю брюшную стенку;
б) при костальном плеврите боль острая в типичном месте грудной
клетки, но степень ее выраженности различна и зависит от локализации и
выраженности воспалительного процесса;
в) междолевые и верхушечные плевриты практически не сопровожда
йся болями;
г) боль усиливается при глубоком вдохе, а также при наклоне в проти
воположную сторону (симптом Шепельмана) и уменьшается в положении
на больном боку.
Плеврит может сопровождаться нарушением общего состояния: недомоганием, болями в суставах, мышцах, повышением температуры тела. Естественно, что на I этапе диагностического поиска имеются жалобы (кашель, выделение мокроты и т.д.), обусловленные заболеванием, приведшим к развитию плеврита (пневмония, туберкулез и пр.).
Проявления сухого плеврита (характерные боли) могут служить дополнительными признаками основного патологического процесса (пневмония, абсцесс легкого, системные заболевания соединительной ткани) или выступать на первый план.
На II этапе диагностического поиска выявляется наиболее существенный признак — шум трения плевры. Этот звуковой феномен имеет ряд особенностей: выслушивается в обе дыхательные фазы; характеризуется прерывистостью, напоминая то скрип снега или новой кожи, то нежную крепитацию; усиливается от давления стетоскопом, может ощущаться ладонью; не исчезает после кашля.
Шум трения плевры не выслушивается при диафрагмальном плеврите. В подобных случаях выявляют болезненные точки между ножками груди-но-ключично-сосцевидной мышцы, в первых межреберных промежутках у грудины, по линии прикрепления диафрагмы к грудной стенке.
Кроме шума трения плевры, обнаруживается учащенное или поверхностное дыхание, причем дыхательная экскурсия грудной клетки иногда ограничена на стороне поражения. Пальпация поможет выявить болезненность или чувствительность трапециевидных мышц.
При этой форме плеврита III этап диагностического поиска малоинформативен: рентгенологические изменения, как правило, отсутствуют; при исследовании крови могут быть выявлены острофазовые показатели (чаще всего повышение СОЭ, лейкоцитоз, иногда со сдвигом лейкоцитарной формулы крови влево).
Таким образом, в диагностике сухого плеврита наиболее важными являются I и II этапы диагностического поиска, а из основных признаков — боль в области поражения плевры, шум трения плевры.
Синдром сухого плеврита сходен с синдромом сухого перикардита, межреберной невралгии и синдромом Титце. Главный отличительный симптом — связь боли с дыханием (иногда с кашлем) и шум трения плевры.
Экссудативный (выпотной) плеврит. На I этапе диагностического поиска важно проследить следующую динамику процесса:
1) в случаях, когда развитию воспалительного выпота предшествовал сухой (фибринозный) плеврит, болевые ощущения ослабевают, сменяются ощущением тяжести, переполнения грудной полости, нарастанием общей слабости;
2) начало экссудативного плеврита может быть острым, с ознобом и повышением температуры тела;
3) иногда выпот накапливается исподволь, после периода небольшого недомогания и повышения температуры тела.
Можно выделить ряд характерных жалоб:
1) основная жалоба — одышка («больной сменил боль на одышку»), появляется при значительном накоплении экссудата;
2) нередко отмечается сухой, по-видимому, рефлекторный кашель;
3) болевой синдром, не исчезающий при накоплении выпота, а иногда и нарастающий, характерен для карциноматоза плевры;
4) боль в грудной клетке может беспокоить также при осумкованном костальном плеврите;
88
5) при медиастинальном плеврите боль локализуется за грудиной и усиливается при дыхании;
6) при медиастинальном осумкованном плеврите возможны дисфагия (от сдавления пищевода), отеки лица, шеи и рук (от сдавления верхней по-тюй вены) и осиплость голоса (сдавление возвратного нерва).
Кроме того, могут быть выявлены жалобы, свойственные тем заболеваниям, проявлением которых является выпотной плеврит (похудение при опухолях, повышение температуры тела при инфекциях, системных заболеваниях соединительной ткани, опухолях и т.д.).
Нередко плевральный выпот может быть первым и долгое время единственным симптомом основного заболевания.
На II этапе диагностического поиска наиболее существенно обнаружение симптомов, обусловленных выпотом в плевральной полости:
1) на стороне поражения отмечается отставание дыхательной экскурсии грудной клетки, а иногда и выбухание межреберных промежутков;
2) при перкуссии в нижних отделах пораженной стороны — выраженное притупление перкуторного тона с характерной верхней границей по линии Дамуазо (свободный плевральный экссудат может быть определен перкуторно, если его объем превышает 300—500 мл). При осумкованном плеврите границы выпота могут четко не определяться;
3) дыхательные шумы над зоной притупления ослаблены, у верхней границы экссудата часто прослушиваются крепитирующие хрипы и шум трения плевры;
4) органы средостения могут смещаться в здоровую сторону;
5) при левостороннем выпоте исчезает пространство Траубе;
6) при значительном выпоте отмечаются набухание шейных вен, цианоз.
Задачи III этапа диагностического поиска:
1) выявление достоверных критериев, позволяющих установить (или подтвердить) наличие выпота в плевре;
2) оценка степени активности патологического процесса;
3) выяснение характера экссудата;
4) уточнение характера заболевания, приведшего к развитию плеврита.
Существенное значение для постановки диагноза имеют рентгенологическое исследование и данные плевральной пункции. По специальным показаниям для уточнения диагноза проводят плевроскопию и пункционную биопсию плевры.
Рентгенологическое исследование грудной клетки позволяет обнаружить выпот с достоверностью, если его не менее 500 мл. При меньшем количестве выпота следует производить латероскопию на больном боку.
На рентгенограмме при свободном выпоте обнаруживается затемнение с не вполне четкой, скошенной книзу и кнутри верхней границей. Большие выпоты затеняют легочное поле и смещают тень средостения в противоположную сторону. Небольшие затемнения занимают лишь реберно-диа-Фрагмальный синус, в подобных случаях отмечается высокое стояние купола диафрагмы.
Рентгенологическое исследование, проведенное после эвакуации выпота, Помогает выявить изменения в легочной ткани, лимфатических узлах средостения и т.д. и уточнить природу основного заболевания. Положение органов средостения может служить дифференциально-диагностическим признаком, Позволяющим отличить скопление жидкости в плевральной полости от ряда лезней и синдромов, дающих сложную рентгенологическую картину:
а) органы средостения не смещены — пневмония, плевральные спайки
KQ
б) смещены в сторону затемнения — ателектаз, цирроз, плевральные
спайки;
в) смещены в сторону, противоположную затемнению, — плевральный
выпот, диафрагмальная грыжа.
Осумкованные плевриты следует дифференцировать от очаговой пневмонии, опухоли легкого и средостения, эхинококковой кисты легкого, плевральной шварты, фиброторакса, цирроза легкого, высокого стояния диафрагмы, диафрагмальной грыжи. Обнаружить плевральный выпот при осум-кованном плеврите помогает ультразвуковое исследование грудной клетки, однако решающее значение имеют результаты плевральной пункции.
Плевральная пункция позволяет: а) окончательно подтвердить наличие выпота; б) получить материал для исследования, имеющего большое диагностическое значение.
Лабораторные исследования включают анализ плеврального выпота: определение относительной плотности, содержания белка, пробы Ривальты, определение содержания ЛДГ, цитологическое исследование. Экссудат отличается высокой относительной плотностью (выше 1,018) и содержанием белка более 3 %, повышением показателей ЛДГ, положительной пробой Ривальты. Относительная плотность менее 1,015 и содержание белка менее 2 %, низкий уровень ЛДГ свидетельствуют о наличии транссудата.
Цитологическое исследование осадка дает существенные данные для диагноза:
1) преобладание лимфоцитов характерно для туберкулезной или опухолевой природы выпота;
2) преобладание нейтрофилов является отличительной чертой выпота при острых воспалительных процессах (пневмония, абсцесс), а нарастание их количества и появление среди них разрушенных клеток свидетельствуют о нагноении экссудата, т.е. о начале развития эмпиемы;
3) преобладание эозинофилов характеризует аллергический плеврит
лишь в случаях, если одновременно имеется эозинофилия крови.
Геморрагический выпот встречается при инфаркте легкого, опухолевом поражении плевры, поражении плевры туберкулезными бугорками, травме грудной клетки, разрыве сосудов плевры при спонтанном пневмотораксе, аутоиммунной тромбоцитопении, циррозе печени, передозировке антикоагулянтов.
Плевральный выпот опухолевой природы, помимо геморрагического, бывает и хилезным (от сдавления грудного лимфатического протока), а изолированное нарушение лимфатического оттока может приводить к появлению в плевральной полости выпота со свойствами транссудата. При плевритах опухолевого генеза в осадке можно выявить атипичные клетки.
В ряде случаев важным для диагностики оказывается определение в плевральной жидкости содержания глюкозы (особенно низкий уровень характерен для ревматоидного артрита), амилазы (высокие цифры при панкреатите), ревматоидного и антинуклеарного фактороров (при системных заболеваниях соединительной ткани).
Микроскопия, посев на специальные среды, а главное, заражение морских свинок плевральным содержимым позволяют выявить туберкулезную природу экссудата.
Другие лабораторные исследования не имеют решающего значения в диагностике плеврита, но могут помочь: а) в выявлении основного заболевания (например, обнаружение LE-клеток при СКВ, ревматоидного фактора при ревматоидном артрите); б) в оценке остроты текущего процесса (обнаружение неспецифических острофазовых показателей).
90
Эмпиема плевры. Если к плевральному экссудату присоединяется гноеродная флора, то развивается гнойный плеврит — эмпиема плевры. К развитию эмпиемы плевры приводят разнообразные причины. Они же часто определяют особенности клинической картины и характер течения (острое лли хроническое) эмпиемы.
Эмпиема плевры относится к хирургической патологии, однако диагностируется в большинстве случаев терапевтом.
На I этапе диагностического поиска выявляется нарастание жалоб: возобновляется (или появляется) боль в груди, ухудшаются общее состояние и самочувствие, вновь повышается температура тела до высоких цифр, что нередко сопровождается ознобом и потоотделением, усиливается одышка.
В анамнезе отмечаются предшествующая пневмония, обострение брон-хоэктатической болезни, прогрессирование туберкулезного процесса, суб-плеврально расположенный абсцесс легких или инфицирование плевральной полости во время и/или после операционной травмы.
На II этапе диагностического поиска выявляют объективные симптомы гнойно-резорбтивного истощения или гнойно-резорбтивной лихорадки; нередки гектический характер лихорадки, бледность кожных покровов с землистым оттенком, похудение.
При массивном выпоте (распространенная или тотальная эмпиема) может появиться болезненность межреберий, присоединяются признаки дыхательной недостаточности. Хроническое течение эмпиемы может осложниться появлением наружных, бронхоплевральных и плевромедиастиналь-ных свищей и развитием амилоидоза внутренних органов (отеки, гепато-лиенальный синдром и др.).
При ограниченной эмпиеме изменения внутренних органов выражены в меньшей степени.
На III этапе диагностического поиска, как и при экссудативном плеврите, наибольшую информацию дают плевральная пункция и рентгенологическое исследование органов грудной клетки.
При плевральной пункции получают мутную жидкость или типичный гной, посев которого на питательные среды позволяет поставить этиологический диагноз и определить чувствительность возбудителя к антибактериальным средствам.
Рентгенологически выявляется эмпиема без деструкции или с деструкцией легочной ткани. Помимо рентгенографии легких, информацию, необходимую для уточнения характера поражения, дает томография плевральной полости и ткани легкого. В ряде случаев, особенно при невыясненной этиологии эмпиемы, необходимо проводить торакоскопию. О тяжести течения процесса можно судить по изменению анализов крови и мочи: нарастают гипохромная анемия и лейкоцитоз со сдвигом лейкоцитарной формулы влево, в моче — белок, могут быть цилиндры.
Диагностика. Основным в распознавании плеврита является следующее: 1) выявление характерных симптомов заболевания (боль в боку, сопровождающаяся шумом трения плевры, выпот в плевральной полости); 2) определение особенностей выпота; 3) диагностика основного заболевания, приведшего к развитию плеврита.
Формулировка развернутого клинического диагноза учитывает: 1) этиологию плеврита (если имеются точные сведения); 2) клинико-морфологи-Ческую форму (сухой, экссудативный, эмпиема плевры); 3) при осумкован-нЫх плевритах указывают его локализацию (диафрагмальный, междолевой, ^едиастинальный и т.д.); 4) характер течения (острый, хронический, рецидивирующий).
В формулировке диагноза допускается два варианта: 1) диагноз начинается с плеврита; 2) диагноз начинается с основного заболевания, а плеврит указывается в осложнениях.
Лечение. Лечебные мероприятия, проводимые больным плевритом, должны предусматривать:
1. Воздействие на основное заболевание (этиологическое лечение).
2. Патогенетическую терапию (с учетом характера выпота и клинико-морфологической формы плеврита).
3. Устранение наиболее выраженного синдрома, определяющего тяжесть состояния.
4. Повышение общей реактивности организма.
• В подавляющем большинстве случаев плеврит бывает проявлением какого-либо самостоятельного заболевания, поэтому необходимо этиологическое лечение.
При плевритах туберкулезной этиологии следует длительно (4—6 мес) проводить антибактериальную терапию. Первые 2 мес назначают противотуберкулезную терапию четырьмя препаратами: изониазид внутрь по 10 мг/кг в сочетании с пиразинамидом внутрь по 20—25 мг/кг, рифампи-цином внутрь по 10 мг/кг, стрептомицином внутримышечно по 16 мг/кг или этамбутолом внутрь по 20—25 мг/кг. Все препараты назначают 1 раз в сутки. Этамбутол назначают при высоком уровне устойчивости мико-бактерии туберкулеза в регионе, где проживает больной, к стрептомицину и изониазиду. Продолжение лечения возможно двумя схемами: изониазид в комбинации с рифампицином ежедневно или через день в течение 4 мес.
Лечение противотуберкулезными препаратами можно начинать также в случаях неясной этиологии плеврита.
При пневмонии следует назначать антибиотики с учетом чувствительности микрофлоры бронхиального содержимого к антибиотикам (см. раздел «Пневмония»).
Если диагностированы системные заболевания соединительной ткани и аллергические состояния, назначают иммуносупрессивную терапию, чаще всего ГКС.
Патогенетическую терапию проводят с помощью противовоспалительных и десенсибилизирующих препаратов, из которых наиболее эффективны ацетилсалициловая кислота (2—3 г/сут), амидопирин (2 г/сут), бу-тадион (0,15 г 3 раза в сутки), хлорид кальция (10 % раствор по 1 столовой ложке 4—5 раз в день). В ряде случаев при экссудативных плевритах, отличающихся торпидным течением с недостаточно быстрым рассасыванием выпота, с этой же целью применяют небольшие дозы преднизолона (10-20 мг/сут).
При сухих плевритах и упорном сухом кашле рекомендуются дионин, кодеин.
• Устранение наиболее выраженного синдрома, определяющего тяжесть состояния, заключается в эвакуации экссудата с помощью плевральной пункции, так как основные клинические симптомы обусловлены накоплением жидкости в плевральной полости. Эвакуация экссудата преследует две цели: предупреждение развития эмпиемы и устранение функциональных расстройств, связанных со сдавлением жизненно важных органов. Плевральную жидкость следует удалять в раннем периоде при больших выпотах, вызывающих одышку, смещение сердца, или если перкуторные границы тупости спереди доходят до II ребра. Рекомендуется эвакуировать одномоментно не более 1,5 л жидкости в целях предупреждения коллапса. 92
Разгрузочные пункции следует производить редко, так как при этом теря-тся много белка. Чтобы уменьшить накопление выпота, ограничивают пи-Le назначают мочегонные препараты и ГКС.
'в остальных случаях плевральную пункцию с удалением экссудата луч-проводить в фазе стабилизации или даже резорбции, так как ранняя вакуаиия выпота ведет к нарастанию отрицательного давления в плевральной полости, что способствует накоплению в ней экссудата.
Небольшой по объему серозный экссудат, связанный с туберкулезом или Другой инфекцией, удалять необязательно, однако при длительном отсутствии положительной динамики лучше прибегнуть к пункции и ввести внутриплеврально гидрокортизон (50—125 мг).
При экссудативных плевритах, обусловленных неспецифическим инфекционным процессом, целесообразно удалять даже небольшой по объему выпот с введением в плевральную полость антибактериальных средств для профилактики эмпиемы.
В комплексе лечебных мероприятий при эмпиеме плевры (острой) удаление гнойного экссудата и повторные вливания в плевральную полость антибиотиков наиболее эффективны в сочетании с общей антибактериальной терапией.
Лечение хронической эмпиемы плевры может быть только оперативным. • Для повышения общей реактивности организма применяют гигиенические мероприятия и физические методы воздействия.
Больным сухим плевритом лечение можно проводить в домашних условиях. Необходимы покой, частые проветривания помещения, а при повышении температуры тела — постельный режим. Сохранили свое значение такие старые методы, как согревающий компресс с тугим бинтованием нижних отделов грудной клетки, банки, смазывание кожи йодной настойкой и т.д. После исчезновения боли, нормализации температуры тела и СОЭ больному рекомендуют дыхательную гимнастику для предотвращения образования шварт.
При экссудативных плевритах важна диетотерапия: богатое витаминами (особенно аскорбиновой кислотой) и белками питание, ограничение приема воды и соли. Занятия лечебной физкультурой с включением дыхательных упражнений необходимо проводить уже в период рассасывания экссудата для предупреждения образования массивных плевральных спаек. После стихания острых явлений с этой же целью и для восстановления функции легких показаны ручной и вибрационный массаж.
После курса медикаментозной терапии больные могут быть направлены на санаторно-курортное лечение в местные лесные санатории и курорты Южного берега Крыма. Лица, перенесшие экссудативный плеврит туберкулезной этиологии, должны находиться под наблюдением противотуберкулезного диспансера не менее 2 лет.
При эмпиеме плевры очень важны средства, повышающие специфическую и неспецифическую резистентность организма (гамма-глобулин, гипериммунная плазма). Для коррекции нарушений белкового и водно-солевого обмена производят внутривенные инфузии белковых препаратов, растворов электролитов, глюкозы и т.д.
Прогноз. Сухие и экссудативные плевриты (негнойные) никогда не определяют прогноз основного заболевания, исход их зависит от эффективности лечения основного заболевания. Прогноз при гнойных плевритах, особенно при эмпиеме плевры, всегда серьезный.
Профилактика. Основное направление в профилактике плевритов — ЗДекватное лечение заболеваний, при которых развивается плеврит.
Легочное сердце
ЛЕГОЧНЫЕ СЕРДЦЕ (ЛС) — это клинический синдром, обусловленный гипертрофией и/или дилатацией правого желудочка, возникшей в результате гипертензии в малом круге кровообращения, которая в свою очередь развивается вследствие заболевания бронхов и легких, деформации грудной клетки или поражения легочных сосудов.
Классификация. Б.Е. Вотчал (1964) предлагает классифицировать легочное сердце по 4 основным признакам (табл. 7): 1) характер течения; 2) состояние компенсации; 3) преимущественный патогенез; 4) особенности клинической картины.
Таблица 7. Классификация легочного сердца
| Характер | Состояние | Преимущест- | |
| течения | компенсации | венный патогенез | Клиническая картина |
| Острое ЛС (развитие в | Декомпенси- | Васкулярный | Массивная тромбоэмболия легочной |
| рованное | Бронхолегоч- | артерии. Клапанный пневмоторакс, | |
| течение не- | ный | пневмомедиастинум. Бронхиальная | |
| скольких ча- | астма, затяжной приступ, астматиче- | ||
| сов, дней) | ский статус. Пневмония с большой площадью поражения, экссудативный плеврит с массивным выпотом | ||
| Подострое Л С | Компенсиро- | Васкулярный | Повторные мелкие тромбоэмболии в |
| (развитие в | ванное | Бронхолегоч- | системе легочной артерии. Повторные |
| течение не- | Декомпенси- | ный | затяжные приступы бронхиальной ас- |
| скольких не- | рованное | Торакодиаф- | тмы. Раковый лимфангит легких |
| дель, месяцев) | рагмальный | Хроническая гиповентиляция центрального и периферического происхождения (ботулизм, полиомиелит, миастения и др.) | |
| Хроническое | Компенси- | Васкулярный | Первичная легочная гипертензия. Ар- |
| Л С (развитие | рованное | Бронхолегоч- | терииты. Повторные эмболии. Резек- |
| в течение ря- | Декомпенси- | ный* | ция легкого |
| да лет) | рованное по | Торакодиаф- | Обструктивные процессы в бронхах и |
| правожелу- | рагмальный | легких различной этиологии (хрони- | |
| дочковому | ческий бронхит, бронхиальная астма, | ||
| типу | эмфизема легких, диффузный пнев-москлероз с эмфиземой). Рестриктив-ные процессы — фиброзы и грануле-матозы; поликистоз легких. Поражение позвоночника и грудной клетки с деформацией ее. Плевральные спайки. Ожирение (синдром Пиквика) |
* При этом варианте могут быть использованы существующие классификации легочно-сер-дечной недостаточности.
Примечания. 1. Диагноз легочного сердца ставят после диагноза основного заболевания; при формулировке диагноза используют только первые две графы классификации. Графы 3 и 4 способствуют углубленному пониманию патофизиологической сущности процесса и выбору терапевтической тактики. 2. Степень недостаточности кровообращения оценивается по общепринятой классификации.
Различают острое, подострое и хроническое ЛС, что определяется темпом развития легочной гипертензии. При остром развитии ЛС легочная
94
гипертензия возникает в течение нескольких часов или дней, при подост-и __ нескольких недель или месяцев, при хроническом — в течение нескольких лет.
Острое ЛС наиболее часто (около 90 % случаев) наблюдается при легочных эмболиях или внезапном повышении внутригрудного давления, подострое — при раковых лимфангитах, торакодиафрагмальных поражениях.
Хроническое ЛС в 80 % случаев возникает при поражении бронхоле-гочного аппарата (причем у 90 % больных в связи с хроническими неспецифическими заболеваниями легких); васкулярная и торакодиафрагмаль-ная формы ЛС развиваются в 20 % случаев.
Этиология. Все заболевания, вызывающие хроническое ЛС, по классификации экспертов ВОЗ (1960), делят на 3 группы: 1) первично влияющие на прохождение воздуха в легких и альвеолах; 2) первично влияющие на движение грудной клетки; 3) первично поражающие легочные сосуды.
К первой группе относятся болезни, первично поражающие бронхоле-гочный аппарат (ХОБЛ, хронические бронхиты и пневмонии, эмфизема легких, фиброзы и гранулематозы легких, туберкулез, профессиональные заболевания легких и пр.).
Вторую группу составляют заболевания, ведущие к нарушению вентиляции вследствие патологических изменений подвижности грудной клетки (кифосколиоз, патология ребер, диафрагмы, болезнь Бехтерева, ожирение
и пр.).
Третья группа включает в качестве этиологических факторов, первично поражающих легочные сосуды, повторные тромбоэмболии легочной артерии, васкулиты и первичную легочную гипертензию, атеросклероз легочной артерии и т.д.
Несмотря на то что к настоящему времени в мировой литературе известно около 100 заболеваний, приводящих к развитию хронического ЛС, самыми частыми причинами остаются ХНЗЛ (в первую очередь ХОБЛ и бронхиальная астма).
Патогенез. Основным механизмом формирования ЛС является повышение давления в системе легочной артерии (легочная гипертензия).
Среди механизмов, приводящих к возникновению легочной гипертензии, различают анатомические и функциональные (схема 7).
К анатомическим механизмам относят:
а) закрытие просвета сосудов системы легочной артерии в результате
облитерации или эмболизации;
б) сдавление легочной артерии извне;
в) значительное уменьшение русла малого круга кровообращения в ре
зультате пульмонэктомии.
К функциональным механизмам относят:
а) сужение легочных артериол при низких значениях Ра02 (альвеолярная
гипоксия) и высоких величинах РаСОг в альвеолярном воздухе;
б) повышение давления в бронхиолах и альвеолах;
в) повышение содержания в крови веществ и метаболитов прессорного
Действия;
г) увеличение минутного объема сердца;
Д) повышение вязкости крови.
Решающая роль в формировании легочной гипертензии принадлежит функциональным механизмам. Основное значение имеет сужение легочных сосудов (артериол).
Наиболее существенной причиной, вызывающей сужение легочных со-УДов, является альвеолярная гипоксия, приводящая к местному выбросу
95
|
|
биогенных аминов (гистамина, серотонина и пр., простагландинов — вазо-активных веществ). Освобождение их сопровождается отеком эндотелия капилляров, скоплением тромбоцитов (микротромбозы?) и вазоконстрик-цией. Рефлекс Эйлера—Лильестранда (спазм легочных артериол при уменьшении Ра02 в альвеолах) распространяется на сосуды, имеющие мышечный слой, в том числе и артериолы. Сужение последних также приводит к росту давления в легочной артерии.
Альвеолярная гипоксия с различной степенью выраженности развивается при всех ХНЗЛ и при вентиляционных нарушениях, сопровождающихся увеличением остаточной емкости легких. Особенно выражена она при нарушениях бронхиальной проходимости. Кроме того, альвеолярная гипоксия возникает и при гиповентиляции торакодиафрагмального происхождения.
Альвеолярная гипоксия способствует повышению давления в легочной артерии и через артериальную гипоксемию, которая приводит: а) к увели-
чению минутного объема сердца через раздражение хеморецепторов аор-тально-каротидной зоны; б) к развитию полицитемии и увеличению вязкости крови; в) к повышению уровня молочной кислоты и других метаболи-т0в и биогенных аминов (серотонин и др.), которые способствуют росту давления в легочной артерии; г) происходит резкая активизация ренин-ан-гиотензин-альдостероновой системы (РААС).
Помимо этого, альвеолярная гипоксия приводит к уменьшению выработки вазодилатирующих субстанций (простациклина, эндотолиального ги-перполяризующего фактора, эндотелиального расслабляющего фактора), продуцируемых клетками сосудистого эндотелия легких в норме.
Давление в легочной артерии повышается при сдавлении капилляров, обусловленном: а) эмфиземой и повышением давления в альвеолах и бронхиолах (при непродуктивном надсадном кашле, интенсивной и физической нагрузке); б) нарушением биомеханики дыхания и повышением внутри-грудного давления в фазе затянувшегося выдоха (при бронхообструктивном синдроме).
Сформировавшаяся легочная гипертензия приводит к развитию гипертрофии правых отделов сердца (вначале правого желудочка, затем правого предсердия). В дальнейшем имеющаяся артериальная гипоксемия вызывает дистрофические изменения в миокарде правых отделов сердца, что способствует более быстрому развитию сердечной недостаточности. Ее развитию способствуют также токсическое влияние на миокард инфекционных процессов в легких, недостаточное кислородное снабжение миокарда, имеющаяся ИБС, артериальная гипертония и другие сопутствующие заболевания.
На основании выявления признаков стойкой легочной гипертензии, гипертрофии правого желудочка при отсутствии признаков сердечной недостаточности ставят диагноз компенсированного ЛС. При наличии признаков правожелудочковой недостаточности диагностируют декомпенсирован-ное ЛС.
Клиническая картина. Проявления хронического ЛС состоят из симптомов:
• основного заболевания, приведшего к развитию хронического ЛС;
• дыхательной (легочной) недостаточности;
• сердечной (правожелудочковой) недостаточности.
Развитию хронического ЛС (как и появлению гипертензии в малом круге кровообращения) обязательно предшествует легочная (дыхательная) недостаточность. Дыхательная недостаточность — состояние организма, при котором не обеспечивается поддержание нормального газового состава крови либо оно достигается за счет более интенсивной работы аппарата внешнего дыхания и повышенной нагрузки сердца, что приводит к снижению функциональных возможностей организма.
Выделяют три степени дыхательной недостаточности.
При дыхательной недостаточности I степени одышка и тахикардия возникают лишь при повышенной физической нагрузке; цианоза нет. Показатели функции внешнего дыхания (МОД, ЖЕЛ) в покое соответствуют Должным величинам, но при выполнении нагрузки изменяются; МВЛ снижается. Газовый состав крови не изменен (недостатка кислорода в организме нет), функция кровообращения и КОС в норме.
При дыхательной недостаточности II степени одышка и тахикардия по-
Моп°ТСЯ ^*e П15И незначительном физическом напряжении. Показатели
щ» И ^^ отклонены от нормы, МВЛ значительно снижена. Выражен
ианоз. В альвеолярном воздухе снижается Ра0з и увеличивается РаСОг Со-
РЖание газов в крови благодаря перенапряжению вентиляции не измене-
но или незначительно изменено. Определяется дыхательный алкалоз. Могут быть первые проявления нарушения функции кровообращения.
При дыхательной недостаточности III степени одышка и тахикардия в покое; резко выражен цианоз. Значительно снижены показатели ЖЕЛ, а МВЛ невыполнима. Обязательны недостаточность кислорода в организме (гипоксемия) и избыток углекислоты (гиперкапния); при исследовании КОС выявляется дыхательный ацидоз. Выражены проявления сердечной недостаточности.
Понятия «дыхательная» и «легочная» недостаточность близки друг к другу, но понятие «дыхательная» недостаточность шире, чем «легочная», так как в него входит не только недостаточность внешнего дыхания, но и недостаточность транспорта газов от легких к тканям и от тканей к легким, а также недостаточность тканевого дыхания, развивающаяся при деком-пенсированном легочном сердце.
ЛС развивается на фоне дыхательной недостаточности II и, чаще, III степени. Симптомы дыхательной недостаточности сходны с таковыми при сердечной недостаточности, поэтому перед врачом стоит трудная задача их дифференциации и определения перехода компенсированного ЛС в декомпенсированное.
Компенсированное легочное сердце. На I этапе диагностического поиска выявить специфические жалобы невозможно, так как их не существует. Жалобы больных в этот период определяются основным заболеванием, а также той или иной степенью дыхательной недостаточности.
На II этапе диагностического поиска можно выявить прямой клинический признак гипертрофии правого желудочка — усиленную пульсацию, определяемую в прекордиальной области (в четвертом межреберье слева от грудины). Однако при выраженной эмфиземе, когда сердце оттеснено от передней грудной стенки эмфизематозно расширенными легкими, обнаружить указанный признак удается редко. В то же время при эмфиземе легких эпигастральная пульсация, обусловленная усиленной работой правого желудочка, может наблюдаться и при отсутствии его гипертрофии в результате низкого стояния диафрагмы и опущения верхушки сердца.
Аускультативных данных, специфичных для компенсированного ЛС, не существует. Однако предположение о наличии легочной гипертензии становится более вероятным при выявлении акцента или расщепления II тона над легочной артерией. При высокой степени легочной гипертензии может выслушиваться диастолический шум Грехема—Стилла. Признаком компенсированного ЛС считается также громкий I тон над правым трехстворчатым клапаном по сравнению с I тоном над верхушкой сердца. Значение этих аускультативных признаков относительно, так как они могут отсутствовать у больных с выраженной эмфиземой легких.
Решающим для диагностики компенсированного ЛС является III этап диагностического поиска, позволяющий выявить гипертрофию правых отделов сердца.
Значение различных инструментальных методов диагностики неодинаково.
Показатели функции внешнего дыхания отражают тип нарушения дыхания (обструктивный, рестриктивный, смешанный) и степень дыхательной недостаточности. Однако они не могут быть использованы для дифферен-цирации компенсированного ЛС и дыхательной недостаточности.
Рентгенологические методы позволяют выявить ранний признак ЛС — выбухание конуса легочной артерии (лучше определяется в 1 -м косом положении) и расширение ее. Тогда может быть отмечено умеренное увеличение правого желудочка.
Электрокардиография является наиболее информативным методом диаг-стики легочного сердца. Существуют убедительные «прямые» признаки яКГ гипертрофии правого желудочка и правого предсердия, коррелирующие со степенью легочной гипертензии: 1) Д,, в V, > 7 мм; 2) R/Sb отведе-и V > 1; 3) R\ +$v ^ 1°>5 мм; 4) время внутреннего отклонения в отве-I^iHV1 > 0,03—0,055с; 5) комплекс QR в отведении V, (при отсутствии мсЬаркта миокарда); 6) неполная блокада правой ножки пучка Гиса при R И отведении V, > 10 мм; 7) полная блокада правой ножки пучка Гиса при R в отведении V, > 15 мм; 8) инверсия зубца Г в отведении V,— V2.
При наличии двух и более «прямых» признаков на ЭКГ диагноз ЛС считается достоверным.
Большое значение имеет также выявление признаков гипертрофии правого предсердия: (P-pulmonale) во II и III, aVF и в правых грудных отведениях.
Фонокардиография может помочь в графическом выявлении высокой
амплитуды легочного компонента II тона, диастолического шума Грехе-ма—Стилла — признака высокой степени легочной гипертензии.
Существенное значение имеют бескровные методы исследования гемоди намики, по результатам которых можно судить о величине давления в легочной артерии:
1) определение давления в системе легочной артерии по длительности фазы изометрического расслабления правого желудочка, определяемой во время синхронной записи ЭКГ, ЦКГ и флебограммы яремной вены или кинетокардиограммы;
2) реопульмонография (наиболее простой и доступный для поликлинических условий метод), позволяющая по изменению апикально-базального градиента судить о нарастании гипертензии малого круга кровообращения.
В последние годы появились новые инструментальные методы, которые используются для ранней диагностики легочного сердца к ним относятся импульсная допплеркардиография, магнитно-резонансная томография и радио-нуклидная вентрикулография.
Самым достоверным способом выявления легочной гипертензии является измерение давления в правом желудочке и в легочной артерии с помощью катетера (в покое у здоровых людей верхний предел нормального систолического давления в легочной артерии равен 25—30 мм рт. ст.) Однако этот метод не может быть рекомендован как основной, так как его использование возможно лишь в специализированном стационаре.
Нормальные показатели систолического давления в легочной артерии в покое не исключают диагноза Л С. Известно, что уже при минимальных физических нагрузках, а также при обострении бронхолегочной инфекции и усилении бронхиальной обструкции оно начинает повышаться (выше 30 мм рт. ст.) неадекватно нагрузке. При компенсированном ЛС венозное Давление и скорость кровотока остаются в пределах нормы.
Декомпенсированное легочное сердце. Диагностика декомпенсированно-го ЛС, если имеются несомненные признаки правожелудочковой недостаточности, является несложной. Начальные стадии сердечной недостаточности при ЛС диагностировать затруднительно, так как ранний симптом сердечной недостаточности — одышка — не может служить подспорьем в данном случае, поскольку существует у больных ХНЗЛ как признак дыхательной недостаточности задолго до развития сердечной недостаточности.
Вместе с тем анализ динамики жалоб и основных клинических симптомов позволяет обнаружить начальные признаки декомпенсации ЛС.
98
99
На I этапе диагностического поиска выявляется изменение характера одышки: она становится более постоянной, меньше зависит от погоды. Увеличивается частота дыханий, но выдох не удлиняется (удлиняется лишь при бронхиальной обструкции). После кашля интенсивность и длительность одышки возрастают, она не уменьшается после приема бронхо-дилататоров. Одновременно нарастает легочная недостаточность, достигая III степени (одышка в покое). Прогрессирует утомляемость и снижается трудоспособность, появляются сонливость и головные боли (результат гипоксии и гиперкапнии).
Больные могут жаловаться на боли в области сердца неопределенного характера. Происхождение этих болей достаточно сложно и объясняется сочетанием ряда факторов, в том числе метаболическими нарушениями в миокарде, гемодинамической перегрузкой его при легочной гипертензии, недостаточным развитием коллатералей в гипертрофированном миокарде.
Иногда боли в сердце могут сочетаться с выраженным удушьем, возбуждением, резким общим цианозом, что характерно для гипертонических кризов в системе легочной артерии. Внезапный подъем давления в легочной артерии объясняется раздражением барорецепторов правого предсердия, повышенным давлением крови в правом желудочке.
Жалобы больных на отеки, тяжесть в правом подреберье, увеличение размеров живота при соответствующем (чаще всего хроническом) легочном анамнезе позволяют заподозрить декомпенсированное ЛС.
На II этапе диагностического поиска выявляется симптом постоянно набухших шейных вен, так как после присоединения к легочной еще и сердечной недостаточности шейные вены набухают не только на выдохе, но и на вдохе. На фоне диффузного цианоза (признак легочной недостаточности) развивается акроцианоз, пальцы и кисти рук становятся холодными на ощупь. Отмечаются пастозность голеней, отеки нижних конечностей.
Появляется постоянная тахикардия, причем в покое этот симптом более выражен, чем при нагрузке. Определяется выраженная эпигастральная пульсация, обусловленная сокращениями гипертрофированного правого желудочка. При дилатации правого желудочка может развиться относительная недостаточность предсердно-желудочкового клапана, что обусловливает появление систолического шума у мечевидного отростка грудины. По мере развития сердечной недостаточности тоны сердца становятся глухими. Возможно повышение АД вследствие гипоксии.
Следует помнить об увеличении печени как раннем проявлении недостаточности кровообращения. Печень может выступать из-под края реберной дуги у больных с эмфиземой и без признаков сердечной недостаточности. При развитии сердечной недостаточности в начальных стадиях выявляется увеличение преимущественно левой доли печени, пальпация ее чувствительна или болезненна. По мере нарастания симптомов декомпенсации выявляется положительный симптом Плеша.
Асцит и гидроторакс наблюдаются редко и, как правило, при сочетании ЛС с ИБС или гипертонической болезнью II—III стадии.
III этап диагностического поиска имеет меньшую значимость в диагностике декомпенсированного ЛС.
Рентгенологические данные позволяют выявить более выраженное увеличение правых отделов сердца и патологию легочной артерии: 1) усиление сосудистого рисунка корней легких при относительно «светлой периферии»; 2) расширение правой нисходящей ветви легочной артерии — важнейший рентгенологический признак легочной гипертензии; 3) усиление пульсации в центре легких и ослабление ее в периферических отделах.
100
На ЭКГ — прогрессирование симптомов гипертрофии правых желудочка и предсердия, часто блокада правой ножки предсердно-желудочкового пучка (пучка Гиса), нарушения ритма (экстрасистолы).
При исследовании гемодинамики обнаруживают нарастание давления в легочной артерии (выше 45 мм рт. ст.), замедление скорости кровотока, повышение венозного давления. Последнее у больных ЛС свидетельствует о присоединении сердечной недостаточности (этот симптом не является ранним).
В анализах крови могут выявляться эритроцитоз (реакция на гипоксию), повышение показателя гематокрита, увеличение вязкости крови, в связи с чем СОЭ у таких больных может оставаться нормальной даже при активности воспалительного процесса в легких.
Диагностика ЛС. При постановке диагноза компенсированного ЛС решающая роль принадлежит выявлению гипертрофии правых отделов сердца (желудочка и предсердия) и легочной гипертензии, в диагностике декомпенсированного ЛС основное значение, помимо этого, имеет выявление симптомов правожелудочковой сердечной недостаточности.
Формулировка развернутого клинического диагноза учитывает: 1) основное заболевание, приведшее к формированию ЛС; 2) дыхательную недостаточность (степень выраженности); 3) легочное сердце (стадия): а) компенсированное; б) декомпенсированное (указывается степень выраженности правожелудочковой недостаточности, т.е. ее стадия).
Лечение. Комплекс лечебных мероприятий включает в себя воздействие: 1) на заболевание, являющееся причиной развития Л С (так как наиболее частой причиной является ХНЗЛ, то в период обострения воспалительного процесса в бронхолегочной системе применяют антибиотики, сульфаниламидные препараты, фитонциды — тактика лечения антибактериальными средствами описана в предыдущих разделах); 2) на звенья патогенеза ЛС (восстановление нарушенной вентиляции и дренажной функции бронхов, улучшение бронхиальной проходимости, снижение легочной гипертензии, устранение правожелудочковой недостаточности).
• Улучшению бронхиальной проходимости способствует уменьшение воспаления и отека слизистой оболочки бронхов (антибиотики, ГКС, вводимые интратрахеально) и ликвидация бронхоспазма (симпатомиметиче-ские средства; эуфиллин, особенно его препараты пролонгированного действия; холинолитические средства и блокаторы кальциевых каналов).
• Бронхиальному дренажу способствуют средства, разжижающие мокроту, отхаркивающие средства, а также постуральный дренаж и специальный комплекс лечебной физкультуры.
• Восстановление бронхиальной вентиляции и улучшение бронхиальной проходимости приводят к улучшению альвеолярной вентиляции и нормализации кислородтранспортной системы крови.
Основную роль в улучшении вентиляции играет газовая терапия, включающая: а) оксигенотерапию (под контролем газов крови и показателей кислотно-основного состояния), в том числе длительную ночную терапию с 30 % содержанием кислорода во вдыхаемом воздухе; при необходимости используется гелий-кислородная смесь; б) терапию с вдыханием С02 при Резком его снижении в крови, что возникает при выраженной гипервентиляции.
По показаниям больной осуществляет дыхание с положительным давлением в конце выдоха (вспомогательная ИВЛ или регулятор искусственного дыхания — небулятор Люкевича). Применяется специальный комплекс дыхательной гимнастики, направленный на улучшение легочной вентиляции.
1П1
В настоящее время при лечении дыхательной недостаточности III степени с успехом применяют новый дыхательный аналептик — арманор, способствующий увеличению напряжения кислорода в артериальной крови за счет стимуляции периферических хеморецепторов.
Нормализация кислородтранспортной системы крови достигается: а) увеличением поступления кислорода в кровь (гипербарическая ок-сигенация); б) повышением кислородной функции эритроцитов с помощью экстракорпоральных методов (гемосорбция, эритроцитоферез и т.п.); в) усилением отщепления кислорода в тканях (нитраты).
• Снижение давления в легочной артерии достигается различными
способами: введением эуфиллина, салуретиков, блокаторов альдостерона,
а-адреноблокаторов, блокаторов ангиотензинпревращающего фермента и
особенно антагонистов рецепторов ангиотензина И. Определенную роль в
снижении давления в легочной артерии играют препараты, замещающие
релаксирующий фактор эндотелиального происхождения (молсидамин,
корватон). Большую роль играет воздействие на микроциркуляторное рус
ло, осуществляемое с помощью ксантинола никотината, действующего на
сосудистую стенку, а также гепарина, курантила, реополиглюкина, оказы
вающих благотворное действие на внутрисосудистое звено гемостаза. Воз
можно проведение кровопусканий (при наличии эритроцитоза и других
проявлений плеторического синдрома).
• Воздействие на правожелудочковую недостаточность проводится со
гласно основным принципам лечения сердечной недостаточности: моче
гонные, антагонисты альдостерона, периферические вазодилататоры (эф
фективны пролонгированные нитраты). Вопрос о применении сердечных
гликозидов решают индивидуально.
Прогноз. Неблагоприятным прогноз становится при появлении признаков декомпенсации сердца и зависит от стадии сердечной недостаточности. Он более благоприятен при положительном эффекте от внутривенного введения эуфиллина и во многом определяется этиологией ЛС.
Профилактика. С целью предупреждения развития ЛС следует проводить активное лечение основных заболеваний: ХНЗЛ, васкулитов, ожирения и других, вести активную профилактику тромбоэмболии легочной артерии (адекватная терапия тромбофлебитов вен нижних конечностей) и т.д.
Контрольные вопросы и задачи
Выберите один, наиболее правильный ответ на вопросы 1—30.
1. У тяжелобольного 50 лет с высокой температурой тела, отхаркивающего гнойно-кровянистую мокроту, на рентгенограмме легких справа выявлено несколько тонкостенных полостей с уровнем жидкости. Лейкоцитоз крови 18 109/л со сдвигом лейкоцитарной формулы влево. Следует думать о: А. Казеозной пневмонии. Б. Микоплазменном воспалении легких. В. Поликистозе легких (нагноившемся). Г. Стафилококковой пневмонии. Д. Пневмококковой пневмонии.
2. К осложнениям долевой пневмонии относится все перечисленное, кроме: А. Затяжного рассасывания воспалительного процесса. Б. Септицемии. В. Менин-гизма. Г. Эмпиемы плевры. Д. Пневмоторакса.
3. Антибиотиками, с которых следует начинать лечение пневмонии, вызванной грамположительной флорой, являются: А. Тетрациклин. Б. Стрептомицин. В. Пенициллин. Г. Эритромицин. Д. Левомицетин.
4. При интерстициальной пневмонии, вызванной микоплазмами, антибиотиками выбора являются: А. Стрептомицин. Б. Пенициллин. В. Эритромицин. Г. Левомицетин. Д. Канамицин.
5. Мужчина 50 лет, злоупотребляющий алкоголем, внезапно заболел: высокая температура тела, кашель с вязкой темной мокротой; при рентгенологическом 102
обследовании отмечается затемнение верхней доли правого легкого. Наиболее вероятный диагноз: А. Пневмококковая пневмония. Б. Стафилококковая пневмония, о фридлендеровская пневмония. Г. Микоплазменная пневмония. Д. Пневмония, вызванная смешанной флорой.
6. Жизненную емкость легких составляет все перечисленное, кроме: А. Емкость вдоха. Б. Резервный объем выдоха. В. Дыхательный объем. Г. Остаточный объем. д функциональная остаточная емкость легких.
7. Диагностика хронического бронхита вытекает из констатации: А. Длительного кашля. Б. Явлений бронхоспазма. В. Эмфиземы легких. Г. Признаков инфекции слизистой оболочки бронхов. Д. Спирографических показателей дыхательной недостаточности.
8. Хронический бронхит следует лечить антибиотиками: А. В осенне-зимний период. Б. Длительно. В. Если мокрота слизистая. Г. В периоды выделения гнойной мокроты. Д. Антибиотики не следует применять вообще.
9. Из перечисленных препаратов муколитиком не является: А. Ацетилцистеин. Б. Йодид калия. В. Фенолфталеин. Г. Трипсин. Д. Мукалтин.
10. Основанием для дифференциальной диагностики хронического бронхита и бронхоэктазий является: А. Физикальное обследование больного. Б. Рентгенограмма легких. В. Бронхоскопия. Г. Бронхография. Д. Спирография.
11. Показанием к хирургическому лечению бронхоэктазий являются: А. Двусторонние диффузные бронхоэктазий, осложненные легочным сердцем. Б. Бронхоэк-тазы в пределах одной доли, осложненные кровотечениями. В. Осложненные брон-хоэктазы при хронической дыхательной недостаточности. Г. Субклинические брон-хоэктазы в пределах одного сегмента. Д. Двусторонние бронхоэктазы с поражением долей легкого.
12. Длительное кровохарканье при сухом кашле заставляет прежде всего подозревать: А. Рак бронха. Б. Кавернозную форму туберкулеза легких. В. Бронхоэктати-ческую болезнь. Г. Пневмокониоз. Д. Хроническую пневмонию.
13. При ХНЗЛ с главным признаком обструктивной эмфиземы легких функциональные исследования позволяют установить: А. Снижение сопротивления в воздухоносных путях. Б. Увеличение максимальной вентиляции легких. В. Снижение односекундной жизненной емкости выдоха (индекс Тиффно). Г. Увеличение жизненной емкости легких. Д. Уменьшение остаточного объема.
14. При бронхиальной астме атопической формы главную роль играют следующие аллергические реакции: А. Тип I — реагиновый. Б. Тип II — цитотоксический. В. Тип III — феномена Артюса и тип IV — замедленной аллергии. Г. Тип I — реагиновый и тип II — цитотоксические реакции. Д. Все типы аллергии.
15. Бронхиальной астме сопутствует: А. Гиперчувствительность (3-адренергиче-ской системы. Б. Блокады сс-адренергической системы. В. Гипотония холинергиче-ской системы. Г. Нарушение равновесия а- и р-адренергических систем. Д. Преобладание активности (^-рецепторов.
16. Одной из частых причин тахикардии у больного в астматическом состоянии является: А. Увеличение Рсо2 в крови. Б. Нарушение кислотно-основного состояния. В. Злоупотребление (3-адреностимуляторами в аэрозоле. Г. Передозировка сердечных гликозидов. Д. Передозировка папаверина.
17. Экссудативный плеврит может осложнить: А. Туберкулез легких. Б. Неспецифические воспалительные процессы в легких. В. Опухоли яичников. Г. Инфаркт легкого. Д. Все заболевания.
18. Сальбутамол (вентолин) расширяет бронхи путем: А. Блокирования а-ре-Цепторов бронхиального дерева. Б. Почти селективного возбуждения Рг-адреноре-Цепторов. В. Непосредственного влияния на гладкую мускулатуру. Г. Снижение тонуса блуждающего нерва. Д. Блокирования гистамина.
19. Противопоказанием к кортикостероидной терапии бронхиальной астмы являются все заболевания, кроме: А. Обострения язвенной болезни. Б. Сахарного Диабета. В. Обострения ревматического процесса. Г. Тяжелого остеопороза. Д. Артериальной гипертонии.
20. Геморрагическая жидкость в полости плевры выявляется при: А. Плеврите туберкулезной этиологии. Б. Эмпиеме плевры. В. Бластоматозном процессе. Г. Недостаточности кровообращения. Д. Циррозе печени.
21. Жидкость в плевральной полости ведет к: А. Смещению органов средостения в больную сторону. Б. Усилению дыхательных шумов. В. Высокому стоянию
 |  |
Ревматизм (ревматическая лихорадка) РЕВМАТИЗМ (РЕВМАТИЧЕСКАЯ ЛИХОРАДКА) - системное воспалительное заболевание соединительной ткани с преимущественной локализацией процесса в сердечно-сосудистой системе, развивающееся у предрас- |
диафрагмы. Г. Втягиванию межреберий при вдохе. Д. Исчезновению голосового дрожания.
22. Очень быстрое повторное накопление жидкости в полости плевры — типичный признак: А. Хронической недостаточности кровообращения. Б. Мезотелиомы плевры. В. Аденокарциномы бронха. Г. Туберкулеза легких. Д. Системной красной волчанки.
23. Пространство Траубе исчезает при: А. Левостороннем экссудативном плеврите. Б. Эмфиземе легких. В. Гипертрофии правого желудочка сердца. Г. Перфорации язвы желудка. Д. Бронхоэктазиях.
24. Выявление малых объемов жидкости или осумкованной жидкости в плевральной полости эффективнее всего при помощи: А. Рентгенологического метода. Б. Бронхоскопии. В. Игольной биопсии плевры. Г. Ультразвукового метода. Д. Фи-зикального исследования.
25. При осложнении острой пневмонии экссудативным плевритом показано все, кроме: А. Смены антибиотика. Б. Назначения бутадиона. В. Электрофизиолечения. Г. Дренажа плевральной полости. Д. Оксигенотерапии.
26. Дыхательную недостаточность диагностировать правильнее всего на основании: А. Анамнеза. Б. Физикального обследования больного. В. Рентгенологического исследования грудной клетки. Г. Исследования газового состава артериальной крови. Д. Спирографического исследования.
27. Физикальные признаки больных с эмфиземой включают следующие, за исключением: А. Усиления бронхофонии. Б. Выраженного акцента II тона на легочной артерии. В. Узкого эпигастрального угла. Г. Удлиненного выдоха. Д. Коробочного легочного звука.
28. Инактивация сурфактанта способствует развитию: А. Эмфиземы легких.
Б. Ателектаза легочной ткани. В. Отека легких. Г. Гипертензии в малом круге кро
вообращения. Д. Бронхиальной астмы.
29. Самым ценным методом, определяющим легочную гипертензию, является: А. Центральное венозное давление. Б. ЭКГ. В. Катетеризация легочной артерии. Г. Определение давления в правом желудочке. Д. Фонокардиография.
30. Альвеолярно-капиллярный рефлекс заключается в: А. Спазме альвеол в ответ на появление в капиллярной крови гистамина. Б. Спазме капилляров в ответ на появление в просвете альвеолы аллергена. В. Уменьшении объема альвеолы в ответ на гиперкапнию в прилегающих капиллярах. Г. Спазме сосудов гиповентилируемой части легких. Д. Расширении сосудов в гиповентилируемой части легких.
В вопросах 31—35 выберите наилучшую комбинацию ответа, пользуясь схемой: А — если верно 1, 2, 3. Б — если верно 1 и 3. В — если верно 2 и 4. Г — если верно только 4. Д — если все верно.
31. Легочная гипертензия встречается при: 1. Врожденных пороках сердца.
2. Стенозе митрального отверстия. 3. Хронических заболеваниях легких. 4. Эмфизе
ме легких.
32. При хронической дыхательной недостаточности наблюдаются: 1. Эритроци-тоз. 2. Увеличение концентрации гемоглобина. 3. Увеличение объема циркулирующей крови. 4. Ускорение кровотока в капиллярах.
33. Бронхиальную астму атопического вида характеризуют реакции: 1. Реакция гиперчувствительности замедленного типа. 2. Цитотоксическая реакция. 3. Реакция типа Артюса. 4. Реакция анафилактического типа.
34. При астматическом состоянии комплекс лечебных мероприятий должен включать: 1. Ингаляции кислорода и ощелачивание. 2. Глюкокортикостероиды.
3. Гидратацию. 4. Симпатомиметики.
35. Эмфизема легких характеризуется: 1. Уменьшением жизненной емкости лег
ких. 2. Увеличением дыхательного сопротивления. 3. Нарушением соответствия
вентиляции перфузии. 4. Увеличением индекса Тиффно.
В вопросе 36 приведены симптомы (1, 2, 3...) и диагнозы (А, Б, В...), выберите правильные комбинации «вопрос—ответ» (симптом—диагноз).
36. Вопрос: 1. Ритм галопа. 2. Диффузный цианоз. 3. Увеличение левого желу
дочка. 4. Увеличение печени. 5. Увеличение левого предсердия. 6. Спадение шей
ных вен. 7. Эритроцитоз. 8. Увеличение венозного давления. 9. Акроцианоз.
10. Увеличение давления в легочной артерии. Ответ: А. Хроническое легочное серд
це. Б. Митральный стеноз. В. Оба заболевания. Г. Ни одно из них.
Глава II
Дата: 2018-12-28, просмотров: 459.