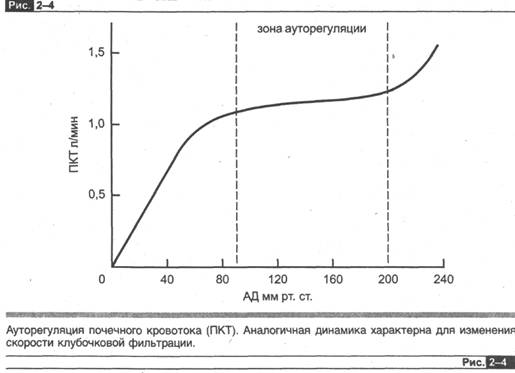
Взгляните еще раз на уравнение (2-1). Это уравнение предполагает, что если градиент давления увеличивается на 50 %, то кровоток увеличивается также на 50 %. В почке тем не менее так не происходит, поскольку в почечной циркуляции совершенно отчетливо имеет место феномен саморегуляции: почечный кровоток остается относительно постоянным в ответ на изменение среднего почечного артериального давления с диапазоном колебаний примерно от 85 до 200 мм рт. ст. (рис. 2-4).
Например, если в эксперименте изолировать почку и перфузировать ее кровью с помощью насоса, то можно продемонстрировать, что увеличение почечного артериального давления на 50 % (допустим, от 100 до 150 мм рт. ст.) ведет к увеличению почечного кровотока менее чем на 10 %. Как может быть выведено из уравнения (2-1), существует только одно возможное объяснение данного факта: сопротивление в почке должно также возрастать по мере увеличения артериального давления. Гладкая мускулатура почечных артериол сокращается в большей степени за счет этого, уменьшая радиус артериол и увеличивая артериальное сопротивление. Поэтому почечный кровоток остается относительно неизменным, несмотря на увеличение артериального давления.
Эта общая дискуссия имеет отношение не только к почечному кровотоку, но и к скорости клубочковой фильтрации, которая только слабо реагирует на выраженные изменения артериального давления. Главный довод в пользу того, что почечный кровоток, так же как и скорость клубочковой фильтрации, поддается
| 51 |
саморегуляции, заключается в том, что афферентные артериолы являются главной зоной изменений сосудистого сопротивления, связанного с ауторегуляцией. Вот почему капиллярное давление в гломерулах и результирующее фильтрационное давление остаются относительно неизменными. Другими словами, увеличение почечного артериального давления стимулирует сокращение афферентной артериолы, тем самым увеличивая перепад давления между артериями и гломеруляр-ными капиллярами и предотвращая передачу увеличенного артериального давления на русло гломерулярных капилляров. Посредством какого механизма увеличение почечного артериального давления поддерживает усиленный спазм гладкой мускулатуры афферентных артериол? Одна вещь хорошо известна: данный механизм является полностью внутрипочечным, если он может работать в условиях изолированной почки, перфузируемой т уйто. Два внутрипочечных механизма в настоящее время считаются ответственными за ауторегуляцию: (1) миогенный механизм; и (2) клубочково-канальцевая обратная связь.
Миогенный механизм аналогичен тому, который обнаружен в других (непочечных) участках сосудистого русла, поддающихся саморегуляции: сосудистая гладкая мускулатура сокращается в ответ на усиленное растяжение. Соответственно, увеличенное внутриартериолярное давление растягивает стенки артериолы, т. е. увеличивает ее пассивное напряжение, а ответной реакцией гладкой мускулатуры сосудистой стенки является реакция сокращения, в результате чего уве- личивается сосудистое сопротивление.
В сравнении с миогенным механизмом канальцево-клубочковая обратная связь является более сложным процессом, который прежде всего регулирует ско-
52
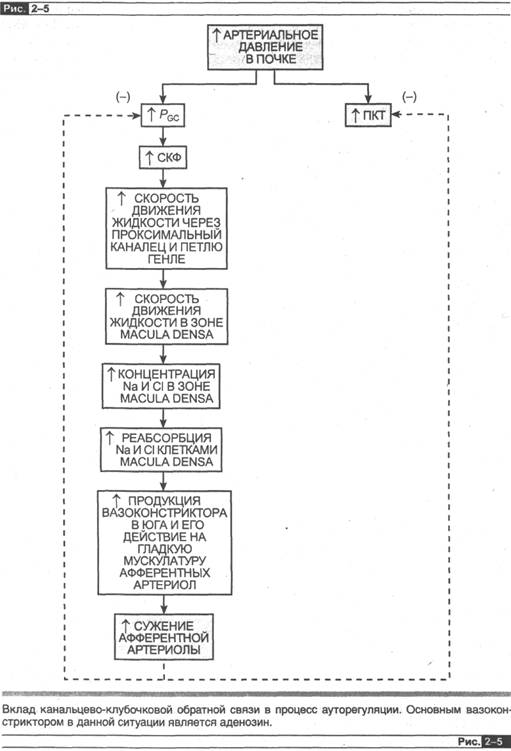
рость клубочковой фильтрации с изменением в почечном кровотоке в качестве побочного действия. Основной путь регуляции представлен на рис. 2-5. (Как введение к этой дискуссии, читатель при необходимости может ознакомиться с анатомией юкстагломерулярного аппарата (ЮГА) в главе 1.) Увеличенное артериальное давление стимулирует рост как капиллярного давления в гломерулах (Рсс)» так и почечного кровотока. Увеличение Рсс ведет к возрастанию скорости клубочковой фильтрации и отсюда скорости тока жидкости через проксимальный каналец и петлю Генле, включая зону таси!а о!епза — группу клеток дисталь-цого участка толстой восходящей части петли Генле. Как результат увеличения тока жидкости через зону таси!а с1епза (см. ниже и рис. 2-5 по поводу механизма, посредством которого «выявляется» поток жидкости), химический вазоконстрик-тор образуется в ЮГА. Этот вазоконстриктор стимулирует гладкую мускулатуру прилежащих афферентных артериол; в результате чего возрастает сопротивление афферентной артериолы, что вызывает снижение Рсс и скорости клубочковой фильтрации9,. так же как и почечного кровотока, возвращая его к первоначальному значению. Другими словами, сужение артериол существенно уменьшает диапазон колебаний (в сторону увеличения) скорости клубочковой фильтрации и ПКТ, что в противном случае будет вызвано повышением почечного артериального давления.
Теперь давайте вернемся назад и обсудим более детально некоторые механизмы, которые лежат в основе канальцево-клубочковой обратной связи. Первое, каким образом таси!а с!епза «выявляет» изменение скорости тока жидкости. Ответ будет следующий (рис. 2-5). Поскольку толстая восходящая часть петли Генле активно реабсорбирует ионы натрия и хлора, но не воду (это будет детально описано в главе 6), то концентрация этих двух ионов в просвете канальца всегда ниже, чем соответствующие величины в плазме, и существует прямая взаимосвязь между скоростью тока жидкости внутри просвета и концентрацией ионов — чем быстрее скорость тока жидкости, тем выше концентрация хлорида натрия. Это повышение концентрации в свою очередь стимулирует таси!а о^епза к реабсорб-ции больших количеств натрия и хлора10, и именно данная повышенная реаб-сорбция каким-то образом увеличивает продукцию фактора, вызывающего вазо-констрикцию и воздействующего на афферентные артериолы.
Какова особенность вазокостриктора в описываемой системе? Аденозин, который суживает афферентные артериолы, в отличие от его вазодилятирующего эффекта на другие участки сосудистого русла в организме, является наиболее важным медиатором11.
Примеры, используемые для иллюстрации миогенного и канальцево-клубоч-кового механизмов для процесса ауторегуляции, показывают, что увеличение почечного артериального давления — начальное событие (первичный толчок). Сни жение артериального давления (в пределах эффективности ауторегуляции) также нейтрализуется процессом саморегуляции: снижение растяжения гладкой мускулатуры афферентной артериолы гладкой мускулатуры вызывает релаксацию, т. е. меньшее сужение и уменьшение потока жидкости через зону таси!а (1епза вызывает меньшую продукцию аденозина в ЮГА (и, возможно, увеличенную продукцию соответствующего вазодилататора — см. примечание11).
Каковы адаптивные возможности процесса ауторегуляции? Как в любом другом саморегулирующемся органе, данный процесс помогает предотвратить значительные изменения кровотока при колебании артериального давления. Но у него
53
54
Почечный кровоток и клубочковая фильтрация
(у процесса) есть еще и вторая роль в почке, а именно предотвращение больших колебаний экскреции воды и растворенных веществ, которые в противном случае будут иметь место из-за значительных колебаний скорости клубочковой фильтрации, если артериальное давление будет изменяться. В этом и заключается адаптивная роль ауторегуляции скорости клубочковой фильтрации. Напомним, что в норме результирующее фильтрационное давление в гломеруле составляет только около 17 мм рт. ст. Соответственно даже относительно небольшие изменения артериального давления, вызывающие существенную динамику величины капиллярного давления в гломерулах, скорости клубочковой фильтрации и объема экскреции воды и растворенных веществ, были следствием неэффективной регуляции за счет саморегулирующих изменений тонуса афферентной артериолы.
В связи с этим следует отметить, что, хотя мы использовали понятие каналь-цево-клубочковой обратной связи при обсуждении темы механизма ауторегуляции, данный процесс обратной связи важен в ситуациях, характеризующихся не изменением артериального давления, но в большей степени при обусловленной болезнью или лекарством блокаде реабсорбции жидкости в проксимальном канальце 12. В таких условиях результирующее увеличение активности триггеров в mасulа dеnsа, благодаря обычной последовательности событий, реагирующих на поток жидкости, приводит к уменьшению скорости клубочковой фильтрации и тем самым снижает потерю с мочой солей и воды в результате нарушения реабсорбции. Обратите внимание, что в этих случаях канальцево-клубочковая обратная связь действительно вызывает снижение скорости клубочковой фильтрации, в то время как в процессе ауторегуляторной реакции данная обратная связь предохраняет скорость клубочковой фильтрации от существенных колебаний.
Подчеркнув важность процесса ауторегуляции, мы теперь должны отметить три факта. (1) Даже в пределах ауторегуляционной деятельности этот процесс не является совершенным; ПКТ и скорость клубочковой фильтрации действительно изменяются при колебаниях почечного артериолярного давления, но гораздо в меньшей степени, чем это могло бы иметь место, если бы процесс ауторегуляции не существовал (рис. 2-4). (2) Ауторегуляция реально отсутствует при среднем артериальном давлении ниже 70 мм рт. ст. и поэтому не может тормозить колебания скорости клубочковой фильтрации и ПКТ ниже этой границы, что является важным моментом для почечной деятельности во время выраженной системной артериальной гипотонии. (3) Несмотря на ауторегуляцию, почечный кровоток и скорость клубочковой фильтрации (в меньшей степени) могут существенно коле баться, даже когда артериальное давление не выходит за пределы ауторегуляци-онного коридора, за счет воздействия нейроэндокринных факторов — в особенности симпатическая нервная система и ангиотензин II — что будет описано в двух последующих разделах.
Из-за последнего указанного фактора мы создаем условия искусственного эксперимента по проблемам упомянутой выше дискуссии по ауторегуляции, когда почечное артериальное давление изменялось без динамики системного артериального давления в организме (аналогичный случай может быть у человека с обструкцией почечной артерии). Такие эксперментальные условия необходимы для демонстрации «чистой» ауторегуляции, поскольку, когда системное артериальное давление снижается во всем интактном организме, нейроэндокринные рефлексы вовлекаются в игру, что маскирует наличие ауторегуляции.
Дата: 2018-09-13, просмотров: 914.