Фосфаты. В цельной крови большая часть фосфора находится в эритроцитах в виде органического фосфата, в плазме крови присутствуют липидный фосфор, следы эфи-ров фосфорной кислоты и неорганический фосфат. 5О%общего фосфора находится в костях, до 20% — во внекле-точной жидкости. Фосфаты играют важную роль в обмен-ных процессах: входят в состав коферментов, нуклеино-вых кислот, фосфопротеинов, фосфолипидов. Из них об-разуются: 2,3-ДФГ, играющий важную роль в регуляции транспорта кислорода, фосфаты — обязательный компон-ент клеточных мембран; составная часть АТФ, креатин- фосфата — выполняющих важную роль в переносе и со-хранении энергии. Вместе с кальцием фосфаты образуют аппетиты — основу костной ткани. Регуляция обмена фосфора аналогична обмену кальция с тем различием, что паратгормон, повышающий содержание кальция в плаз-ме крови, снижает содержание фосфатов, повышая их Экскрецию почками.
Кальций. В.организме содержится 1-1,5кг каль-ция. Внеклеточный ион. Содержание в плазме — 2,29-2,99 ммоль/л, в эритроцитах — следы. 90% находится в костях, 1% — во внеклеточной жидкости. Меньше поло-вины кальция в плазме крови находится в ионизирован-ном виде и является физиологически активным, большая часть —связана с белками или представлена солями: фос-фатом, цитратом, сульфатом кальция. Наибольшей каль-цийсвязывающей способностью обладают альбумины и в-глобулины.
Ионы кальция, участвуя во многих процессах жи-знедеятельности, действуют на уровне клетки и на уровне внеклеточных систем. Его биологическая роль:
— необходим для секреторной активности практичес-ки всех эндо- и экзокринны:х железистых клеток;
— участвует в свертывании крови;
— является вторичным посредником при мембранной передаче сигнала, активируя 40 ферментов;
— выполняет опорную ф-ию явл. Основным компонентом костного скелета
— обеспечивает целостность мембран (влияет на прони-цаемость), так как способствует плотной упаковке бел-ков, стабилизируя клеточные мембраны;
— участвует в нервно-мышечном возбуждении и сокра-щении; Кальций принимает. Участие в создании по-тенциала покоя (7О — 9О мВ), уменьшая скорость про-никновения положительно заряженных ионов в клетку
— стимулирует выработку гастрина, обусловливая вы-работку пищеварительных соков;
Многообразные функции ионов кальция на поверх-ности и внутри клетки обусловлены его способностью со-единяться с немембранными комплексами — АТФ, фос-фатами, белками.
Са вместе с инсулином облегчает поступление глю-козы в клетки. Основные биологические процессы: раз-множение,пролиферация, гибель клетки, — осуществ-ляются при участии кальция.
Содержание ионов кальция в плазме крови опреде-ляют следующие механизмы:
1. Состояние костной ткани — все факторы, ускоряю-щие рассасывание костей, увеличивают содержание кальция и фосфатов в крови за счет деминерализа-ции скелета (резорбции, мобилизации из кости). Все факторы, способствующие образованию костной тка-ни уменьшают его за счет минерализации.
2. Витамин D3 и его аналоги способствуют всасыванию кальция и фосфатов в кишечнике и препятствуют их выведению с мочой.
3. Паратгормон стимулирует мобилизацию кальция и фосфатов из костей, на уровне почек усиливает реаб-сорбцию кальция и уменьшает реабсорбцию фосфа-тов, повышает содержание ионов кальция в плазме.
4. Кальцитонин способствует минерализации костей, увеличивает экскрецию фосфатов с мочой, снижает содержание ионов кальция в плазме.
5. КOC. Ацидоз приводит к рассасывания костей (со-держание кальция возрастает) алкалоз-к их минерализации (уменьш. концентрация ионов каль-ция в плазме).
Регуляцию обменов фосфора и кальция осуществля-ют паращитовидные, щитовидные железы через декрети-руемые ими гормоны; кальцитонин, паратгормон, а так-же витамин D3 и кальцитриол.
Паратгормон. Гормон-полипептид, состоящий из 84 аминокислотных остатков. Секретируется клетками па-ращитовидной железы в ответ на уменьшение концентра-ции ионов кальция в крови. Основными клетками-мише-нями для паратгормона являются клетки костей, почек, тонкой кишки (действует опосредованно через усиление биосинтеза кальцитриола). Паратгормон действует на клетки-мишени через ц-АМФ и протеинкиназы.
Паратгормон стимулирует резорбцию костной ткани с освобождением кальция за счет активации ферментов остеокластов, разрушающих промежуточное вещество ко-сти. В почках, в клетках дистальных канальцев, стиму-лирует реабсорбцию ионов кальция из первичной мочи, но ингибирует реабсорбцию фосфатов, и они выводятся из организма. Таким образом, действуя на кости и почки,-паратгормон увеличивает концентрацию кальция (это активирует секрецию кальцитонина) и уменьшает уровень фосфатов в крови.
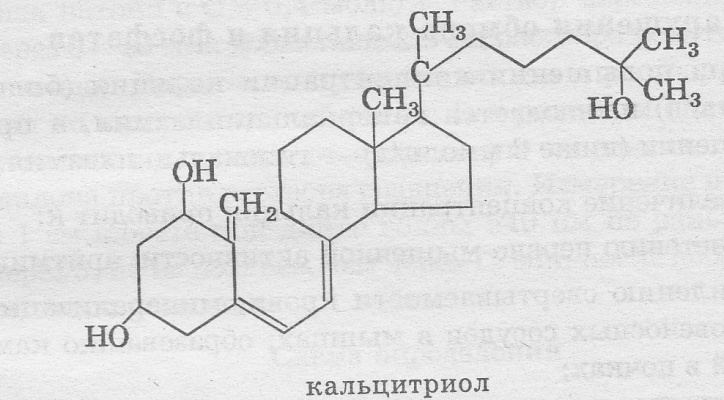
КАЛЬЦИТРИОЛ
Химическая природа — производное циклопентанпергидрофенантрена.
Клетками-мишенями являются клетки почек, костей, кишечника.
Вырабаты-вается при уменьшении концентрации кальция в крови и усилении секреции паратгормона. Его предшественником является витамин Д3 который гидроксилируется в пече-ни (фермент 25-гидроксилаза), затем в почках (1-гидро-ксилаза). С места синтеза (в почках) он транспортируется кровью в кишечник, где в клетках слизистой стимулиру-ет синтез кальций-связывающего белка. Он располагается на поверхности клеток слизистых и, благодаря своей высокой способности связывать кальций, облегчает его всасывание. Из клетки кальций попадает в кровоток по-средством действия Са"/Na' — АТФ-азы.
На костную ткань кальцитриол действует аналогич-но паратгормону: активируя ферментную систему остеокластов, вызывает деминерализацию кости и увеличива-ет концентрацию кальция и фосфатов в крови. В клетках дистальных канальцев почек он усиливает реабсорбцию кальция и фосфатов. Результатом действия кальцитрио-ла является: увеличение концентрации кальция и фосфа-тов в крови, ингибирование секреции паратгормона.
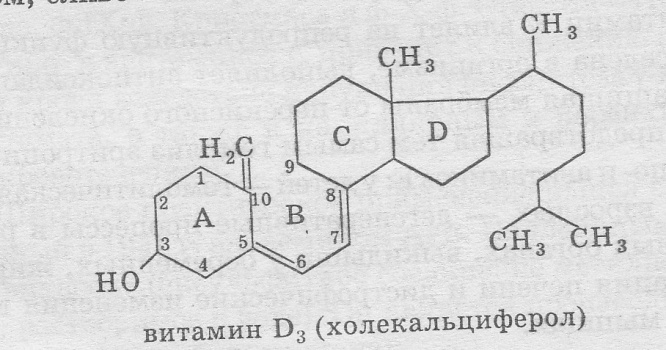
ВИТАМИН Д3
Витамин Д3 (антирахитический) по химической при-роде представляет собой -холекальциферол (производное циклопентанопергидрофенантрена), суточная потребность которого в организме человека составляет О,025 мг. Из витамина D3 под действием 25-гидроксилазы (в печени) и 1-гидроксилазы (в почках) синтезируется гормон кальци-триол, регулирующий обмен кальция и фосфора в орга-низме.
Источники
Витамин D образуется в коже под влиянием ультра-фиолетовых лучей из холестерина и поступает с рыбьим жиром, сливочным маслом .желтком яиц, печенью
Биологическая роль
Витамин D3 регулирует обмен кальция и фосфора в организме, участвуя в биосинтезе кальций-связывающе-го белка в слизистой желудочно-кишечного тракта, тем самым способствуя всасыванию ионов кальция и фосфора из пищи.
Гипо- и авитаминоз D3: в детском возрасте — рахит, у взрослых — снижение ионов Са в крови, что приво-дит к:
1) повышению нервно-мышечной возбудимости;
2) инактивации кальций-зависимых ферментов;
3) нарушению свертывания крови;
4) остеомаляции.
Вопрос 46.
Эритроциты лишены митохондрий, поэтому в качестве энергетического материала они могут использовать только глюкозу. В эритроцитах катаболизм глюкозы обеспечивает сохранение структуры и функции гемоглобина, целостность мембран и образование энергии для работы ионных насосов. Глюкоза поступает в эритроциты путём облегчённой диффузии с помощью ГЛЮТ-2. Около 90% поступающей глюкозы используется в анаэробном гликолизе, а остальные 10% - в пентозофосфатном пути.
Конечный продукт анаэробного гликолиза лактат выходит в плазму крови и используется в других клетках, прежде всего гепатоцитах. АТФ, образующийся в анаэробном гликолизе, обеспечивает работу Nа+, К+-АТФ-азы и поддержание самого гликолиза, требующего затраты АТФ в гексокиназной и фосфофруктокиназной реакциях (см. раздел 7).
Важная особенность анаэробного гликолиза в эритроцитах по сравнению с другими клетками - присутствие в них фермента бисфосфоглицератмутазы. Бисфосфоглицератмутаза катализирует образование 2,3-бисфосфоглицерата из 1,3-бисфосфоглицерата (рис. 14-3). Образующийся только в эритроцитах 2,3-бисфосфоглицерат служит важным аллостерическим регулятором связывания кислорода гемоглобином (см. раздел 1).
Глюкоза в эритроцитах используется и в пентозофосфатном пути, окислительный этап которого обеспечивает образование кофермента NADPH, необходимого для восстановления глу-татиона
Метгемоглобинредуктаза представляет собой комплекс нескольких систем ферментов эритроцитов, катализирующих восстановление метгемоглобина, постоянно образующегося в небольшом (не более 1%) количестве в эритроците, в гемоглобин. Эти системы используют глюкозу и молочный сахар в виде источников Н+ и связаны с редуцированными формами НАДН2 и НАДФН2.
Большую роль в защите клетки от свободных радикалов играют ферментативные антиоксиданты. Эритроциты содержат высокоактивную супероксиддисмутазу, которая осуществляет дисмутацию двух O2- с образованием перекиси водорода:
O2- + O2- Û H2O2 + O2
Образовавшаяся перекись водорода, являющаяся сильнейшим окислителем, частично нейтрализуется неферментативным путём при непосредственном участии аскорбата или других антиоксидантов (a-токоферол, глутатион восстановленный). Основное количество Н2О2 расщепляется в реакциях, катализируемых каталазой и глутатионпероксидазой:
Н2О2 + Н2О2 Þ 2Н2О + О2
Н2О2 + RH2 Þ 2Н2О + R
Важную роль в антиоксидантной системе эритроцитов играют легкоокисляющиеся пептиды, содержащие аминокислоты с SH-группой: метионин, цистеин. Особое место занимает глутатион – трипептид, образованный цистеином, глутаматом, глицином. В организме он присутствует в окисленной и восстановленной форме (GSH). Основной антиоксидантный эффект глутатион оказывает, участвуя в работе ферментативных антиоксидантов. Глутатион является ингибитором активированных кислородных радикалов и стабилизатором мембран. Это связано с тем, что SH- содержащие соединения подвергаются окислению в первую очередь, что предохраняет от окисления другие функциональные группы.
Вопрос 47.
Гемоглобин — сложный белок, хромопротеид, дыхательный пигмент крови человека, позвоночных и некоторых
беспозвоночных животных. Основная функция гемоглобина — перенос кислорода от органов дыхания к тканям.
Химически гемоглобин относится к группе хромопротеидов. Молекула гемоглобина состоит из белковой части —
глобина и простетичной группы небелковой природы — гема, в состав которого входит железо. В одной молекуле
гемоглобина содержится 4 простетических группы
РЕАКЦИЯ ОКСИГЕНАЦИИ
Обратимое присоединение кислорода (оксигенация), позволяющее гемоглобину выполнять свою основную функцию переносчика, обеспечивается возможностью образовать прочные пятую и шестую координационные связи и перенести электрон на кислород не от железа (то есть окислить Fe2 +), а от имидазольного кольца проксимального гистидина. Это схематически изображено на рис. 1, б. Вместо молекулярного кислорода железо гема может присоединить окись углерода СО (угарный газ). Даже небольшие концентрации СО приводят к нарушению кислородпереносящей функции гемоглобина и отравлению угарным газом.
Выше было сказано, что одна молекула гемоглобина содержит четыре субъединицы и, следовательно четыре гема, каждый из которых может обратимо присоединить одну молекулу кислорода. Поэтому реакцию оксигенации можно разделить на четыре стадии:
Hb + O2 _ HbO2
HbO2 + O2 _ Hb(O2)2
Hb(O2)2 + O2 _ Hb(O2)3
Hb(O2)3 + O2 _ Hb(O2)4
Дата: 2016-10-02, просмотров: 390.