Значение: Источник восстановленных эквивалентов НАДН+Н+ в организме, кот используются в синтезе жирных к-т, ХС, стероидов, желчных к-т, вит.Д3. Поставляет пентозы для синтеза нуклеотидов и нуклеиновых к-т.
ПФП: окислительная и неокислительная ветви.
Окислительная ветвь:
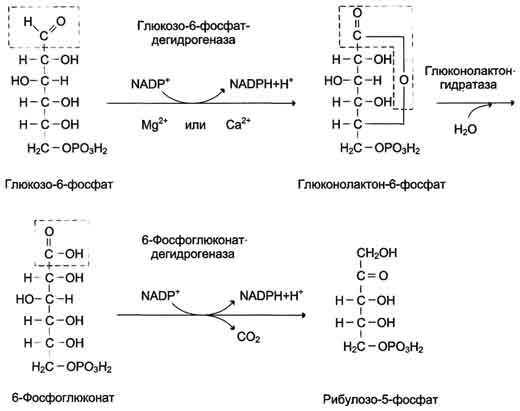
Неокислительная ветвь:

Переваривание и всасывание пищевых жиров.
Этапы:
1) Эмульгирование – под действием желчных к-т из крупной капли липидов обр-ся 10^6 мелких капель.
2) Гидролиз липидов – под влияним липолитических ферментов (панкреатической и кишечной липаз).
3) Обр-е смешанных мицелл из простой мицеллы.
4) Транспорт и всасывание смешанной мицеллы в эпителий слизистой кишечника.
Ресинтез жиров в слистой ЖКТ:
Смешанные мицеллы в слиз. ЖКТ распадаются на желчные к-ты, липидные компоненты. Желчные к-ты всасываются обратно в кровь и возвращаются в печень. В энтероците происх. 1й ресинтез специфических липидов.
Ресинтезированные липиды используются для биосинтеза транспортных форм: хиломикронов(ХМ) и ЛОНП, кот. Попадают в лимфу, затем в общий круг кровообращения.
Функция ХМ – доставка органам и тканям экзогенных жиров.
Роль желчных к-т в переваривании и всасывании липидов:
1) Эмульгирование липидов.
2) Активация липолитических ферментов
3) Всасывание в виде мицелл бета-МАГ, альфа,бета-ДАГ, ВЖК, ХС.
4) Всасывание жирорастворимых витаминов
5) Выведение из организма холестерина.
Бета-окисление жирных к-т, связь ЦТК и ЦПЭ. Аллостерическая регуляция. Биологическое значение.
Бета-окисление – процесс, в ходе кот. Жирная к-та распадается на неск. Двууглеродных ферментов.
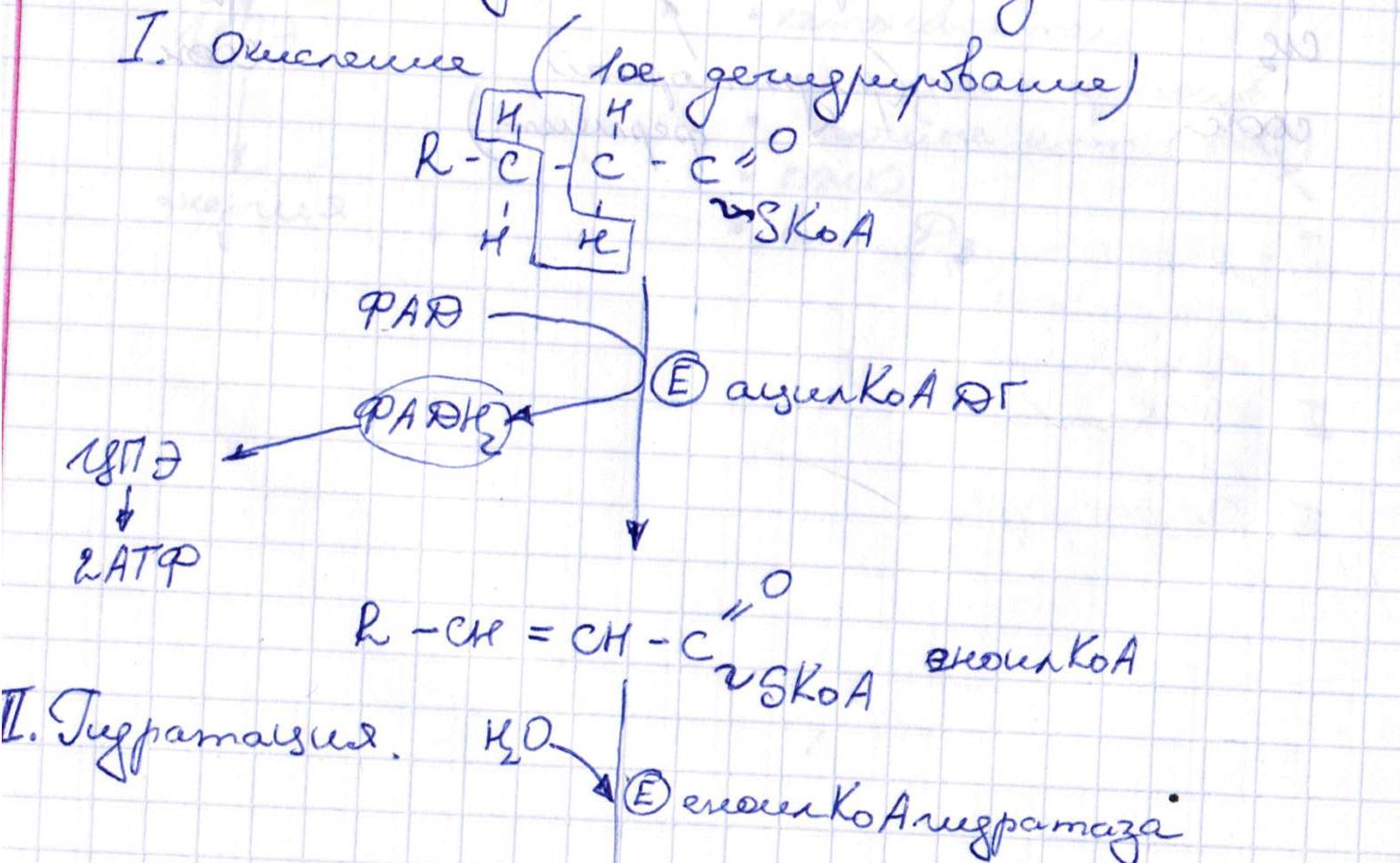
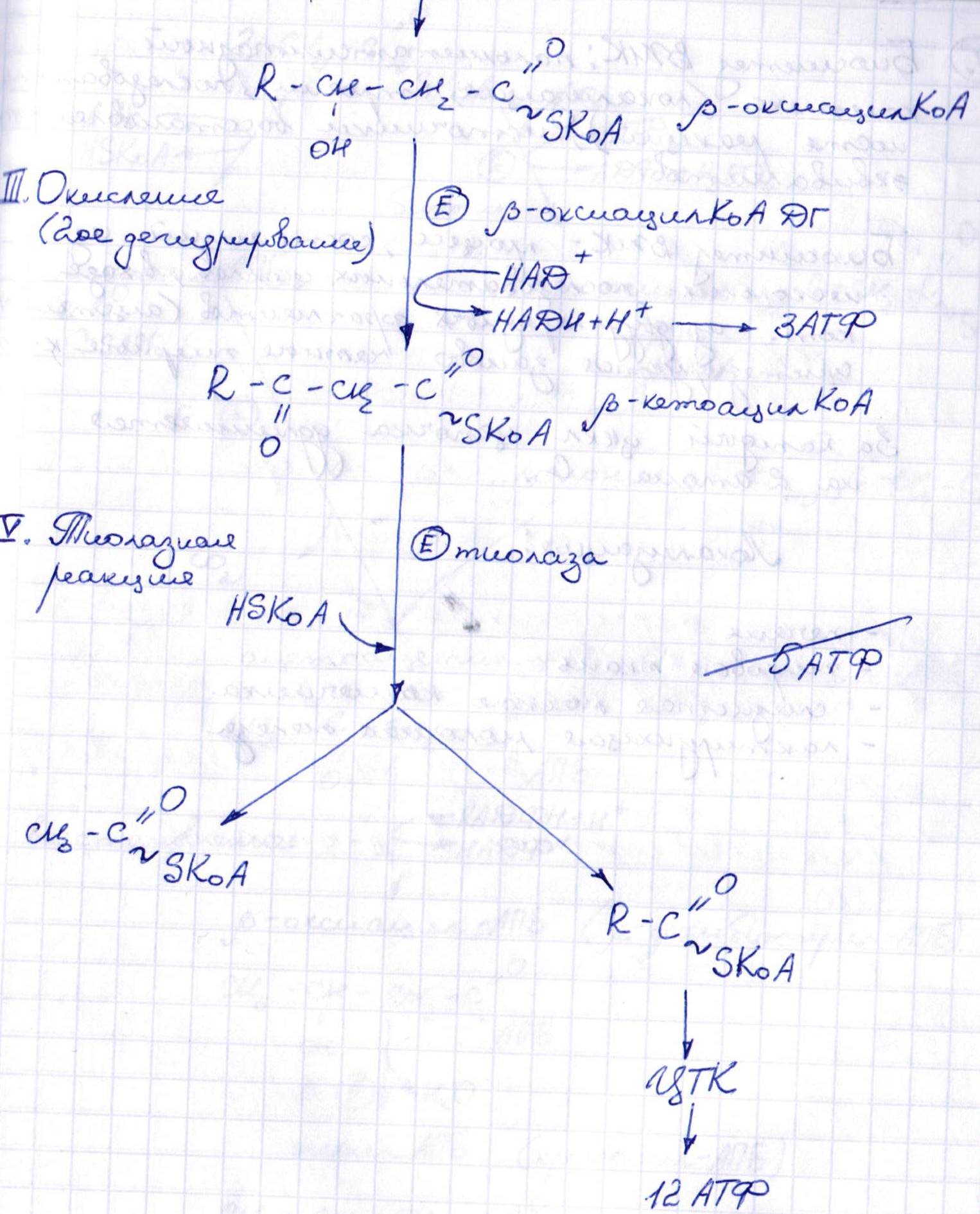
Синтез жирных к-т в печени.
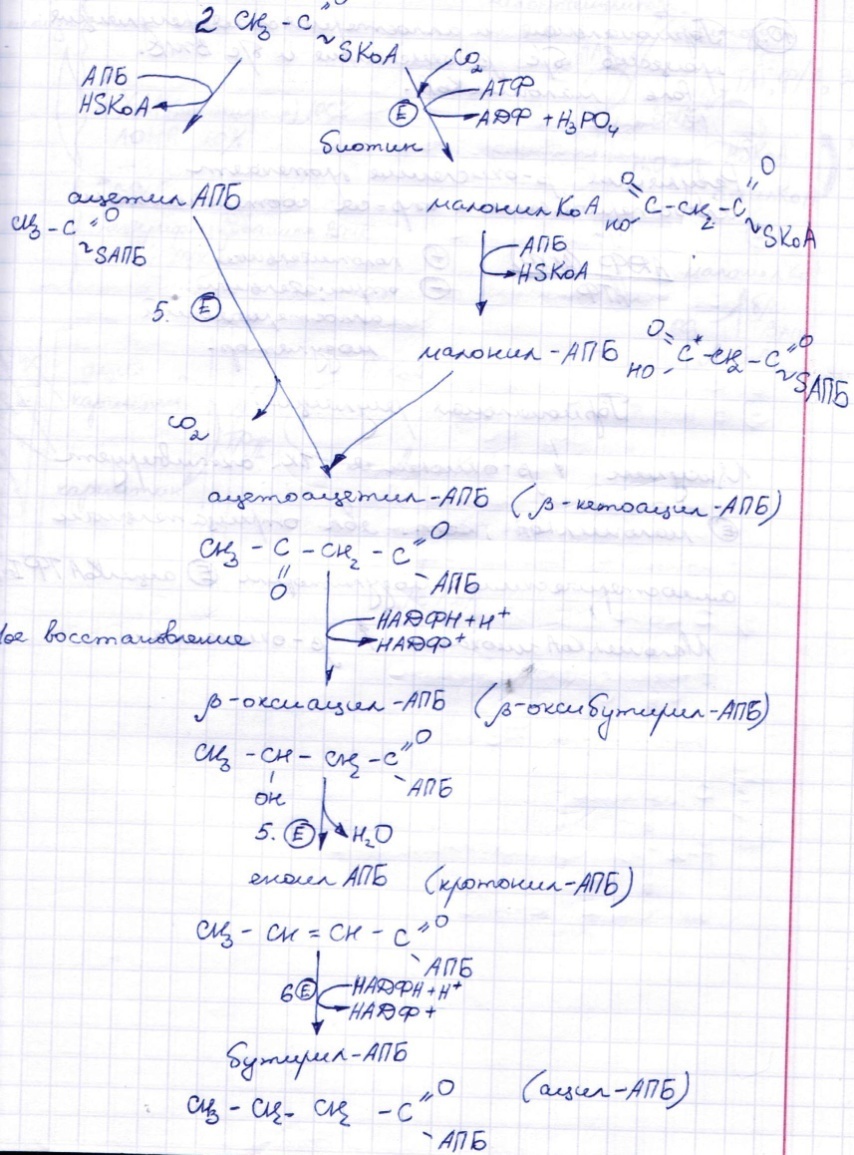
Мобилизация и депонирование жира, регуляция гормонами.
Депонирование и мобилизация жиров
Жиры, как и гликоген, являются формами депонирования энергетического материала. Причем жиры — наиболее долговременные и более эффективные источники энергии . При голодании запасы жира у человека истощаются за 5—7 недель, тогда как гликоген полностью расходуется примерно за сутки. Если поступление жира превышает потребности организма в энергии , то жир депонируется в адипоцитах — специализированных клетках жировой ткани. Кроме того, если количество поступающих углеводов больше, чем надо для депонирования в виде гликогена, то часть глюкозы также превращается в жиры . Таким образом, жиры в жировой ткани накапливаются в результате трех процессов:
- поступают из хиломикронов, которые приносят экзогенные жиры из кишечника
- поступают из ЛОНП, которые транспортируют эндогенные жиры, синтезированные в печени из глюкозы
- образуются из глюкозы в самих клетках жировой ткани.
В первом и во втором случае жиры в составе липопротеинов гидролизуются ЛП—липазой и в клетку поступают жирные кислоты, которые затем используются для синтеза ТАГ. Перед включением в ТАГ жирные кислоты сначала активируются путем образования тиоэфиров кофермента А, а затем взаимодействуют с глицеролфосфатом. Так как глицерол не может быть фосфорилирован в адипоцитах (в этих клетках отсутствует глицеролкиназа), то глицеролфосфат образуется при восстановлении диоксиацетонфосфата.
Мобилизацию (липолиз) депонированных ТАГ катализирует тканевая липаза. В результате жиры распадаются на глицерин и свободные жирные кислоты.
Кетоновые тела.
Кето́новые тела́ (синоним: ацето́новые тела, ацето́н [распространённый медицинский жаргонизм]) — группа продуктов обмена веществ, которые образуются в печени из ацетил-КоА[2]:
· ацетон (пропанон) [H3C—CO—CH3]
· ацетоуксусная кислота (ацетоацетат) [H3C—CO—CH2—COOH]
· бета-гидроксимасляная кислота (β-гидроксибутират) [H3C—CHOH—CH2—COOH]
Метаболизм кетоновых тел
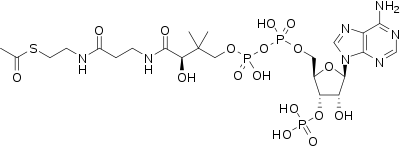

Ацетил-КоА
Ацетон в плазме крови в норме присутствует в крайне низких концентрациях, образуется в результате спонтанного декарбоксилирования ацетоуксусной кислоты и не имеет определённого физиологического значения[2] (в сущности являясь токсическим веществом для головного мозга (не хватает ссылки, подтверждающей написанное!), циркулирует в мизе́рной концентрации).
Нормальное содержание кетоновых тел в плазме крови человека и большинства млекопитающих (за исключением жвачных) составлет 1…2 мг% (по ацетону). При увеличении их концентрации свыше 10…15 мг% они преодолевают почечный порог и определяются в моче. Наличие кетоновых тел в моче всегда указывает на развитие патологического состояния.
Кетоновые тела синтезируются в печени из ацетил-КоА:[2]
На первом этапе из двух молекул ацетил-КоА синтезируется ацетоацетил-КоА. Данная реакция катализируется ферментом ацетоацетил-КоА-тиолазой.
Ac—КоА + Ac—КоА → H3C—CO—CH2—CO—S—КоА
Затем под влиянием фермента гидроксиметилглутарил-КоА-синтазы присоединяется ещё одна молекула ацетил-КоА.
H3C—CO—CH2—CO—S—КоА + Ac—КоА → HOOC—CH2—COH(CH3)—CH2—CO—S—КоА
Образовавшийся β-гидрокси-β-метилглутарил-КоА (OMG-KoA) способен под действием фермента гидроксиметилглутарил-КоА-лиазы расщепляться на ацетоуксусную кислоту (ацетоацетат) и ацетил-КоА.
HOOC—CH2—COH(CH3)—CH2—CO—S—КоА → H3C—CO—CH2—COOH + Ac—КоА
Ацетоуксусная кислота способна восстанавливаться при участии НАД-зависимой D-β-оксибутиратдегидрогеназы; при этом образуется D-β-оксимасляная кислота (D-β-оксибутират). Фермент специфичен по отношению к D-стереоизомеру и не действует на КоА-эфиры.[2]
H3C—CO—CH2—COOH + NADH → H3C—CHOH—CH2—COOH
Ацетоуксусная кислота в процессе метаболизма способна окисляться до ацетона с выделением молекулы углекислого газа:[1]
H3C—CO—CH2—COOH → CO2 + H3C—CO—CH3
[править]Альтернативный путь
Существует второй путь синтеза кетоновых тел:
образовавшийся путём конденсации двух молекул ацетил-КоА ацетоацетил-КоА способен отщеплять Кофермент A с образованием свободной ацетоуксусной кислоты[3]. Процесс катализирует фермент ацетоацетил-КоА-гидролаза (деацилаза), однако данный путь не имеет существенного значения в синтезе ацетоуксусной кислоты, так как активность деацилазы в печени низкая.[2]
H3C—CO—CH2—CO—S-КоА + H2O → H3C—CO—CH2—COOH + КоА-SH
Дата: 2016-10-02, просмотров: 331.