| Пандемический подтип | Наименование пандемии | Годы циркуляции |
| A(H1NI) | Испанский грипп | 1918- 1956 |
| A (H2N2) | Азиатский грипп | 1957- 1967 |
| A(H3N2) | Гонконгский грипп | 1968 по наст. время |
| A(H1N1) | Русский грипп | 1977 по наст. время |
| A(H5N1) | Птичий грипп | 1971 по наст. время |
| А/H1N1, А/H1N2, А/H3N1, А/H3N2 и А/H2N3 | Свиной грипп | 2009 г. по наст. время |
5. Клинические проявления;
Патогенез. Входными воротами инфекции является эпителий слизистых оболочек верхних дыхательных путей, куда вирусы гриппа заносятся аэрогенно. Во время короткого инкубационного периода вирус интенсивно репродуцируется в эпителиальных клетках, накапливаясь в количестве, достаточном для появления клинических симптомов. При попадании вирионов непосредственно в альвеолы может развиться первичная гриппозная пневмония. Пораженные эпителиальные клетки некротизируются и отторгаются, под действием нейраминидазы оголяются базальные мембраны, усиливается воспалительная реакция, что создает условия для массивного проникновения вирусов в кровь и присоединения вторичной бактериальной инфекции.
Вирусы гриппа легко преодолевают защитные барьеры организма и проникают в кровь. Вирусемия возникает еще в инкубационном периоде и продолжается в течение нескольких дней. Проникшие в кровь вирусы распространяются по организму, заносятся в мышцы, сердце, ЦНС, почки и другие органы. Вирусы вызывают повреждение эритроцитов (действие гемагглютинина), эндотелия капилляров, нередко приводят к нарушению электролитного и кислотно-щелочного баланса. Как следствие, нарушается микроциркуляция, возникают множественные геморрагии и тромбоз, может развиться отек мозга и легких, дистрофия миокарда и другие осложнения.
С первых дней болезни наблюдается интоксикация и лихорадка. Основную роль в их развитии отводят поступающим в кровь биологически активным веществам - серотонину, гистамину, простагландинам, кининам, которые образуются при распаде клеток.
При гриппе угнетается клеточный иммунитет, снижается активность лизоцима, комплемента, пропердина; развивается аллергизация организма. Все это способствует присоединению вторичной бактериальной инфекции.
Обратное развитие патологического процесса при гриппе и выздоровление обусловлено действием противовирусных защитных факторов - в большей степени неспецифических, а также специфических, формирование которых запаздывает.
Клинические формы гриппа делят на неосложненные и осложненные (указывая вид осложнений). И те и другие подразделяют на легкие, средней тяжести, тяжелые и крайне тяжелые (гипертоксические) формы.
6. Лабораторная диагностика, характер исследуемого материала;
Лабораторная диагностика гриппа включает в себя вирусологический, серологический и экспресс-методы. Раннюю и ретроспективную диагностику - проводят для подтверждения клинического диагноза, дифференциации гриппа от ОРВИ другой этиологии и для эпидемиологических целей.
Ранняя диагностика. В ранние сроки заболевания (в первые 3 дня и не позднее 5-го дня болезни) обнаруживают антигены вирусов гриппа с помощью экспресс методов и(или) выделяют и идентифицируют вирус путем вирусологического исследования.
Исследуемые материалы: слизь из носовых ходов и носоглотки, взятая тампонами, путем смывов, методом мазков-отпечатков со слизистой нижних носовых раковин. От погибших людей берут участки пораженных слизистых оболочек трахеи и бронхов, кусочки легких.
Экспресс-диагностика. Позволяет установить предварительный диагноз гриппа в течение 2-5 часов. Чаще всего применяют иммунофлюоресцентный метод (прямой и непрямой). Специфические антигены вируса гриппа и внутриклеточные включения выявляют по их яркому изумрудно-зеленому свечению в участках цитоплазмы и ядра инфицированных эпителиальных клеток. МИФ позволяет дифференцировать гриппозную инфекцию от других ОРВИ и, при необходимости, выяснять этиологию последних.
Вирусные антигены в смывах из носоглотки обнаруживают также методом ИФА, (выявляют присутствие М-белка), в РТГА, РОНГА и других серологических реакциях со специфическими сыворотками.
Разрабатывается методика ПЦР для диагностики гриппа.
Ретроспективная диагностика гриппа заключается в сероло гическом исследовании парных сывороток, взятых в начале заболевания и через 7-14 дней. Повышение титра специфических антител в течение заболевания не менее, чем в 4 раза (у детей младшего возраста — в 2 раза) позволяет установить точную этиологию гриппа даже при отрицательных результатах других методов лабораторной диагностики (или, если она вообще не проводилась), а также при бессимптомном или атипичном течение гриппа.
Серологическая диагностика гриппозной инфекции широко применяется и для эпидемиологических целей.
7. Особенности вирусологического метода диагностики (культивирование, индикация, идентификация вируса);
Вирусологический метод. Вирусологические исследования с целью выделения вируса гриппа проводят преимущественно в период массовой заболеваемости гриппом. Выделенные штаммы идентифицируют, изучают динамику их антигенной изменчивости, что помогает прогнозированию дальнейших эпидемических волн гриппа, отбору актуальных штаммов, пригодных для изготовления вакцин.
Материалом для выделения вирусов являются носоглоточные смывы и секционный материал после их специальной обработки.
Вирусы выделяют путем заражения куриных эмбрионов и однослойных клеточных культур.
Выделение вируса в куриных эмбрионах. Перед заражением куриных эмбрионов необходимо поместить исследуемый материал в раствор с антибиотиками для уничтожения бактериальной флоры. После этого проводят комбинированное заражение исследуемым материалом 10-11 дневных эмбрионов в амниотическую или аллантоисную полости. После 3 дней инкубации при 35°С проверяют присутствие вирусов в амниотической и аллантоисной жидкости с помощью реакции гемагагглютинации с эритроцитами кур, морской свинки или человека, устанавливают титр вируса.
Получив вируссодержащий материал - амниотическую и аллантоисную жидкости с высокой гемагглютинирующей активностью, проводят серологическую идентификацию выделенного вируса с помощью РТГА для установления подтипа или штамма вируса гриппа. Эти реакции ставят с соответствующими диагностическими противогриппозными сыворотками.
Выделение вирусов в культурах клеток. Осуществляют путем заражения нескольких типов культур клеток, чаще используют первичные культуры почек человека и некоторых животных. Клеточные культуры инкубируют в течение недели при 33°С, ежедневно регистрируя изменения монослоя клеток с целью выявления ЦПД (цитопатического действия). При его отсутствии, вирус выявляют с помощью реакции гемадсорбции или гемагглютинации, а также ИФ-методом (иммунофлюоресцентным методом). Далее вируссодержащей культуральной жидкостью заражают куриные эмбрионы, получают аллантоисную жидкость с высоким содержанием вирусов, и проводят идентификацию выделенного вируса, как указано выше.
8. Противовирусный иммунитет;
Иммунитет. Человек, перенесший грипп, приобретает стойкий постинфекционный клеточный и гуморальный иммунитет, который отличается своей узкой специфичностью и направлен против сероварианта (штамма) вируса гриппа, вызвавшего данное заболевание. Следовательно, противогриппозный иммунитет является подтипо- и штаммоспецифичным. Поэтому появление новых штаммов того же подтипа вируса А даже с очень незначительным дрейфом поверхностных антигенов существенно снижает эффективность имеющегося иммунитета. Дальнейшая антигенная изменчивость того же подтипа вируса, а тем более появление, вследствие шифта антигенов, нового подтипа вируса А, делает человека беззащитным против гриппозной инфекции.
Восприимчивость человека к вирусам гриппа очень высока, особенно при первой встрече с вирусом. Поэтому чаще всего болеют маленькие дети. Грипп у детей протекает тяжелее, чем у взрослых, часто с развитием осложнений.
Высокая ранимость детей обусловлена несовершенством неспецифических и специфических механизмов иммунитета, уязвимостью других систем и органов, что связано с анатомо-физиологической незрелостью организма.
Пассивный иммунитет, приобретенный ребенком от матери, сохраняется около 6 месяцев при грудном вскармливании и не более 3 месяцев при искусственном.
До повторного появления в популяции людей в 1977 г. вируса гриппа подтипа А (Н1N1) после его 20-летнего отсутствия, считалось, что постгриппозный иммунитет нестоек и сохраняется в течение 2-3 лет. Однако, вызванная этим штаммом пандемия поражала детей и молодых людей, родившихся после 1957 г., и почти не затрагивала людей более старшего возраста. При массовом обследовании этих людей у подавляющего большинства из них были обнаружены специфические IgG антитела к вирусу A (H1N1). Эти факты свидетельствуют о сохранении постинфекционного иммунитета не менее 20 лет.
Однако, практически, человек часто повторно заболевает гриппом через 2-3 года, что связано с постоянной антигенной изменчивостью и одновременной циркуляцией нескольких типов и подтипов вирусов гриппа.
9. специфическая профилактика;
Основными противогриппозными мероприятиями являются:
- массовая вакцинация населения перед ожидаемым сезонным повышением заболеваемостью гриппом (октябрь - ноябрь)
- экстренная профилактика людей в начале и во время эпидемического распространения гриппа с помощью специфических и неспецифических препаратов.
- раннее специфическое лечение гриппа.
- проведение общих противоэпидемических и организационных мероприятий
Вакцинопрофилактика. Является важным средством борьбы с гриппом. Существует несколько типов гриппозных вакцин, которые постоянно совершенствуются — повышается их иммуногенность, улучшаются технология получения и очистки. Эффективность гриппозных вакцин зависит, главным образом, от степени антигенного соответствия штаммов гриппа, входящих в вакцину, и штаммов, вызывающих данную эпидемию. Поэтому современные вакцины содержат штаммы разных подтипов вируса, которые заменяют каждые 2-3 года в соответствии с эпидемиологическим прогнозом. В настоящее время вакцины готовят из актуальных штаммов вирусов A (H3N2), A (H1N1) и вируса типа В. Существуют:
1. Цельновирионные вакцины (1-го поколения) - инактивированные и живые. Живые вакцины содержат аттенуированные штаммы вирусов гриппа (имеются отдельные вакцины для взрослых и детей).
2. Расщепленные — сплит-вакцины (2-го поколения), содержат внутренние и наружные антигены вирусов гриппа и не содержат липидов, удаленных после обработки вирионов растворителями или детергентами.
3. Субъединичные вакцины (3-го поколения). Являются наиболее очищенными, содержат наружные Н- и N-антигены вирусов гриппа.
Все типы вакцин обладают достаточной иммуногенностью, цельновирионные вакцины наиболее реактогенны, они могут давать аллергические реакции на куриный белок; интраназальное введение обычно предотвращает их развитие. Живые вакцины вызывают более полноценный иммунитет, в том числе клеточный и местный.
Заболеваемость гриппом среди привитых людей, в среднем, снижается в 2-2,5 раза, гриппозная инфекция имеет более легкое течение, снижается количество осложнений.
Экстренная профилактика. Ее проводят во время эпидемического подъема заболеваемости. Различают плановую профилактику, организуемую в детских учреждениях, рабочих коллективах и очаговую в семьях гриппозных больных.
Для экстренной профилактики применяют противовирусные химиопрепараты: ремантадин (активен только против вирусов типа А), арбидол, амиксин, оксалиновую мазь и др. Используют также интерферон, дибазол, различные индукторы интерферона (например, элеутерококк, продигиозан). В дошкольных детских коллективах иногда проводят иммуноглобулинопрофилактику.
Этиотропное лечение
Лечение. Для лечения гриппа применяют те же средства, что и для экстренной профилактики. Основными из них являются различные препараты интерферона и ремантадин, которые обладают противовирусной активностью в отношении различных подтипов вируса гриппа А и антитоксическим действием при гриппе В. Ремантадин ингибирует синтез М-белка, что приводит к нарушению цикла репродукции и препятствует формированию полноценных вирионов. Применяют также арбидол и амиксин, являющиеся индукторами интерферонов и иммуномодуляторами, которые воздействуют на все типы вирусов гриппа.
При тяжелых формах гриппа, особенно у детей, в первые 3 дня болезни показано введение противогриппозного иммуноглобулина.
Все противовирусные препараты необходимо применять с первых дней болезни, строго следуя разработанным схемам их приема.
Кроме этиотропного лечения гриппа проводят симптоматическое лечение. При наличие бактериальных осложнений назначают антибиотики и сульфаниламидные препараты.
ПАРАМИКСОВИРУСЫ
Таксономия, классификация
Парамиксовирусы (семейство Paramyxoviridae от лат. para - около, myxa - слизь) - семейство РНК-содержащих вирусов. Семейство содержит респираторно-синтициальный вирус, вирусы кори, паротита, парагриппа, передающиеся респираторным механизмом. В семейство Paramyxoviridae в соответствии с общепринятой классификацией вирусов до последнего времени входили три рода: Paramyxovirus, Morbillivirus, Pneumovirus. Но недавно в классификацию внесены изменения.
Семейство Paramyxoviridae разделено на два подсемейства, увеличено количество родов:
1. Подсемейство Paramyxovirinae включает роды Respirovirus (прежнее название - Paramyxovirus ), Morbillivirus и Rubulavirus (новый род);
2. Подсемейство Pneumovirinae содержит роды Pneumovirus и Metapneumovirus .
2. Морфология, размеры, особенности генома
Строение вириона. Все представители семейства Paramyxoviridae имеют сходное строение. Это сложный РНК-геномный вирус крупных размеров. Типовым представителем является вирус Сендай (он патогенен для мышей), и ультраструктура парамиксовирусов рассматривается на этом примере (рис.5). Вирион имеет округлую форму, его диаметр 150-300 нм. Снаружи находится липопротеиновый суперкапсид с множеством шипиков двух типов на поверхности (рис.4). Изнутри к суперкапсиду прилегает слой матриксного М-белка. В центральной части вириона находится тяж нуклеокапсида (РНП) со спиральным типом симметрии, свернутый в рыхлый клубок.

Рис. 4 Схема парамиксовируса Рис. 5 Электоронограмма вируса Сендай
Геном представлен крупной молекулой линейной однонитчатой минус-РНК, кодирующей 7 белков. Среди них основной капсидный белок NP, белки полимеразного комплекса L и Р, неструктурный С белок (все они входят в состав нуклеокапсида), а также М-белок и поверхностные гликопротеины. Это прикрепительные белки и белок слияния (F-белок). Прикрепительные белки образуют шипики одного типа, а F-белок — шипики другого типа. У разных парамиксовирусов прикрепительные белки представлены: HN (гемагглютинин-нейраминидаза), Н (гемагглютинин) или G-белком.
Парагрипп. По антигенам вирусных белков HN, NP, F различают 4 основных серотипа вирусов парагриппа. Типы 1, 2, 3 перекрестно реагируют с антителами к вирусу паротита. Вирус 4 типа отличается и имеет 2 подтипа (таким образом, предпологается наличие 5 типов вирусов парагриппа). Все вирусы парагриппа имеют HN - белок и поэтому проявляют гемагглютинирующую и нейраминидазную активность. Вирус парагриппа 1, 2 типа агглютинирует эритроциты кур, вирус парагриппа 3 агглютинирует только эритроциты морских свинок.
Этапы репродукции
Парамиксовирус (рис. 5) связывается гликопротеинами (HN, H, или G) оболочки с поверхностью клетки (1). F-белок обеспечивает слияние оболочки вируса с плазматической мембраной клетки, без образования эндосом. Репликация генома сходна с репликацией минус РНК-геномных вирусов: РНК-полимераза вносится в клетку с нуклеокапсидом вируса. Геном транскрибируется в отдельные иРНК (2) для каждого белка и полноценную плюс-матрицу (3) для геномной РНК. Новые геномы взаимодействуют с L-, P- и NP-белками, образуя нуклеокапсиды. Синтезированный матриксный белок перемещается к внутреннему слою мембраны клетки. Предшественники гликопротеиновых шипов оболочки синтезируются на рибосомах, связанных с мембранами эндоплазматического ретикулума (ЭР). Они гликозилируются, перемещаясь через ЭР и аппарат Гольджи (АГ), встраиваясь в мембрану клетки. Нуклеокапсид связывается с матриксным белком и гликопротеинмодифицированной мембраной (суперкапсидом). Вирионы выходят из клетки (4)почкованием.
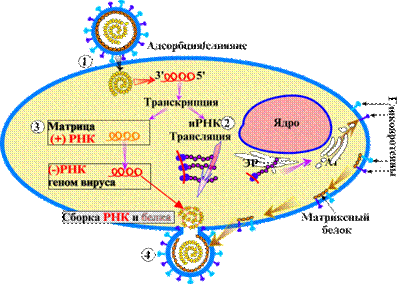
Рис. 5 Репродукция парамиксовирусов
Парамиксовирусы обладают способностью с помощью F-белка переходить в соседние клетки, вызывая их слияние. При этом образуются многоядерные гигантские клетки - синцитии (симпласты). Такой механизм позволяет вирусам распространяться непосредственно из клетки в клетку, избегая действия вируснейтрализующих антител. Способность к симпластооброзаванию - характерный признак парамиксовирусов.
Эпидемиология
Большинство парамиксовирусов являются возбудителями острых респираторных вирусных инфекций (ОРВИ), при которых поражается дыхательная система, клинически эти заболевания неотличимы от ОРВИ, вызываемых многими другими вирусами. Механизм передачи – аэрозольный, пути – воздушно-капельный и воздушно-пылевой. Некоторые парамиксовирусы способны вызывать инфекции иного типа, отличающиеся от ОРВИ. Это корь и эпидемический паротит, при которых поражаются преимущественно другие органы и системы, эти заболевания имеют специфические клинические симптомы, циклическое течение.
Клинические проявления
Вызывают катаральные проявления верхних дыхательных путей; ларинго-трахеобронхит, бронхиолит, пневмонии.
Дата: 2019-07-24, просмотров: 425.