Краткие теоретические сведения
Общая информация
Неконденсированные системы изучают с помощью как изобарических сечений диаграмм их состояния (в координатах температура и состав), так и изотермических сечений в координатах давление - состав.
В уравнении, определяющем число степеней свободы системы по правилу фаз Гиббса, число внешних переменных уменьшается до единицы
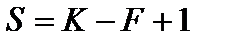 .
.
Максимальное число фаз, находящихся в равновесии в таких системах, не превышает трех, системы с двумя фазами имеют одну степень свободы, а с одной - две степени свободы.
Типовые диаграммы состояния
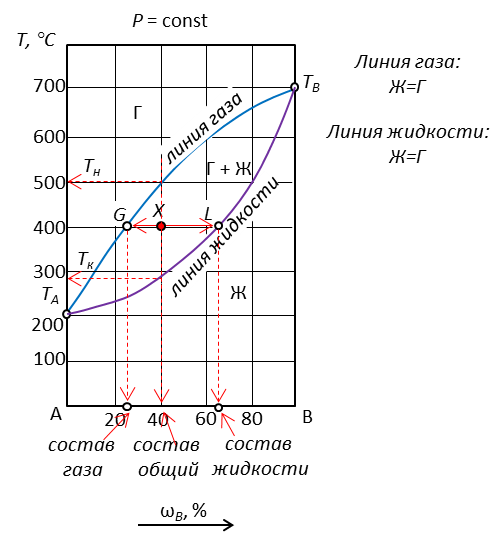
Рис. 1. Диаграмма с неограниченной растворимостью компонентов, без точек азеотропа
Свойства систем, заданных фигуративными точками
| Точка | Исходный состав, % В | Кол-во фаз в точке | Наименование фаз | Состав каждой фазы, % В | Относительное кол-во фаз, % | Температура конденсации | Число степеней свободы | |
| ТН | ТK | |||||||
| X | 40 | 2 | Ж | 65 | 37,5 | 500 | 290 | 2-2+1=1 |
| Г | 25 | 62,5 | ||||||
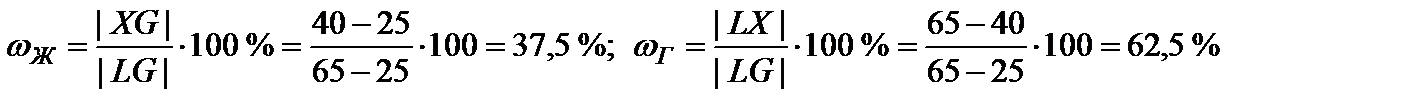
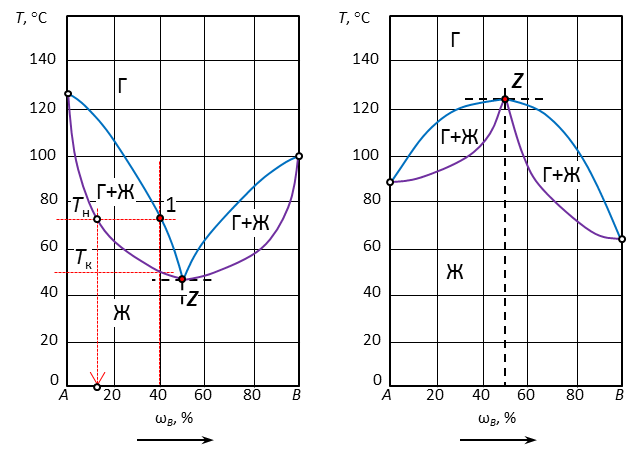
Рис. 2. Диаграмма с неограниченной растворимостью компонентов и нижним азеотропом
| Точка | Исходный состав, % В | Кол-во фаз в точке | Наименование фаз | Состав каждой фазы, % В | Относительное кол-во фаз, % | Температура конденсации | Число степеней свободы | |
| ТН | ТK | |||||||
| 1 | 40 | 2 | Ж | 12 | Ж=Г | 72 | 50 | 2-2+1=1 |
| Г | 40 | |||||||
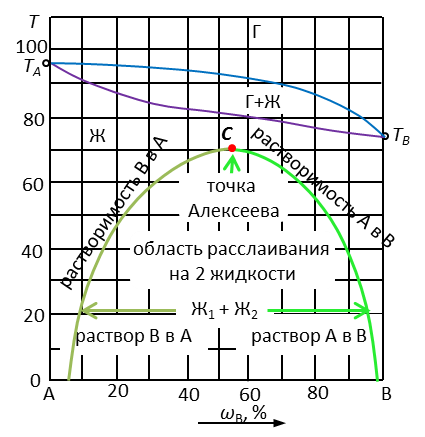
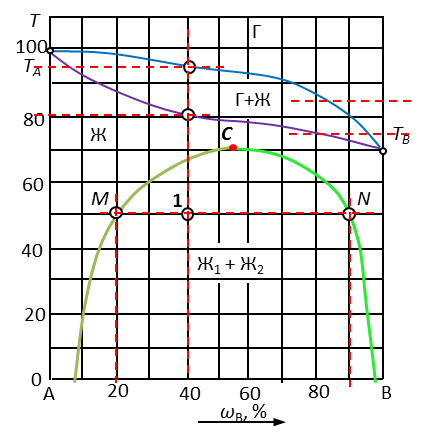
Рис. 3. Диаграмма с областями полной и частичной растворимостью жидкостей
| Точка | Исходный состав системы, % В | Кол-во фаз в точке | Наименование фаз | Состав каждой фазы, % В | Относительное кол-во фаз, % | Температура конденсации | Число степеней свободы F=K-Ф+1 | |
| ТН | ТK | |||||||
| 1 | 40 | 2 | ж1 | 20 | 75 | 95 | 80 | 2-2+1=1 |
| ж2 | 90 | 25 | ||||||
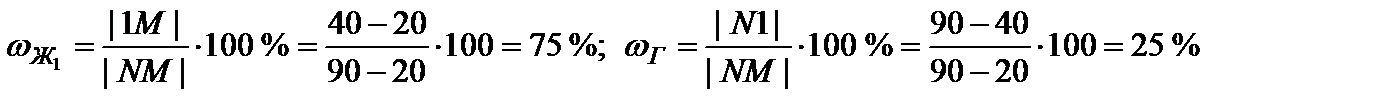
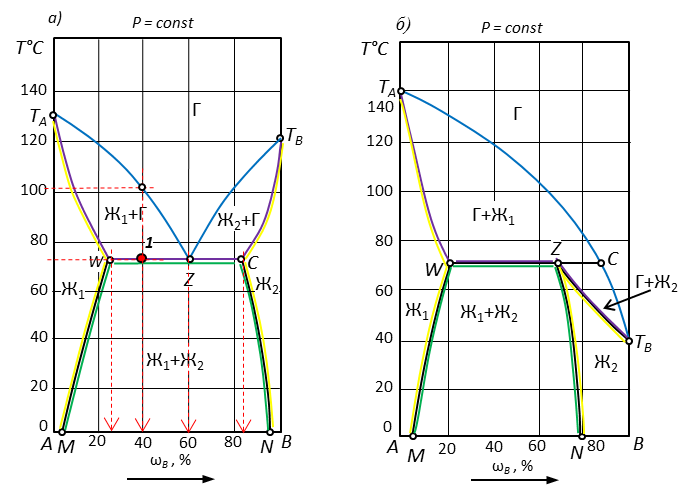
Рис. 4. Диаграмма с ограниченной растворимостью компонентов, полной растворимости нет.
| Точка | Исходный состав системы, % В | Кол-во фаз в точке | Наименование фаз | Состав каждой фазы, % В | Относительное кол-во фаз, % | Температура конденсации | Число степеней свободы F=K-Ф+1 | |
| ТН | ТK | |||||||
| 1 | 40 | 3 | Ж1 | 25 | Ж1=Ж2=Г | 101 | 72 | 2-3+1=0 |
| Г | 60 | |||||||
| Ж2 | 82 | |||||||
Порядок рассмотрения диаграммы
1. Перечертить диаграмму, соблюдая топологию, в заданном масштабе.
2. Дать общую характеристику диаграммы.
3. Отметить линию газа, линию жидкости, линии растворимости компонентов; написать равновесия на линиях.
4. Обозначить поля диаграммы греческими или римскими цифрами.
5. Указать фазовый состав полей диаграммы.
6. Описать значимые точки диаграммы (точки кипения компонентов, точки азеотропа, точки Алексеева): указать температуру, состав, уравнение равновесия.
7. Рассмотреть свойства систем, заданных соответствующими фигуративными точками и заполнить таблицу
| Точка | Исходный состав, % В | Кол-во фаз в точке | Наименование фаз | Состав каждой фазы, % В | Относительное кол-во фаз, % | Температура конденсации | Число степеней свободы | |
| ТН | ТK | |||||||
Примеры решения задач
Пример 9. Обозначить поля диаграммы (рис. 5), дать характеристику компонентов системы. Описать путь конденсации системы, содержащей 45 % компонента В (точка М), заполнить таблицу.

Рис. 5. Диаграмма состояния двухкомпонентной неконденсированной системы пентан – гептан.
Решение. 1. Пронумеровать поля диаграммы (обычно – римскими цифрами).
2. Дать наименование полей диаграммы. Поле I – газ (пар); поле II – пар + жидкость; поле III – жидкость.
3. Дать характеристику диаграммы. Двухкомпонентная неконденсированная система с неограниченной растворимостью компонентов в жидкой фазе.
4. Путь конденсации системы – вертикальная пунктирная линия вниз от точки М (рис. 6), на которой отмечены фигуративные точки М', М'', М''', соответствующие началу процесса (М'), образованию двухфазной системы (М'') и окончанию конденсации (М''').
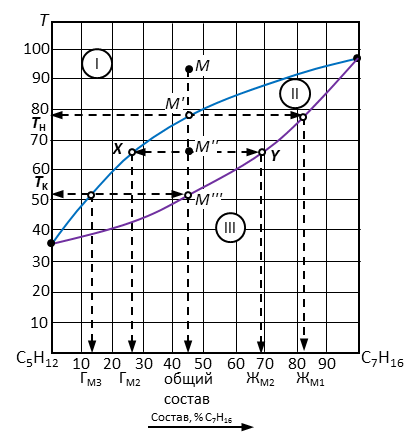
Рис. 6. Решение примера 1.
5. Таблица
| Точка | Исходный состав системы, % В | Кол-во фаз в точке | Наим. фаз | Состав каждой фазы, % В | Относит. кол-во фаз, % | Температура конденсации | C | |
| ТН | ТK | |||||||
| М | 45 | 1 | Г | 45 | 100 | 78 | 51 | 2 |
| М' | 45 | 2 | Г | 45 | Г=Ж | 78 | 51 | 1 |
| Ж | 82 | |||||||
| М'' | 45 | 2 | Г | 27 | 55 | 78 | 51 | 1 |
| Ж | 69 | 45 | ||||||
| М''' | 45 | 2 | Г | 13 | Г=Ж | 78 | 51 | 1 |
| Ж | 45 | |||||||
5. Определить состав системы в точке М, для чего следует опустить перпендикуляр от точки М на ось составов. Состав точки М – 45 % гептана C7H16 – компонента В. Он же будет общим составом системы для всех остальных точек. Точка М находится в поле I, следовательно, число фаз – 1 шт. Наименование фазы – пар; состав совпадает с общим составом системы.
6. Температуру начала конденсации определить по месту пересечения перпендикуляра из точки М и линии газа (граничной линии между полем I и II) – точка М'. От точки М' провести горизонталь на ось температур. Температура начала конденсации равна 78°С. Она остается одинаковой для всех рассматриваемых точек.
7. Определить число степеней свободы в точке М:
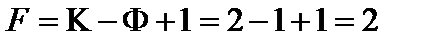 .
.
8. Определить фазовый состав в точке М'. Точка М' находится на линии конденсации, следовательно, количество фаз – 2 шт.: газ и жидкость.
9. Определить состав жидкости в точке М', для чего от этой точки провести ноду до пересечения с линией жидкости (или линией испарения) и от точки пересечения опустить перпендикуляр на ось составов (позиция ЖМ' на рис. 6). Состав жидкости – 82 % C7H16.
10. Определить относительное количество фаз в точке М': так как М' находится на линии равновесия между двумя фазами, то относительное их количество не определяется. В такой ситуации следует записать уравнение равновесия. В данном случае – Ж = Г.
11. Определить число степеней свободы в точке М':
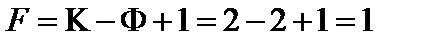 .
.
12. Определить фазовый состав точки М'', которая находится в поле II, следовательно, число фаз – 2 шт.: жидкость и газ.
13. Определить состав жидкости и газа в точке М'': провести ноду до пересечения с линий испарения (точка X) с одной стороны и с линией конденсации (точка Y) с другой стороны. От точек пересечения опустить перпендикуляры на ось составов. Перпендикуляр от линии конденсации определяет состав газа (27 % гептана – точка ГМ'' на рис. 6), от линии испарения – состав жидкой фазы (69 % гептана – точка ЖМ'' на рис. 6).
14. Определить относительное количество фаз в точке М''. В соответствии с правилом рычага
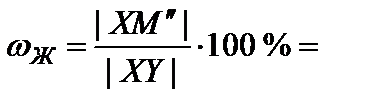 45%;
45%; 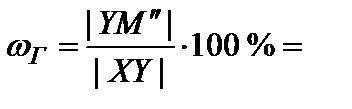 55 %.
55 %.
15. Определить число степеней свободы в точке М'':
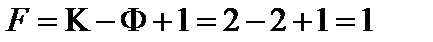 .
.
16. Температуру завершения процесса конденсации определить по месту пересечения перпендикуляра из точки М с линией испарения – точка М'''. От точки М''' провести горизонталь на ось температур. Температура завершения конденсации равна 51°С. Она остается одинаковой для всех рассматриваемых точек.
17. Определить фазовый состав в точке М'''. Точка М''' находится на линии испарения, следовательно, количество фаз – 2 шт.: газ и жидкость.
18. Определить состав пара в точке М''', для этого от этой точки провести ноду до пересечения с линией конденсации и от этой точки опустить перпендикуляр на ось составов (позиция ГМ''' на рис. 6). Состав пара – 13 % C7H16.
19. Определить относительное количество фаз в точке М''': так как М''' находится на линии равновесия между двумя фазами, то относительное их количество не определяется. В такой ситуации следует записать уравнение равновесия. В данном случае – Ж = Г.
20. Определить число степеней свободы в точке М''':
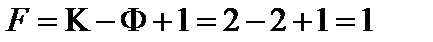 .
.
Пример 10. Обозначить поля диаграммы (рис. 7), дать характеристику компонентов системы. Определить изменение состава и количества фаз в системе, содержащей 25 % анилина при охлаждении ее от 170 до 60°С с интервалом 40°С. Нанести на диаграмму соответствующие фигуративные точки систем и фаз, заполнить таблицу.
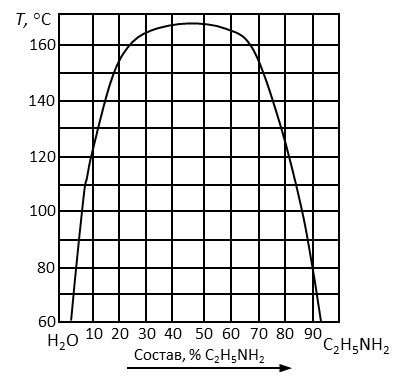
Рис. 7. Диаграмма состояния вода – этаноламин.
Решение. 1. Пронумеровать поля диаграммы (обычно – римскими цифрами).
2. Дать наименование полей диаграммы: поле I – жидкость (пар); поле II – область расслоения двух жидкостей.
3. Дать характеристику диаграммы: двухкомпонентная неконденсированная система с ограниченной растворимостью компонентов в жидкой фазе.
4. Отметить исследуемый состав системы, соответствующий содержанию анилина C2H5NH2 25 % и отметить фигуративные точки N, N', N'', соответствующие заданному температурному интервалу.
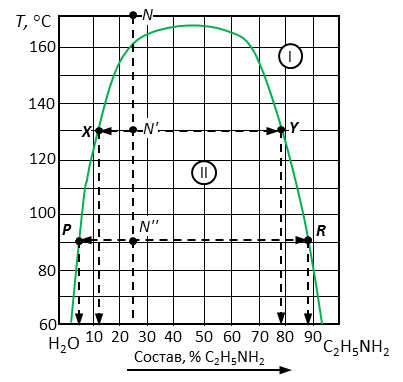
Рис. 8. Решение примера 2.
5. Определить фазовый состав в каждой точке. Точка N принадлежит к полю I, следовательно, количество фаз – 1 шт. – жидкость, содержащая 25 % анилина. Точки N' и N'' принадлежат полю II, где происходит расслаивание системы на две жидкости разного состава, следовательно, количество фаз – 2 шт. Состав жидкостей зависит от температуры.
6. Определить состав расслаивающихся жидкостей в точках N' и N'', как показано на рис. 8 и зафиксировано в табл. 2. При этом следует учитывать, что жидкость 1 представляет насыщенный раствор анилина в воде, а жидкость 2 – раствор воды в анилине. Соответственно точки X и P отображают состав Ж1, а точки Y и R – состав жидкости 2.
7. Пользуясь правилом рычага, определить относительное количество каждой фазы.
Для точки N':
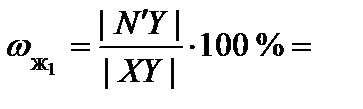 80 %;
80 %; 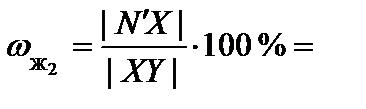 20 %.
20 %.
Для точки N'':
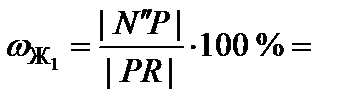 75 %;
75 %; 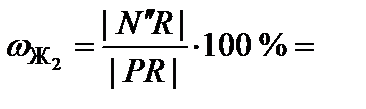 25 %.
25 %.
| Точка | Исходный состав системы, % В | Количество фаз в точке | Наименование фаз | Состав каждой фазы, % В | Относительное количество фаз, % | |
| N | 25 | 1 | Ж | 25 | 100 | |
| N' | 25 | 2 | Ж1 | 12 | 20 | |
| Ж2 | 78 | 80 | ||||
| N'' | 25 | 2 | Ж1 | 5 | 25 | |
| Ж2 | 88 | 75 |
Задачи для решения
Обозначить поля диаграммы, дать характеристику компонентов системы, заполнить таблицу и т.д. см. пример 9 или пример 10.
181. Описать путь испарения системы с массовой долей CCl4 20 %, рис. 9.
182. Описать путь испарения системы с массовой долей CCl4 40 %, рис. 9.
183. Описать путь испарения системы с массовой долей CCl4 50 %, рис. 9.
184. Описать путь испарения системы с массовой долей CCl4 60 %, рис. 9.
185. Описать путь испарения системы с массовой долей CCl4 80 %, рис. 9
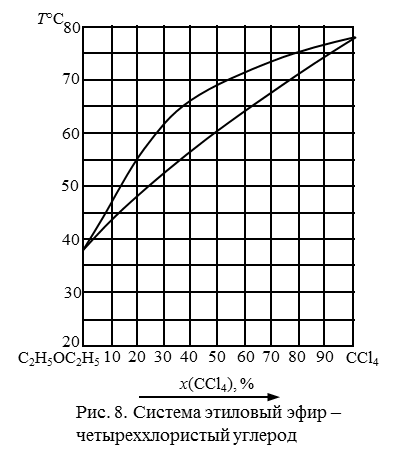
Рис. 9. Система диэтиловый эфир-четыреххлористый углерод.
186. Определить изменение состава и количества фаз в системе, содержащей 15 % воды (рис. 10) при охлаждении от 170 до 60°С с интервалом 40°С.
187. Определить изменение состава и количества фаз в системе, содержащей 25 % воды (рис. 10) при охлаждении от 170 до 60°С с интервалом 40°С.
188. Определить изменение состава и количества фаз в системе, содержащей 35 % воды (рис. 10) при охлаждении от 170 до 60°С с интервалом 40°С.
189. Определить изменение состава и количества фаз в системе, содержащей 45 % воды (рис. 10) при охлаждении от 170 до 60°С с интервалом 40°С.
190. Определить изменение состава и количества фаз в системе, содержащей 55 % воды (рис. 10) при охлаждении от 170 до 60°С с интервалом 40°С.
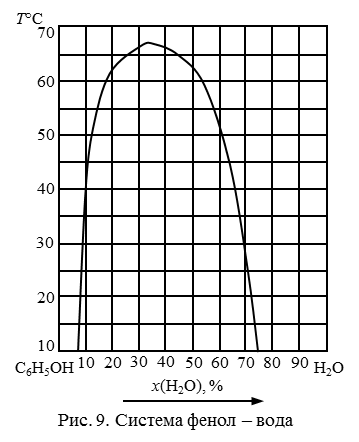
Рис. 10. Система фенол-вода.
191. Описать процессы, происходящие при конденсации системы, содержащей 20 % спирта (рис. 11). Можно ли из раствора заданного исходного состава выделить чистый спирт путем перегонки?
192. Описать процессы, происходящие при конденсации системы, содержащей 40 % спирта (рис. 11). Можно ли из раствора заданного исходного состава выделить чистый спирт путем перегонки?
193. Описать процессы, происходящие при конденсации системы, содержащей 50 % спирта (рис. 11). Можно ли из раствора заданного исходного состава выделить чистый спирт путем перегонки?
194. Описать процессы, происходящие при конденсации системы, содержащей 70 % спирта (рис. 11). Можно ли из раствора заданного исходного состава выделить чистый спирт путем перегонки?
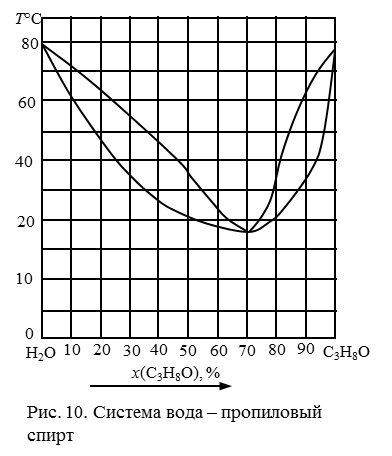
Рис. 11. Система вода – пропанол.
195. Описать процессы, происходящие при испарении раствора, содержащего 30 % кислоты (рис. 12).
196. Описать процессы, происходящие при испарении раствора, содержащего 50 % кислоты (рис. 12).
197. Описать процессы, происходящие при испарении раствора, содержащего 70 % кислоты (рис. 12).
198. Описать процессы, происходящие при испарении раствора, содержащего 10 % уксусной кислоты (рис. 12). Можно ли методом перегонки получить из этого раствора чистую уксусную кислоту?
199. Описать процессы, происходящие при испарении раствора, содержащего 80 % кислоты (рис. 12).
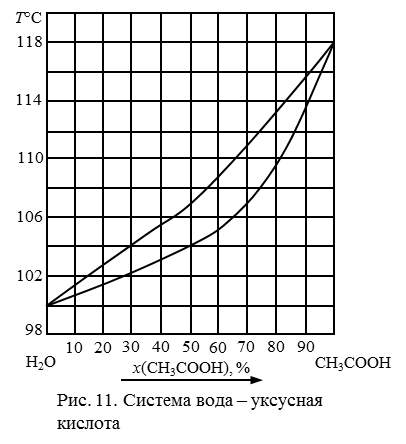
Рис. 12. Диаграмма состояния системы вода – уксусная кислота.
200. Перечертить диаграмму состояния неконденсированной системы (рис. 13), обозначить ее поля. Определить состав азеотропной жидкости. Описать последовательность процессов, происходящих при испарении раствора, содержащего 15 % HNO3. Заполнить таблицу 1. Можно ли методом перегонки этого раствора получить чистую азотную кислоту?
201. Перечертить диаграмму состояния неконденсированной системы (рис. 13), обозначить ее поля. Определить состав азеотропной жидкости. Описать последовательность процессов, происходящих при испарении раствора, содержащего 25 % HNO3. Заполнить таблицу 1. Можно ли методом перегонки этого раствора получить чистую азотную кислоту?
202. Перечертить диаграмму состояния неконденсированной системы (рис. 13), обозначить ее поля, дать характеристику компонентов этой системы, описать последовательность фазовых превращений при охлаждении и конденсации паров в системе, содержащей 40 % HNO3, а также при нагревании и испарении раствора, содержащего 75% HNO3.
203. Перечертить диаграмму состояния неконденсированной системы (рис. 13), обозначить ее поля. Определить состав азеотропной жидкости. Описать последовательность процессов, происходящих при испарении раствора, содержащего 55 % HNO3. Заполнить таблицу 1. Можно ли методом перегонки этого раствора получить чистую азотную кислоту?
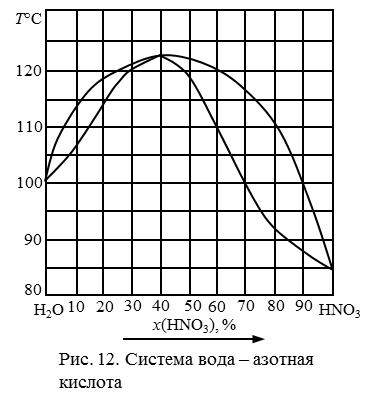
Рис. 13. Диаграмма состояния системы вода – азотная кислота.
204. Определить изменение состава и количества фаз в системе, содержащей 20 % анилина (рис. 14) при охлаждении от 165 до 60°С с интервалом 40°С.
205. Определить изменение состава и количества фаз в системе, содержащей 80 % анилина (рис. 14) при охлаждении от 165 до 60°С с интервалом 40°С.
206. Определить изменение состава и количества фаз в системе, содержащей 60 % анилина (рис. 14) при охлаждении от 165 до 60°С с интервалом 40°С.
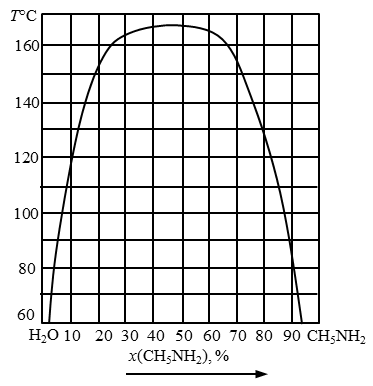
Рис. 14. Диаграмма состояния системы вода – анилин.
207. Определить изменение состава и количества фаз в системе, содержащей 40 % воды (рис. 15) при охлаждении от 220 до 40°С с интервалом 40°С.
208. Определить изменение состава и количества фаз в системе, содержащей 80 % воды (рис. 15) при охлаждении от 165 до 60°С с интервалом 40°С.
209. Определить изменение состава и количества фаз в системе, содержащей 60 % воды (рис. 15) при охлаждении от 165 до 60°С с интервалом 40°С.
210. Определить изменение состава и количества фаз в системе, при температуре 140 °С (рис. 15), содержащей от 0 до 80 % никотина с интервалом 40%.
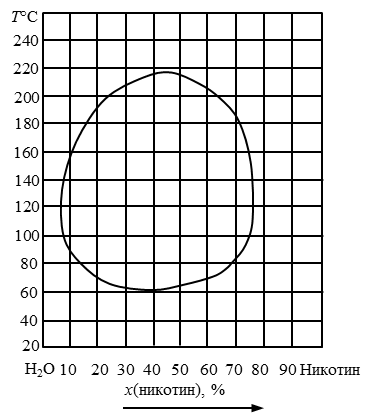
Рис. 15 Диаграмма состояния никотин-вода.
Дата: 2019-03-05, просмотров: 1160.