Температура. Поскольку реакция гидролиза эндотермическая, то повышение температуры смещает равновесие в системе вправо, степень гидролиза возрастает.
Концентрация продуктов гидролиза. Гидролиз - обратимый процесс. В соответствие с принципом Ле Шателье, повышение концентрации ионов водорода (для примера 1) приведет к смещению равновесия влево. Степень гидролиза будет уменьшаться. Также будет влиять увеличение концентрации гидроксид-ионов для реакции рассмотренной в примере 2.
Разбавление. В соответствии с принципом Ле Шателье, при разбавлении равновесие смещается в сторону протекания этой реакции, вправо, степень гидролиза возрастает.
Добавки посторонних веществ. На положение равновесия влияет добавление веществ, которые могут реагировать с одним из участников реакции.
Если в результате гидролиза образуются ионы водорода (гидролиз по катиону):
Men+ + H-OH 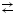 MeOH(n-1)+ + H+
MeOH(n-1)+ + H+
сдвинуть равновесие вправо можно:
- добавлением раствора гидроксида натрия (NaOH), содержащего гидроксид-ионы, которые будут взаимодействовать с ионами водорода;
- добавлением раствора соли, образованной сильным основанием и слабой кислотой (например, раствор сульфита натрия Na2SО3)
Вопрос 36
Окислительно-восстановительные реакции (ОВР), также редокс (сокр. англ. redox, от reduction-oxidation — восстановление-окисление) — это встречно-параллельные химические реакции, протекающие с изменением степеней окисления и не более 2 атомов, входящих в состав реагирующих веществ (или ионов веществ), реализующимся путём перераспределения электронов между атомом-окислителем (акцептором) и атомом-восстановителем (донором). В процессе окислительно-восстановительной реакции восстановитель отдаёт электроны, то есть окисляется; окислитель присоединяет электроны, то есть восстанавливается.
Восстановители: металлы, водород, уголь, окись углерода 2, сероводород, оксид серы, сернистая кислота+ее соли, галогеноводородные кислоты+их соли, катионы металлов в низших степенях окисления:
SnCl2, FeCl2, MnSO4, Cr2(SO4)3, азотистая кислота HNO2, аммиак NH3, гидразин NH2NH2, оксид азота(II) (NO)
Окислители: Галогены, Перманганат калия(KMnO4), манганат калия (K2MnO4), оксид марганца (IV) (MnO2), Дихромат калия (K2Cr2O7), хромат калия (K2CrO4), Азотная кислота (HNO3), Серная кислота (H2SO4) концентрированная, Оксид меди(II) (CuO), оксид свинца(IV) (PbO2), оксид серебра (Ag2O), пероксид водорода (H2O2), Хлорид железа(III) (FeCl3), Бертоллетова соль (KClO3)
Метод электронного баланса
1. Сначала необходимо составить схему реакции: записать вещества в начале и конце реакции, учитывая, что в кислой среде MnO4— восстанавливается до Mn2+:
Na2SO3 + KMnO4 + H2SO4 = Na2SO4 + MnSO4 + K2SO4 + H2O
2. Далее определим какие из соединений являются окислителем и восстановителем; найдем их степень окисления в начале и конце реакции:
Na2S+4O3 + KMn+7O4 + H2SO4 = Na2S+6O4 + Mn+2SO4 + K2SO4 + H2O
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6, таким образом, S+4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn+7 принимает 5 электронов и является окислителем.
3. Составим электронные уравнения и найдем коэффициенты при окислителе и восстановителе.
S+4 – 2e— = S+6 ¦ 5 восстановитель, процесс окисления
Mn+7 +5e— = Mn+2 ¦ 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
· Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
· Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn+7, ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S+4 коэффициентом перед окислителем:
5Na2S+4O3 + 2KMn+7O4 + H2SO4 = 5Na2S+6O4 + 2Mn+2SO4 + K2SO4 + H2O
Дата: 2019-02-19, просмотров: 443.