Экстракционный процесс характеризуется коэффициентом распределения D, представляющем собой отношение аналитических концентраций данного элемента в органической Сорг и водной Сводн фазах, D= Сорг/ Сводн. Мы уже говорили о большом технологическом значении этого показателя экстракционного равновесия. От чего зависит коэффициент распределения?
Следует заметить, что определяющее экстракцию взаимодействие извлекаемого вещества и экстрагента по необходимости должно быть сравнительно слабым, т.е. уменьшение энергии Гиббса экстракции DGо должно составлять 2-10 ккал/моль. При менее отрицательных значениях DGо константы равновесия и коэффициенты распределения слишком малы, при более отрицательных значениях DGо (т.е. при более сильных взаимодействиях) экстракция протекает успешно, но затрудняется другая необходимая операция – реэкстракция.
Предположим, что в процессе экстракции образуется простое моноядерное соединение:
Mводн + хAводн + уSорг « (MАxSy) орг
Константа равновесия этой реакции:
К = (MАxSy) орг /(M) водн. (A)х водн (S)уорг = [MАxSy]орг gорг/ [M]водн . [A]х водн [S]уорг gч+1водн
Но [M]орг = [MАxSy]орг; а = [M]оргD/[M]водн . Здесь круглые скобки обозначают активность, а прямоугольные – концентрацию. После несложных преобразований имеем:
D = К [A]х водн (S)уорг gч+1водн / gорг
т.е. коэффициент распределения – сложна функция концентраций и коэффициентов активностей, а поэтому в общем случае представляет собой переменную величину. Из этого уравнения, в частности, видна зависимость D от концентрации аниона [A]водн, что определяет его высаливающее действие.
Для целей технологии очень важно знать основные факторы или параметры, влияющие на значение коэффициента распределения. Рассмотрим важнейшие из них.
Природа экстрагента. Экстрагенты значительно отличаются друг от друга по своей способности экстрагировать металлы, в частности, уран, т.е. образовывать незаряженные координационные соединения между солью и растворителем, растворимые в избытке растворителя (или разбавителя). Это различие относится как к коэффициенту распределения, так и к емкости (т.е. максимальной растворимости) экстрагируемого соединения в данном экстрагенте. Очень важно обеспечить высокие коэффициенты распределения при низких концентрациях урана, так как это существенно на последних ступенях экстракции для получения сбросного рафината. Этот случай характеризуется крутой линией изотермы экстракции.
Природа экстрагируемого элемента. Способность к экстракции – специфическое свойство элементов. Ниже приводятся значения D различных элементов при использовании растворителей трех групп:
| 10 %-ный ТБФ | Д2ЭГФК |
Третичные амины | |||
| U6+ | 3,3 | U6+ | 250 | U6+ | 90 |
| Fe3+ | 0,0003 | V5+ | 2,1 | Mo6+ | 150 |
| Al3+ | 0,00000 | Al3+ | 1,6 | Zr4+ | 200 |
| Ca2+ | 0,0005 | Fe2+ | 0,1 | Th4+ | 0,1 |
| PO43- | 0,00000 | Mg2+, Ca2+, Al3+, Fe2+, Fe3+, РЗЭ, Се4+ | 0,01 | ||
| SO42- | 0,0065 | ||||
| РЗЭ | 0,005 | ||||
Как видно из этих данных, различие в экстракционной способности элементов по отношению к растворителям выражено чрезвычайно резко.
Окислительно-восстановительный потенциал среды и состояние элементов. Различные валентные состояния одного и того же элемента экстрагируются неодинаково. Например значения D для U6+ и U4+, Рu3+ и Рu4+, Ре3+ и Ре4+ отличаются друг от друга на многие порядки. Это позволяет влиять на экстрагируемость одного и того же металла варьированием окислительно-восстановительных условий среды.
Присутствие и концентрация комплексообразующих веществ. К экстрагируемой системе возможно добавлять различные комплексообразователи, повышающие или понижающие D.
Присутствие и концентрация высаливателей. В некоторых случаях добавка ряда растворимых веществ - так называемые высаливателей - в водную фазу способствует увеличению коэффициента распределения. Это относится главным образом к экстрагентам 1-й группы (диэтиловый эфир, ТБФ и др.). Введение высаливателей приводит к возрастанию концентрации анионов, т. е. повышению их активности в водной фазе, и увеличивает переход экстрагируемого вещества в органическую фазу. Аналогично влияет и азотная кислота в определенных пределах. Присутствующий нитрат-ион смещает реакцию UO22+ + 2NO3- « UO2(NO3)2 в правую сторону, т. е. в сторону образования экстрагируемой формы урана, входящей в образовавшийся сольват. Влияние повышения концентрации нитрат-иона будет показано дальше.
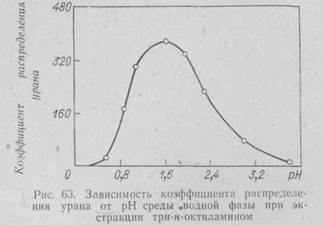
Влияние концентрации водородных ионов. Во многих случаях это влияние очень значительно и проявляется по-разному, в зависимости от механизма экстракции. На рис. 63 показано влияние рН среды на экстракцию урана три-н-октиламином из сернокислой среды. Регулирование рН среды может быть использовано для разделения некоторых близких по свойствам элементов экстракцией кислыми алкилфосфатами.
Влияние синергетического эффекта. Наблюдаются случаи, когда в системе водный раствор — органическая фаза присутствуют два экстрагента, каждый из которых может экстрагировать уран. Иногда эффективность действия смеси экстрагентов значительно выше суммарного действия экстрагентов в отдельности. В других случаях такой эффект, называемый синергетическим, или синергизмом, не наблюдается; коэффициент распределения остается неизменным или даже уменьшается.
В экстракционной технологии синергизм имеет большое практическое значение. В частности, важное свойство диалкилфосфорных кислот (например, Д2ЭГФК) состоит в том, что при сочетании их с нейтральными фосфорорганическими соединениями (ТБФ, ТОФО) можно получить очень большое (синергетическое) увеличение D для урана (VI), причем экстракционная способность такой смеси значительно выше суммарной экстракционной способности отдельных экстрагентов. Так, при рН=1 в сернокислой среде и 25° С, 0,1 М Д2ЭГФК имеет D по урану (VI) равный 135. В тех же условиях для 0,1 М ТБФ D ==0,0002, а для 0,1 М ТБФО D= 0,0025. Для смеси Д2ЭГФК и 0,05 М каждого из этих нейтральных экстрагентов D равно соответственно 500 и 7000. Синергетический эффект иллюстрирует рис. 64.
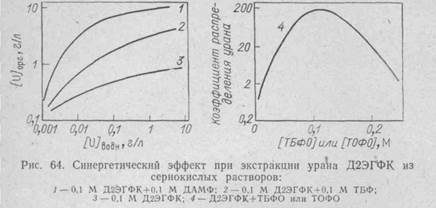
Чем объясняется этот эффект? Химическая природа синергизма еще не вполне ясна. Усиление экстракционной способности диалкилфосфорных экстрагентов в присутствии нейтральных фосфорорганических соединений иногда объясняют сочетанием двух факторов:
1) взаимодействием нейтральных фосфорорганических соединений (НФОС) с димерами кислых фосфорорганических соединений (КФОС) в результате присоединения нейтрального реагента к уранилдиалкилфосфатному комплексу посредством водородной связи, в результате чего увеличивается «активная концентрация» КФОС в органической фазе:
UO2X4H2 + R3PO = UO2X4H2 … OPR3
т. е. принимают, что синергетический эффект вызван экстракцией дополнительно образовавшегося смешанного сольвата;
2) участием нейтрального реагента в построении координационно-насыщенного комплексного соединения уранил-иона с органическими лигандами.
Синергетический эффект можно объяснить и тем, что КФОС нейтрализует заряд иона металла, а НФОС вытесняет (замещает) остаточную кристаллизационную воду, делая комплекс металла более гидрофобным, т. е. происходит сочетание двух механизмов: катионообменного и сольватного.
Константа димеризации для алкилфосфорных кислот очень велика, например, для дибутилфосфорной кислоты в керосине она равна 105. Это соответствует изменению DG при димеризации около—8 ккал/моль. Поскольку мономерные ТБФ или ТОФО устраняют необходимость мономеризации молекул димера (НR)2 или (НR2)2, изменение DG в процессе этого замещения составляет также не менее—8 ккал/моль, что может объяснить, по крайней мере частично, повышение извлечения достигаемое при добавлении нейтральных экстрагентов.
Синергетическое влияние повышается в том же порядке, который наблюдается для коэффициентов распределения с чистыми эсктрагентами, используемыми в качестве добавок, а именно: фосфат <фосфонат<фосфинат<фосфиноксид.
Как правило, синергетический эффект наблюдается только для урана, что открывает пути к повышению селективности действия кислых алкилфосфатов, особенно в условиях насыщения органической фазы ураном. Основное же значение синергетического эффекта в возможности сокращения ступеней (числа контактов) экстракции и более глубокого извлечения урана из рафината на последних ступенях экстракционного каскада.
Для моноалкилфосфатов (например, для моногептилфосфоновой кислоты) наблюдается антагонистический эффект вследствие добавки НФОС, в результате чего коэффициент распределения урана заметно уменьшается.
Дата: 2019-02-25, просмотров: 467.