| экстрагент | Ткип, оС | Растворимость в воде, г/100 г | Плотность, г/см3 | Твсп, оС | Вязкость, сПз |
| ДДФК С12Н25РО4Н2 | - | 0,65 | 1 | Не горит | 3 – 4 |
| Д2ЭГФК [СН2СН(С2Н5)(СН2)4]2РООН | 85 | 0,012 | 0,975 | 475 | 4,22 |
| ОПФК (С8Н17О2)РО5Н2 | - | 0,03 | - | 100 | - |
*- октилпирофософрная кислота
Общей закономерностью является уменьшение растворимости алкилфосфатов в воде в ряду: моно->ди->три- и возрастание в ряду неполярных растворителей: моно-<ди-<три-.
3-я группа – органические соединения, для которых растворимость в неполярных растворителях обусловлена образованием солей с органическим катионом, поэтому металлы, в том числе уран, экстрагируются, если они образуют комплексные анионы. Примером подобных экстрагентов служат органические амины (табл. 25).
Таблица 25
Характеристика аминов, применяемых в технологии урана
| экстрагент | Молекулярная масса | Ткип, оС | Растворимость в воде, г/100 г | Плотность, г/см3 | Твсп, оС | Вязкость, сПз |
| Три-н-октиламин (ТОА) (С8Н17)3N | 353 | 340 | 0,007 | 0,82 | 145 | 6,02 |
| Три-н-дециламин (ТДА) [(СН3-(СН2)9]3N | 437,8 | 245 | 0,01 | 0,81 | - | - |
Ниже приведена структура аминов как производных аммиака.
| Амины | Структура | ||||||||||||
| Первичные |
| ||||||||||||
| Вторичные |
| ||||||||||||
| Третичные |
|
К аминам относятся также четвертичные аммониевые основания (ЧАО) и их соли:
| [ | R2 | ] | |||
| ½ | |||||
| R1¾ | N | ¾R3 | (OH) | ||
| ½ | |||||
| R4 |
В аминах, как и в аммиаке, азот имеет неподеленную пару электронов, что обуславливает их способность к образованию координационных соединений.
Подобно аммиаку амины реагируют с кислотами, давая соль амина (алкиламмония):
NH3 + HCl ® NH4Cl
R3N + HCl ® [R3NHCl];
2R3N + H2SO4 ® [(R3NH)2SO4].
Эти соли аминов и служат экстрагентами:
(R3NН)2SO4 + [UO2(SO4)2]2- Û [(R3NH)2UO2(SO4)2]+ SO42-
т.е. по существу реализуется анионнообменный механизм экстракции и амины ведут себя подобно анионнообменной смоле (только жидкой). В общем случае такое взаимодействие с амином может быть выражено так:
UO2 2+ водн + SO42-водн + n[(R3NH)2SO4]орг Û [UO2SO4] . n[(R3NН)2SO4 ]орг
Характерная особенность экстракции аминами в том, что равновесие устанавливается в течение нескольких секунд. И при экстракции аминами в органической фазе происходит полимеризация, причем фактор полимеризации n=4¸4,8.
Существенно, что экстракция аминами протекает только в том случае, когда водная фаза содержит ионы водорода в количестве, достаточном для превращения амина в замещенную соль аммония, так как экстрагентами могут быть только соли аминов.
С позиций координационной химии более правильно описать реакцию комплексообразования при экстракции аминами следующим образом:
(R3NН)2SO4 + [UO2(SO4)(H2O)3] Û (R3NH)2[UO2(SO4)2(H2О)2] + H2O
т.е. и в этом случае наблюдается вытеснение воды, что подтверждает ее важную роль при экстракции. Отсюда крылатое выражение: «без воды нет экстракции!».
Как и многие другие реакции комплексообразования соединений уранила реакции их а аминами имеют ступенчатый характер. В зависимости от концентрации реагентов, рН среды, температуры и других факторов возможно образование соединений в органической фазе, где на 1 моль уранила приходится 4 и более молей амина:
2(R3NН)2SO4 + [UO2(SO4)(H2O)3] ® (R3NH)4[UO2(SO4)3] + 3H2O
33(R3NН)2SO4 + [UO2(SO4)(H2O)3] ® (R3NH)6[UO2(SO4)4] + 3H2O
Структурная формула координационных соединений этого типа выглядит следующим образом:
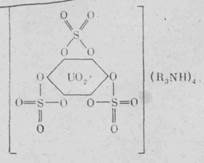
Экстракционная способность аминов увеличивается в ряду: первичные < вторичные < третичные < четвертичные. В экстракционной технологии урана, как правило, применяют третичные амины, в частности три-н-октиламин и три-изо-октиламин.
Иногда при экстракции аминами соединений урана образуется так называемая третья фаза, что нарушает нормальное течение процесса. Это явление наиболее характерно для систем аминосульфат уранила — алифатический углеводород (керосин). Образование третьей фазы предотвращают обычно добавлением небольшого количества длинноцепочечного спирта, изменяющего диэлектрические свойства соли амина.
РАЗБАВИТЕЛИ
Некоторые комплексные соединения урана, образующиеся в процессе взаимодействия с экстрагентом, слабо растворимы в избытке экстрагента. Кроме того, некоторые из них имеют плотность, близкую к 1, и большую вязкость. Существуют также экстрагенты, являющиеся твердыми веществами, например триоктилфосфиноксид (ТОФО). Поэтому при экстракции урана широко применяют разбавители органических фаз, такие, как керосин, гексан, бензол, уайт-спирит, или высококипящие фракции ароматических углеводородов. Впрочем, последние используют редко, так как они представляют собой канцерогенные вещества.
Чаще всего разбавитель химически не взаимодействует с извлекаемым металлом, поэтому его называют инертным разбавителем. Однако этот термин условен, так как иногда разбавитель существенно влияет на многие показатели экстракции (избирательность, коэффициенты распределения и др.). Основные требования к разбавителям в технологии урана — экономичность и безопасность. Желательно, чтобы разбавитель был дешев, не токсичен, имел возможно более высокую температуру вспышки. Из этих соображений обычно в качестве разбавителя используют гидрированный керосин, представляющий собой керосиновую фракцию разгонки нефти после ее гидрирования для перевода непредельных углеводородов в предельные.
Укажем некоторые свойства керосина: в воде практически не растворим, Ткип=170—240°С, плотность 0,74 г/см3, вязкость 0,3—0,5 сПз.
Дата: 2019-02-25, просмотров: 372.