Электрофильное присоединение к алкенам происходит через стадию образования более устойчивого карбокатиона (правило Марковникова).
Рассмотрим двухстадийный механизм присоединения бромоводорода к алкенам: медленная стадия - образование карбокатиона, быстрая стадия - присоединение нуклеофила (BrΘ).
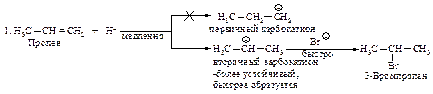
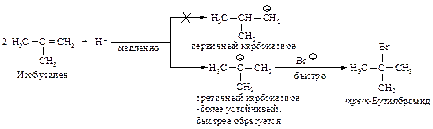
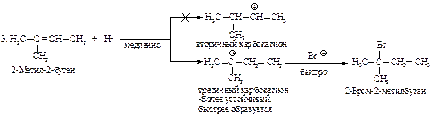
Рассмотрение механизма реакций показывает, что в первой стадии вторичный карбокатион образуется быстрее, чем первичный по реакции 1, а третичный - быстрее, чем первичный и вторичный, как следует из реакций 2 и 3.
Легкость образования карбокатионов увеличивается в следующей последовательности: метильный < первичный < вторичный < третичный.
С другой стороны, устойчивостькарбокатионов возрастаетв таком же порядке: метильный < первичный < вторичный < третичный.
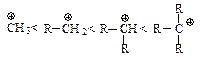
Такой порядок изменения устойчивости можно объяснить следующим образом. Согласно законам физики, устойчивость заряженной системы повышается при распределении заряда. Связь sp3-гибридизованного атома углерода с различными группами (X, Y) в той или иной степени поляризована из-за различной электроотрицательности элементов. Полярность этих связей сравнивается с полярностью связи C–H, выбранной в качестве стандарта. Перераспределение электронной плотности σ-связи под влиянием какой-либо группы по сравнению с распределением электронной плотности связи С–Н называется индукционным (индуктивным) эффектом (I).
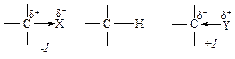
Группа X, которая притягивает пару электронов s-связи сильнее, чем атом водорода, проявляет электроноакцепторный эффект (минус I). Группа Y, которая отталкивает пару электронов s-связи, проявляет электронодонорный эффект (+I). Под влиянием заряда, образующегося на атоме углерода, поляризуются соседние связи, но этот эффект быстро затухает по цепи связей C–C.
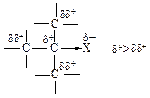
Алкильные группы имеют тенденцию подавать электроны по сравнению с атомом водорода, следовательно, алкильная группа проявляет электронодонорный индукционный эффект (+I). Подавая электроны s-связи на положительно заряженный атом углерода, она приобретает некоторый положительный заряд, а заряд на центральном атоме в некоторой степени уменьшается. В третичном карбокатионе положительный заряд распределен между третичным углеродом и тремя алкильными группами, поэтому третичный карбокатион наиболее устойчив. Наоборот, метильный - наименее устойчив, т.к. в нем заряд локализован на одном атоме углерода. Чем большераспределен заряд в карбокатионе, тем он устойчивее.
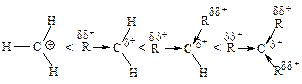
Устойчивость карбокатионов изменяется в таком же порядке, как и легкость, их образования.
Дата: 2018-12-21, просмотров: 416.