Михаил Бушма

«Чернила писателя более сокровенны, чем кровь мученика»
Противосудорожные лекарственные средства
Определение. Это лекарственные средства, угнетающие функции моторных центров ЦНС и применяющиеся при эпилепсии.
Эпилепсия. Второе по частоте заболевание головного мозга после инсульта. У детей – в 2 раза чаще. Это хроническое заболевание, характеризующееся периодическим возникновением судорог. Судороги – состояние временной дисфункции ЦНС, вызванное аномальными нейрональными разрядами. Причины судорог: инфекции, новообразования, травмы и др. Они приводят к кратковременно повторяющимся ненормальным движениям или восприятиям. Судороги могут сопровождаться зрительными, слуховыми, обонятельными галлюцинациями. В возникновении некоторых видов судорог большую роль играет наследственность.
Этиология. Судороги – результат чрезмерного возбуждения малой группы нейронов, локализованных в специфической области головного мозга, называемой первичный очаг (рис. 12.1).
|
 + + + +
+ + + +

 − − − −
− − − −
|

+ +

 − −
− −
Рисунок 12.1. Патогенез эпилепсии
Различают эпилепсию: первичную, вторичную.
Первичная эпилепсия. Нет специфических анатомических причин для судорог (травма, опухоль). Это идиопатическая эпилепсия. Судороги вызваны наследственной ненормальностью в ЦНС. Больные длительно принимают противоэпилептические лекарственные средства для сохранения жизни.
Вторичная эпилепсия. Встречается при опухолях, заболеваниях сердца, гипогликемии, менингитах, симптомах быстрой отмены алкоголя у алкоголиков и т.д.
Классификация эпилепсии (рис. 12.2)

Рисунок 12.2. Классификация эпилепсии
Частичная эпилепсия. Очаг в ЦНС локализован. Не распространяется на другие отделы.
Простые судороги. Больной в сознании. Подергивается одна группа мышц 1-2 минуты.
Сложные судороги. Человек совершает действия с выключенным сознанием. Он может уехать в другое место и не помнить, как здесь оказался. Опасны для жизни.
Генерализованная эпилепсия. В судорожную активность вовлечена вся ЦНС. Может быть: первично или вторично генерализованная. Последняя начинается как частичная, а затем распространяется на другие отделы ЦНС.
Тонико-клонические судороги. Вначале тонические судороги. ↑ Тонус мышц. Человек падает. Вытягиваются ноги в течение 30 секунд. Затем сокращаются конечности. Теряется сознание. Не помнит о случившемся.
Абсанс. Потеря сознания на несколько секунд. Мгновенные движения мышц лица, глаз, конечностей. Припадок настолько короткий, что больной не успевает упасть. Может выронить то, что держал в руках. Припадок многократно повторяется в течение суток.
Миоклонические судороги. Клонические сокращения различных мышц.
Атонические судороги. Внезапная потеря мышечного тонуса. Человек падает. Для профилактики травм ЦНС носят мотоциклетные шлемы.
Инфантильные спазмы. Сгибание и разгибание тела и конечностей («ванька-встанька») в возрасте до 1 года. Умственная отсталость.
Фебрильные судороги. У детей до 1 года. Развиваются при ↑ температуры тела.
Эпилептический статус. Большие судорожные припадки, следующие один за другим. При отсутствии лечения – смерть от тяжелых дыхательных и метаболических расстройств. Неотложное состояние.
Стратегия лечения эпилепсии – нормализация сниженного порога трансмембранного потенциала нейронов эпилептогенного очага. Ее реализуют: 1) ↑ положительный заряд наружной поверхности плазматической мембраны нейронов, 2) ↑ отрицательный заряд внутренней поверхности (рис. 12.3).
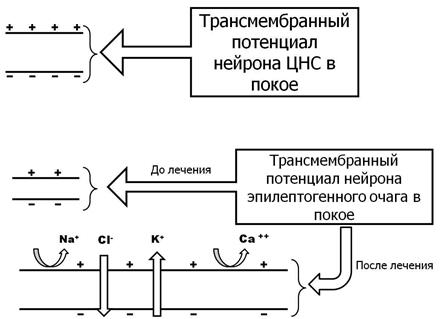
Рисунок 12.3. Стратегия лечения эпилепсии
Применяют: блокаторы Na+- и Ca++-каналов; средства, способствующие выходу К+ из нейронов и поступлению Cl- в нейроны.
Классификация. Лекарственные средства: первой, второй линии.
Противоэпилептические лекарственные средства первой линии
Классификация (рис. 12.4)


Рисунок 12.4. Противоэпилептические лекарственные средства
первой линии
Простые, сложные и тонико-клонические судороги
Фенитоин
Механизм действия. Блокирует натриевые каналы нейронов эпилептогенного очага.
Действие. ↓ Распространение ненормальных импульсов в ЦНС (высокоэффективен). Антиаритмик.
Применение. Простые, сложные, тонико-клонические судороги, эпилептический статус, тахиаритмии.
Побочное действие. Нистагм, потеря плавности движений глаз, диплопия, атаксия, тошнота, рвота, гиперплазия десен. Гипертрихоз, ↓ рефлексов, галлюцинации, сонливость, кожная сыпь. Эксфолиативные дерматиты, агранулоцитоз. Гипергликемия и глюкозурия (↓ секрецию инсулина). Тератоген (заячья губа, врожденные пороки сердца, замедление роста, умственное недоразвитие).
Взаимодействие. С другими противосудорожными, антикоагулянтами, оральными противозачаточными, хинидин ом, доксициклин ом, циклоспорин ом, мексилетин ом, метадон ом, леводоп ой. Результат – ↑ метаболизма и ↓ их действия в результате индукции фенитоин ом цитохромов Р450.
Карбамазепин
Строение. Похож на антидепрессанты.
Механизм действия. См. фенитоин. Затрудняет синаптическую передачу.
Применение. Простые и сложные судороги (наилучший). Тонико-клонические судороги (высокоэффективен). Маниакально-депрессивный психоз. Невралгия тройничного нерва.
Побочное действие. Диплопия, атаксия, расстройства ЖКТ, потеря равновесия, сонливость, ↓ дыхания, ступор, гепатотоксичность, эритематозная кожная сыпь (показатель непереносимости), смерть.
Абсанс
Этосуксимид (наилучший).
Механизм действия. Ингибирует ГАМК-аминотранс-феразу, метаболизирующую ГАМК. Уровень последней в ЦНС ↑. ↑ Поступление Cl- в нейроны. Гиперполяризация мембран нейронов.
Побочное действие. Боль в эпигастрии, тошнота, рвота. [Примечание. Для их профилактики лечение этосуксимид ом начинают с малых доз, постепенно повышая до лечебных]. Сонливость, вялость, головокружение, беспокойство, возбуждение, тревога, неспособность к концентрации внимания. Синдром Стивенса-Джонсона, мелкоточечная сыпь. Лейкопения, апластическая анемия, тромбоцитопения.
Клоназепам
Механизм действия. Возбуждает бензодиазепиновый рецептор. Улучшается взаимодействие ГАМК с рецептором. ↑ Частота открытия хлорных каналов. Больше Cl- входит в нейроны. Гиперполяризация мембран нейронов элиптогенного очага. Их активность ↓.
Действие. Противосудорожное и седативное, особенно в начале лечения. Действует долго.
Побочное действие. Успокоение, сонливость, вялость, утомляемость, атаксия, головокружение, изменения поведения. При быстром внутривенном введении – угнетение дыхания и сердечной деятельности.
Вальпроевая кислота. Противосудорожное действие обнаружено при ее использовании в качестве растворителя в процессе поиска других противосудорожных лекарственных средств.
Механизм действия. Вызывает гиперполяризацию нейронов эпилептогенного очага за счёт: ↓ поступления Na+ и Са++ в нейроны; ↑ поступления Cl- в нейроны и К+ из нейронов.
Действие. Высокоэффективна.
Побочное действие. Тошнота, рвота, успокоение, атаксия, дрожь. Гепатотоксична (особенно у детей до 2-х лет). В плазме ↑ активность печеночных ферментов. Тромбоцитопения, ↓ агрегации тромбоцитов. Тератогенность: spina bifida, сердечно-сосудистые, оро-фациальные аномалии и аномалии пальцев.
Миоклонические судороги
Вальпроевая кислота. Эффективность поразительна.
Клоназепам (см. выше).
Атонические судороги
Вальпроевая кислота (см. выше).
Инфантильные спазмы
Нитразепам
Механизм действия. См. клоназепам.
Фебрильные судороги
Фенобарбитал
Механизм действия. 1. Связывается с аллостерическим регуляторым участком ГАМК-рецептора. ↑ ГАМК-зависимый ток Cl- в нейроны за счёт продления времени открытия хлорных каналов. 2. Блокирует возбуждение ЦНС, особенно опосредованное глутаматными рецепторами.
Побочное действие. Атаксия, мышечная слабость, раздражительность (постепенно исчезают). Тошнота, рвота, кожная сыпь. ↓ Познавательные способности детей.
Эпилептический статус
Фенитоин
Механизм действия. См. стр. 191.
Диазепам
Механизм действия. ↑ Ток Cl- в нейроны.
Действие. При внутривенном введении оба быстро устраняют судороги.
Лоразепам
Механизм действия. См. клоназепам.
Действие. Эффективнее диазепам а.
Геминейрин
Механизм действия. Неизвестен.
Дозирование. Внутривенно до наступления сна.
Тиопентал
Механизм действия. См. фенобарбитал.
Действие. Общий анестетик.
Противоэпилептические лекарственные средства второй линии. Применяют при неэффективности или непереносимости лекарственных средств первой линии, как наилучших.
Классификация (рис. 12.5)


Рисунок 12.5. Противоэпилептические лекарственные средства
второй линии
Простые судороги
Фенобарбитал. См. выше.
Вигабатрин
Механизм действия. Необратимо ингибирует ГАМК-аминотрансферазу, катализирующую деградацию ГАМК. ↑ Концентрация ГАМК в синапсах и, как следствие, поступление Cl- в нейроны.
Действие. Торможение ЦНС. Устраняется повышенная возбудимость нейронов эпилептогенного очага.
Фармакокинетика. Всасывается в ЖКТ. Метаболизируется в печени. Выводится с мочой.
Побочное действие. Сонливость, головокружение, ↑ массы тела, психомоторное возбуждение, психоз.
Противопоказания. Психические заболевания.
Ламотриджин
Механизм действия. Блокирует Na+-каналы нейронов.
Фармакокинетика. Период полувыведения 24 часа. Выводится с мочой в форме глюкуронидов.
Примидон
Механизм действия. См. фенобарбитал.
Действие. Эффективнее фенобарбитала.
Фармакокинетика. Метаболизируется до фенобарбитала и фенилэтилмалонамида. [Примечание. Противосудорожным действием обладают примидон и его метаболиты].
Побочное действие. См. фенобарбитал.
Применение. Простые, сложные, тонико-клонические судороги.
Топирамат
Механизм действия. См. фенитоин + усиливает тормозное действие ГАМК на нейроны эпилептогенного очага, повышая уровень Cl- в нейронах.
Тиагабин
Механизм действия. Блокирует обратный нейрональный захват ГАМК. ↑ Уровень Cl- в нейронах.
Сложные судороги
Примидон, ламотриджин. См. выше.
Клоразепат
Строение. Производное бензодиазепина.
Механизм действия. См. клоназепам.
Применение. Для комбинированной терапии сложных судорог у взрослых.
Побочное действие. Сонливость.
Топирамат, тиагабин. См. выше.
Тонико- клонические судороги
Вальпроевая кислота, фенобарбитал, примидон. См. выше.
Абсанс, миоклонические судороги
Ламотриджин. См. выше.
Паркинсонизм
Патогенез. В норме нейроны Substantia nigra посылают аксоны в neostriatum. Выделяется дофамин. Тормозит neostriatum. Нейроны neostriatum посылают аксоны в substantia nigra. Выделяется ГАМК. Тормозит substantia nigra. Эти обоюдные тормозные пути поддерживают ингибирование двух отделов ЦНС. Кроме того, нейроны коры головного мозга и таламуса посылают аксоны в неостреатум. Выделяется ацетилхолин. Он возбуждает ГАМК-нейроны. Регулирует грубые осознанные движения.
При паркинсонизме погибают дофаминовые нейроны substantia nigra. ↓ Торможение neostriatum (рис. 12.6).
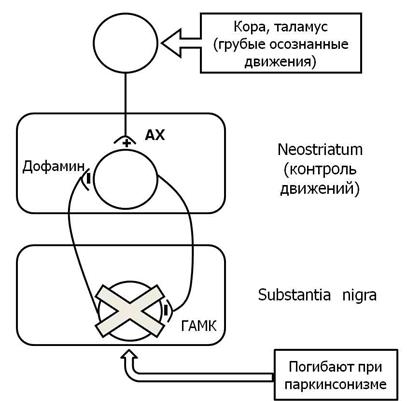
Рисунок 12.6. Патогенез паркинсонизма
Снижение образования дофамина и преобладание ацетилхолина в неостриатуме приводит к ↓ возбуждения: 1) моторной зоны коры головного мозга глутаминовой кислотой, 2) мотонейронов передних рогов спинного мозга. Это проявляется нарушениями движений (паркинсонизм).
Этиология. Нейротоксины, свободные радикалы, неизвестные факторы внешней среды вызывают гибель дофаминовых нейронов substantia nigra. При отсутствии лечения болезнь быстро прогрессирует.
Клиника. Тремор, ригидность мышц, брадикинезия (замедление произвольных движений), ненормальная поза и походка. Чаще болеют мужчины (один из ста в возрасте > 70 лет).
Лекарственный паркинсонизм. Нейролептики, блокируя дофаминовые рецепторы в неостриатуме, могут вызвать симптомы паркинсонизма. Противопоказаны больным паркинсонизмом.
Лечение паркинсонизма. 1. Усиление торможения нео-стриатума дофамином. 2. Снижение возбуждения неостриатума ацетилхолином.
Классификация лекарственных средств (рис. 12.7)


Рисунок 12.7. Противопаркинсонические лекарственные средства
Лекарственные средства, ↑ торможение неостриатума дофамином
Предшественники дофамина
Леводопа
Строение. Тирозин, проникая в адренергический нейрон, превращается в ДОФА. Леводопа – левовращающийся изомер ДОФА.
Механизм действия. Дофамин не проходит через гематоэнцефалический барьер. Леводопа проникает в ЦНС. Превращается в дофамин.
Действие. Леводопа восстанавливает сниженный уровень дофамина в неостриатуме. Образованный из леводопы дофамин возбуждает рецепторы на телах нейронов неостриатума и тормозит их. Устраняются симптомы поркинсонизма.
Применение. Облегчение, вызванное леводопа, проявляется только в период её наличия в организме. Эффективна в первые несколько лет приема. Это связано с постоянной гибелью дофаминовых нейронов substantia nigra.
Фармакокинетика. 97-99% Леводопы на периферии превращается в дофамин (рис. 12.8).
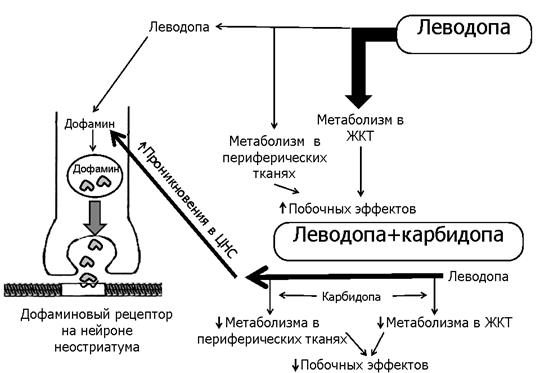
Рисунок 12.8. Фармакокинетика леводопы
(отдельно, и в комбинации с карбидопой)
Побочное действие дофамина, образованного из леводопы.
ЦНС. Дискинезии. [Примечание. Противоположны проявлениям паркинсонизма и отражают сверхактивность дофаминовых рецепторов в неостриатуме]. Депрессия, тревожность, возбуждение, нарушения сознания, бред, галлюцинации, ночные кошмары, эйфория.
Глаз. Расширение зрачка, приступ острой закрытоугольной глаукомы.
ЖКТ. Анорексия, тошнота, рвота.
Сердечно-сосудистая система. Аритмии.
Взаимодействие леводопы . С ингибиторами МАО (селегилин). Результат – гипертонический криз в результате ↑ образования катехоламинов.
Противопоказания. Психические заболевания. [Примечание. Обостряется течение].
Комбинированные противоэпилептические лекарственные средства. Эффекты леводопы на ЦНС усиливаются ингибиторами дофаминдекарбоксилазы, которые не проникает через ГЭБ: 1) карбидопой, 2) бенсеразидом. Они ↓ метаболизм леводопы в ЖКТ и периферических тканях. ↑ Её содержание в ЦНС. Дозу леводопы ↓ в 4–5 раз. ↓ Побочное действие образуемого на периферии дофамина.
«Наком»
Состав. Леводопа + карбидопа (10+1).
«Синемет»
Состав. Леводопа + карбидопа (10+1) или (4+1).
Фармакокинетика. Имеются пролонгированные формы «синемет», что позволяет снизить кратность приема.
Побочное действие. При комбиноции леводопы с карбидопой частота дискинезий возрастает до 80%. Чаще регистрируются нарушения поведения (см. леводопа).
Мадопар
Состав. Леводопа + бенсеразид (4+1).
Леводопа в комбинации с карбидопой и бенсеразидом – сильнодействующие лекарственные средства, используемые для длительного лечения паркинсонизма.
Ингибиторы МАО-В
Селегилин
Механизм действия. Избирательный ингибитор МАО-В, которая метаболизирует дофамин. [Примечание. Не ингибирует МАО-А, которая метаболизирует норэпинефрин и серотонин]. ↑ Содержание дофамина в neostriatum .
Взаимодействие. С леводопой. Результат – ↑ действия последней. Дозу леводопы ↓.
Лекарственные средства, ↑ синтез, высвобождение и ↓ обратный нейрональный захват дофамина
Амантадин
Механизм действия. ↑ Синтез, высвобождение и ↓ обратный нейрональный захват дофамина в сохранившихся нейронах substantia nigra.
Действие. Противопаркинсоническое (слабее леводопы), протиивогриппозное.
Побочное действие. Депрессия, беспокойство, раздражительность, малосонница, галлюцинации, нарушения сознания. Менее выражены, чем у леводопы.
Глудантан
Действие. В сравнении с амантадин ом, слабее влияет на ригидность и акинезию. Сильнее устраняет тремор.
Фармакокинетика. Лучше леводопы проникает в ЦНС.
Применение. В комбинации с леводопой и тригексифенидил ом.
Побочное действие. См. леводопа.
Ингибиторы КОМТ. Подавление ДОФА-декарбоксилазы карбидопой и бенсеразидом приводит к компенсаторной активации КОМТ. ↓ Эффективность леводопы. В связи с этим применяют селективные ингибиторы этого фермента (толкапон) в комбинации с леводопой.
Стимуляторы рецепторов дофамина. В мозгу больных паркинсонизмом истощены ферменты биосинтеза дофамина. Поэтому полезны агонисты дофамина.
Бромокриптин
Происхождение. Алкалоид спорыньи.
Строение. Производное эрготамина.
Механизм действия. Частичный агонист D2-рецепторов.
Применение. В комбинации с леводопой.
Побочное действие. См. леводопа. При психических заболеваниях бромокриптин вызывает ухудшение психического состояния. Серьезные проблемы с сердцем могут развиться у больных, перенесших инфаркт миокарда. У больных с заболеваниями периферических сосудов возможно ухудшение состояния в результате их сужения. Обостряется язвенная болезнь желудка.
Лизурид
Происхождение. Производное алкалоидов спорыньи.
Перголид
Механизм действия. Агонист D1- и D2-рецепторов.
Применение. Больные паркинсонизмом, не получающие леводопу. [Примечание. При длительном применении развивается толерантность].
Побочное действие. См. бромокриптин.
Лекарственные средства, ↓ возбуждение неостриатума ацетилхолином
Тригексифенидил
Механизм действия. Антагонист мускарина.
Действие. Слабее леводопы. Облегчает тремор, ригидность мышц, но не брадикинезию.
Побочное действие. Сухость во рту, запоры, нарушения аккомодации.
Паркинсонизм, вызванный лекарственными средствами. Резерпин и тетрабеназин опустошают запасы дофамина в везикулах. Галопидол и фенотиазиновые нейролептики блокируют дофаминовые рецепторы. Следовательно, они могут вызвать паркинсонизм. При их применении лекарственный паркинсонизм возникает ≈ через 3 месяца от начала лечения. Симптомы исчезают в течение нескольких недель или месяцев после отмены.
В 1983 году открыта лекарственная форма паркинсонизма у химиков, пытавшихся синтезировать и применить наркотик меперидин. В действительности синтезировали и ввели себе
1-метил-4-фенил-1,2,5,6-тетрагидропиридин. Он избирательно накапливается в дофаминовых нейронах substantia nigra. Они погибают. Развивается тяжелая форма паркинсонизма.
Спастичность. Характеризуется спазмами мышц сгибателей и мышечной слабостью. Возникает у больных рассеянным склерозом и инсультом. Механизм развития спастичности – повреждение нисходящих тормозных путей, приводящих к гипервозбудимости a-мотонейронов спинного мозга.
Классификация лекарственных средств (рис. 12.9)

Рисунок 12.9. Лекарственные средства, применяемые
при спастичности
Действующие на ствол мозга
Циклобензаприн
Действие. Седативное средство на уровне ствола мозга.
Применение. Острые мышечные спазмы, развивающиеся при церебральном параличе, травмах спинного мозга.
Побочное действие. Антагонист мускарина (успокоение, нарушения сознания, зрительные галлюцинации).
Действующие на спинной мозг
Диазепам
Механизм действия. ГАМК-миметик в спинном мозге.
Применение. Мышечные спазмы любого генеза, в том числе при пересечении спинного мозга, травмах мышц.
Побочное действие. Заторможенность.
Баклофен
Механизм действия. 1. Агонист ГАМК-В рецепторов. 2. ↓ Высвобождение возбуждающих нейромедиаторов. 3. Тормозит высвобождение из нейронов спинного мозга субстанции Р. [Примечание. Субстанция Р – медиатора боли. Торможение её выделения приводит к ↓ мышечной боли при спастичности].
Действие. Менее выраженное, чем у диазепам а.
Применение. Для устранения спазма мышц и боли при спастичности.
Фармакокинетика. Вводят только в спинномозговой канал. Плохо выходит из ликвора.
Побочное действие. Заторможенность. [Примечание. Менее выражена, чем у диазепам а].
Тизанидин
Механизм действия. α2-Адренергический агонист. Тормозит передачу болевых импульсов в дорсальных рогах спинного мозга.
Действие. Антиспастическое, обезболивающее.
Применение. Короткими курсами.
Побочное действие. ↓ АД, успокоение, сухость во рту, запор, нарушения зрения, галлюцинации.
Толперисон
Действие. Блокирует полисинаптические спинномозговые рефлексы. Угнетает ретикулярную формацию. Слабый спазмолитик и вазодилататор.
Применение. 1. Заболевания, сопровождающиеся ↑ тонуса скелетной мускулатуры (спинномозговые и центральные параличи, травмы спинного мозга, парапарезы, параплегии, рассеянный склероз, облитерирующий эндартериит). 2. Эпилепсия. 3. Энцефалопатия у детей. 4. Церебральный болевой синдром. 5. Для профилактики переломов костей перед электросудорожной терапией.
Фармакокинетика. Низкая биодоступность (≈ 18 %) при приёме внутрь из-за интенсивной биотрансформации.
Побочное действие. Раздражительность, малосонница, ↑ АД, диспепсия, аллергия.
Взаимодействие. С общими анестетиками, миорелаксантами, клонидин ом. Результат – ↑ действия толперисон а.
Противопоказания. Миастения, беременность, кормление грудью, детям до 3 лет.
Лекарственные средства при спастичности, действующие на аксоны мотонейронов
Ботулотоксин А. См. «Холинергические антагонисты».
Лекарственные средства при спастичности, действующие на скелетную мускулатуру
Дантролен
Механизм действия. Блокирует высвобождение Са+2 из саркоплазматического ретикулума.
Действие. Ослабляет проявления спастичности. ↓ Сократимость мышц.
Применение. 1. Спастичность. 2. Злокачественная гипертермия. [Примечание. Возникает редко при применении галотан а и суксаметония. У таких больных имеется наследственное нарушение способности саркоплазматического ретикулума удерживать Са++. Внешние сигналы приводят к внезапному и длительному высвобождению Са++ в клетках скелетных мышц. Это сопровождается массивным сокращением мышц, образованием молочной кислоты и повышением температуры тела]. Лечение. Внутривенно дантролен, контроль ацидоза и температуры тела.
Побочное действие. Мышечная слабость, успокоение, гепатит.
Лекарственные средства, применяемые при судорогах, вызванных различными ядами. Диазепам + специфические антидоты.
РЕЗЮМЕ
Принципы терапии эпилепсии
1. Лечение годами.
2. Монотерапия. При неэффективности – комбинированная.
3. Непрерывный прием лекарственного средства. При резкой отмене возможен эпилептический статус.
4.Минимально возможная доза (сочетание эффективности и отсутствие побочного действия).
5. Мониторинг концентрации лекарственного средства в крови.
Общие комментарии к фармакотерапии паркинсонизма. Эффективность леводопы со временем ↓. Возникают побочные эффекты, осложняющие лечение. Чаще назначают «синемет». Для оптимального действия дополнительно назначают амантадин или тригексифенидил (или оба одновременно).
Дата: 2018-12-21, просмотров: 1007.