Рудные месторождения, особенно месторождения сульфидных руд, являются благоприятной экологической нишей для активной жизнедеятельности специфичных микроорганизмов, т.к. в них постоянно протекают геохимические процессы, в которых принимают участие элементы с различными химическими свойствами. Окислительные условия в рудных телах этих месторождений способствуют протеканию процессов окисления и выщелачивания сульфидных минералов, при которых металлы и сера переходят в водорастворимое состояние и выщелачиваются. Ранее окисление сульфидных минералов рассматривалось как чисто химический процесс, в котором основными агентами являются кислород воздуха и продукты окисления сульфидов - серная кислота и сульфаты металлов. Как известно, хорошим окислителем сульфидов является сульфат закиси железа, который взаимодействует с ними по реакции
MemSn + mFe2(SO4)3 = mMeSO4 + 2mFeSO4 + nS. (11)
Получаемый в результате этой реакции сульфат закиси железа в кислых растворах очень медленно окисляется до сульфата окиси железа. Однако в присутствии тионовых железоокисляющих бактерий Асidithiobacillus ferrooxidans скорость окисления железа увеличивается в 180 тысяч раз. В рудных месторождениях кроме этих микроорганизмов встречаются другие, которые обитают в широком диапазоне pH (от 0,5 до 10) и населяют практические все экологические ниши месторождений сульфидсодержащих руд.
Тионовые микроорганизмы, как было указано выше, являются хемолитоавтотрофными, т.е. источником электронов в энергетическом процессе с участием этих микроорганизмов являются неорганические вещества, а система автотрофной ассимиляции углекислоты в органические вещества является основным типом питания бактерий.
Наиболее легко окисляемым субстратом для железоокисляющих бактерий является закисное железо, которое в кислой среде окисляется с их учаcтием до оксидного:
4Fe2+ + 4H+ + O2 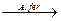 4Fe3+ + 2H2O + 11ккал.
4Fe3+ + 2H2O + 11ккал.  (12)
(12)
Кроме закисного железа A.ferrooxidans используют также в качестве энергетического источника такие восстановленные соединения серы как тиосульфты S2O32-, тритионаты S2O62-, тетратионаты и элементную серу, конечным продуктом окисления которых является сульфат-ион. Многочисленными исследованиями установлено, что бактерии A.ferrooxidans принимают участие в окислении практически всех сульфидных минералов.
Основными условиями существования и активной жизнедеятельности A.ferrooxidans является кислотность среды, ее температура, наличие воды и кислорода. Оптимальным значением pH среды для развития бактерий является 2,0-2,4 однако в природных рудничных водах эти микроорганизмы обнаруживаются даже при pH 1,2 и 7,6, но в этих условиях они неактивны. Среда с pH 9 является для них летальной. Эти бактерии являются чрезвычайно толерантными к кислой среде. Они могут выдерживать концентрацию серной кислоты в растворе до 18 г/л и гибнут лишь при концентрации ее 22 г/л, т.е. при pH 0,3, в то время как внутри клетки pH поддерживается на уровне 4,8 - 5,0.
Бактерии A.ferrooxidans относятся к мезофилам, для которых оптимальной температурой их роста и развития является 28 - 35 0С, при 40 0С прекращается их рост, а при 50 0С они гибнут ввиду денатурации белков.
Для нормального роста и развития бактерий требуется наличие в среде минеральных солей и прежде всего соединений азота и фосфора, которые используются бактериями в энергетическом метаболизме. Как уже отмечалось выше, бактерии A.ferrooxidans присутствуют повсеместно в рудничных кислых водах сульфидных месторождений, угольных шахт и залежей урановых руд, содержащих пирит. Различия между природными штаммами A.ferrooxidans, заключаются в основном в устойчивости к активной кислотности среды, тяжелым металлам, различным микроэлементам, а также в скорости окисления различных сульфидов и серы. Все эти различия носят адаптивный характер. Так микроорганизмы, выделенные из кислых вод Дегтярского рудника были впоследствии использованы после соответствующей адаптации при выщелачивании арсенопирита, сфалерита, халькопирита и других сульфидных минералов. Способность железоокисляющих бактерий адаптироваться к изменяющимся условиям среды обитания имеет большое значение для технологии БВ, т.к. микроорганизмы могут довольно легко адаптироваться, например, к повышенным содержанием в среде тяжелых металлов. Показана возможность адаптации бактерий к содержанию в среде до 55 г/л меди, до 30 - 40 г/л цинка, до 8 - 12 г/л мышьяка. Это уникальное свойство бактерий позволяет использовать их в промышленном масштабе, например, при чановом выщелачивании в плотных пульпах.
Для аэробных бактерий, какими являются микроорганизмы A.ferrooxidans, присутствие кислорода в среде является обязательным. Большая часть его поглощается клеткой с участием ферментных дыхательных систем. Другая часть участвует в чисто химическом процессе, при котором производит окисление химических веществ клетки, например, S - групп белков.
У бактерий A.ferrooxidans электроны от внешнего энергетического субстрата (Fe2+, сульфид) передаются по цепи переносчиков на молекулярный кислород с образованием воды:
4Fe2+ + O2 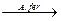 4Fe3+ + 2O22- (13)
4Fe3+ + 2O22- (13)
2O22- + 4H+ ® 2H2O.  (14)
(14)
Кроме переноса электронов в этом процессе используется освобождающаяся энергия путем ее трансформирования в химическую энергию фосфатных связей при синтезе АТФ из АДФ и неорганического фосфора.
Таким образом, уникальные свойства тионовых железоокисляющих бактерий принимать участие в окислении таких неорганических субстратов, как двухвалентное железо, элементная сера и сульфидные минералы, позволяют использовать их при извлечении металлов из сульфидсодержащих руд. Для интенсификации их роста и повышения активности необходимо создать оптимальные условия для их жизнедеятельности, которые определяются параметрами процесса и свойствами выщелачиваемого продукта.
Вопрос о взаимодействии бактерий с сульфидными минералами является основным в теории бактериального выщелачивания. Изучение этого взаимодействия имеет важное значение не только в познании сложного механизма этого процесса, но и для интенсификации бактериальных окислительных реакций и управления ими. Трудности изучения этого механизма объясняются тем, что помимо взаимодействия трех фаз (жидкой, твердой и газовой) в нем активное участие принимают бактериальные клетки - живые организмы, которые для роста и обеспечения своей жизнедеятельности используют компоненты всех трех фаз. Кроме того, в этом взаимодействии принимают участие различные продукты метаболизма бактерий - неорганические и органические, которые действуют на биохимическом уровне.
В настоящее время существуют несколько точек зрения на роль микроорганизмов A.ferrooxidans в окислении и выщелачивании сульфидных минералов. Ранее считалось, что окисление и выщелачивание сульфидных минералов при участии микроорганизмов происходит в результате действия продуктов окисления сульфата закиси железа бактериями и сер-ной кислоты, образующейся при бактериальном окислении сульфидной серы. Например, наиболее вероятными реакциями бактериального окисления пирита считаются реакции с образованием сульфата закиси железа
FeS2 + 7Fe2(SO4)3 + 8H2O ® 15FeSO4 + 8H2O (15)
и элементной серы
FeS2 + ® 3FeSO4 + 2S0, (16)
которые затем окисляются бактериями до сульфата окиси железа и серной кислоты:
4FeSO4 + O2 + 2H2SO4 . 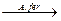 Fe2(SO4)3 (17)
Fe2(SO4)3 (17)
2S0 + 3O2 + 2H2O 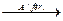
 2H2SO4.
2H2SO4.  (18)
(18)
Таким образом, в результате реакций окисления сульфата закиси железа и элементной серы образуются окислители сульфидных минералов - сульфат окиси железа и серная кислота. Кроме этих реакций при бактериальном окислении и выщелачивании сульфидных минералов на поверхность минералов действуют ферментные системы клеток. Это так называемый механизм прямого бактериального окисления сульфидов или “прямой” механизм.
Бактерии окисляют сульфидные минералы даже в тех случаях, когда их железоокисляющие системы подавлены. Минералы в этом случае окисляются путем прямого воздействия микроорганизмов на элементы кристаллической решетки минералов. Этот механизм окисления сульфидных минералов считается определяющим, в то время как биохимические реакции окисления закиси железа, сульфидной и элементной серы выполняют косвенную роль.
Однако долю участия этих механизмов в окислении сульфидных минералов определить довольно трудно. Следует учитывать то, что реакции преобразования неорганических субстратов с участием микроорганизмов имеют одну и ту же природу, осуществляются они непосредственно на поверхности минерала или в жидкой фазе пульпы.
Поэтому процесс бактериального окисления и выщелачивания минерального субстрата можно условно разделить на:
¨ взаимодействие клеток и их метаболитов с элементами кристаллической решетки непосредственно на минеральной поверхности,
¨ взаимодействия клеток с этими же элементами и продуктами метаболизма в жидкой фазе.
Первой стадией взаимодействия бактерий А.ferrooxodans с сульфидным субстратом является закрепление микроорганизмов на его поверхности, после чего начинается химическое превращение самого субстрата. Известно, что микроорганизмы способны закрепляться на любой поверхности. Адгезия их может происходить избирательно и неизбирательно, на положительно и отрицательно заряженных, на гидрофобных и гидрофильных поверхностях. Механизм их прикрепления является генетически запрограммированным и чрезвычайно сложным. Считается, что ответственными за этот механизм являются плазмиды. При адгезии клеток могут иметь место самые различные виды взаимодействия, начиная от прикрепления за счет обычной липкости их слизистой капсулы и кончая взаимодействием электростатических сил.
Однако наличие бактерий на поверхности сульфидных минералов, фиксируемое визуально, не является еще доказательством их участия в бактериальном окислении этой поверхности, ведь они закрепляются и на поверхностях, которые не используются ими в качестве субстрата. Адгезия на поверхности сульфидов носит специфический характер и имеет глубокий биологический смысл, т.к. в этом случае минерал является субстратом - источником энергии для роста и жизнедеятельности бактерий. Следует также учесть, что при микробиологическом выщелачивании бактерии не только закрепляются на поверхности минерального субстрата, но и имеются в жидкой фазе пульпы, где они окисляют закисное железо и элементную серу. Определение окислительной активности биомассы, находящейся на твердой фазе и в жидкой фазе дает преставление о роли микроорганизмов, которую они выполняют в этих фазах.
При бактериальном выщелачивании золотомышьяковых концентратов микроорганизмы, находящиеся в жидкой фазе пульпы, т.е. “свободно плавающие”, потребляют не более 1% от общего количества поглощаемого пульпой кислорода.
Это объясняется тем, что концентрация закисного железа, являющегося субстратом для бактерий, которых в жидкой фазе пульпы содержится 108 - 109 кл/мм, составляет лишь 5% от общего количества железа, в то время как содержание окисного железа доходит до 10 - 15 г/л. Поэтому потребление кислорода жидкой фазой пульпы связано с бактериальным окислением закисного железа, перешедшего в раствор в результате химического взаимодействия сульфата окиси железа с поверхностью сульфидных минералов. Эти бактерии являются потенциально активными и способны принимать участие в окислении при наличии окисляемого субстрата.
Почти весь потребляемый при БВ концентратов кислород (95%) расходится при непосредственном окислении сульфидных минералов, закрепившимися на них клетками.
На поверхности минералов бактерии закрепляются очень прочно. Так при бактериальном выщелачивании золотомышьякового концентрата даже после трех отмывок потребление кислорода снизилось всего в 1,16 раза.
На твердой фазе пульпы при БВ золотомышьякового концентрата закрепляется обычно около 70 - 80% клеток и только 20 -30% свободно “плавают” в жидкой фазе. Около 15 - 16% от общей поверхности выщелачиваемого концентрата занято сорбированными бактериальными клетками, причем наиболее активно они сорбируются на арсенопирите, к выщелачиванию которого они были адаптированы. В процессе непрерывного выщелачивания равновесная концентрация бактерий на твердой фазе достигается за 20 минут. Использование адаптированной культуры увеличивает количество сорбированных клеток с 8 до 95% от их общего количества.
До изучения механизма бактериального окисления и выщелачивания сульфидных минералов используются основные термодинамические закономерности, характерные для окисления этих минеральных субстратов. Диаграммы Пурбэ (j-pH), используемые для этой цели позволяют определить термодинамически стабильные состояния системы в зависимости от величины pH среды, потенциала минерала и среды.
Анализ термодинамического состояния пирита, арсенопирита и пирротина в условиях бактериального выщелачивания, а также электрохимические изменения подтвердили, что микроорганизмы при БВ непосредственно окисляют элементы кристаллической решетки сульфидных минералов благодаря биокаталитическим свойствам их ферментов. В области активного бактериального окисления и выщелачивания сульфидных минералов они термодинамически неустойчивы и обладают достаточным запасом свободной энергии, необходимой для обеспечения жизнедеятельности микроорганизмов А.ferrooxidàns, которые принимают участие в реакциях с выходом свободной энергии не менее 12 ккал.
При БВ арсенопирита окисное железо непрерывно накапливается как в растворе, так и в осадке. Увеличение его концентрации объясняется бактериальным окислением закисного железа, образующегося при окислении арсенопирита:
2Fe2SO4 + H2O + 0,5O2®Fe2(SO4)3 + H2O. (19)
Кислотность среды при БВ арсенопирита ниже, чем pH осаждения железа из сернокислых растворов в виде гидроксида (pH 2,3), поэтому при достижении определенной концентрации сернокислое окисное железо гидролизуется с образованием гидроксида, выпадающего в осадок с одновременным подкислением среды:
Fe2(SO4)3 + 6H2O® 2Fe2(OH)3 + 3H2SO4. (20)
Окисное железо, кроме того, может образовывать с мышьяком арсенаты железа, которые также выпадают в осадок, однако это происходит при более низких значениях pH среды, нежели осаждение железа.
В образовавшемся осадке железо находится преимущественно в трехвалентной форме. Например, при БВ чистого арсенопирита количество его в осадке составляет более 50% от общего содержания железа в растворе и осадке. Количество закисного железа в растворе зависит от плотности биомассы и ее активности. Так при БВ концентрата Бакырчикского месторождения при плотности биомассы 2,5 г/л и ее активности 3 - 4 г/л×ч количество двухвалентного железа не превышает 2 - 10% от общего содержания железа.
Мышьяк при БВ арсенопирита переходит в раствор и осадок как в трех, так и пятивалентной форме. В растворе он находится преимущественно в виде о-мышьяковой и о-мышьяковистой кислот. Количество мышьяка в осадке зависит от pH раствора, концентрации и валентности находящихся в растворе мышьяка и железа. Если в растворе соотношение As3+ к As5+ составляет 5:1, то в осадке это соотношение равно 2,5 : 1, при соотношении суммарного железа и суммарного мышьяка в осадке 1,1 : 1, в растворе 0,9 : 1.
При выщелачивании золотомышьяковых концентратов биомассой, которая имеет активность до 6 г/л.ч в растворе мышьяк находится преимущественно в пятивалентной форме. В среднем более 75% мышьяка в растворе представлено соединениями пятивалентного мышьяка.
Более четкая зависимость наблюдается между количеством мышьяка в осадке и величиной pH, причем эта зависимость изменяется со временем выщелачивания. В первые часы выщелачивания количество мышьяка в осадке уменьшается с увеличением кислотности и при pH менее 1,6 почти весь мышьяк находится в растворенном состоянии. Однако в дальнейшем, когда в пульпе накапливается большое количество органических веществ и мышьяка, содержание которого доходит до 15 г/л, количество его в осадке повышается с увеличением кислотности среды и может достигать 80% от общего количества выщелоченного мышьяка.
При изучении поведения сульфидной серы в условиях БВ арсенопирита и золотомышьякового концентрата установлено, что в пульпе происходит накопления элементной серы, количество которой к концу процесса может достигать 60% от общей выщелоченной серы (при БВ арсенопирита) и 30 - 40 % при БВ золотомышьякового концентрата.
Накапливаются также промежуточные соединения серы (до 20%), но содержание их уменьшается к концу процесса за счет окисления их до сульфат-ионов .
Большое различие наблюдается в составе продуктов, образующихся на арсенопирите при химическом и бактериальном окислении. Химическое окисление приводит к образованию на поверхности арсенопирита гетита HFeO или гидрогетита HFeO2 . nH2O, которые образовались из гидроксида трехвалентного железа при сушке образцов и количество которого составляет 30 - 40% от общего количества поверхностных соединений, среди которых присутствует элементная сера (10%). Таким образом в процессе химического окисления на поверхности арсенопирита образуется сернокислое окисное железо, часть которого переходит в раствор, и элементная сера. Процесс химического окисления при этом практически заканчивается.
При бактериальном окислении арсенопирита на его поверхности основным продуктом является элементная сера, количество которой составляет уже 50%, т.е. в 5 раз больше, чем при химическом окислении. Эта элементная сера непрерывно окисляется бактериями до SO42-, также как закисное железо до оксидного.
Таким образом, при взаимодействии микроорганизмов с поверхностью сульфидных минералов образуется единственный твердый продукт окисления сульфидов - элементная сера и закисное железо, которые затем окисляются бактериями на поверхности минерала и в объеме раствора.
Отмечается также, что элементная сера, образующаяся при бактериальном окислении арсенопирита, имеет кристаллическую структуру, отличную от структуры стандартной серы орторомбической. Эта сера была названа b - серой, аналогично b - модификации селена. Элементная b - сера обнаружена в горячих серных источниках Португалии, в которых присутствуют тионовые термофильные бактерии.
Процесс бактериального окисления и выщелачивания, таким образом, можно разделить на два цикла, которые самым тесным образом связаны между собой протекающими реакциями. Первый цикл - это непосредственное окисление элементов кристаллической решетки минералов, которое происходит при участии как химических агентов - кислорода и окисного железа, так и ферментативных систем бактерий. При этом окислении происходит деструкция минерала, т.е. его выщелачивание. Второй цикл - непосредственное бактериальное окисление продуктов выщелачивания сульфидных минералов - закисного железа и элементной серы.
Дата: 2019-07-30, просмотров: 405.