Чтобы сжать некоторый газ поршнем, к нему необходимо приложить силу. Так как поршень перемещается на некоторое расстояние, то над ним совершается работа. При перемещении поршня на некоторую величину происходит изменение объема газа. Следовательно, работа идет на изменение объема газа.
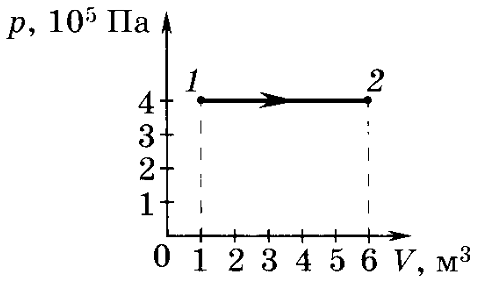
Рассмотрим изобарный процесс. Во время нагревания газа при постоянном давлении газ начинает расширяться, то есть совершает работу по передвижению свободного поршня. В случае его охлаждения, газ сжимается, в это время так же совершается работа: 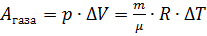 . Если данный процесс изобразить на графике, то получится прямая. Значение совершенной работы можно определить, вычислив площадь под прямой p(t) на графике.
. Если данный процесс изобразить на графике, то получится прямая. Значение совершенной работы можно определить, вычислив площадь под прямой p(t) на графике.
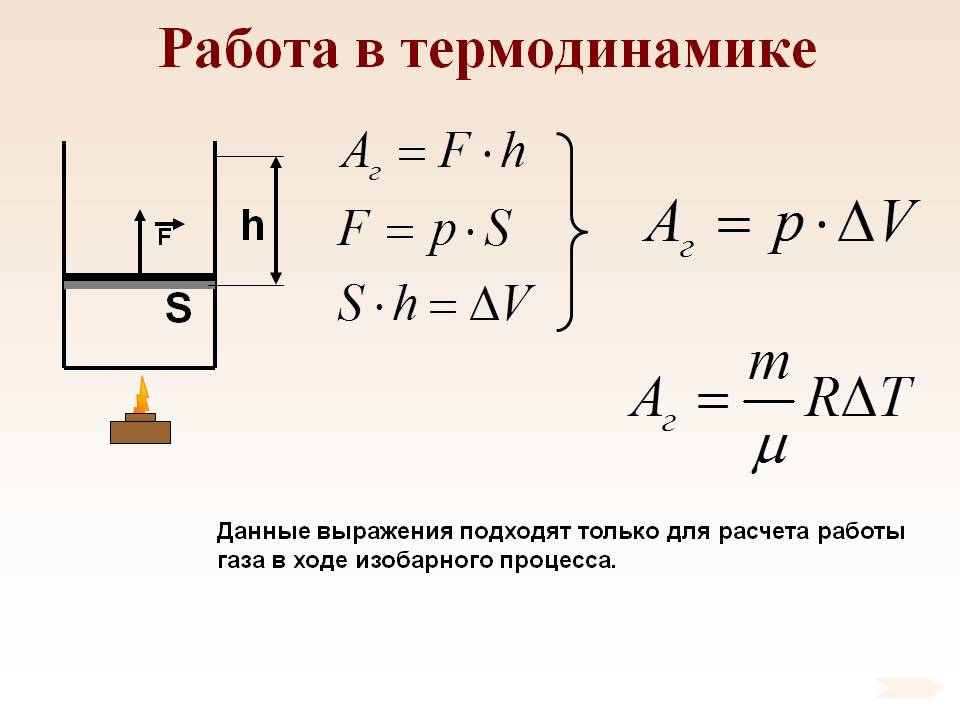
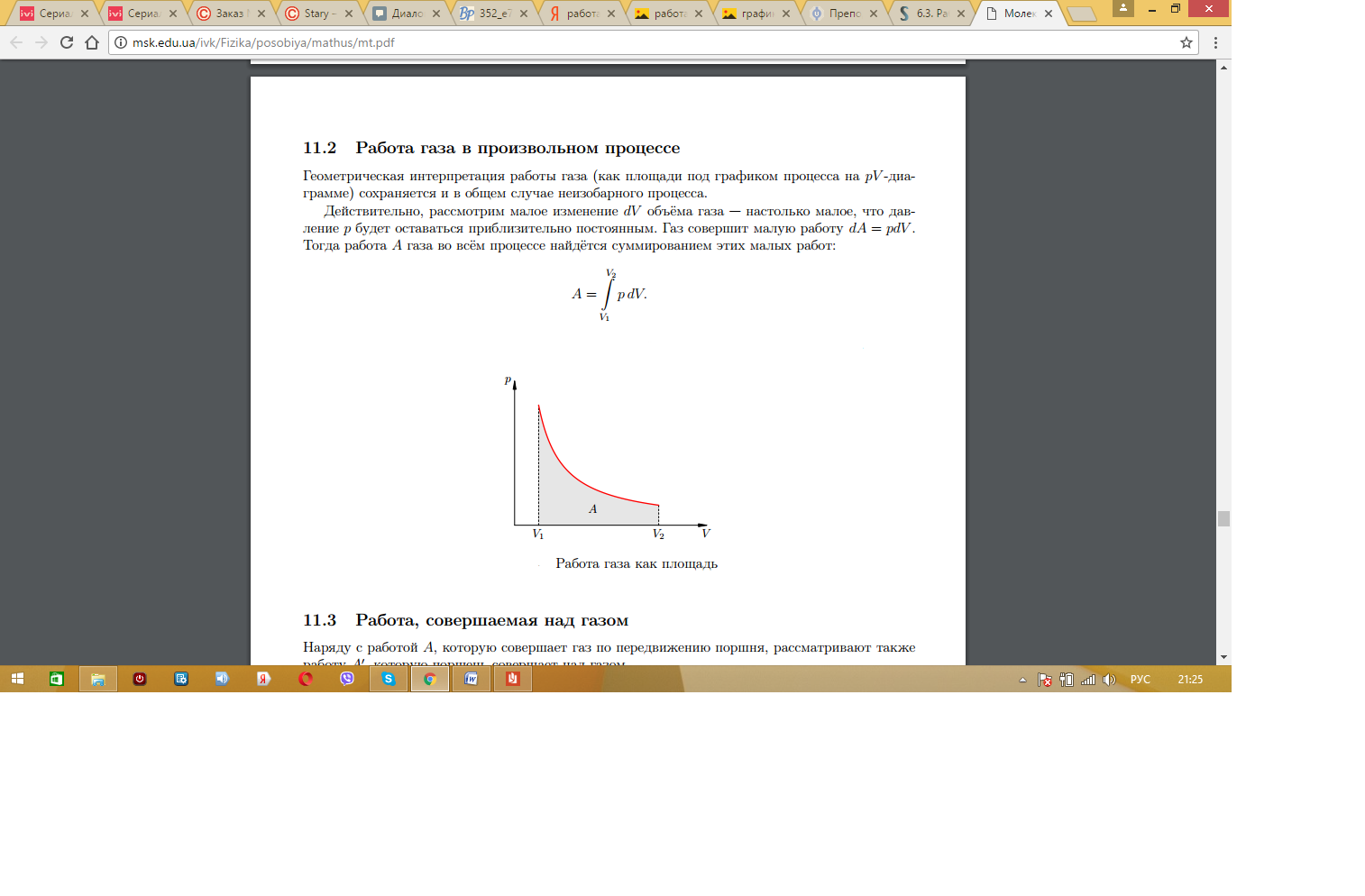
Если же в произвольном процессе во время совершения работы над газом происходит изменения и давления, и объема, то для её определения используют определенный интеграл: 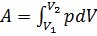 .
.
Согласно третьему закону Ньютона, тела действуют друг на друга силами, с равными по модулю и противоположными по значению. Значит, работа самого газа имеет такой же модуль, как и работа совершается над газом, но противоположное направление.
Законы термодинамики.
При рассмотрении предыдущих вопросов мы отметили, что для изменения внутренней энергии газа его можно нагреть или же совершить над ним работу. Эти два процесса могут происходить отдельно или же одновременно. Но, несмотря на это, они оба приводят к изменению энергии структурных единиц. В таком случае, можно сделать вывод, что изменение внутренней энергии газа равно сумме количеству переданной теплоты и совершенной над ним работой.
Первый закон термодинамики гласит: изменение внутренней энергии системы при переходе термодинамической системы из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе. 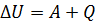 .
.
Замечание. Если же работу совершает сама термодинамическая система, а не внешние силы, то 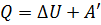 .
.
Вывод: количество теплоты, переданной термодинамической системе идет на изменение ее внутренней энергии и совершении работы.
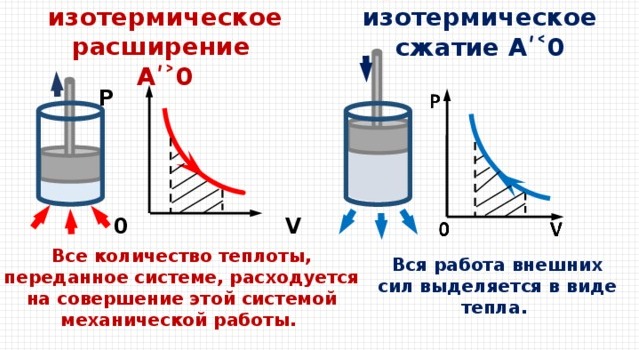
При изотермическом процессе температура остается неизменна, то все количество энергии, которое может быть передано газу, идет только на совершение работы над внешними телами, без изменения внутренней энергии, которая повлекла бы за собой изменение температуры: 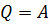 .
.
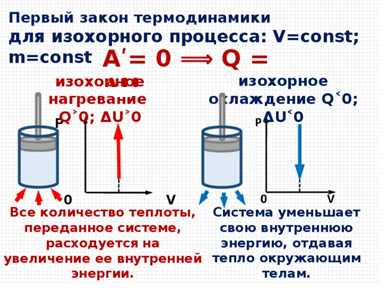
При изохорном процессе не происходит изменение объема. Значит, работа над газом не совершается, все полученное тепло идет на его нагревание. Изменяется внутренняя энергия : 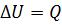 .
.
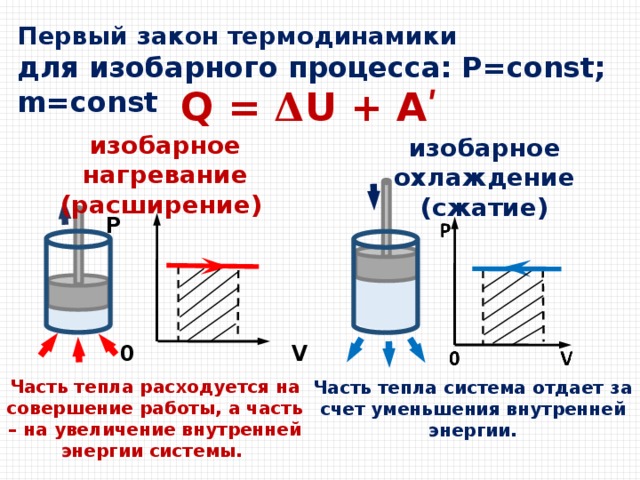
Во время изобарного нагревания для сохранения постоянного давления газ должен находиться под свободным поршнем, который способен перемещаться при нагревании. В результате этого происходит изменение его объема. А это значит, что внутренняя энергия газа изменяется во время совершения работы и при теплообмене.
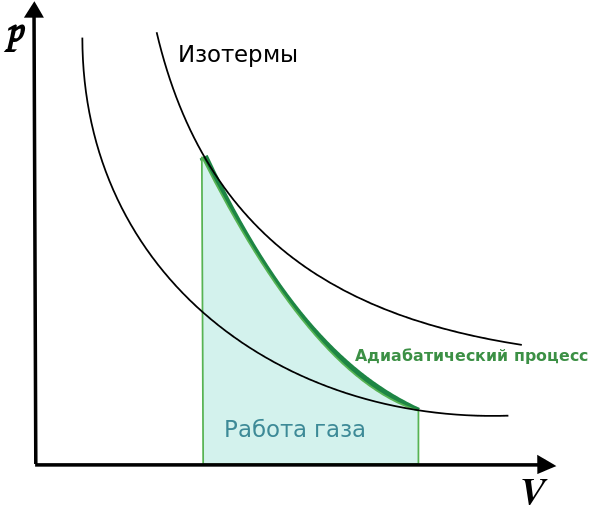
Когда газ изолирован от внешней среды, когда не происходит теплообмена с окружающей средой, все изменения с газом происходят настолько быстро, что он не успевает отдать или взять тепло. Такой процесс называют адиабатный процесс. Первый закон термодинамики имеет следующий вид: 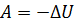 . Газ совершает работу за счет убыли его внутренней энергии. График адиабатного процесса можно получить с помощью двух изотерм:
. Газ совершает работу за счет убыли его внутренней энергии. График адиабатного процесса можно получить с помощью двух изотерм:
Сосуд, который не позволяет производить теплообмен, называется сосудом Дьюара, иначе говоря - термос.
Второй закон термодинамики говорит о том, что во время теплопередачи все тепло всегда передается от более нагретого тела к менее нагретому, а механическая энергия способствует изменению внутренней энергии.
Постулат Клаузиуса говорит о том, что холодное тело не может передавать холод более нагретому телу без дополнительных источников работы. То есть в холодильных машинах всегда есть дополнительное тело, которое способствует движению холодильного вещества без изменения его температуры за счет горячего тела. Именно поэтому фреон в бытовых холодильниках не нагревается из-за того, что в холодильник кладут пищу.
Дата: 2019-07-31, просмотров: 340.