Температуру мы в быту определяем только с точки зрения "холодно-тепло". Более того, тактильные ощущения могут отличаться в зависимости от типа материала.
Температуру в термодинамике можно трактовать с точки зрения теплового равновесия. Измерять её необходимо не по средствам собственных ощущений, а с помощью средств измерительной технике. Тепловое равновесие - это состояние системы, при котором отсутствует передача тепла. Например, если положить в холодную воду раскаленную металлическую деталь в конечном итоге охлаждение металлической детали и нагревание воды прекратятся, и оба тела станут одинаковой температуры. Для достижения теплового равновесия горячее тело передает тепло холодному до тех пор, пока они оба не станут одинаковой температуры.
Для измерения температуры используют термометры. Рабочим веществом в термометре может быть жидкость или газ, а также термопара. Принцип работы термометра основан на зависимости расширения рабочего вещества в зависимости от его нагревания; жидкость передвигается по проградуированной шкале и указывает температуру рассматриваемой системы.
Во время соприкосновения холодного и горячего тела система стремится к тепловому равновесию; горячее тело будет отдавать тепло, а холодное его получать: 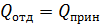 . Если в контакт приводится несколько тел, то все процессы обмена тепла подкрепляются уравнением теплового баланса:
. Если в контакт приводится несколько тел, то все процессы обмена тепла подкрепляются уравнением теплового баланса: 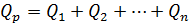
Внутренняя энергия.
Все структурные единицы вещества находятся в постоянном движении. Так как они имеют определенную скорость, это значит, что каждая молекула обладает кинетической энергией. Более того, они постоянно взаимодействуют друг с другом, или же находятся на некотором расстоянии друг от друга, поэтому каждая структурная единица вещества имеет и потенциальную энергию. Сумма этих двух энергий порождают новую энергию - внутреннюю. Внутренняя энергия вещества - это сумма кинетической и потенциальной энергии его структурных единиц. Обобщив, скажем, что внутренняя энергия состоит из: кинетической энергии движения, потенциальной энергии частиц, энергии движения электронов по своим оболочкам, энергии, которую имеют структурные единицы ядра.
Напомним, что идеальный газ - это модель, в которой структурные единицы не взаимодействуют друг с другом. Поэтому можно сделать вывод, что внутренняя энергия идеального газа не имеет потенциальную составляющую, а состоит только из кинетической энергии молекул. Если умножить количество атомов идеального газа на кинетическую энергию каждого из них, то можно получить формулу для внутренней энергии одного моля одноатомного идеального газа:
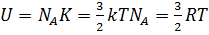 . Итак, внутренняя энергия зависит только от температуры. Внутренняя энергия является функцией состояния системы и не зависит от предыстории.
. Итак, внутренняя энергия зависит только от температуры. Внутренняя энергия является функцией состояния системы и не зависит от предыстории. 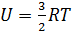 .
.
Чтобы получить внутреннюю энергию иного количества вещества, формулу следует умножить на количество моль. Так же эта формула изменится в случае, если газ не одноатомный: 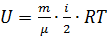 , где i – количество степеней свободы.
, где i – количество степеней свободы.
Дата: 2019-07-31, просмотров: 354.