Суммарное количество кислорода, (кг/ч): 35,03+9,939+11,563+3,55+2,662+ 1,765+0,865 +0,543+0,407+0,182+0,159+0,049+0,037+0,023+0,013+0,009+0,005+0,003+ 0,008+ 0,014+0,002+0,008=75,043
Теоретический расход воздуха (из расчета. Оа - 23% по массе)
75,043*0,23=326,274 кг/ч
Количество азота: 326,274 - 75,043= 251,231 кг/ч
Количество влаги, вносимое с воздухом при Т=20°С и относительной влажности 80%
(содержание влаги "0,012 кг. на 1кг. сухого воздуха):
326,274* 0,012 = 3,915 кг/ч
Теоретический расход влажного воздуха (кг/ч)
326,274 + 3,915 = 330,189 кг/ч.
Таблица 8. Состав огарка.
| Со203 |
| 11,105 |
| 6,793 |
| WC | ТЮ | Со | Zn | Си | Fe | WO3 | ТЮ2 | СоО | ZnO | Си2О | Fe203 | H20 | Бент. всего | ||
| кг/ч | 1,746 | 0,336 | 0 | 0 | 0 | 0 | 124,760 | 12,975 | 0,165 | 0,997 | 0,251 | 0,181 | 0 | 10,686 163,469 | |
| % | 1,068 | 0, 206 | 0 | 0 | 0 | 0 | 76,320 | 7,937 | 0,101 | 0,610 | 0,154 | 0,111 | 0 | 6,537 100,000 | |
| СиО FeO | |||||||||||||||
| 0,232 0,035 | |||||||||||||||
| 0,142 0,021 | |||||||||||||||
Таблица 9. Состав циклонной пыли.
| WC | TiC | Со | Zn | Си | Fe | WO3 | ТЮ2 | СоО | ZnO | Си2О | Fe2O3 | Н2О | Бент. | всего | |
| кг/ч | 2,686 | 0,516 | 0 | 0 | 0 | 0 | 35,766 | 7,757 | 2,925 | 0,289 | 0,133 | 0,084 | 0 | 3,288 | 53,444 |
| % | 5,026 | 0,965 | 0 | 0 | 0 | 0 | 66,922 | 14,514 | 5,473 | 0,541 | 0,249 | 0,157 | 0 | 6,152 | 100,000 |
Таблица 10. Состав пыли рукавного фильтра.
| Со2ОЗ |
| 2,583 |
| 6,587 |
| WC | TiC | Со | Zn | Си | Fe | WO3 | ТЮ2 | СоО | ZnO | Си2О | Fe2O3 | H2O | Бент. | всего | |||
| кг/ч | 0, 201 | 0,039 | 0 | 0 | 0 | 0 | 29,030 | 4,485 | 0,019 | 0,230 | 0,057 | 0,040 | 0 | 2,466 | 39,211 | ||
| % | 0,513 | 0,099 | 0 | 0 | 0 | 0 | 74,035 | 11,438 | 0,048 | 0,587 | 0,145 | 0,102 | 0 | 6,289 | 100,000 | ||
|
|
| ||||||||||||||||
| СиО | FeO | ||||||||||||||||
| 0,053 | 0,008 | ||||||||||||||||
| 0,135 | 0,020 | ||||||||||||||||
Таблица 11. Состав газов.
| N2 кг/ч 251,231 | Н2О 42,275 | СО2 41,414 | всего 334,920 |
| % 75,012 | 12,622 | 12,365 | 100,000 |
Таблица 12. Материальный баланс обжига.
| Г | Приход | Об | разуется | ||
| Вещество | кг/ч | % | Вещество | кг/ч | % |
| WC | 134,636 | 22,366 | WC | 4,633 | 0,786 |
| TiC | 25,531 | 4,241 | TiC | 0,891 | 0,151 |
| Со | 10,000 | 1,661 | |||
| Zn | 1,000 | 0,166 | WO3 | 189,556 | 32,172 |
| Си | 0,500 | 0,083 | ТЮ2 | 25,217 | 4,280 |
| Fe | 0,167 | 0,028 | СоО | 3,109 | 0,528 |
| Со203 | 13,688 | 2,323 | |||
| W03 | 35,766 | 5,941 | ZnO | 1,516 | 0,257 |
| ТЮ2 | 7,757 | 1,289 | Си20 | 0,441 | 0,075 |
| СоО | 2,975 | 0,494 | СиО | 0,285 | 0,048 |
| ZnO | 0,289 | 0,048 | Fe203 | 0,305 | 0,052 |
| Си2О | 0,133 | 0,022 | FeO | 0,043 | 0,007 |
| Fe203 | 0,084 | 0,014 | |||
| бент | 16,440 | 2,790 | |||
| бент | 16,440 | 2,731 | |||
| H20 | 40,424 | 6,715 | H20 | 40,424 | 6,861 |
| N2 | 251,231 | 42,640 | |||
| 02 | 75,043 | 12,466 | C02 | 41,414 | 7,029 |
| N2 | 251,231 | 41,734 | |||
| Всего | 601,976 | 100 | Всего | 589, 193 | 100 |
| Нее пр | язка от ихода | 12,783 | 2,124 |
тшо: 3,036*МШо/201,38=0,270
тшо: 0,594*МШо/165,54=0,065
тшо: 0,178*МШо/165,54=0,019 Остаток воды: 547,236-21,251=525,985 кг.
Количество NH3 пошедшее на реакции, (кг/ч):
тотв: 201,227*2*MNH3 (17) 7303,3=22,557
тшз: 0,520* 6*МШЗ /211,93=0,250
тшз: 34,980*12* Мню /211,93=33,670
ткш: 3,036* 6*МШЗ /201,38=1,537
тшз: 0,594*4* Мынз /165,54=0,240
6) тщз: ОД78* 4*МШЗ /165,54=0,078 Остаток NH3: 60,804-58,324=2,480 кг.
Таблица 13. Материальный баланс выщелачивания.
| Приход | Образуется | ||||||
| Вещество WC | кг/ч 1,947 | % 0,236 | Вещество (NH4) 2WO4 | кг/ч 201,227 | % 25,084 | ||
| TiC | 0,375 | 0,046 | [Co(NH3) 6] (OH) 3 | 35,500 | 4,425 | ||
| WO3 | 153,790 | 18,662 | [Zn (NH3) 6] (OH) 2 [Cu (NH3) 6j (OH) 2 | 3,036 0,774 | 0,378 0,096 | ||
| ТЮ2 | 17,460 | 2,119 | |||||
| СоО | 0,184 | 0,022 | WC | 1,947 | 0,243 | ||
| Со203 | 13,688 | 1,661 | TiC | 0,375 | 0,047 | ||
| ZnO | 1,227 | 0,149 | |||||
| Cu20 | 13,688 | 1,661 | ТЮ2 | 17,460 | 2,177 | ||
| CuO | 0,285 | 0,035 | Fe203 | 0,221 | 0,028 | ||
| Fe2O3 | 0,221 | 0,027 | FeO | 0,043 | 0,005 | ||
| FeO | 0,043 | 0,005 | |||||
|
| бент | 13,152 | 1,639 | ||||
| бент | 13,152 | 1,596 | |||||
|
| |||||||
| NH3 | 60,804 | 7,378 | NH3 | 2,480 | 0,309 | ||
| H20 | 547,236 | 66,404 | H20 | 525,985 | 65,568 | ||
| Всего | 824,100 | 100 | Всего | 802,2 | 100 | ||
|
| Невязка от прихода | 21,900 | 2,657 | ||||
Сущность метода рассмотрим на примере условной схемы переработки молибденитового концентрата, включающей возгонку триоксида молибдена и гидрометаллургическую переработку остатка от возгонки (рис.7). •
Примем, что пооперационные балансы молибдена характеризуются следующими цифрами:
1) грануляция и обжиг в кипящем слое: в пыль и в огарок переходит соответственно 0,2 и 0,8 количества молибдена, поступающего на операцию;
2) возгонка: в остатке от возгонки 0,3, в возгонах 0,7 количества молибдена;
3) выщелачивание: в растворе 0,98, в отвалах выщелачивания 0,02;
4) очистка от тяжелых металлов: в сульфидном кеке 0,05, в очищенном растворе 0,95;,.
5) нейтрализация: в кислом маточном растворе 0,01, в кристаллах тетрамолибдата аммония 0,99;
6) перекристаллизация: в маточном растворе 0,1, в кристаллах парамолибдата аммония (конечный продукт) 0,9. /
Зададимся производительностью по молибдену в конечном продукте 1000 т/год.
Обозначим потоки молибдена (т.е. количества его в различных материалах), т/год, неизвестными x-i; Хг, - ', Х^2, *13 в соответствии с рис.7.
Для определения неизвестных составим систему, состоящую их уравнений трех типов.
1. Уравнение, в котором задана производительность:
х-i з=1000. " ".
2. Уравнения, в которых использованы соотношения между потоками. Это могут быть непосредственно содержащиеся в исходных данных сведения о доле ценного компонента от количества, поступающего на операцию, переходящей в каждый из продуктов этой операции, например:,
Х2 = 0,2 (xl + Х2), Х3 = 0,8 (Xi + X2), Х4 = 0,3 Х3,
Х5 = 0,7, Х3,
или вытекающие из этих сведений соотношения между потоками, выходящими с одной и той же операции, например:
Х3 = 4Х2,... .
Х5= 7/3 Х4.
Кроме того, возможно использование соотношения между потоками, относящимися к разным операциям схемы. Дело в том, что в реальных технологических схемах количества ценного компонента в тех или иных материалах (особенно в выводимых из схемы) часто задают как долю от количества ценного компонента в исходном материале или конечном продукте. Так, например, исходные данные. могли бы содержать,:; следующее указание: "Потери молибдена с, остатком выщелачивания составляют в среднем 0,6% от количества, поступающего с молибденитовым концентратом"; соответствующее, уравнение имело бы вид
Х7= 0,006 Xi.
Следует отметить, что в тех случаях, когда вместо данных, относящихся к потокам одной и той же операции, заданы соотношения между потоками разных операций, расчет методом "от операции к операции" невозможен.
3. Уравнения, отражающие равенство количества - ценного компонента, поступающего на операцию, количеству, выходящему с нее:;
Ха + Хз = Xi + *2 • или Хз = xl;
х4 + х5 = х3, Х6 + Х7 = Х4,
Х8 + Х9 = Хб + Х12 И Т.Д.
Легко убедиться, что общее число уравнений всех типов, которые можно составить, во много раз превышает число неизвестных, хотя система должна иметь единственное решение и соответственно число уравнений должно быть равно числу неизвестных. Причина, очевидно, состоит в том, что большая часть уравнений представляет собой линейные комбинации других; например, из
Х2 = 0,2 (Хт + Х2),
Х3 = 0,8 (Xi + Х2) следует
Ха + Хз = Xi + х2, или Хз = Xi;
Хз: Х2 = 0,8: 0,2, или Х3 = 4Х2.
В то же время решение возможно только при условии, что при числе уравнений, равном числу неизвестных, все уравнения линейно независимы. Поэтому после составления системы уравнений необходим тщательный контроль отсутствия в ней линейно зависимых (дублирующих) уравнений.
По-видимому, дублирования уравнений проще всего избежать, используя в системе, кроме уравнения, задающего производительность, только соотношения между количеством ценного компонента в потоке, выходящем с операции, и количеством, поступающим на эту операцию. Для схемы, показанной на рис.7, можно составить, например, следующую систему уравнений для определения потоков ценного компонента при производительности по конечному продукту, равной 1000:
1. Х2 = 0,2 (х-i + Х2), или Х2 = 0,25 Xi;
2. х3 = 0,8(х1 +х2);
3. х4 = о. з Хз;
4. Х5 = 0,7 Хз;
5. Хб = 0,98 Х4;
б ху = 0,02 х4;
7. х8 = 0,05 (х6 + х12);
8. Х9 = 0,95(Х6 + Х12);
э. хю = 0,01 х9;
10. Хц =0,99 Xg;
11. х12 = о,1 (хб + хц);
12. Х13 = 0,9(Х5 + Хц);
13. Х13 = 1000.
Подобную систему уравнений можно довольно легко решить вручную, путем последовательной подстановки, сокращения переменных при вычитании одних уравнений из других и т.д. Однако если число неизвестных очень велико (а в реальных схемах число потоков может достигать многих десятков и даже сотен), возрастает трудоемкость расчетов и вероятность ошибок. В подобных случаях для сокращения числа уравнений можно рекомендовать обозначать неизвестными не количества ценного компонента в каждом из потоков, а суммарные количества, поступающие на операции схемы; при этом, очевидно, число уравнений на 1 больше числа операций. Например, для той же схемы (рис.7) получаем:
1. У1 = G ucx + 0,2 /!, или 0,8 у! = G исх;
2. у2 = 0,8 yi;
3. уз = о, з у2;
4. у4 = 0,98 Уз + 0,1 Уб',
5. у5 = 0,95 у4;
6. у6 = 0,7 у2 + 0,99 у5;
7. G исх = 0,9 у6.
После решения подобной системы уравнений расчет количества ценного компонента в каждом из потоков не вызывает затруднений.
Однако наиболее эффективным способом преодоления трудностей расчета сложных технологических схем является использование компьютеров.
В отличие от человека, выбирающего для каждой конкретной системы уравнений наиболее рациональный путь решения, в программах для цифровых вычислительных машин можно использовать только универсальные, единые для всех систем линейных уравнений способы вычисления. Среди таких способов наиболее распространены метод Гаусса с выбором главного элемента столбца или строки и метод обращения матрицы [2].
До начала вычислений необходимо ввести исходные данные: при использовании метода Гаусса - расширенную матрицу коэффициентов системы линейных уравнений (значения коэффициентов при неизвестных и свободные члены каждого из уравнений):

а при использовании метода обращения матрицы - отдельно квадратную матрицу коэффициентов и вектор-столбец свободных членов:
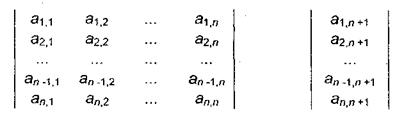
Для составления матрицы коэффициентов члены уравнений, содержащие неизвестные, необходимо расположить слева от знака равенства в порядке возрастания индекса неизвестного, оставив справа только свободные члены; отсутствующие неизвестные вносят в уравнения с коэффициентами, равными нулю. После этого можно приступить к вводу матрицы коэффициентов.
Однако применительно к системе уравнений, получаемой при описании распределения ценного компонента по потокам технологической схемы, этот способ нерационален, так как подавляющая часть коэффициентов равна нулю. Например, при вводе коэффициентов составленной ранее системы из 13 уравнений первые две строки должны быть записаны в следующем виде: - 0,25 Xi + 1 Х2 + О Х3 + О Х4 + О Х5 + О Х6 + О Х7 + О Х8 + О Х9 +
+ о х10 + о хп + ох12+ о х13 = о;
- 0,8 х1 - 0,8 х2 + 1 хЗ + 0 х4 + 0 х5 + 0 хб + 0 х7 + 0 х8 + О Х9 +
+ о Хю+ о х-и +о X-I2 + о х13 = о,
а первые две строки расширенной матрицы коэффициентов
соответственно
-0,25 1 000000000000 - 0,8 - 0,8 000000000000
При большом числе неизвестных количество вводимых нулей становится громадным: например, при 40 неизвестных расширенная матрица состоит из 40 х 41 = 1640 коэффициентов, из которых более 1500 будут равны нулю. Очевидно, что ввод подобной матрицы настолько трудоемок и неизбежно сопровождается таким количеством ошибок, что превращается в сложную задачу.
Это затруднение устраняется, если ввод матрицы осуществлять в два этапа: сначала заполнить всю матрицу нулями (эта операция выполняется очень легко), а затем ввести ненулевые коэффициенты, заменяя ими нули.
Ниже описан расчет балансов по ценному компоненту методом Гаусса с помощью программы на языке BASIC и методом обращения матрицы с помощью табличного процессора EXCEL [3, 4].
mCu(H20) 4ci2: (0,594+0,178) Mcu(mo) 4 012 206,44/165,54 = 0,963
mcocn: 7,756 M 7,756 Mc0ci2129,83/165,25= 6,093
Количество МНЦ С1, (кг/ч):
(165,765*2*53,5/249,85) +(7,756*6*53,5/165,28) +(3,683*6*53,5/244,28) +(0,963* 4*53,5/
206,44) =91,891
Количество поглощаемой реакциями H2O, (кг/ч):
(3,683*4*18/244,28) +(0,963*2*18/206,44) +(6,093*0,5*18/129,83) =1,676
Количество образующейся Н2О, (кг/ч):
7,756*3*18/165,765=2,527
Количество Н2О, приходящее с кислотой, (кг/ч):
Состав кислоты 19,8% НС1 80,2% Н2О
Количество требуемого НС1, (кг/ч):
(165,765*2*36,45/249,85) + (7,756 * 9 * 36,45 / 165,28) + (3,683 * 8 * 36,45 / 244,28) +(0,963*6*36,45/206,
44) =69,177
Приходящей с кислотой Н2О, (кг/ч):
69,177*0,802/0, 198= 280, 202
Суммарное количество приходящей Н2О, (кг/ч):
280, 202+525,985=806,187
Суммарное количество уходящей Н2О, (кг/ч):
806,187+2,527-1,676=807,03 8
Таблица 14. Материальный баланс осаждения.
| Приход | Образуется | ||||||
|
| |||||||
| Вещество | кг/ч | % | Вещество | кг/ч | % | ||
| (NH4) 2 WO4 | 201,227 | 18,033 | H2W04 | 165,765 | 15,414 | ||
| [Co(NH3) 6] (OH) 3 | 35,500 | 3,181 | Zn(H2O) 6Cl2 | 3,683 | 0,342 | ||
| [Zn (NH3) 6] (OH) 2 | 3,036 | 0,272 | Си(Н2О) 4С12 | 0,963 | 0,090 | ||
| [Си (NH3) 6] (OH) 2 | 0,774 | 0,069 | СоС12 | 6,093 | 0,567 | ||
| NH4C1 | 91,891 | 8,545 | |||||
| НС1 | 69,177 | 6, 199 |
| ||||
| Н2О | 806,187 | 72,245 | Н20 | 807,038 | 75,043 | ||
| Всего | 1115,901 | 100 | Всего | 1075,433 | 100 | ||
| Невя: | ка от прихода | 40,468 | 3,626 | ||||
Блок 5 Прокалка и сушка.
WOs получают термическим разложением H2WC4 при 750-800 °С
При прокалке идет следующая реакция:
H2WO4^WO3+H2O
Количество продуктов, (кг/ч):
Масса WO3 =153,79 (кг/ч)
Масса Н2О = 165,765-153,76= 11,075 (кг/ч)
Вывод: полученная нарастающая с каждой стадией невязка до 3,626% вызвана погрешностью расчетов.
Операция №1
Переведем заданный базис из объема в массу.
m = V * ρ
m = 1000 * 1,120 = 1120т или 1120000кг.
1). G01 = 1120000
2Fe3+ + Fe → 3Fe2+
m (Fe) = mр-ра / ρр-ра * (с(Fe3+) / М(Fe2O3)) * M(Fe)
Для того, чтобы считать восстановление полным, введем 10% избыток железной стружки.
G011 = G01 / 1,120 * 0,005 /159,7 * 55,8 * 1,1 = 0,001715828 * G01
2). G011 - 0,001715828 * G01 = 0
Операция №2
3). G12 – G01 – G011 = 0
При экстракции соотношение объемов водной (сернокислый раствор) и органической (раствор 0,1 моль/л Д2ЭГФК в керосине) равно 10, т.е. Vв: Vо = 10: 1. Такое соотношение фаз берётся для большего концентрирования ценного компонента.
V = m / ρ
Vв = G12 / ρ12; Vо = G050 / ρ050
10 * ρ12 * G050 = G12 * ρ050
G050 = G12 * ρ050 / 10 * ρ12
G050 = G12 * 0,744 / 10* 1,120 = 0,0664285 * G12
4). G050 – 0,0664285 * G12 = 0
G200 = G12 - G01 / 1,120 * 0,05 (ThO2) - G01 / 1,120 * 0,2 (TiO2) - G01 / 1,120 * 0,57 (РЗЭ) - G01 / 1,120 * 0,4 (V2O5) - G01 / 1,120 * 0,02 * 0,999 (Sc2O3)
5). G200 - G12 + 0,001107125 = 0
6). G23 - G050 - G12 + G200 = 0
Операция №3
При реэкстракции примесей соотношение объемов водной (Раствор 4,5 моль/л H2SO4) и органической (Экстракт содержащий Sc, Ti, Fe3+, РЗЭ и др.) равно 1, т.е. Vв: Vо = 1: 1. Такое соотношение фаз берётся для лучшего извлечения примесей.
G030 = G23 * ρ030 / ρ23
G030 = 1,260 / 0,744 * G23 = 1,693548387 * G23
7). G030 - 1,693548387 * G23 = 0
G300 = G030 + (G01 / 1,120 * 0,05 (ThO2) + G01 / 1,120 * 0,2 (TiO2) + G01 / 1,120 * 0,57 (РЗЭ) + G01 / 1,120 * 0,4 (V2O5)) - G01 / 1,120 * 0,02 * 0,999 (Sc2O3)
8). G300 - G030 – 0,001089285 * G01
9). G34 – G030 – G23 + G300 = 0
Операция №4
При реэкстракции скандия соотношение объемов водной (Раствор 2,5 моль/л NaOH) и органической (Органическая фаза содержащая Sc) равно 0,1, т.е. Vв: Vо = 1: 10. Такое соотношение фаз берётся для большего концентрирования ценного компонента (скандия).
G040 = G34 * ρ040 / 10 * ρ34
G040 = 1,110 / 10 * 0,744 * G34 = 0,147849462 * G34
10). G040 - 0,147849462 * G34 = 0
G45 = G34 – m(Sc3+) + m(Na+)
ScA3 + 3 NaOH → Sc(OH) 3 + 3 NaA
m(Sc3+) = (G01 /1,120 * 0,02 * 0,999) / M(Sc2O3) * 2 * M(Sc(OH) 3) = (G01 /1,120 * 0,02 * 0,999) /137,91 * 2 * 95,97792 = 0,00002483 * G01
m(Na+) = (G01 /1,120 * 0,02 * 0,999) / M(Sc2O3) * 6* M(Na) = (G01 /1,120 * 0,02 * 0,999) / 137,91 * 6* 22,9897 = 0,000017842 * G01
G45 = G34 – 0,000006987 * G01
11). G45 – G34 + 0,000006987 * G01 = 0
12). G46 – G040 – G34 + G45 = 0
Операция №5
При регенерации экстрагента соотношение объемов водной (Раствор 0,5 моль/л H2SO4) и органической (Раствор Д2ЭГФК (натриевая форма)) равно 1, т.е. Vв: Vо = 1: 1.
G051 = G45 * ρ051 / * ρ45
G051 = 1,030 / 0,744 * G45 = 1,384408602 * G45
13). G051 - 1,384408602 * G45 = 0
14). G500 – G051 – G45 + G050 = 0
Операция №6
15). G600 – G46 + G67 = 0
После прохождения операции центрифугирования осадок Sc(OH) 3 имеет влажность 20%.
G67 = m(Sc(OH) 3) / 0,8
G67 = (G01 /1,120 * 0,02 * 0,999) / M(Sc2O3) * 2 * M(Sc(OH) 3) / 0,8 = (G01 /1,120 * 0,02 * 0,999) /137,91 * 2 * 95,97792 / 0,8 = 0,00002483 * G01 / 0,8 = 0,000031037 * G01
16). G67 - 0,000031037 * G01 = 0
Операция №7
G700 = G01 / M(Sc2O3) * 0,999 * 3 * M(H2O) + G67 * 0,2 = 0,000006985 * G01 + 0,2 * G67
17). G700 - 0,000006985 * G01 - 0,2 * G67
18). G70 – G67 + G700 = 0
Заменим потоки в уравнениях на соответствующие неизвестные X.
Общий вид уравнений материального баланса.
1). X1 = 1120000
2). X2 – 0,0017158280*X1 = 0
3). X3 – X1 – X2 = 0
4). X4 – 0,0664285*X3 = 0
5). X5 – X3 + 0,001107125*X1 = 0
6). X6 – X4 – X3 + X5 = 0
7). X7 – 1,693548387*X6 = 0
8). X8 – X7 – 0,001089285*X1 = 0
9). X9 – X7 – X6 + X8 = 0
10). X10 – 0,147849462*X9 = 0
11). X11 – X9 + 0,000006987*X1 = 0
12). X12 – X10 – X9 + X11 = 0
13). X13 – 1,384408602*X11 = 0
14). X14 – X13 – X11 + X4 = 0
15). X15 – X12 + X16 = 0
16). X16 – 0,000031037*X1 = 0
17). X17 – 0,000006985*X1 – 0,2*X16 = 0
18). X18 – X16 + X17 = 0
Расчет полученных уравнений материального баланса ведем с помощью табличного процессора EXCEL [15]. (см. Приложение 1).
Сводные таблицы материального баланса.
| приход | кг | % | расход | кг | % |
| Сернокислый раствор, содержащий Fe, РЗЭ, Sc и др. | 1120000 | 99,83 | Сернокислый раствор | 1121921,73 | 100 |
| Железная стружка | 1921,73 | 0,17 | |||
| итого | 1121921,73 | 100 | итого | 1121921,73 | 100 |
1. Восстановление железа.
| риход | кг | % | расход | кг | % |
| Сернокислый раствор | 1121921,73 | 93,77 | Рафинат, содержащий Fe2+ | 1120681,75 | 93,67 |
| Раствор 0,1 моль/л Д2ЭГФК в керосине | 74527,58 | 6,23 | Экстракт, содержащий Sc, Ti, РЗЭ и др. | 75767,56 | 6,33 |
| итого | 1196449,31 | 100 | итого | 1196449,31 | 100 |
2. Экстракция.
3. Реэкстракция примесей.
| приход | кг | % | расход | кг | % |
| Экстракт, содержащий Sc, Ti, РЗЭ и др. | 75767,56 | 37,13 | Реэкстракт, содержащий V, Ti, Th, РЗЭ и др. | 129536,02 | 63,47 |
| Раствор 4,5 моль/л H2SO4 | 128316,02 | 62,87 | Органическая фаза, содержащая Sc | 74547,56 | 36,53 |
| итого | 204083,58 | 100 | итого | 204083,58 | 100 |
4. Реэкстракция скандия.
| приход | кг | % | расход | кг | % |
| Органическая фаза, содержащая Sc | 74547,56 | 87,12 | Раствор Д2ЭГФК(натриевая форма) | 74539,73 | 87,11 |
| Раствор 2,5 моль/л NaOH | 11021,81 | 12,88 | Sc(OH) 3+H2O (пульпа) | 11029,64 | 12,89 |
| итого | 85569,37 | 100 | итого | 85569,37 | 100 |
5. Регенерация экстрагента.
| приход | кг | % | расход | кг | % |
| Раствор Д2ЭГФК(натриевая форма) | 74539,73 | 41,94 | Раствор Na2SO4 | 103205,60 | 58,07 |
| Раствор 0,5 моль/л H2SO4 | 103193,45 | 58,06 | Раствор 0,1 моль/л Д2ЭГФК в керосине | 74527,58 | 41,93 |
| итого | 177733,18 | 100 | итого | 177733,18 | 100 |
6. Центрифугирование.
| приход | кг | % | расход | кг | % |
| Sc(OH) 3+H2O (пульпа) | 11029,64 | 100 | H2O после центрифугирования | 10994,88 | 99,68 |
| Sc(OH) 3 (осадок с влажностью 20%) | 34,76 | 0,32 | |||
| итого | 11029,64 | 100 | итого | 11029,64 | 100 |
7. Сушка и прокаливание.
| приход | кг | % | расход | кг | % |
| Sc(OH) 3 (осадок с влажностью 20%) | 34,76 | 100 | H2O после сушки | 14,77 | 42,49 |
| Sc2O3 | 19,99 | 57,51 | |||
| итого | 34,76 | 100 | итого | 34,76 | 100 |
Вывод
В процессе производственной деятельности образуются отходы, которые нарушают экологическое равновесие, загрязняя окружающую среду, и снижают степень извлечения ценных компонентов, содержащихся в исходном сырье. Эти отходы необходимо перерабатывать.
В настоящее время подсчеты показали, что удельные капитальные затраты на сбор и переработку вторичного металла в 25 раз меньше, чем на производство металла из руды.
Производительность труда во вторичной цветной металлургии примерно в два раза выше, чем в первичной. Сбор и переработка вторичных металлов имеют не только экономический, но и социальный эффект.
Отходы подразделяют на отходы производства и отходы потребления (лом).
В настоящее время для производства режущих инструментов широко используются твердые сплавы. Они состоят из карбидов вольфрама, титана, тантала, сцементированных небольшим количеством кобальта. Карбиды вольфрама, титана и тантала обладают высокой твердостью, износостойкостью. Скорости резания инструментами, оснащенными твердыми сплавами, в 3-4 раза превосходят скорости резания инструментами из быстрорежущей стали.
Недостатком твердых сплавов, по сравнению с быстрорежущей сталью, является их повышенная хрупкость, которая возрастает с уменьшением содержания кобальта в сплаве. И, следовательно, возникает вопрос утилизации таких сплавов. Переработка лома и отходов позволяет вернуть металл в кругооборот.
5. Сплавы редких металлов перерабатывают окислением, хлорированием, электролизом и гидрометаллургическим способом. Их переработка осложнена более высоким содержанием других металлов и взаимным влиянием компонентов сплавов на технологические процессы. - Окислительные методы.
Их можно использовать и для переработки сплавов и кусковых отходов твердых сплавов. Применяемые в настоящее время инструментальные твердые сплавы базируются на карбидах вольфрама, титана и тантала или на смеси указанных соединений с добавлением связующего металла - кобальта. - Методы хлорирования.
При хороших технологических показателях следует отметить громоздкость оборудования для хлорных схем, а также трудности, связанные с агрессивностью и токсичностью хлора и хлоридов, необходимостью специальных коррозионностойких материалов для аппаратуры и значительными затратами на реагенты - Способы электрохимического растворения отходов.
Электрохимическое растворение отходов сплавов используют на отечественных и зарубежных предприятиях. Этот метод наиболее дешев и не требует сложной аппаратуры. Электрохимическое растворение целесообразно вести в щелочных растворах, так как образуются легко растворимые соли рения, вольфрама и молибдена.
6. Как показали расчеты:
- невязка материального баланса обжига 2,124%, она связана с погрешностью расчетов, - невязка теплового баланса 0,12% рассчитана с удовлетворительной точностью, - площадь пода равна 1,5м2, для расчета печи с такой площадью пода нужна спец литература, целью данной работы не является данный расчет.
Список литературы
1. Твердость и прочность тугоплавких материалов при высоких температурах, В.А. Борисенко. - Киев: издательство Академии наук Украинской ССР, 1984. - 212с.
2. Металлические порошки и порошковые материалы. Справочник.
3. Б.Н. Глебов, под редакцией д-ра техн. Наук Ю.В. Левинского. - М:
4. Экомет, 2005. - 520.
5. Коровин С. С, Дробот Д.В., Федоров П.И. "Редкие и рассеянные элементы. Химия и технология". В трех книгах. Книга 2. учебник для вузов - М.: МИСИС, 1999. - 464с.
6. Коровин С. С, Дробот Д.В., Федоров П.И. "Редкие и рассеянные элементы. Химия и технология". В трех книгах. Книга 3. учебник для вузов - М.: МИСИС, 1999. - 464с.
7. Дробот Д.В., Резник А.М., Юрченко Л.Д. "Оборудование заводов редкометалльной промышленности и основы проектирования". Учеб. пособие. – М.: МИХМ, 1985-72с.
8. Букин В.И., Игумнов М.С., Сафонов В.В., Сафонов Вл.В., Переработка производственных отходов и вторичных сырьевых ресурсов, содержащих редкие, благородные и цветные металлы.
9. Металлы и сплавы. Справочник. Афонин В.К., Ермаков Б.С., и др. под редакцией Солнцева Ю.П. − Санкт – Петербург: НПО Профессионал. 2003. – 376с.
10. NETZSCH-Group // http: // www. rudgormash. ru/
11. Дейнека С.С., Трусова В.Г., Хазан А.З. Хлоридная и регенеративная переработка отходов металлического вольфрама и твердых сплавов // Цветные металлы. 1995. №10. С.17 – 19.
12. УГМК - РУДГОРМАШ. "Обогатительное и горношахтное оборудование" http: // www. rudgormash. ru/
13. Лидин Р.А., Молочко В.А., Андреева Л.Л., Химические свойства неорганических вешеств,− М.: Колос, 2003.
14. Болотников Л.Е., Технологическое проектирование производства редких металлов.
15. Морозов В.А., Миткалийный В.И., Егоров А.В., Сборщиков Г.С. "Металлургические печи атлас". - М.: Металлургия. 1987. - 384с.
16. Краткий справочник физико-химических величин/ Под ред. Мищенко К.П., Равделя А.А.
17. http: // www. mechanik. spb. ru
18. http: // www. upmt. ru
19. http: // www. fingo. ru/fri-360/
20. http: // stankinprom. com. ua/products/images/PDF/rci. pdf
21. http: // wwwЛenterm. n] /lenterm_laboratory_fumaces. html И. http: // www. bank. referatoff. ru
22. http: // www. chemport. ru
23. http: // www. drillmat. ru
24. http: // www. npftin. spb. ru
Дата: 2019-05-29, просмотров: 351.