Процессы парообразования и конденсации широко распространены в химической технологии. Важной теплофизической характеристикой при расчете процессов перегонки, выпаривания, ректификации, кипения и сушки является теплота парообразования r.
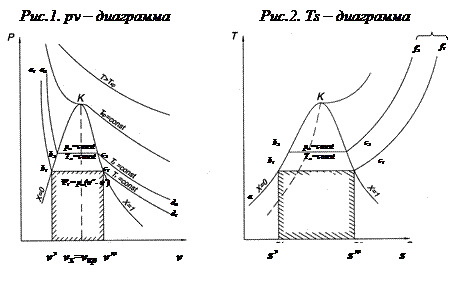
Для исследования термодинамических процессов, происходящих с реальными газами, большое значение имеют pv- и Ts-диаграммы (рис. 1 и 2). Кривые a1 b1 c1 d1, a2 b2 c2 d2… на pv-диаграмме соответствуют процессу расширения вещества при t = const, а кривые ab1 c1 f1, ab2 c2 f2… на Ts-диаграмме – процессу нагревания вещества при p = const.
| ||||
| ||||
|
|
|
|
|
|
|
|
|
|
|
|
Степень сухости:
х = 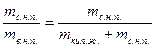 ,
,
где 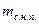 - масса сухого насыщенного пара;
- масса сухого насыщенного пара;
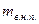 - масса влажного насыщенного пара;
- масса влажного насыщенного пара;
 - масса кипящей жидкости.
- масса кипящей жидкости.
На участках b1 c1, b2 c2,…, где происходит переход жидкости в пар, в равновесии находятся системы, состоящие из двух фаз (двух агрегатных состояний) – жидкой и парообразной, причем температура и давление этих фаз одинаковы. Линии b1 c1, b2 c2,… на обеих диаграммах являются одновременно изобарой и изотермой, т.е. переход жидкости в пар совершается при рн = const, tн = const.
Таким образом, на обеих диаграммах можно выделить пять характерных состояний водяного пара:
· область жидкого состояния, расположенную левее кривой х = 0, 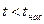 при данном давлении;
при данном давлении;
· линию кипящей (насыщенной) жидкости, х = 0, 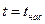 ;
;
· область влажного насыщенного пара – двухфазное состояние, где пар и жидкость находятся в равновесии и имеют одинаковые рн и tн; она расположена между пограничными кривыми х = 0 и х = 1, т.е. в этой области 0 < x < 1, 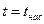 ;
;
· линию сухого насыщенного пара, х = 1, 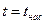 ;
;
· область перегретого пара, расположенную правее кривой х = 1, 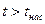 при данном давлении.
при данном давлении.
Переход вещества из одной фазы в другую называется фазовым переходом. Вещества, находящиеся в разных агрегатных состояниях, имеют различные физические свойства. Это различие объясняется характером межмолекулярного взаимодействия.
Количество теплоты, которое необходимо подвести к 1 кг кипящей жидкости для перехода её в сухой насыщенный пар, называется теплотой парообразования r, кДж/кг. Этот процесс протекает при постоянном давлении насыщения и температуре насыщения (рнас= const и tнас = const).
Теплота парообразования может быть рассчитана следующим образом:
 , (1)
, (1)
где 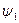 - внешняя составляющая теплоты парообразования, которая расходуется на работу расширения, преодолевая давление рнас:
- внешняя составляющая теплоты парообразования, которая расходуется на работу расширения, преодолевая давление рнас:
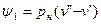 , (2)
, (2)
где 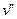 и
и 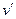 - удельные объемы сухого насыщенного пара и кипящей жидкости соответственно;
- удельные объемы сухого насыщенного пара и кипящей жидкости соответственно;
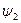 - внутренняя составляющая теплоты парообразования, расходуется на преодоление сил межмолекулярного взаимодействия.
- внутренняя составляющая теплоты парообразования, расходуется на преодоление сил межмолекулярного взаимодействия.
На pv-диаграмме (рис. 1), как следует из уравнения (2), величина работы расширения  показана заштрихованной областью. На Ts-диаграмме (рис.2) заштрихованной областью показана величина теплоты парообразования, которая может быть рассчитана как
показана заштрихованной областью. На Ts-диаграмме (рис.2) заштрихованной областью показана величина теплоты парообразования, которая может быть рассчитана как
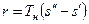 , (3)
, (3)
где 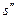 и
и 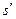 - энтропия сухого насыщенного пара и кипящей жидкости соответственно,
- энтропия сухого насыщенного пара и кипящей жидкости соответственно, 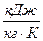 ;
;
Тн - температура насыщения, К.
Из pv- и Т s-диаграмм видно, что с увеличением давления р точки b1, b2,… на нижней пограничной кривой сближаются с точками с1, с2, … на верхней пограничной кривой, и в критической точке они сходятся. Для воды критические параметры в точке К имеют следующие значения: ркр. = 22,13 МПа, tкр. = 374,2 °С, vкр. = 0,00326 м3/кг.
Выше критической точки К при p > pкр. и Т > Ткр. двухфазного состояния не наблюдается. Жидкая фаза находится под весьма большим внутренним давлением. Фактором, определяющим интенсивность межмолекулярных взаимодействий, является не давление, а температура. С ростом температуры и давления теплота парообразования r уменьшается, а в критической точке r = 0, 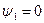 и
и 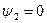 , так как в этом состоянии исчезает различие между жидкостью и ее паром и процесс парообразования отсутствует.
, так как в этом состоянии исчезает различие между жидкостью и ее паром и процесс парообразования отсутствует.
| |
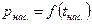 называется кривой насыщения (рис. 3).
называется кривой насыщения (рис. 3).
 Связь между температурой и давлением насыщения выражается уравнением Клапейрона-Клаузиуса [4, 5]:
Связь между температурой и давлением насыщения выражается уравнением Клапейрона-Клаузиуса [4, 5]:
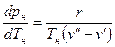 , (4)
, (4)
 где
где 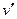 ,
, 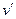 - удельные объемы соответственно сухого насыщенного пара и жидкости на линии насыщения при Тнас. и рнас., м3/кг. Поскольку
- удельные объемы соответственно сухого насыщенного пара и жидкости на линии насыщения при Тнас. и рнас., м3/кг. Поскольку  >
> 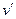 , из уравнения (4) следует, что при фазовом переходе жидкость-пар производная
, из уравнения (4) следует, что при фазовом переходе жидкость-пар производная 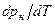 всегда больше нуля, т.е. с ростом давления температура насыщения увеличивается до значения критической точки.
всегда больше нуля, т.е. с ростом давления температура насыщения увеличивается до значения критической точки.
В термодинамике внутренняя энергия u (кДж/кг), энтальпия h (кДж/кг), теплоемкость c (кДж/кг К), теплота парообразования r= h”- h’ (кДж/кг) называются калорическими свойствами вещества (1 калория = 4,19 Дж), удельный объем v (м3/кг), давление p (Па) (1 Па = 1 н/м2), и температура T (К) – термическими. Известно, что термические параметры определяются намного проще, чем калорические, поскольку устанавливаются прямыми или косвенными измерениями соответствующими приборами. Таким образом, уравнение Клапейрона-Клаузиуса (4) устанавливает связь между термическими и калорическими свойствами, а также свойствами насыщенной жидкости и сухого насыщенного пара. Поэтому уравнение Клапейрона-Клаузиуса можно использовать для определения калорической характеристики – удельной теплоты парообразования воды r по измеренным в опыте термическим параметрам рн и Тн.
Проведение опытов
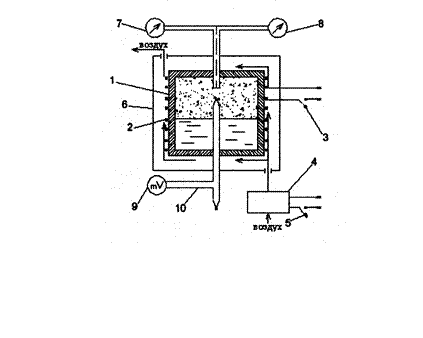
Экспериментальная установка (рис. 4) представляет собой замкнутый сосуд высокого давления, содержащий такое количество воды, при котором удельный объем vx двухфазной системы жидкость-пар (влажный насыщенный пар) равен критическому значению в точке К:
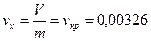 , м3/кг, (5)
, м3/кг, (5)
где V - внутренний объем сосуда, м3;
т - масса системы жидкость-пар, кг;
vкр - удельный объем системы в критической точке, м3/кг.
 | |||
| |||

|
Проведение опытов
1. Установка включается преподавателем, она прогревается, и давление начинает расти.
2. Измерения начинать по достижении показания манометра 5 делений и далее через каждые 5 делений по шкале манометра. Одновременно с показаниями манометра в таблицу (табл.1) записывать показания ЭДС термопары е, мВ, измеряемые милливольтметром 9.
3. По достижении показаний манометра 50 делений показать результаты преподавателю.
4. Определить температуру окружающей среды tокр и атмосферное давление В. Заполнить таблицу (табл.1).
5. С разрешения преподавателя установку можно отключить.
Таблица 1
Результаты измерений и обработки
| ризб . | рн, МПа | е , мВ |
| tокр, °С | tн, °С | В, | |
| делений | кгс/см2 | ||||||
| 5 |
|
| |||||
| 10 | |||||||
| 15 |
| Дата и подпись преподавателя: | |||||
| 20 | |||||||
| 25 | |||||||
| 30 | |||||||
| 35 | |||||||
| 40 | ФИО студента № гр.
| ||||||
| 45 | |||||||
| 50 | |||||||
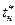 - задается преподавателем каждому студенту индивидуально.
- задается преподавателем каждому студенту индивидуально.
Обработка опытных данных
1. Рассчитать абсолютное давление насыщенного пара для всех точек:
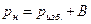 , Па;
, Па;
1 кгс/см2 = 735,6 мм рт. ст.;
750 мм рт. ст. = 105 Па = 0,1 МПа.
2. По величинам е из градуировочного графика определить значения 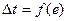 , где
, где 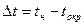 . Искомая температура насыщения
. Искомая температура насыщения  , °С. Результаты занести в таблицу (табл.1).
, °С. Результаты занести в таблицу (табл.1).
3. На миллиметровой бумаге или страничке в клеточку опытные данные рн и tн нанести на диаграмму 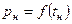 и построить кривую насыщения (рис. 3), выбрав масштабы по осям:
и построить кривую насыщения (рис. 3), выбрав масштабы по осям:
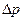 = 1МПа
= 1МПа 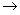 1 см;
1 см;
 = 10 °С
= 10 °С 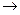 1 см.
1 см.
Методом графической интерполяции построить плавную сглаживающую кривую насыщения, используя гибкую линейку (количество точек над и под кривой должно быть примерно одинаковым). При заданной температуре 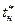 провести касательную к кривой насыщения. При этом расстояния от касательной до кривой на равных плечах от заданной точки должны быть примерно одинаковыми.
провести касательную к кривой насыщения. При этом расстояния от касательной до кривой на равных плечах от заданной точки должны быть примерно одинаковыми.
4. С помощью уравнения (4) рассчитать теплоту парообразования r при заданной температуре 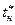 :
:
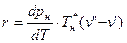 , кДж/кг.
, кДж/кг.
Значение производной 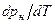 определить графически как тангенс угла наклона касательной
определить графически как тангенс угла наклона касательной 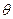 к кривой насыщения в точке с температурой
к кривой насыщения в точке с температурой 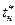 (геометрический смысл первой производной!) (рис. 3), т.е. с учетом размерностей:
(геометрический смысл первой производной!) (рис. 3), т.е. с учетом размерностей:
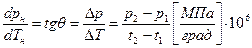 , Па/град.
, Па/град.
Точность определения теплоты парообразования r будет зависеть от тщательности построения диаграммы и проведения графических измерений.
Значение удельных объемов 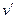 и
и  приведены в табл.2.
приведены в табл.2.
Таблица 2
Параметры насыщенного водяного пара
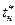 , °С , °С
| v’, м3/кг | v“,м3/кг | h’, кДж/кг | S’, кДж/кг К | r, кДж/кг |
| 250 | 0,001251 | 0,05005 | 1086,1 | 2,7034 | 1715,0 |
| 255 | 0,001263 | 0,04591 | 1110,2 | 2,8394 | 1689,0 |
| 260 | 0,001275 | 0,04215 | 1135,0 | 2,8851 | 1661,0 |
| 265 | 0,001289 | 0,03872 | 1160,2 | 2,9307 | 1634,0 |
| 270 | 0,001302 | 0,03560 | 1185,3 | 2,9764 | 1605,0 |
| 275 | 0,001317 | 0,03274 | 1210,7 | 3,0223 | 1574,2 |
| 280 | 0,001332 | 0,03013 | 1236,8 | 3,0685 | 1542,9 |
| 285 | 0,001348 | 0,02774 | 1263,1 | 3,1146 | 1510,2 |
| 290 | 0,001365 | 0,02533 | 1290,0 | 3,1611 | 1476,3 |
| 295 | 0,001384 | 0,02351 | 1317,2 | 3,2079 | 1441,0 |
| 300 | 0,001404 | 0,02164 | 1344,8 | 3,2548 | 1404,2 |
| 305 | 0,001425 | 0,01992 | 1373,1 | 3,3026 | 1365,6 |
| 310 | 0,001447 | 0,01831 | 1402,2 | 3,3507 | 1325,2 |
| 315 | 0,001472 | 0,011683 | 1431,7 | 3,3996 | 1282,3 |
| 320 | 0,001499 | 0,01545 | 1462,0 | 3,4495 | 1237,8 |
| 325 | 0,001529 | 0,01417 | 1493,6 | 3,5002 | 1190,3 |
| 330 | 0,001562 | 0,01297 | 1626,1 | 3,5522 | 1139,6 |
| 335 | 0,001599 | 0,01184 | 1559,8 | 3,6056 | 1085,7 |
| 340 | 0,001639 | 0,01078 | 1594,8 | 3,6605 | 1027,0 |
| 345 | 0,001689 | 0,00977 | 1639,0 | 3,7184 | 963,5 |
| 350 | 0,001741 | 0,00880 | 1671,0 | 3,7786 | 893,5 |
| 355 | 0,001807 | 0,00787 | 1714,0 | 3,8439 | 813,0 |
| 360 | 0,001894 | 0,00694 | 1762,0 | 3,9162 | 719,3 |
Примечание: 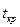 = 374,15 оС,
= 374,15 оС, 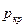 =22,129 МПа,
=22,129 МПа,  =0,00326 м3/кг.
=0,00326 м3/кг.
При критических параметрах r =0.
Построить графическую зависимость теплоты парообразования от температуры насыщения 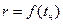 . Для этого отложить экспериментальные значения
. Для этого отложить экспериментальные значения 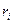 , рассчитанные при
, рассчитанные при  , на диаграмме
, на диаграмме 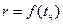 , выбрав масштабы по осям:
, выбрав масштабы по осям:
ордината  = 50 кДж/кг → 1 см;
= 50 кДж/кг → 1 см;
абсцисса  = 5оС → 1 см.
= 5оС → 1 см.
При этом следует использовать результаты, полученные другими участниками своей бригады. Объяснить полученную зависимость, пользуясь Ts - диаграммой водяного пара (рис.2).
5. По уравнениям (2) и (1) рассчитать значение внешней ( 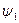 ) и внутренней (
) и внутренней ( 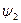 ) теплоты парообразования при температуре
) теплоты парообразования при температуре 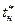 .
.
6. Рассчитать степень сухости х влажного насыщенного пара при температуре 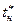 исследованной двухфазной системы: х
исследованной двухфазной системы: х  , где vx = 0,00326 м3/кг в соответствии с выражением (5).
, где vx = 0,00326 м3/кг в соответствии с выражением (5).
7. Вычислить энтальпию влажного насыщенного пара:
 х, кДж/кг,
х, кДж/кг,
где 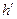 - энтальпия жидкости на линии насыщения при температуре
- энтальпия жидкости на линии насыщения при температуре 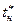 (табл. 2).
(табл. 2).
8. Определить внутреннюю энергию влажного насыщенного пара при температуре 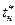 :
:
 , кДж/кг.
, кДж/кг.
9. Рассчитать энтропию влажного насыщенного пара при температуре 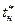 :
:
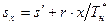 , кДж/(кг×К),
, кДж/(кг×К),
где 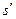 - энтропия жидкости на линии насыщения при температуре
- энтропия жидкости на линии насыщения при температуре 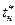 (табл.2).
(табл.2).
10. Изобразить на pv- и Ts-диаграммах (без соблюдения масштаба) исследованный изохорный процесс.
11. Сравнить полученную в опыте величину теплоты парообразования r со справочными данными rтабл. (табл. 2):
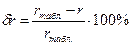 .
.
Величина δ r характеризует качество проведенных измерений и обработки опытных данных.
Контрольные вопросы
1. pv- и Ts-диаграммы водяного пара.
2. Процессы фазового перехода на pv- и Ts-диаграммах.
3. Области состояния водяного пара. Кипящая жидкость, влажный насыщенный, сухой насыщенный и перегретый пар. Степень сухости.
4. Температура и давление насыщения. Кривая насыщения.
5. Методика определения и физический смысл r, 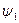 ,
, 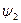 , x,
, x, 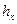 ,
, 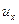 ,
,  .
.
6. Термические и калорические параметры.
7. Уравнение Клапейрона-Клаузиуса. Достоинства этого уравнения и их использование для определения теплоты парообразования.
8. Схема экспериментальной установки и методика проведения эксперимента.
9. Источники погрешностей измерения. Виды погрешностей. Методика расчета.
Библиографический список
1. Теплофизические свойства теплоносителей и рабочих тел энерготехнологических процессов и установок. метод. указания / сост.: В. А. Аляев [и др.]. - Казань: Изд-во Казан. гос. технол. ун-та, 2000. – 62 с.
2. Лабораторный практикум по термодинамике и теплопередаче / В.Н. Афанасьев [и др.]; под ред. В. И. Крутова, Е. В. Шишова. – М.: Высшая школа, 1988. – 216 с.
3. Гумеров, Ф. М. Суб- и сверхкритические флюиды в процессе переработки полимеров / Ф. М. Гумеров, А. Н. Сабирзянов, Г. И. Гумерова. – Казань: ФЭН, 2007. – 336 с.
4. Техническая термодинамика: учебник для энергомашиностроит. спец. вузов /В. И. Крутов [и др.]. – М.: Высшая школа, 1991. – 384 с.
5. Нащокин, В.В. Техническая термодинамика и теплопередача: учебное пособие для вузов / В.В. Нащокин. – М.: Аз-book, 2008. – 468 с.
Содержание
ВВЕДЕНИЕ.. 3
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ.. 4
ТЕПЛОТЕХНИЧЕСКИЕ ИЗМЕРЕНИЯ.. 5
ОЦЕНКА ПОГРЕШНОСТИ ЭКСПЕРИМЕНТА.. 8
Лабораторная работа 21
ИССЛЕДОВАНИЕ ПАРАМЕТРОВ ВЛАЖНОГО
ВОЗДУХА В ПРОЦЕССАХ СУШКИ.. 13
Лабораторная работа 22
ОПРЕДЕЛЕНИЕ ТЕПЛОЕМКОСТИ ВОЗДУХА.. 26
Лабораторная работа 23
ИССЛЕДОВАНИЕ pv-ДИАГРАММЫ УГЛЕКИСЛОГО
ГАЗА. ОПЫТ ЭНДРЮСА.. 37
Лабораторная работа 24
ИССЛЕДОВАНИЕ КРИВОЙ НАСЫЩЕНИЯ
ВОДЯНОГО ПАРА.. 48
Библиографический список. 59
Редактор Л. Г. Шевчук
| Подписано в печать 10.06.2015 | Формат 60´84 1/16 | |
| Бумага офсетная | Печать Riso | 3,48 усл. печ. л. |
| 3,75 уч.-изд. л. | Тираж 100 экз. | Заказ «С» 67 |
|
Издательство Казанского национального исследовательского
| ||
| Офсетная лаборатория Казанского национального исследовательского технологического университета
420015, Казань, К. Маркса, 68 | ||
Дата: 2019-05-29, просмотров: 350.
 , °С
, °С