Ответ: Схема цепочки химических превращений:
C2H2 → C2H4→C2H6→C2H5Cl→C2H5OH→CH3CHO→CH3COOH
↓ ↓ ↓ ↓
C6H6 C2H5OH CH2=CH-CH=CH2 CH3COOC2H5
↓ ↓ ↓
C6H5Cl CH3O-C2H5 C4H10
↓
C6H5Cl
↓
C6H5OH
↓
C6H2Br3OH
Реакции :
C2H2 + H2 = C2H4,
алкин алкен
C2H4 + H2 = C2H6,
алкен алкан
C2H6 + Cl2 = C2H5Cl + HCl,
C2H5Cl + NaOH = C2H5OH + NaCl,
хлоралкан спирт
С2H5OH + 1/2O2 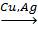 CH3CHO + H2O,
CH3CHO + H2O,
спирт альдегид
CH3CHO + 2Cu(OH)2 = CH3COOH + 2CuOH + H2O,
кислота
C2H4 + H2O 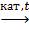 C2H5OH,
C2H5OH,
алкен спирт
C2H5OH + CH3OH = CH3O-C2H5 + H2O,
спирт спирт простой эфир
3С2H2 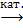 С6Н6,
С6Н6,
алкин арен
C6H6 + Cl2 = C6H5Cl + HCl,
C6H5Cl + NaOH = C6H5OH + NaCl,
фенол
C6H5OH + 3Br2 = C6H2Br3OH + 3HBr;
2С 2 H5OH = CH2 = CH-CH = CH2 + 2H2O + H2,
спирт диен
CH2 = CH-CH = CH2 + 2H2 = C4H10.
диен алкан
Алканы - углеводороды с общей формулой СnH2n+2, которые не присоединяют водород и другие элементы.
Алкены - углеводороды с общей формулой СnH2n , в молекулах которых между атомами углерода имеется одна двойная связь.
К диеновым углеводородам относят органические соединения с общей формулой СnH2n-2, в молекулах которых имеются две двойные связи.
Углеводороды с общей формулой СnH2n-2, в молекулах которых имеется одна тройная связь, относят к ряду ацетилена и называют алкинами.
Соединения углерода с водородом, в молекулах которых имеется бензольное кольцо, относят к ароматическим углеводородам.
Спиртами называются производные углеводородов, в молекулах которых один или несколько атомов водорода замещены гидроксильными группами.
К фенолам относят производные ароматических углеводородов, в молекулах которых гидроксильные группы связаны с бензольным ядром.
Альдегиды- органические вещества, содержащие функциональную группу- СНО ( альдегидную группу).
Карбоновые кислоты- это органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединенных с углеводородным радикалом или атомом водорода.
К сложным эфирам относятся органические вещества, которые образуются в реакциях кислот со спиртами и содержат группу атомов С(О)-О-С.
Вопрос 2. Типы кристаллических решеток. Характеристика веществ с различными типами кристаллических решеток.
Ответ. Кристаллическая решетка – пространственное, упорядоченное взаиморасположением частиц вещества, имеющее однозначный, распознаваемый мотив.
В зависимости от вида частиц, расположенных в узлах решетки, различают : ионные (ИКР), атомные (АКР), молекулярные (МКР), металлические (Мет. КР), кристаллические решетки.
МКР – в узлах находится молекула. Примеры : лед, сероводород, аммиак, кислород, азот в твердом состоянии. Силы, действующие между молекулами, сравнительно слабые, поэтому вещества имеют малую твердость, низкие температуры кипения и плавления, плохую растворимость в воде. В обычных условиях это газы или жидкости (азот, пероксид водорода, твердый CO2). Вещества с МКР относятся к диэлектрикам.
АКР- в узлах атомы. Примеры : бор, углерод (алмаз), кремний, германий. Атомы соединены прочными ковалентными связями, поэтому для веществ характерны высокие температуры кипения и плавления, высокая прочность и твердость. Большинство таких веществ не растворимо в воде.
ИКР – в узлах катионы и анионы. Примеры : NaCl, KF, LiBr. Такой тип решетки имеется у соединений с ионным типом связи (металл-неметалл). Вещества тугоплавкие, малолетучие, сравнительно прочные, хорошие проводники электрического тока, хорошо растворимы в воде.
Мет. КР – решетка веществ, состоящих только из атомов металла. Примеры : Na, K, Al, Zn, Pb и т.д. Агрегатное состояние твердое, нерастворимо в воде. Кроме щелочных и щелочно-земельных металлов, проводники электрического тока, температуры кипения и плавления колеблются от средних до очень высоких.
Дата: 2019-05-28, просмотров: 326.