Возможность кислотных и/или основных свойств у гетероциклических соединений обусловлена присутствием в их молекулах соответственно кислотных и/или основных реакционных центров.
Кислотные свойства.
Наиболее активные кислотные центры гетероциклов сформированы протонами, обычно, на пиррольных гетероатомах: делокализация электронной плотности пиррольного гетероатома в кольцо увеличивает подвижность протона за счет увеличения полярности связи протона с гетероатомом и увеличения устойчивости соответствующего аниона. Поэтому кислотные свойства гетероциклов увеличиваются при переходе от насыщенных соединений с sp3 – гибридными гетероатомами к ароматическим. Кислотные свойства гетероциклических соединений с двумя
гетероатомами (пиридиновый гетероатом - электроноакцептор) более выражены, чем у соединений с одним гетероатомом.
Например, среди пятичленных ароматических гетероциклических соединений N-H кислотные свойства характерны, для пиррола, пиразола, имидазола, индола и других подобных соединений. Кислотные свойства всех этих соединений существенно выше, чем у насыщенного пирролидина. Кислотные свойства имидазола, индола и бензимидазола более выражены, чем у пиррола.
Изменение N-H кислотных свойств (рКа в ДМСО):
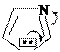
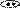 ЭА
ЭА
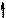 sp3 N
sp3 N
H
<< < <

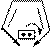
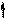
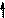
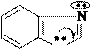
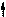 sp2 N N N
sp2 N N N
H H H
пирролидин рКа 23 рКа~19 рКа 44
меньше
N
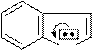
 H pKa~21
H pKa~21
 |
электронная плотность
увеличение кислотных свойств
Пиррол как N-H кислота образует соли в реакциях с калием К, твердым гидроксидом калия КОН (при температуре выше 100оС), NaNH2 в жидком аммиаке. Продуктом этих реакций является соль пирролкалий (или пирролнатрий).
Примеры реакций:
 K
K
-H2
 KOH тв., to
KOH тв., to
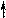 N -HOH
N -HOH
H KNH2
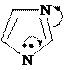 -NH3
-NH3
KOH тв., to

-HOH
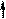
H
пирролкалий
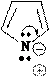 K
K
 имидазолкалий
имидазолкалий
K 
Отрицательный заряд в анионе делокализован. Например, в пиррол- анионе:
 |  | ||
N N N
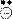
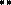
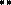

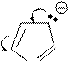
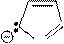 Кислотные свойства пиррола (N – H кислота) выражены слабо (слабее, чем у одноатомных спиртов – О-Н кислоты), поэтому соли пиррола в воде полностью гидролизованы:
Кислотные свойства пиррола (N – H кислота) выражены слабо (слабее, чем у одноатомных спиртов – О-Н кислоты), поэтому соли пиррола в воде полностью гидролизованы:
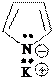 + HOH
+ HOH
+ KOH

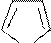
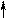 N
N
H
сильное основание в растворе
Основные свойства.
Основный центр в молекулах гетероциклических соединений сформирован на гетероатомах, имеющих подходящую неподеленную пару электронов; в молекулах ароматических гетероциклов основные свойства имеет пиридиновый гетероатом. Поэтому основные свойства не характерны для пятичленных ароматических гетероциклических соединений с одним гетероатомом (он пиррольный), в кислой среде эти соединения не образуют солей (устойчивых катионов), а N- и О- содержащие пятичленные ароматические гетероциклы показывают ацидофобность.
Основные свойства характерны для пятичленных ароматических гетероциклов с двумя гетероатомами (второй гетероатом пиридиновый). Пиррольный гетероатом действует при этом как электронодонор, способствуя проявлению соединением основных свойств. Пятичленные ароматические гетероциклические соединения в целом являются довольно слабыми основаниями. Их основные свойства выражены существенно слабее, чем у насыщенных гетероциклических соединений. Основные свойства насыщенных гетероциклов максимально выражены у азотсодержащих соединений. Это сильные основания, их основные свойства соответствуют основности алифатических аминов. Кислород- и серусодержащие насыщенные гетероциклы имеют более слабые (особенно, содержащие серу) основные свойства, аналогичные свойствам простых эфиров и сульфидов.
Изменение основных свойств:
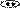
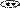 NH(C2H5)2~
NH(C2H5)2~
sp2
 N
N
>>
основный центр
 >
>
основный центр
sp3
N основный
 H центр
H центр
N ЭД
 H
H
O более слабый ЭД
|
| пирролидин | имидазол | оксазол | |
| рКВН | 11 | 11.3 | 7 | |

Примеры реакций:
увеличение основных свойств


 HCl
HCl


 N N
N N
H H H
Cl-
пирролидиний хлорид





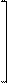 N Cl-
N Cl-
H H
имидазолий хлорид
|
 H2SO4 N
H2SO4 N


 N N
N N
H H
HSO -
Дата: 2019-05-28, просмотров: 326.