Двуокись углерода оказывает двоякое действие на крг!вуи л негоциации окси гемоглобина. С одной стороны, содержание СО2 влияет на внутриклеточный рН (;я|)фект Бора). С другой стороны, накопление ССЬ вызывает образование ^//70<т.лш-нотяхсоединений'вследствиеее взаимодействия с аминогруппами i емоглобина. Эти кирбаминовые соединения служат в качестве аллостерических эффекторов молекулы гемоглобина и непосредствен]го влияют на связывание О?.. Низкий уровень кар-баминовых соединений вызывает сдвиг кривой вправо и снижение сродства гемоглобина к О2, что сопровождается увеличением высвобождения (>, б тканях. По мере роста РаСО2 сопутствующее ему увеличение карбаминовы х с< единений сдвигает кривую влево, повышая связывание ()2 гемоглобином.
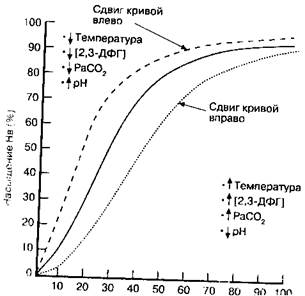
Рис. J0-,'f. Отклонения крином /; и i v.<; ц i ы 11 и и i < • \\ (; г л (>61111 а, я ы л -манные 'к'-лпк'ра гурой. копнет -рацией '-],3-ДФ1 , Расо, и рН. От-клон(пне нп})ан^ ука:шнает на у f i (' /f и ч ( 11 и е Р -,,;. * ( у м < > н i) 111 e 11 и е сродства гемоглобина к О2; ньг свобожЖ'П ие О2 у нел и ч и нается. Отклонение влгнп ука.чьп^и.'т на умс'пыиение Р 1() и унеличепиг сро/1.ства гемоглобина к О,-: m.ic-иобожлсниг О:: уме.пынаеч'ся
Концентрация органических фосфатов
Органические фосфаты, в частности 2,3-дифосфоглицерат (2,3-ДФГ), образуются в эритроцитах в процессе гликолиза. Концентрация органических фосфатов в эритроците в несколько раз выше, чем концентрация аденозинтрифосфата - главного источника энергии в других клетках человека. В эритроците нет митохондрий, в которых происходит окислительное фосфорилирование, поэтому в нем в качестве энергетического субстрата используется 2,3-ДФГ. Продукция 2,3-ДФГ увеличивается во время гипоксемии, что является важным механизмом адаптации. Ряд условий, вызывающих снижение О2 в периферических тканях, таких как анемия, острая кровопотеря, хроническое заболевание легких, застойная сердечная недостаточность, пребывание на больших высотах, право-левостороннее шунтирование (гл. 12 и 13), характеризуются увеличением продукции органических фосфатов в эритроцитах. При этом уменьшается сродство гемоглобина к О2 и повышается его высвобождение в тканях. И наоборот, при некоторых патологических состояниях, таких как септический шок и гипофосфатемия, наблюдается низкий уровень 2,3-ДФГ, что приводит к сдвигу кривой диссоциации оксигемоглобина влево.
Температура
Температура тела влияет на кривую диссоциации оксигемоглобина менее выражено и клинически значимо, чем факторы, описанные выше. Гипертермия вызывает повышение РГ)(Ь т. е. сдвиг кривой вправо, что является благоприятной приспособительной реакцией на повышенный кислородный запрос клеток при лихорадочных состояниях. Гипотермия, напротив, снижает РГ)(Ь т. е. сдвигает кривую диссоциации влево.
Окись углерода
Окись углерода - газ, обычно используемый при измерении диффузионной способности легких (гл. 9). Он быстро диффундирует через альвеолярно-капилляр-ную мембрану и связывается с гемоглобином, занимая место кислорода. Сродство гемоглобина к СО в 240 раз превосходит таковое для О2. СО, связываясь с гемоглобином (образуется карбоксигемоглобин), ухудшает оксигенацию периферических тканей посредством двух механизмов: (1) СО непосредственно уменьшает кислородную емкость крови, снижая количество гемоглобина, доступного для связывания О2; (2) СО снижает РГ)0 и сдвигает кривую диссоциации оксигемоглобина влево. Важным следствием этих механизмов для клиники является то, что при высоких уровнях карбоксигемоглобина может наблюдаться тяжелая тканевая гипоксия, несмотря на нормальное Ра()2.
Метгемоглобинемия
Окисление части двухвалентного железа гемоглобина до трехвалентного при- J водит к образованию метгемоглобина. В норме у здоровых людей метгемоглобин У составляет менее 3 % общего гемоглобина. Низкий его уровень поддерживается внут-'./| риклеточными ферментными механизмами восстановления. Метгемоглобинемия J может наблюдаться как следствие врожденной недостаточности этих восстанови-1! тельных ферментов или образования аномальных молекул гемоглобина, резистент-| ных к ферментативному восстановлению (например, гемоглобин М). Некоторые;! лекарства, обладающие оксидантными свойствами (например, противомалярийные! средства, фенацетин, местные анестетики), также вызывают метгемоглобинемию. 1 .....—^""' ^nnura^r K-nwnvKi диссоциации оксигемоглобина влево, блоки*!
л
Дата: 2019-03-05, просмотров: 338.