Техническая термодинамика
1.1 Термодинамическая система. Основные понятия и определения
Термодинамика изучает законы превращения энергии в различных физико-химических процессах, происходящих в макроскопических системах и сопровождающихся тепловыми эффектами.
Техническая термодинамика изучает закономерности взаимного превращения тепловой и механической энергии и является (вместе с теорией теплообмена) теоретическим фундаментом теплоэнергетики.
На её основе осуществляют расчет и проектирование всех тепловых двигателей (паровых и газовых турбин; реактивных и ракетных двигателей; двигателей внутреннего сгорания; различного технологического оборудования).
Для наглядности в термодинамике используются молекулярно-кинетические представления о структуре вещества.
Термодинамическая система (ТДС) – совокупность материальных тел, находящихся в механическом и тепловом взаимодействии друг с другом и с окружающими систему внешними телами.
Окружающая среда (ОС) – это тела, не входящие в систему.
Контрольная поверхность (оболочка) – граница термодинамической системы и окружающей среды.
Механическое и тепловое взаимодействия ТДС осуществляются через контрольные поверхности.
При механическом взаимодействии система сама или над ней совершается работа.
Тепловое взаимодействие заключается в переходе теплоты между отдельными телами системы и между системой и окружающей средой.
Открытая система – система, обменивающаяся с ОС энергией и веществом (массообменное взаимодействие). Пример – потоки газа или пара в турбинах или трубопроводах.
Закрытая система – система, обменивающаяся с ОС только энергией без массообмена. Дальше будут рассматриваться закрытые системы.
Теплоизолированная (адиабатная) система – термодинамическая система, которая не обменивается теплом с окружающей средой.
Изолированная (замкнутая) система – система, не обменивающаяся с ОС ни энергией, ни веществом.
Рабочее тело – система в термодинамике, осуществляющая взаимное превращение теплоты и работы. Обычно это газы и пары.
Равновесное состояние системы - такое состояние системы, когда все термодинамические параметры постоянны по времени и одинаковы во всех точках системы.
Неравновесная система – система, между различными точками в которой существуют разности температур, давлений и т.д. В такой системе под действием градиентов параметров возникают потоки теплоты, вещества и т.д., стремящиеся вернуть её в состояние равновесия.
Изолированная система с течением времени всегда приходит в состояние равновесия и никогда самопроизвольно выйти из него не может. В классической термодинамике рассматриваются только равновесные системы.
Идеальный и реальный газ. Уравнение состояния идеального и реального газа
Работа расширения
Работа определяется произведением действующей на рабочее тело силы на путь её действия.
В случае изменения объёма системы на бесконечно малую величину 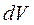 будет совершаться работа
будет совершаться работа
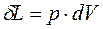 . (1.10)
. (1.10)
При конечном изменении объёма
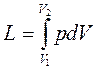 . (1.11)
. (1.11)
Работа расширения – это работа 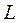 против сил внешнего давления, связанная с увеличением объёма системы.
против сил внешнего давления, связанная с увеличением объёма системы.
Выражение (1.10) справедливо в общем случае и не зависит от формы сосуда, в который помещено рабочее тело, и показывает, что работа изменения объёма закрытой системы равна произведению давления на приращение объёма.
Так как 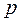 - величина положительная, то
- величина положительная, то 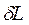 и
и 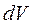 всегда имеют одинаковые знаки:
всегда имеют одинаковые знаки:
если 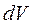 >0, то и
>0, то и 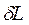 >0, т.е. при расширении работа тела положительна, при этом тело само совершает работу;
>0, т.е. при расширении работа тела положительна, при этом тело само совершает работу;
если 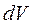 <0, то и
<0, то и 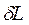 <0, т.е. при сжатии работа тела отрицательна – не тело совершает работу, а на его сжатие затрачивается работа извне.
<0, т.е. при сжатии работа тела отрицательна – не тело совершает работу, а на его сжатие затрачивается работа извне.
Единицей измерения работы в системе СИ является Джоуль (Дж).
Работа расширения 1 кг рабочего тела:
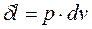 . (1.12)
. (1.12)
Величина 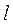 , представляющая собой удельную работу, совершаемую системой, содержащей 1 кг газа, равна:
, представляющая собой удельную работу, совершаемую системой, содержащей 1 кг газа, равна:
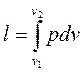 . (1.13)
. (1.13)
В термодинамике для исследования равновесных процессов используют 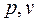 - диаграмму, в которой осью абсцисс служит удельный объём, а осью ординат – давление. Так как состояние термодинамической системы определяется двумя параметрами, то на
- диаграмму, в которой осью абсцисс служит удельный объём, а осью ординат – давление. Так как состояние термодинамической системы определяется двумя параметрами, то на 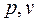 - диаграмме оно изображается точкой. Работа процесса на
- диаграмме оно изображается точкой. Работа процесса на 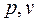 - диаграмме изображается площадью, ограниченной кривой процесса, осью абсцисс и крайними ординатами (рис. 2). Работа изменения объёма эквивалентна площади под кривой процесса в диаграмме
- диаграмме изображается площадью, ограниченной кривой процесса, осью абсцисс и крайними ординатами (рис. 2). Работа изменения объёма эквивалентна площади под кривой процесса в диаграмме 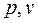 . (Её величина зависит от характера процесса, поэтому у бесконечно малой величины
. (Её величина зависит от характера процесса, поэтому у бесконечно малой величины 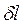 используется символ
используется символ 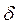 , т.к. величина
, т.к. величина 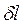 в отличие от
в отличие от 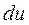 не является полным дифференциалом).
не является полным дифференциалом).
Т.к. величина 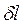 пропорциональна увеличению объёма, то в качестве рабочих тел при преобразовании тепловой энергии в механическую выбирают тела, допускающие значительное увеличение объёма. Это газы и пары жидкостей (для ТЭС – пары воды, для ДВС – газообразные продукты сгорания жидкого топлива).
пропорциональна увеличению объёма, то в качестве рабочих тел при преобразовании тепловой энергии в механическую выбирают тела, допускающие значительное увеличение объёма. Это газы и пары жидкостей (для ТЭС – пары воды, для ДВС – газообразные продукты сгорания жидкого топлива).
Теплота
Теплота – это мера микрофизической формы передачи энергии, т.е. осуществляемого на молекулярном уровне обмена энергией между системой и окружающей средой без совершения работы.
Теплота может передаваться при непосредственном контакте между телами – теплопроводностью, конвекцией, или на расстоянии - излучением. Этот процесс возможен только при наличии разницы температур.
Элементарное количество теплоты 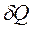 , так же как и
, так же как и 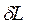 , не является полным дифференциалом в отличие от дифференциала внутренней энергии
, не является полным дифференциалом в отличие от дифференциала внутренней энергии 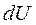 . Эта символика имеет глубокий физический смысл различия понятий внутренней энергии, теплоты и работы.
. Эта символика имеет глубокий физический смысл различия понятий внутренней энергии, теплоты и работы.
Внутренняя энергия – это свойство самой системы, характеризующее состояние системы. Теплота и работа – это энергетические характеристики процессов теплового и механического взаимодействий системы с окружающей средой, характеризующие те количества энергии, которые переданы системе через её границы в определённом процессе.
Основы теории теплообмена
Техническая термодинамика
1.1 Термодинамическая система. Основные понятия и определения
Термодинамика изучает законы превращения энергии в различных физико-химических процессах, происходящих в макроскопических системах и сопровождающихся тепловыми эффектами.
Техническая термодинамика изучает закономерности взаимного превращения тепловой и механической энергии и является (вместе с теорией теплообмена) теоретическим фундаментом теплоэнергетики.
На её основе осуществляют расчет и проектирование всех тепловых двигателей (паровых и газовых турбин; реактивных и ракетных двигателей; двигателей внутреннего сгорания; различного технологического оборудования).
Для наглядности в термодинамике используются молекулярно-кинетические представления о структуре вещества.
Термодинамическая система (ТДС) – совокупность материальных тел, находящихся в механическом и тепловом взаимодействии друг с другом и с окружающими систему внешними телами.
Окружающая среда (ОС) – это тела, не входящие в систему.
Контрольная поверхность (оболочка) – граница термодинамической системы и окружающей среды.
Механическое и тепловое взаимодействия ТДС осуществляются через контрольные поверхности.
При механическом взаимодействии система сама или над ней совершается работа.
Тепловое взаимодействие заключается в переходе теплоты между отдельными телами системы и между системой и окружающей средой.
Открытая система – система, обменивающаяся с ОС энергией и веществом (массообменное взаимодействие). Пример – потоки газа или пара в турбинах или трубопроводах.
Закрытая система – система, обменивающаяся с ОС только энергией без массообмена. Дальше будут рассматриваться закрытые системы.
Теплоизолированная (адиабатная) система – термодинамическая система, которая не обменивается теплом с окружающей средой.
Изолированная (замкнутая) система – система, не обменивающаяся с ОС ни энергией, ни веществом.
Рабочее тело – система в термодинамике, осуществляющая взаимное превращение теплоты и работы. Обычно это газы и пары.
Равновесное состояние системы - такое состояние системы, когда все термодинамические параметры постоянны по времени и одинаковы во всех точках системы.
Неравновесная система – система, между различными точками в которой существуют разности температур, давлений и т.д. В такой системе под действием градиентов параметров возникают потоки теплоты, вещества и т.д., стремящиеся вернуть её в состояние равновесия.
Изолированная система с течением времени всегда приходит в состояние равновесия и никогда самопроизвольно выйти из него не может. В классической термодинамике рассматриваются только равновесные системы.
Термодинамические параметры состояния (давление, температура, удельный объем)
Термодинамические параметры состояния тела (системы) – это свойства, не зависящие от количества вещества в системе и определяющие состояние тела или группы тел (термодинамической системы).
Наиболее распространёнными параметрами состояния являются абсолютная температура, абсолютное давление и удельный объем (или плотность) газа.
Давление обусловлено взаимодействием молекул рабочего тела с поверхностью и численно равно силе, действующей на единицу площади поверхности тела по нормали к последней.
В соответствии с молекулярно-кинетической теорией давление газа определяется соотношением (1.1)
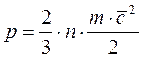 , (1.1)
, (1.1)
где 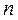 - число молекул в единице объёма;
- число молекул в единице объёма; 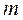 - масса молекулы;
- масса молекулы; 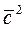 - средняя квадратичная скорость поступательного движения молекул.
- средняя квадратичная скорость поступательного движения молекул.
Единицы измерения давления:
| в технике: 1 ат = 1 кгс/см2 = 9,81·104Па = 735 мм рт.ст. = 10 м вод. ст. |
Давление измеряется манометрами, барометрами и вакуумметрами. Манометры измеряют избыточное давление, представляющее собой разность между полным или абсолютным давлением 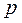 измеряемой среды и атмосферным давлением
измеряемой среды и атмосферным давлением 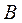 :
:
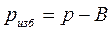 , (1.2)
, (1.2)
Вакуумметры - приборы для измерения давления ниже атмосферного; их показания дают значение разрежения (или вакуума)
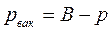 , (1.3)
, (1.3)
т.е. избыток атмосферного давления над абсолютным.
Дата: 2019-02-19, просмотров: 445.