Так как электронное строение элементов изменяется периодически, то соответственно периодически изменяются и свойства элементов, определяемые их электронным строением, такие, как атомный радиус, энергия ионизации, энергия сродства к электрону, электроотрицательность.
Атомный радиус
Атомы и ионы не имеют строго определенных границ вследствие волновой природы электронов. Поэтому введены два условных понятия атомных радиусов:
- эффективный;
- орбитальный.
Эффективный атомный радиус определяется экспериментально (из спектрографических данных) как ½ расстояния между центрами ядер двух соседних атомов в молекуле или кристалле.
Орбитальный атомный радиус – это расстояние от ядра атома до наиболее удаленного максимума электронной плотности.
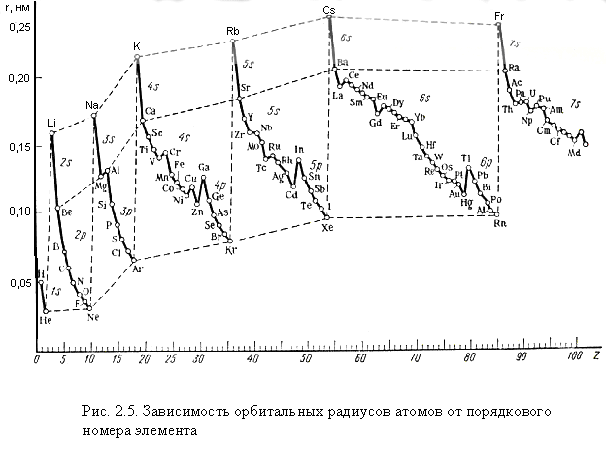
Атомные радиусы элементов периодически изменяются в зависимости от величины заряда ядра (рис. 2.5):
1. В периоде атомные радиусы с ростом порядкового номера уменьшаются (от щелочного металла к инертному газу). Атом Na имеет радиус 1,8 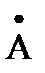 , Mg – 1,6
, Mg – 1,6 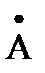 , Сl – 0,73
, Сl – 0,73 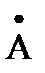 .Объяснить это можно тем, что с увеличением заряда ядра увеличивается сила кулоновского притяжения электронов к ядру, которая превалирует над силами взаимного отталкивания электронов.
.Объяснить это можно тем, что с увеличением заряда ядра увеличивается сила кулоновского притяжения электронов к ядру, которая превалирует над силами взаимного отталкивания электронов.
Наибольшее уменьшение радиусов наблюдается у элементов малых периодов, у которых происходит заполнение электронами внешнего энергетического уровня. В больших периодах у d – и f – элементов наблюдается более плавное уменьшение радиусов при увеличении заряда ядра атома. Это уменьшение называется соответственно d – и f – сжатием.
2. В пределах каждой подгруппы элементов радиусы, как правило, увеличиваются при увеличении номера периода (или Z), так как возрастает число энергетических уровней.
У элементов III группы наблюдается исключение из этого правила – радиус атома галлия Ga (1,22 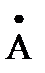 ) меньше радиуса атома алюминия Al (1,26
) меньше радиуса атома алюминия Al (1,26 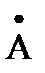 ). Причина состоит в том, что в 4-м периоде между s– и p– элементами расположены десять d–элементов, поэтому свойства галлия не укладываются в ряд B – Al – Ga, зато для триады B – Al – Sс атомные радиусы возрастают в соответствии с общим правилом, хотя B и Alp–элементы, а Scd–элемент. Однако увеличение радиусов, при том же возрастании заряда ядра, в подгруппах s– и p–элементов больше такового в подгруппах d– элементов, например в V группе1:
). Причина состоит в том, что в 4-м периоде между s– и p– элементами расположены десять d–элементов, поэтому свойства галлия не укладываются в ряд B – Al – Ga, зато для триады B – Al – Sс атомные радиусы возрастают в соответствии с общим правилом, хотя B и Alp–элементы, а Scd–элемент. Однако увеличение радиусов, при том же возрастании заряда ядра, в подгруппах s– и p–элементов больше такового в подгруппах d– элементов, например в V группе1:
p-элементы d-элементы
Zr, нм Zr, нм
As……….33 0,148 V…………23 0,134
Sb……….51 0,161 Nb………..41 0,145
Bi………..83 0,182 Ta…………73 0,146
Как следует из представленных данных, в подгруппе мышьяка при переходе от As к Bi атомный радиус увеличивается на 0,034 нм, а в подгруппе ванадия при переходе от V к Ta – всего на 0,012 нм.
Существенно подчеркнуть еще одну особенность для подгрупп d-элементов. Увеличение атомных радиусов в подгруппах d–элементов в основном отвечает переходу от элемента 4-го к элементу 5-го периода. Соответствующие же радиусы d–элементов 5-го и 6-го периодов данной подгруппы примерно одинаковы. Это объясняется тем, что увеличение радиусов за счет возрастания числа электронных слоев при переходе от 5-го к 6-му периоду компенсируется f–сжатием2, вызванным заполнением 4f– подуровня у f–элементов 6-го периода. При аналогичных электронных конфигурациях внешних слоев и примерно одинаковых размерах атомов для d–элементов 5-го и 6-го периодов данной подгруппы характерна особая близость свойств.
Радиусы ионов отличаются от радиусов атомов, т. к. они или лишились нескольких электронов, или присоединили последние. Поэтому радиусы положительно заряженных ионов меньше, а радиусы отрицательно заряженных ионов больше радиусов соответствующих атомов.
Энергия ионизации
Энергия, необходимая для отрыва электрона от невозбужденного атома, называется первой энергией ионизации I1:
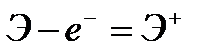 .
.
В результате ионизации атомы превращаются в положительно заряженные ионы. Энергию ионизации выражают либо в кДж/моль, либо в эВ/атом (1эВ = 1,6∙10-19 Дж).
Энергия ионизации характеризует восстановительную способность элемента или его металлические свойства (см. р. 9.2). Первая энергия ионизации (рис. 2.6) определяется электронным строением элементов и ее изменение имеет периодический характер:
| Рис. 2.6. Зависимость первой энергии ионизации атома от порядкового номера элемента |
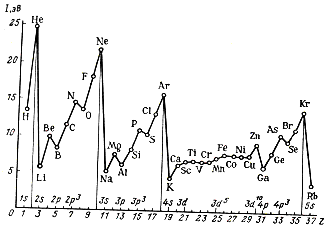
1. В периоде слева направо первая энергия ионизациивозрастает и восстановительные свойства элементов убывают. Наименьшие значения энергии ионизации имеют щелочные элементы, находящиеся в начале периода, наибольшими значениями энергии ионизации характеризуются благородные газы, находящиеся в конце периода, что обусловлено возрастанием заряда ядра и уменьшением размеров атомов.
Наряду с резко выраженными максимумами и минимумами на кривой энергии ионизации наблюдаются слабо выраженные, что можно объяснить с помощью двух взаимосвязанных представлений: об экранировании заряда ядра и о проникновении электронов к ядру.
Эффект экранирования заряда ядра обусловлен наличием в атоме между данным электроном и ядром других электронов, которые экранируют, ослабляют воздействие на этот электрон положительного заряда ядра и тем самым ослабляют связь его с ядром. Понятно, что экранирование возрастает с увеличением внутренних электронных слоев.
Эффект проникновения электронов к ядру обусловлен тем, что, согласно квантовой механике, все электроны (даже внешние) определенное время находятся в области, близкой к ядру. Поэтому можно сказать, что внешние электроны проникают к ядру через слои внутренних электронов.
Концентрация электронной плотности у ядра (степень проникновения электронов) при одном и том же главном квантовом числе наибольшая для s-электрона, меньше – для р–электрона, еще меньше для d–электрона и т. д. Например, при n = 3 степень проникновения убывает в последовательности 3s>3p>3d.
Эффект проникновения увеличивает прочность связи внешних электронов с ядром. Этим, в частности, определяется порядок заполнения в многоэлектронных атомах s-, p-, d-, f-, …орбиталей при данном n.
Можно также сделать вывод, что вследствие более глубокого проникновения s – электроны в большей степени экранируют ядро, чем р- электроны, а последние – сильнее, чем d–электроны, и т. д.
Влияние на прочность связи электронов с ядром оказывает также взаимное отталкивание электронов одного и того же уровня и в особенности одной и той же орбитали.
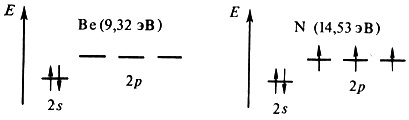
Воспользуемся сказанным для объяснения рис. 2.6. Как видно, внутренние максимумы на кривой первой энергии ионизации соответствуют элементам, у которых внешние уровни завершены – (Be, Mg, Zn) или заполнены наполовину – p3 (N,P,As), что свидетельствует о повышенной устойчивости подобных конфигураций:
Следующий непосредственно затем минимум отвечает появлению электрона в новом, более далеком от ядра р–подуровне (B, Al, Ga), экранированном от ядра конфигурацией s2, либо взаимным отталкиванием двух электронов одной и той же р–орбитали (O, S, Se):
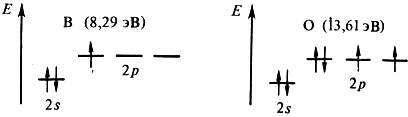
В соответствии с особенностями электронных структур у элементов d(f)–семейства энергии ионизации близки.
2. В главных подгруппах сверху вниз с увеличением порядкового номера первая энергия ионизации уменьшается и восстановительные свойства элементов увеличиваются, что обусловлено увеличением размеров атомов и усиливающимся (по мере увеличения числа электронных слоев) экранированием заряда ядра электронами, предшествующими внешним электронам.
3. В подгруппах d–элементов при переходе от 3d– к 5d–элементу энергии ионизации увеличиваются, что видно, например, на элементах V группы:
| р–элементы | d–элементы | ||||
| Z | I1, эВ | Z | I1, эВ | ||
| As………... | 33 | 9,82 | V……….... | 23 | 6,74 |
| Sb………... | 51 | 8,64 | Nb……….. | 41 | 6,88 |
| Bi………... | 83 | 7,29 | Ta………... | 73 | 7,89 |
Повышение энергии ионизации в подгруппах d-элементов можно объяснить эффектом проникновения электронов к ядру. Так, если у d- элементов 4-го периода 4s–электроны попадают под экран 3d-электронов, то у элементов 6-го периода 6s-электроны попадают уже под двойной экран 5d- и 4f-электронов. Отсюда при переходе от 4-го к 6-му периоду прочность связи внешнихs-электронов с ядрам повышается, а поэтому и энергия ионизации d-элементов возрастает.
Кроме первой энергии ионизации, элементы с многоэлектронными атомами могут характеризоваться второй I2, третьей I3 и более высокой энергией ионизации, поскольку можно удалить 1, 2, 3,… электрона из атома.
В этом случае энергия ионизации увеличивается в следующем порядке:I1<I2<I3<…<In, т. к. удаление электрона от электронейтрального атома происходит легче, чем от иона.
Дата: 2019-02-19, просмотров: 449.