До конца 19 века большинство учёных представляло атом как неразложимую и неделимую частицу элемента – "конечный узел" материи. Считалось также, что атомы неизменны: атом данного элемента ни при каких условиях не может превращаться в атом какого – либо другого элемента.
Конец 19 и начало 20 вв характеризуются новыми открытиями в физике и химии, изменившими взгляд на атом, как на неизменимую частицу, свидетельствовавшими о сложном составе атомов и о возможности их взаимопревращений.
К этим открытиям, прежде всего, относятся: открытие электрона английским физиком Томсоном в 1897 г.; открытие и изучение радиоактивности в конце 90-х годов 19 в. А. Беккерелем, Марией и Пьером Кюри, Э. Резерфордом.
В начале ХХ в. исследования ряда явлений (излучений раскалённых тел, фотоэффект, атомные спектры) привели к выводу, что энергия распространяется и передаётся, поглощается и испускается не непрерывно, а дискретно, отдельными порциями – квантами. Энергия системы микрочастиц также может принимать только определённые значения, которые являются кратными числами квантов.
Предположение о квантовой энергии впервые было высказано М. Планком (1900). Энергия кванта Е пропорциональна частоте излучения ν:
Е=h·ν,
где:h – постоянная Планка (6,626 10-34 Дж×с), ν= с/l, с – скорость света, l – длина волны.
В 1905 г. А. Эйнштейн предсказал, что любое излучение представляет собой поток квантов энергии, называемых фотонами. Из теории Эйнштейна следует, что свет имеет двойственную природу.
В 1911 г. Резерфорд предложил ядерную планетарную модель атома, состоящего из тяжёлого ядра, вокруг которого двигаются по орбитали электроны, подобно планетам солнечной системы. Однако, как показывает теория электромагнитного поля, электроны в этом случае должны двигаться по спирали, непрерывно излучая энергию, и падать на ядро.
Датский учёный Н. Бор, используя модель Резерфорда и теорию Планка, предложил первую квантовую модель (1913г.) строения атома водорода, согласно которой электроны движутся вокруг ядра не по любым, а лишь по разрешённым орбитам, на которых электрон обладает определёнными энергиями. При переходе электрона с одной орбиты на другую атом поглощает или испускает энергию в виде квантов.
Теория Бора позволила рассчитать энергию электронов, значения квантов энергии, испускаемых при переходе электрона с одного уровня на другой. Она не только объяснила физическую природу атомных спектров как результат перехода электронов с одних стационарных орбит на другие, но и впервые позволила рассчитывать спектры. Расчёт спектра простейшего атома – атома водорода, выполненный Бором, дал блестящие результаты: вычисленное положение спектральных линий в видимой части спектра совпало с их действительным местоположением в спектре.
Но теория Бора не смогла объяснить поведение электрона в магнитном поле и все атомные спектральные линии, оказалась непригодной для многоэлектронных атомов.
Возникла необходимость в новой модели атома, основанной на открытиях в микромире.
Исходные представления квантовой механики
1. Гипотеза Луи де Бройля о корпускулярно – волновом дуализме материальных частиц.
В 1924 г. Луи де Бройль (Франция) выдвинул предположение, что электрон, как и другие микрочастицы, характеризуется двойственностью свойств – корпускулярно-волновым дуализмом. Он предложил уравнение, связывающее длину волны(λ)электрона или любой другой частицы с массой (m) и скоростью (v):
λ=h/(mv).
Волны частиц материи де Бройль назвал материальными волнами. Они свойственны всем частицам или телам, но, как следует из уравнения, для макротел длина волны настолько мала, что в настоящее время не может быть обнаружена.
Так, для тела с массой 1000 кг, двигающегося со скоростью 108 км/ч (30 м/с), λ=2,21 10-38 м.
Гипотеза де Бройля была экспериментально подтверждена обнаружением дифракционного и интерференционного эффектов потока электронов. В настоящее время дифракция потоков электронов, нейтронов, протонов широко используется для изучения структуры веществ.
2. Принцип неопределённости В. Гейзенберга (Германия, 1927 г.), согласно которому положение и импульс движения субатомной частицы (микрочастицы) принципиально невозможно определить в любой момент времени с абсолютной точностью. В каждый момент времени можно определить только лишь одно из этих свойств.
3. Уравнение Шредингера.
Э. Шредингер (Австрия1926 г.)вывел математическое описание поведения электрона в атоме. Сущность его заключается в том, что движение электронов в атоме описывается волновым уравнением, а определение местоположения электрона производится по вероятностным принципам. Уравнение Шредингера, являющееся основой современной квантово- механической теории строения атома, в простейшем случае имеет:
– 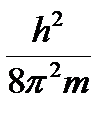 (
( 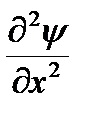 +
+ 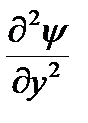 +
+ 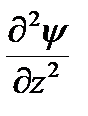 ) + U
) + U 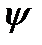 = E
= E 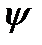 ,
,
где:h – постоянная Планка; m – масса частицы; U – потенциальная энергия; Е – полная энергия; x, y, z – координаты; ψ – волновая функция.
Для характеристики состояния электрона особо важное значениеимеет волновая функция ψ. Определённый физический смысл имеет её квадрат – ψ2. Величина ψ2dv выражает вероятность нахождения электрона в объёме пространства dv, окружающего атомное ядро.
В настоящее время уравнение имеет точное решение только для водорода и водородоподобных частиц Не+, Li2+, т.е. для одноэлектронных частиц. Решение этого уравнения– задача сложная и рассмотрение её выходит за рамки данного курса.
Работы Планка, Эйнштейна, Бора, де Бройля, Гейзенберга, Шредингера заложили основу квантовой механики, изучающей движение и взаимодействие микрочастиц. Она основывается на представлении о квантовой энергии, волновом характере движения микрочастиц и вероятностном (статистическом) методе описания микрообъектов.
Дата: 2019-02-19, просмотров: 434.