Реакции углеводородов при каталитическом крекинге протекают по цепному карбкатионному механизму. Карбкатионы – чрезвычайно реакционноспособные соединения. Константы скорости ионных реакций на несколько порядков выше аналогичных радикальных реакций. Например, скорость каталитического крекинга алканов при температуре 500 ºС в 40-60 раз больше скорости их термического крекинга.
Рассмотрим основные стадии карбкатионного механизма [11, 13]:
А. Образование карбкатионов:
1 направление: часть молекул алканов подвергается вначале термическому крекингу, образующиеся олефины присоединяют протоны, находящиеся на катализаторе, и превращаются в карбкатионы:

2 направление: карбкатион образуется из молекулы алкана при гетеролитическом расщеплении связи С–Н, которое происходит под действием кислотного центра катализатора:
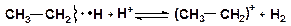
Третичные карбкатионы более устойчивы, чем вторичные и первичные. Положительный заряд на третичном атоме углерода частично компенсирован смещением электронов от трех алкильных групп.
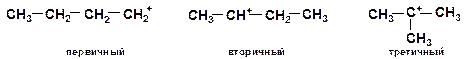
Б. Реакции карбкатионов:
Карбкатионы – нестабильные частицы, стремятся к стабилизации. Карбкатионы могут подвергаться различным превращениям, что приводит к развитию процесса каталитического крекинга. Основными реакциями карбкатионов, как и радикалов, являются распад по
b-правилу, реакции замещения и присоединения. Отличие карбкатионов от радикалов – их способность к изомеризации.
Изомеризация. Первичные карбкатионы стремятся превратиться во вторичные за счет переноса как гидрид-иона, так и метиланиона:

Образующиеся вторичные ионы сохраняют прямую углеводородную цепь. Тепло, выделяющееся при изомеризации, затрачивается на расщепление.

Подобное перемещение происходит быстро от первичного карбония к вторичному и далее к наиболее устойчивому – третичному.
Изомеризация карбкатиона с перемещением метиланиона дает продукты с разветвлением углеводородного скелета.
В процессе каталитического крекинга вследствие изомеризации преобладают вторичные и третичные карбкатионы, при их расщеплении образуются углеводороды С3 и С4, которые и составляют газы каталитического крекинга. В газах термического крекинга преобладают углеводороды С1 и С2.
Расщепление карбкатионов. Расщепление карбкатионов происходит по наиболее слабой b-связи С–С с образованием алкена и нового карбкатиона:



Склонность к распаду снижается при переходе от первичного иона ко вторичному, от вторичного к третичному.
Расщепление карбкатиона может проходить и по b-связи С–Н по отношению к заряженному атому углерода:

Взаимодействие карбкатионов с углеводородами. Сталкиваясь с молекулой алкана, карбкатион отрывает от нее гидрид-ион:
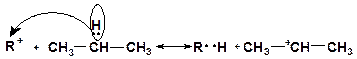
В эту реакцию вступают низшие карбкатионы СН3+, С2Н5+, С3Н7+. Карбкатионы большей молекулярной массы легче расщепляются.
В. Обрыв цепи:
Обрыв цепи происходит при встрече карбкатиона с анионом катализатора.


Превращения циклоалканов
Скорость каталитического крекинга циклоалканов близка к скорости крекинга алканов с равным числом атомов углерода и увеличивается при наличии третичного атома углерода [13].
Стадия инициирования – возникновения карбкатионов – для насыщенных углеводородов циклического и ациклического строения протекает одинаково. За счет высокой температуры возникает небольшое количество алкенов, которые присоединяя протон от катализатора, превращаются в карбкатионы.
Образовавшиеся ионы карбония отрывают гидрид-ион от молекулы циклоалкана. Отщепление гидрид-иона от третичного углеродного атома протекает легче, чем от вторичного, поэтому глубина крекинга возрастает с увеличением числа заместителей в кольце.
Распад циклогексильного иона может происходить двумя путями:
1) С разрывом кольца:

При разрыве С–С-связи образуется алкенильный ион, который легко изомеризуется в ион аллильного типа:

Последний может расщепиться по β-правилу, оторвать гидрид-ион от исходного углеводорода или передать протон молекуле алкена или катализатору.
При крекинге по этому пути из циклогексана образуются алкены и диены.
2) Без разрыва кольца. Циклогексильный ион может передать протон алкену или катализатору и превратиться в циклоалкен:
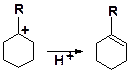
Этот путь энергетически выгоднее, чем распад по С–С-связи (1).
Циклоалкены крекируются быстрее, чем циклоалканы, со значительным выходом аренов. Выход аренов достигает более 25 % от продуктов превращения циклогексанов, а газы крекинга циклоалканов содержат повышенное по сравнению с газами крекинга алканов количество водорода.
Превращения аренов
Незамещенные арены в условиях каталитического крекинга устойчивы. Метилзамещенные арены реагируют со скоростью, близкой к алканам. Алкилпроизводные аренов, содержащие два и более углерода в цепи, крекируются примерно с такой же скоростью, что и алкены. Основной реакцией алкилпроизводных аренов является деалкилирование. Это объясняется большим сродством ароматического кольца к протону, чем к алкильному иону:
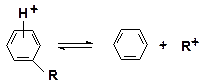
Скорость реакции возрастает с увеличением длины цепи алкильного заместителя.
В случае метилзамещенных аренов отщепление карбкатиона энергетически затруднено, поэтому в основном протекают реакции диспропорционирования (а) и изомеризации по положению заместителей (б):
а)

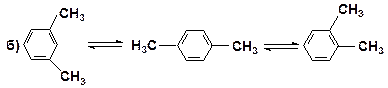
Полициклические арены прочно сорбируются на катализаторе и подвергаются постепенной деструкции и перераспределению водорода с образованием кокса.
3.1.8 Сопоставление качества продуктов каталитического
крекинга перед термическим крекингом
По сравнению с термическим крекингом каталитический крекинг имеет ряд особенностей [2, 11]:
1. Скорость каталитического крекинга алканов в 40-60 раз больше скорости их термического крекинга при одной и той же температуре (500 ºС).
2. Жидкие продукты каталитического крекинга алканов имеют преимущественно изостроение. В отличие от термического крекинга при каталитическом крекинге интенсивно протекает изомеризация.
3. Газообразные продукты каталитического крекинга состоят из углеводородов состава С3 и С4 (пропилен, пропан, изобутилен, изобутан, бутены), в то время как в газообразных продуктах термического крекинга преобладают углеводороды состава С1 и С2 (метан, этан, этилен).
4. Скорость каталитического крекинга чистых алканов резко возрастает в присутствии следов олефинов.
5. Изоалканы крекируются с большей скоростью, чем алканы с прямой цепью.
6. Скорость каталитического крекинга алкенов на 2-3 порядка выше скорости их термического крекинга.
7. Каталитический крекинг нафтенов протекает в ~ 1000 раз быстрее, чем термический крекинг.
8. Голоядерные ароматические углеводороды (бензол, нафталин) в условиях каталитического крекинга практически не подвергаются превращениям; крекинг толуола проходит незначительно. Высшие алкилбензолы крекируются легко, скорость их превращения в процессе каталитического крекинга выше скорости термического крекинга. В отличие от термического крекинга расщепляется не b-связь, а a-связь С–С боковой цепи алкилбензола.
9. В продуктах каталитического крекинга благодаря реакциям
Н-переноса отсутствуют диолефины и значительно меньше содержатся моноолефины.
10. Каталитический крекинг позволяет получать бензины с более высоким октановым числом, высокой химической стабильностью и большим выходом.
Вопросы
1. Каково целевое назначение процесса каталитического крекинга?
2. Каково влияние фракционного состава сырья на процесс каталитического крекинга?
3. Дайте характеристику промышленным катализаторам каталитического крекинга. Отчего происходит дезактивация катализаторов?
4. Какова кристаллическая структура цеолитов?
5. Объясните химизм основных реакций каталитического крекинга. Укажите основные стадии карбкатионного механизма.
6. Укажите по качеству продуктов преимущества каталитического крекинга перед термическим крекингом.
7. Приведите принципиальную технологическую схему установки каталитического крекинга с лифт-реактором.
Каталитический риформинг
Каталитический риформинг – один из самых распространенных и крупнотоннажных процессов нефтепереработки, предназначен для повышения детонационной стойкости прямогонных бензинов и получения индивидуальных ароматических углеводородов: бензола, толуола, ксилолов – сырья для нефтехимии.
Прямогонные бензиновые фракции, содержание которых в нефти составляет примерно 15-20 % мас., имеют низкую детонационную стойкость из-за своего химического состава (октановое число ОЧ = 50÷55). Бензиновые фракции нефтей содержат 60-70 % парафиновых, 10 % ароматических и 20-30 % пяти- и шестичленных нафтеновых углеводородов. Среди парафиновых преобладают углеводороды нормального строения и монометилзамещенные изомеры. Нафтены представлены алкилгомологами циклогексана и циклопентана, а ароматические – алкилбензолами.
Риформат имеет высокую детонационную стойкость (октановое число по моторному методу ОЧММ = 80-90 и октановое число по исследовательскому методу ОЧИМ = 90-100) в результате протекания реакций дегидрирования и дегидроциклизации углеводородов. В процессе каталитического риформинга протекают также реакции изомеризации, деструктивной гидрогенизации и уплотнения.
На рис. 3.6 представлено два варианта риформинга [8]. Первый вариант – производство высокооктанового компонента бензина (КРб), и второй вариант – получение ароматических углеводородов (КРа). Основное отличие этих схем – в риформировании различных бензиновых фракций.
В качестве сырья риформинга используются прямогонные бензиновые фракции, бензины гидрокрекинга и термического крекинга. Сырье риформинга определяется фракционным и химическим составом. Фракционный состав сырья выбирается в зависимости от целевого назначения процесса. Если процесс проводится с целью получения индивидуальных ароматических углеводородов, то для получения бензола, толуола и ксилолов используют соответственно фракции, содержащие углеводороды С6 (62-85 °С), С7 (85-105 °С) и С8 (105-140 °С) [2]. Ароматические углеводороды выделяются из риформата экстракцией. Если риформинг проводится с целью получения высокооктанового бензина, то сырьем служит фракция 85-180 °С, соответствующая углеводородам С7-С10.
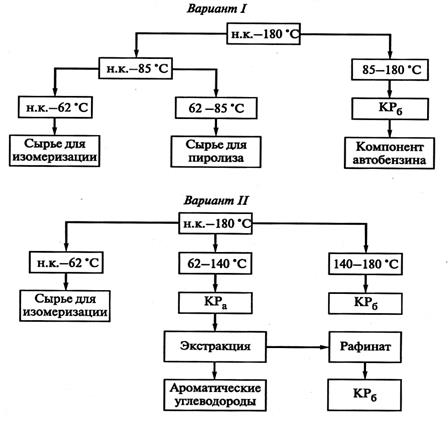
Рис. 3.6. Варианты риформинга с целью производства высокооктанового компонента бензина (I) и ароматических углеводородов (II)
Дата: 2019-02-25, просмотров: 457.