Семинар 1
Молекулярное строение вещества.
1. Определить молярную массу Mr:
1) углекислого газа СО2;
2) поваренной соли NaCl.
2. Определите число молекул в 10 г кислорода?
3. Кислород при нормальных условиях заполняет сосуд вместимостью V=11,2 л. Определить количество вещества v газа и его массу m.
4. Определить число 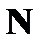 молекул, содержащихся в объеме
молекул, содержащихся в объеме 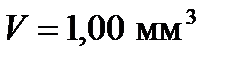 воды, и массу
воды, и массу 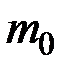 одной молекулы воды. Найти эффективный диаметр
одной молекулы воды. Найти эффективный диаметр 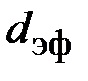 молекулы, считая, что молекулы воды имеют вид шариков, соприкасающихся друг с другом и упакованных слоями толщиной
молекулы, считая, что молекулы воды имеют вид шариков, соприкасающихся друг с другом и упакованных слоями толщиной 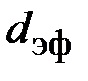 .
.
5. В сосуде вместимостью V=5л находится однородный газ количеством вещества v==0,2 моль. Определить, какой это газ, если его плотность 1,12 кг/м3.
6. Найти молярную массу М смеси кислорода массой m1=25 г и азота массой m2=75 г.
7. В сосуде емкостью 4,00 л находится 1,00 г водорода. Какое число молекул содержится в 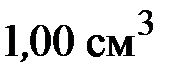 этого газа?
этого газа?
8. В баллоне вместимостью V=6,9 л находится азот массой m=2,3 г. При нагревании часть молекул диссоциировали на атомы. Коэффициент диссоциации a=0,2. Определить: 1) общее число N1 молекул и концентрацию n1 молекул азота до нагревания; 2) концентрацию n2 молекул и n3 атомов азота после нагревания.
Д.З.
1. Определить относительную молекулярную массу Mr: 1) воды; 2) углекислого газа СО2; 3) поваренной соли NaCl.
2. В сосуде вместимостью V=2 л находится кислород, количество вещества v которого равно 0,2 моль. Определить плотность газа.
3. Определить количество вещества v и число N молекул азота массой m=0,2 кг.
4. Плотность алмаза 3500 кг/м3. Какой объем займут 1022 атомов этого вещества?
5. Определить количество вещества v водорода, заполняющего сосуд вместимостью V=3 л, если концентрация молекул газа 2  1018
1018 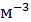 .
.
6. Колба вместимостью V=0,5 л содержит газ при нормальных условиях. Определить число N молекул газа, находящихся в колбе.
7. Сколько атомов содержится в газах массой 1 г каждый:
1) гелии, 2) углероде, 3) фторе, 4) полонии?
Семинар 2.
Д.З.
1. Газ при температуре Т=309 К и давлении p=0,7 МПа имеет плотность r=12 кг/м3. Определить относительную молекулярную массу Mr газа.
2. Определить плотность r насыщенного водяного пара в воздухе при температуре 300 К. Давление р насыщенного водяного пара при этой температуре равно 3,55 кПа.
3. 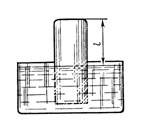 В большой сосуд с водой был опрокинут цилиндрический сосуд (рис.). Уровни воды внутри и вне цилиндрического сосуда находятся на одинаковой высоте. Расстояние l от уровня воды до дна опрокинутого сосуда равно 40 см. На какую высоту Dh поднимется вода в цилиндрическом сосуде при понижении температуры от T1=310К до Т2=273 К? Атмосферное давление нормальное.
В большой сосуд с водой был опрокинут цилиндрический сосуд (рис.). Уровни воды внутри и вне цилиндрического сосуда находятся на одинаковой высоте. Расстояние l от уровня воды до дна опрокинутого сосуда равно 40 см. На какую высоту Dh поднимется вода в цилиндрическом сосуде при понижении температуры от T1=310К до Т2=273 К? Атмосферное давление нормальное.
4. Какой объем V занимает идеальный газ, содержащий количество вещества v=l кмоль при давлении p=1 МПа и температуре T=400 К?
5. Баллон вместимостью V=30 л содержит смесь водорода и гелия при температуре T=300 К и давлении р=828 кПа. Масса m смеси равна 24 г. Определить массу m1 водорода и массу m2 гелия.
6. . В U-образный манометр налита ртуть. Открытое колено манометра соединено с окружающим пространством при нормальном атмосферном давлении р0, и ртуть в открытом колене стоит выше, чем в закрытом, на Dh=10 см. При этом свободная от ртути часть трубки закрытого колена имеет длину l=20 см. Когда открытое колено присоединили к баллону с воздухом, разность уровней ртути увеличилась и достигла значения Dh1=26 см. Найти давление r воздуха в баллоне.
7. При нагревании идеального газа на DТ=1 К при постоянном давлении объем его увеличился на 1/350 первоначального объема. Найти начальную температуру T газа.
8.
| 3 |
| 2 |
| 1 |
| P |
| V |
| 4 |
9. Дан график изменения идеального газа в координатах (P,V). Представить этот процесс в координатах (P,T), (V,T)
Семинар 3.
Д.З.
1. Определить число N молекул ртути, содержащихся в воздухе объемом V=1м3 в помещении, зараженном ртутью, при температуре t=20 °C, если давление р насыщенного пара ртути при этой температуре равно 0,13 Па.
2. В сосуде объемом 125 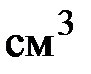 содержится некоторый идеальный газ при температуре 25,0 °С. Насколько понизится давление газа в сосуде, если вследствие утечки из него выйдет
содержится некоторый идеальный газ при температуре 25,0 °С. Насколько понизится давление газа в сосуде, если вследствие утечки из него выйдет 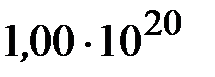 молекул?
молекул?
3. Сколько молекул содержится в одном кубическом сантиметре воздуха при нормальных условиях?
4. В колбе вместимостью V=0,5 л находится кислород при нормальных условиях. Определить среднюю энергию 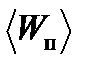 поступательного движения всех молекул, содержащихся в колбе.
поступательного движения всех молекул, содержащихся в колбе.
5. В колбе вместимостью V =240 см3 находится газ при температуре Т=290 К и давлении р=50 кПа. Определить количество вещества v газа и число N его молекул.
6. Определить среднее значение <e> полной кинетической энергии одной молекулы гелия, кислорода и водяного пара при температуре T=400 К.
Семинар 4.
Д.З.
1. Разность удельных теплоемкостей с p — сv некоторого двухатомного газа равна 260 Дж/(кг×К). Найти молярную массу М газа - его удельные теплоемкости сv и с p .
2. В баллоне находятся аргон и азот. Определить удельную теплоемкость сv смеси этих газов, если массовые доли* аргона (w1) и азота (w2) одинаковы и равны w=0,5.
3. Смесь газов состоит из хлора и криптона, взятых при одинаковых условиях и в равных объемах. Определить удельную теплоемкость с p смеси.
4. Смесь газов состоит из аргона и азота, взятых при одинаковых условиях и в одинаковых объемах. Определить показатель адиабаты g такой смеси.
5. Определить степень диссоциации a газообразного хлора, если показатель адиабаты у такого частично диссоциировавшего газа равен 1,55.
6. На нагревание кислорода массой m=160 г на DT=12 К было затрачено количество теплоты Q=1,76 кДж. Как протекал процесс: при постоянном объеме или постоянном давлении?
Семинар 5.
Д.З.
1. Какая часть молекул кислорода при t=0°С обладает скоростями v от 100 до 110 м/с?
2. Найти относительное число молекул ΔN/N гелия, скорости которых отличаются от наиболее вероятной - не более чем на 10 м/с, при температуре газа T=300 К.
3. Вычислить среднюю скорость < vкв > молекул кислорода при температуре Т = 300 К. Найти относительное число молекул, скорости которых отличаются от средней квадратичной скорости не более чем на 1%.
4. Найти выражение средней кинетической энергии <E> поступательного движения молекул. Функцию распределения молекул по энергиям считать известной.
5. По функции распределения молекул по скоростям определить среднюю квадратичную скорость < vкв >.
6. Используя функцию распределения молекул по энергиям, определить наиболее вероятное значение энергии Ев.
7. Вывести формулу наиболее вероятного импульса pв молекул идеального газа.
8. Вывести формулу, определяющую среднее значение компонента импульса <px> молекул идеального газа.
9. Преобразовать функцию f(E)dE распределения молекул по кинетическим энергиям в функцию f(Θ)dΘ распределения молекул по относительным кинетическим энергиям (где 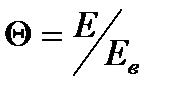 ; Eв - наиболее вероятное значение кинетической энергии молекул).
; Eв - наиболее вероятное значение кинетической энергии молекул).
Семинар 6.
Д.З.
1. Пылинки, взвешенные в воздухе, имеют массу m=10-18 г. Во сколько раз уменьшится их концентрация n при увеличении высоты на ∆h=10 м? Температура воздуха T=300К.
2. На сколько уменьшится атмосферное давление p=100кПа при подъеме наблюдателя над Землей на высоту h=100 м? Считать, что температура T воздуха равна 290 К и не меняется с высотой.
3. На какой высоте h над поверхностью Земли атмосферное давление вдвое меньше, чем на ее поверхности? Считать, что температура T воздуха равна 290 К и не изменяется с высотой.
4. Масса m каждой из пылинок, взвешенных в воздухе, равна 10 -18г. Отношение концентрации n1 пылинок на высоте h1=1 м к концентрации n0 их на высоте h0=0 равно 0,787. Температура воздуха T=300 К. Найти по этим данным значение постоянной Авогадро NA.
5. На какой высоте h давление воздуха составляет 75% от давления на уровне моря? Температуру воздуха считать постоянной и равной t=0°С.
6. На какой высоте h плотность водорода вдвое меньше его плотности на уровне моря? Температуру газа считать постоянной и равной t=0°С.
7. Определить во сколько раз плотность ρ2 воздуха в кабине самолета больше плотности ρ1 воздуха вне ее, если температура наружного воздуха t1=-20°С, а температура воздуха в кабине t2=20°С. Считать также, что давление в салоне самолета p2=78 кПа, а снаружи p1=30 кПа.
8. Найти давление воздуха в горах на высоте h=3380м. Температуру газа считать постоянной и равной t=5°С.
9. Частный самолет президента летает на высоте h=8500 м. Давление в салоне соответствует давлению на высоте h=2600 м. Определить разность давлений в салоне и снаружи самолета. Температуру наружного воздуха считать равной t1=0°С.
Семинар 7.
Часть 1.
№1. Найти среднюю длину свободного пробега <l> молекул водорода при давлении p=0,1 Па и температуре Т=100 К. (эффективный диаметр молекулы водорода 0,28нм).
№2. Баллон вместимостью V=10 л содержит водород массой m=1 г. Определить среднюю длину свободного пробега <l> молекул.
№3. Найти среднее число <z> столкновений, испытываемых в течение t=1 с молекулой кислорода при нормальных условиях. (эффективный диаметр молекулы кислорода 0,36нм).
№4. Диффузия D кислорода при температуре t=0°С равна 0,19 см2/с. Определить среднюю длину свободного пробега <l> молекул кислорода.
№5. Два горизонтальных диска радиусами R=20 см расположены друг над другом так, что оси их совпадают. Расстояние d между плоскостями дисков равно 0,5 см. Верхний диск неподвижен, нижний вращается относительно геометрической оси с частотой n=10с-1. Найти вращающий момент М, действующий на верхний диск. Динамическая вязкость h воздуха, в котором находятся диски, равна 17,2 мкПа×с.
№6. Пространство между двумя большими параллельными пластинами, расстояние d между которыми равно 5 мм, заполнено гелием. Температура T1 одной пластины поддерживается равной 290 К, другой — T2=310 К. Вычислить плотность теплового потока |q|. Расчеты выполнить когда давление р гелия равно 0,1 МПа.
№7. На высоте 20см над горизонтальной трансмиссионной лентой, движущейся со скоростью 70м/с, параллельно ей подвешена пластинка площадью 4см2. Какую силу надо приложить к этой пластинке, чтобы она оставалась неподвижной? ( вязкость воздуха 1,7 105 Па с , температура 270С, давление атмосферное).
№8. Два тонкостенных коаксиальных цилиндра длиной l= 10 см могут свободно вращаться вокруг их общей оси z. Радиус R большого цилиндра равен 5 см. Между цилиндрами имеется зазор размером d =2 мм. Оба цилиндра находятся в воздухе при нормальных условиях. Внутренний цилиндр приводят во вращение с постоянной частотой n1=20 с-1. Внешний цилиндр заторможен. Определить, через какой промежуток времени с момента освобождения внешнего цилиндра он приобретет частоту вращения n2=1c-1. При расчетах изменением относительной скорости цилиндров пренебречь. Масса m внешнего цилиндра равна 100 г.
Часть 2.
Разреженные газы.
№1. В разреженном газе (масса молекулы ma) движется диск радиуса r с постоянной скоростью v, направленной вдоль оси диска. Скорость диска много больше тепловой скорости молекул. Оценить силу сопротивления, действующую на диск, если концентрация газа n.
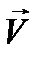
|
№3. Два коаксиальных цилиндра радиуса r1 и r2 находится в разреженном газе. Внутренний цилиндр вращается с постоянной угловой скоростью w1. Оценить угловую скорость внешнего цилиндра.
№4. Оцените подъемную силу пластины площадью 1м2, если нижняя поверхность пластины 373К, а верхняя 273К. Температура воздуха 293К, давление 0,1Па.
№5. Между двумя плоскими параллельными платинами. Расположенными на расстоянии d друг от друга, находится одноатомный газ в разреженном состоянии (<l> >d). Оцените плотность потока тепла, если температура пластин поддерживается равной Т и Т+DТ соответственно, а газ характеризуется массой атома mа и концентрацией n.
Д.З.
1. Найти среднюю длину свободного пробега <l> атомов гелия, если известно, что плотность гелия ρ=0,021кг/м3.
2. Найти среднюю продолжительность 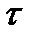 свободного пробега молекул кислорода при температуре Т=250К и давлении р=100Па.
свободного пробега молекул кислорода при температуре Т=250К и давлении р=100Па.
3. Найти среднюю длину свободного побега <l> молекул углекислого газа при температуре t = 100°С и давление p=13,3 Па. Диаметр молекул углекислого газа d=0,32 нм.
4. Идеальный газ совершил изотермический процесс, в результате которого его давление возросло в n раз. Как и во сколько раз изменились длинf свободного побега <l> и число столкновений молекул <z>?
5. Баллон вместимостью V=10 л содержит водород массой m=1 г. Определить среднюю длину свободного пробега <l> молекул.
6. При каком давлении p средняя длина свободного пробега <l> молекул азота равна 1 м, если температура T газа равна 300 К?
7. Найти среднее число <z> столкновений, испытываемых в течении t=1 с молекул кислорода при нормальных условиях.
8. Азот находится при нормальных условиях. Найти: а) число столкновений, испытываемых в среднем каждой молекулой за секунду; б) число всех столкновений, происходящих между молекулами в 1 см3 азота ежесекундно.
9. Найти среднюю длину свободного пробега и среднее расстояние между столкновениями молекул газообразного азота, находящегося: а) при нормальных условиях; б) при температуре t=0°С и давлении p=1,0 нПа.
10. Определить среднюю длину свободного побега <l> молекул водорода при температуре t=150°С и давление p=13,3 Па.
11. Найти теплопроводность λ водорода, вязкость которого η= 8,6мкПа*с.
12. 5*1021 молекул двухатомного газа находится в сосуде объемом V=2л. Теплопроводность газа 15*10-3Вт/м*К. Найти коэффициент диффузии D газа.
Семинар 8.
Д.З.
1. Определить работу А адиабатного расширения водорода массой m=4 г, если температура газа понизилась на ΔT=10 К.
2. Азот массой 2 г, имевший температуру T1=300 К, был адиабатно сжат так, что его объем уменьшился в n=10 раз. Определить конечную температуру T2 газа и работу А сжатия.
3. При изохорном нагревании кислорода объемом V=50 л давление газа изменилось на Δp=0,5 МПа. Найти количество теплоты Q, сообщенное газу.
4. Водяной пар расширяется при постоянном давлении. Определить работу А расширения, если пару передано количество теплоты Q=4 кДж.
5. Водород занимает объем V1=10 м3 при давлении p1=100 кПа. Газ нагрели при постоянном объеме до давления p2=300 кПа. Определить: 1) изменение ΔU внутренней энергии газа; 2) работу А, совершенную газом; 3) количество теплоты Q, сообщенное газу.
6. Водород массой m=10 г нагрели на ΔT=200 К, причем газу было передано количество теплоты Q=40 кДж. Найти изменение ΔU внутренней энергии газа и совершенную им работу А.'
7. При адиабатном расширении кислорода с начальной температурой T1=320 К внутренняя энергия уменьшилась на ΔU=8,4 кДж, а его объем увеличился в n=10 раз. Определить массу т кислорода.
8. Воздух, занимавший объем V1=10 л при давлении p1=100 кПа, был адиабатно сжат до объема V2=1 л. Под каким давлением p2 находится воздух после сжатия?
Семинар 9.
Д.З.
1. В цилиндре под поршнем находится водород массой m=0,02 кг при температуре T1=300K. Водород начал расширяться адиабатно, увеличив свой объем в пять раз, а затем был сжат изотермически, причем объем газа уменьшился в пять раз. Найти температуру Т2, в конце адиабатного расширения и работу А, совершенную газом. Изобразить процесс графически.
2. Идеальный газ, совершающий цикл Карно, 2/3 количества теплоты Q1, полученного от нагревателя, отдает охладителю. Температура Т2 охладителя равна 280 К. Определить температуру T1 нагревателя.
3. Идеальный двухатомный газ, содержащий количество вещества v=l моль, находится под давлением p1=250кПа и занимает объем V1=10 л. Сначала газ изохорно нагревают до температуры T2=400 К. Далее, изотермически расширяя, доводят его до первоначального давления. После этого путем изобарного сжатия возвращают газ в начальное состояние. Определить термический КПД h цикла.
4. Тепловая машина работает по циклу Карно. Температура нагревателя 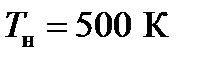 . Определить термический КПД цикла и температуру
. Определить термический КПД цикла и температуру 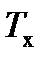 холодильника тепловой машины, если за счет каждого килоджоуля теплоты, полученной от нагревателя, машина совершает работу
холодильника тепловой машины, если за счет каждого килоджоуля теплоты, полученной от нагревателя, машина совершает работу 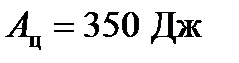 .
.
5. Идеальный газ совершает цикл Карно. Температура T1 нагревателя равна 470 К, температура Т2 охладителя равна 280 К. При изотермическом расширении газ совершает работу A=100 Дж. Определить термический КПД η цикла, а также количество теплоты Q2, которое газ отдает охладителю при изотермическом сжатии.
6. Идеальный двухатомный газ, содержащий количество вещества v=l моль, находится под давлением p1=250кПа и занимает объем V1=10 л. Сначала газ изохорно нагревают до температуры T2=400 К. Далее, изотермически расширяя, доводят его до первоначального давления. После этого путем изобарного сжатия возвращают газ в начальное состояние. Определить термический КПД h цикла.
Семинар 10.
Часть 2. Энтропия.
1. . Некоторый идеальный газ, при температуре 313 К совершает обратимый изотермический процесс, в ходе которого совершает работу, равную 545 Дж. Найти изменение энтропии.
2. Некоторый идеальный газ при температуре 293 К совершает обратимый изотермический процесс, в ходе которого над газом производится работа, равная 845 Дж. Найти изменение энтропии.
3. Во сколько раз надо изотермически увеличить объем 4 моль идеального газа, чтобы его энтропия возросла на 23,0 Дж/К?
4. Найти изменение энтропии при изобарном расширении 20,0 г водорода 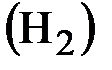 от объема 10,0 л до объема 20,0 л.
от объема 10,0 л до объема 20,0 л.
5. Найти изменение энтропии 7 моль идеального трехатомного газа при изохорном увеличении его абсолютной температуры в 2 раза.
6. Найти изменение DS энтропии при нагревании воды массой m=100 г от температуры t1=0°C до температуры t2=100 °С и последующем превращении воды в пар той же температуры.
7. Лед массой 10,0 кг, имеющий температуру минус 25,0 °C, был последовательно превращен в воду, затем при атмосферном давлении – в сухой насыщенный пар. Найти изменение энтропии в каждом из процессов?
 Д.З.
Д.З.
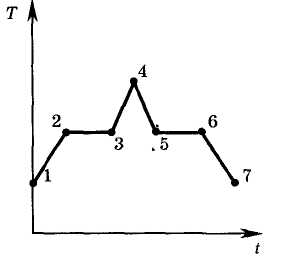
1. На рисунке показан график зависимости температуры Т вещества от времени t. В начальный момент времени вещество находилось в кристаллическом состоянии. Какая из точек соответствует окончанию процесса плавления вещества?
2. 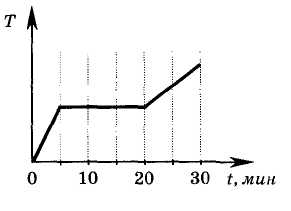 В печь поместили некоторое количество алюминия. Диаграмма изменения температуры алюминия с течением времени показана на рисунке. Печь при постоянном нагреве передает алюминию 1 кДж энергии в минуту. Какое количество теплоты потребовалось для плавления алюминия, уже нагретого до температуры его плавления?
В печь поместили некоторое количество алюминия. Диаграмма изменения температуры алюминия с течением времени показана на рисунке. Печь при постоянном нагреве передает алюминию 1 кДж энергии в минуту. Какое количество теплоты потребовалось для плавления алюминия, уже нагретого до температуры его плавления?
3. Для определения удельной теплоты плавления льда в сосуд с водой массой 300 г и температурой 20°С стали бросать кусочки тающего льда при непрерывном помешивании. К моменту времени, когда лед перестал таять, масса воды увеличилась на 84 г. Определите по данным опыта удельную теплоту плавления льда. Ответ выразите в кДж/кг.
4. Для охлаждения лимонада массой 200 г в него бросают кубики льда при 0°С. Масса каждого кубика 8 г. Первоначальная температура лимонада 30°С. Сколько целых кубиков надо бросить в лимонад, чтобы установилась температура15°С? Тепловыми потерями пренебречь. Удельная теплоемкость лимонада такая же, как у воды.
5. Найти изменение энтропии при переходе 200 г азота 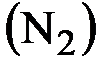 от объема 30,0 л при температуре 300 К к объему 90,0 л при температуре 600 К.
от объема 30,0 л при температуре 300 К к объему 90,0 л при температуре 600 К.
6. Вода массой 24,5 г испаряется при температуре 20,0 °C. Найти изменение энтропии.
7. Лед массой 10,0 кг, имеющий температуру минус 25,0 °C, был последовательно превращен в воду, затем при атмосферном давлении – в сухой насыщенный пар. Найти изменение энтропии в каждом из процессов?
6. Найти изменение энтропии при изотермическом расширении 3 моль идеального газа от давления 100 кПа до давления 25,0 кПа.
Семинар 11.
Поверхностное натяжение.
1. . Какую температуру Т имеет масса m=2г азота, занимающего объём V=820см2 при давлении р=0,2МПа? Газ рассматривать как: а) идеальный; б) реальный.
2. В баллоне вместимостью V=8л находится кислород массой m=0,3кг при температуре Т=300К. Найти, какую часть вместимости сосуда составляет собственный объём молекул газа. Определить отношение внутреннего давления 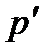 к давлению р газа на стенки сосуда.
к давлению р газа на стенки сосуда.
3. Тонкое алюминиевое кольцо радиусом 8см соприкасается с мыльным раствором. Каким усилием можно оторвать кольцо от раствора? Масса кольца 7г. Температуру раствора считать комнатной.
4. Деревянная палочка длиной 4см плавает на поверхности воды. По одну сторону от палочки осторожно налили мыльный раствор. С каким ускорением начнет двигаться палочка, если ее масса 1г.? Сопротивление воды при движении палочки не учитывать.
5.  Какая масса ртути содержится в единице объема воздуха зараженного ртутью помещения при температуре 200С, если давление насыщенного пара ртути при этой температуре 0,15Па? Молярная масса ртути 200г/моль.
Какая масса ртути содержится в единице объема воздуха зараженного ртутью помещения при температуре 200С, если давление насыщенного пара ртути при этой температуре 0,15Па? Молярная масса ртути 200г/моль.
6. В отростке сосуда, закрытого поршнем, находится некоторая масса воды в равновесии с насыщенным паром. Диаметры сосуда и отростка 5см и 2мм. Поддерживаемая температура 200С, поршень опускается на высоту 10см; уровень воды в отростке при этом повышается на высоту 1мм. Определите давление насыщенного пара воды при 200С.
7. Термос заполнен кипящей водой и герметически закрыт крышкой. Какая сила потребуется (после охлаждения) для того, чтобы вытащить пробку диаметра 3см? Трением пренебречь. Давление пара над остывшей водой мало.
8. Смешали 1м3 воздуха с относительной влажностью 20% и 2м3 воздуха с относительной влажностью 30%. При этом обе порции были взяты при одинаковой температуре. Смесь занимает 3м3. Определить ее относительную влажность.
9. Найти давление p воздуха в воздушном пузырьке диаметром d =0,01 мм, находящемся на глубине h = 20 см под поверхностью воды. Атмосферное давление p0 = 101,7 кПа.
10. Диаметр d канала стеклянной трубки чашечного ртутного барометра равен 5 мм. Какую поправку ∆p нужно вводить в отсчеты по этому барометру, чтобы получить верное значение атмосферного давления?
11. На какую высоту h поднимается вода между двумя параллельными стеклянными пластинами, если расстояние d между ними равно 0,2 мм?
12. В дне сосуда с ртутью имеется отверстие. Каким может быть наибольший диаметр d отверстия, чтобы ртуть из сосуда не выливалась при высоте столба ртути h = 3 см?
Д.З.
1. В закрытом сосуде объемом V=0,5м3 находится количество ν=0,6кмоль углекислого газа при давлении p=3МПа. Пользуясь уравнением Ван-дер-Ваальса, найти, во сколько раз надо увеличить температуру газа, чтобы давление увеличилось вдвое.
2. Вычислите критическую температуру Tкр и давление pкр: 1) кислорода; 2) воды.
3. Какая энергия освобождается при слиянии мелких водяных капель радиусом 0,002мм в одну каплю радиусом 2мм.
4. Разность уровней смачивающей жидкости в коленах U-образной трубки 23мм. Диаметр каналов в коленах трубки 2 и 0,4мм. Плотность жидкости 800кг/м3. Определите поверхностное натяжение жидкости.
5. В цилиндре под поршнем сечением 100см2 находится 18г воды при температуре 00С. Цилиндр нагревается до температуры 2000С. На какую высоту поднимется поршень с лежащим на ней грузом массой 100кг? Атмосферное давление 105Па. Давление насыщенного пара при температуре 2000С – 1,6МПа.
6. .В вертикально расположенном цилиндре под поршнем массы 10кг находится некоторое количество воздуха, воды и водяного пара при температуре 1000С. В положении равновесия поршень отстоит от дна цилиндра на расстояние 20см. Когда цилиндр расположили горизонтально, поршень занял новое положение равновесия, переместившись на расстояние 3см от первоначального положения. Какая масса воды была на дне сосуда? Площадь поршня 400см2.
7. В капиллярной трубке радиусом 0,5 мм жидкость поднялась на 11 мм. Найти плотность данной жидкости, если ее коэффициент поверхностного натяжения 22 мН/м.
8. На какой глубине h под водой находится пузырек воздуха, если известно, что плотность воздуха в нем ρ=2 кг/м3? Диаметр пузырька d=15 мкм, температура t=20°С, атмосферное давление p0=101.3 кПа.
9. Из вертикальной трубки внутренним радиусом r = 1,5 мм вытекает керосин. Найти радиус R капли в момент отрыва. Каплю считать сферической. Диаметр шейки капли в момент отрыва считать равным внутреннему диаметру трубки.
Семинар 12.
Гидродинамика.
Уравнение неразрывности струи
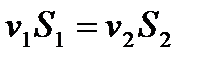 ,где S 1 и S 2 – площади поперечного сечения трубки тока в двух местах; v1 и v2 –соответствующие скорости течений.
,где S 1 и S 2 – площади поперечного сечения трубки тока в двух местах; v1 и v2 –соответствующие скорости течений.
· Уравнение Бернулли для идеальной несжимаемой жидкости в общем случае
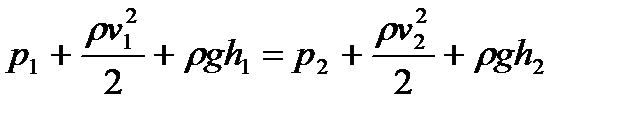 ,
,
где p 1 и р2 – статические давления жидкости в двух сечениях трубки тока; v1 и v2 –скорости жидкости в этих сечениях; 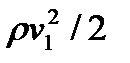 и
и 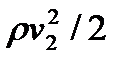 – динамические давления жидкости в этих же сечениях; h 1 и h 2 – высоты их над некоторым уровнем (рис. 12.1); pgh 1 и pgh 2 – гидростатические давления.
– динамические давления жидкости в этих же сечениях; h 1 и h 2 – высоты их над некоторым уровнем (рис. 12.1); pgh 1 и pgh 2 – гидростатические давления.
Уравнение Бернулли в случае, когда оба сечения находятся на одной высоте ( h 1 = h 2 )
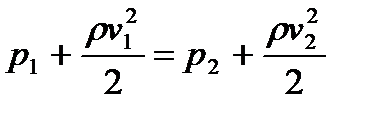 .
.
· Скорость течения жидкости из малого отверстия в открытом широком сосуде
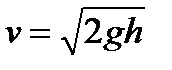 ,
,
где h — глубина, на которой находится отверстие относительно уровня жидкости в сосуде.
· Формула Пуазейля. Объем жидкости (газа), протекающей за время t через длинную трубку,
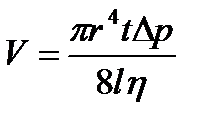
где r — радиус трубки; l – ее длина; Δp – разность давлений на концах трубки; η – динамическая вязкость (коэффициент внутреннего трения) жидкости.
· Число Рейнольдса для потока жидкости в длинных трубках
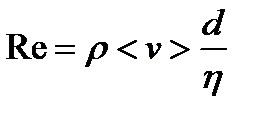 ,
,
где <v> – средняя по сечению скорость течения жидкости; d – диаметр трубки, и для движения шарика d жидкости
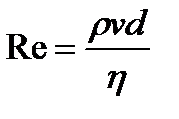 ,
,
где v – скорость шарика; d—его диаметр.
Число Рейнольдса Re есть функция скорости v тела, линейной величины l, определяющей размеры тела, плотности р и динамической вязкости η жидкости, т. е.
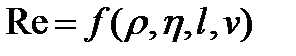 .
.
При малых значениях чисел Рейнольдса, меньших некоторого критического значения Reкp, движение жидкости является ламинарным. При значениях Re>>Reкр движение жидкости переходит в турбулентное.
Критическое число Рейнольдса для движения шарика в жидкости Reкр=0,5; для потока жидкости в длинных трубках Reкр=2300.
· Формула Стокса. Сила сопротивления F , действующая со стороны потока жидкости на медленно движущийся в ней шарик,
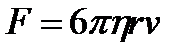 ,
,
где r – радиус шарика; v – его скорость.
Формула справедлива для скоростей, при которых число Рейнольдса много меньше единицы (Re<<l).
Гидродинамика.
1. Деревянный цилиндр плавает на поверхности воды так, что он погружен в воду на 90%. Какая часть цилиндра будет погружена в воду, если поверх воды налить слой масла, полностью закрывающий цилиндр? Плотность масла 800 кг/м3.
2. Два тела плотностью ρ1 и ρ2 в пустоте имеют один и тот же вес. Их подвешивают к концам рычага и помещают в жидкость плотностью ρ. Каково должно быть отношение плеч рычага, чтобы не нарушилось равновесие?
3. Из отверстия в дне высокого сосуда вытекает вода. Сечение сосуда S1, сечение струи S2. Найдите ускорение, с которым перемещается уровень воды в сосуде.
4. 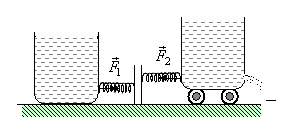 В сосуде с жидкостью сделано отверстие площадью S. Размеры отверстия малы по сравнению с высотой столба жидкости. В одном случае отверстие закрыто пластинкой и измеряется сила давления жидкости на пластинку F1 при высоте столба жидкости h (рис.). В другом случае тот же сосуд стоит на тележке, отверстие открыто, и измеряется сила отдачи F2 при установившемся токе жидкости в момент, когда высота столба жидкости будет та же, что и в первом случае. Будут ли силы F1 и F2 равны?
В сосуде с жидкостью сделано отверстие площадью S. Размеры отверстия малы по сравнению с высотой столба жидкости. В одном случае отверстие закрыто пластинкой и измеряется сила давления жидкости на пластинку F1 при высоте столба жидкости h (рис.). В другом случае тот же сосуд стоит на тележке, отверстие открыто, и измеряется сила отдачи F2 при установившемся токе жидкости в момент, когда высота столба жидкости будет та же, что и в первом случае. Будут ли силы F1 и F2 равны?
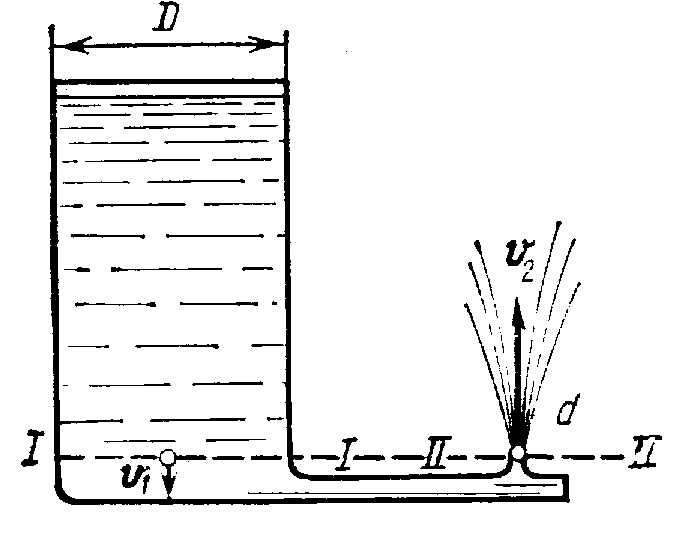
5. Из отверстия II—II в цилиндрическом бака бьет вода со скоростью v2 =12 м/с. Диаметр D бака равен 2 м, диаметр d сечения II—II равен 2 см. Найти: 1) скорость v1 понижения воды в баке; 2) давление p 1 , под которым вода подается в фонтан; 3) высоту h 1 уровня воды в баке и высоту h 2 струи, выходящей из фонтана.
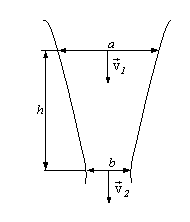
6. Из крана выливается вода. Начиная с некоторого места, диаметр струи уменьшается на протяжении h от а до b (рис. ). Сколько воды вытечет из крана за время t?
7. Площадь поршня в шприце S1 = 2 см2, а площадь отверстия S2 = 1 мм2 (рис. 4). Сколько времени будет вытекать вода из шприца, если действовать на поршень с силой F = 5 H и если ход поршня l = 5 см?
8. В сосуде с глицерином падает свинцовый шарик. Определить максимальное значение диаметра шарика, при котором движение слоев глицерина, вызванное падением шарика, является еще ламинарным. Движение считать установившимся.
Семинар 1
Молекулярное строение вещества.
1. Определить молярную массу Mr:
1) углекислого газа СО2;
2) поваренной соли NaCl.
2. Определите число молекул в 10 г кислорода?
3. Кислород при нормальных условиях заполняет сосуд вместимостью V=11,2 л. Определить количество вещества v газа и его массу m.
4. Определить число 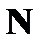 молекул, содержащихся в объеме
молекул, содержащихся в объеме 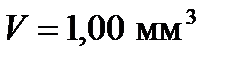 воды, и массу
воды, и массу 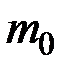 одной молекулы воды. Найти эффективный диаметр
одной молекулы воды. Найти эффективный диаметр 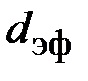 молекулы, считая, что молекулы воды имеют вид шариков, соприкасающихся друг с другом и упакованных слоями толщиной
молекулы, считая, что молекулы воды имеют вид шариков, соприкасающихся друг с другом и упакованных слоями толщиной 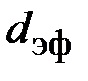 .
.
5. В сосуде вместимостью V=5л находится однородный газ количеством вещества v==0,2 моль. Определить, какой это газ, если его плотность 1,12 кг/м3.
6. Найти молярную массу М смеси кислорода массой m1=25 г и азота массой m2=75 г.
7. В сосуде емкостью 4,00 л находится 1,00 г водорода. Какое число молекул содержится в 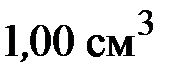 этого газа?
этого газа?
8. В баллоне вместимостью V=6,9 л находится азот массой m=2,3 г. При нагревании часть молекул диссоциировали на атомы. Коэффициент диссоциации a=0,2. Определить: 1) общее число N1 молекул и концентрацию n1 молекул азота до нагревания; 2) концентрацию n2 молекул и n3 атомов азота после нагревания.
Д.З.
1. Определить относительную молекулярную массу Mr: 1) воды; 2) углекислого газа СО2; 3) поваренной соли NaCl.
2. В сосуде вместимостью V=2 л находится кислород, количество вещества v которого равно 0,2 моль. Определить плотность газа.
3. Определить количество вещества v и число N молекул азота массой m=0,2 кг.
4. Плотность алмаза 3500 кг/м3. Какой объем займут 1022 атомов этого вещества?
5. Определить количество вещества v водорода, заполняющего сосуд вместимостью V=3 л, если концентрация молекул газа 2  1018
1018 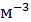 .
.
6. Колба вместимостью V=0,5 л содержит газ при нормальных условиях. Определить число N молекул газа, находящихся в колбе.
7. Сколько атомов содержится в газах массой 1 г каждый:
1) гелии, 2) углероде, 3) фторе, 4) полонии?
Семинар 2.
Дата: 2019-02-25, просмотров: 535.