Филиал УГНТУ в г. Салавате
Кафедра химико-технологических процессов
РАСЧЕТ реакторов технологических процессов получения компонентов автомобильных бензинов
Учебно-методическое пособие для студентов специальности 240403 «Химическая технология природных энергоносителей и углеродных материалов»
Уфа
2011
Учебно-методическое пособие предназначено для студентов специальности 240403 «Химическая технология природных энергоносителей и углеродных материалов» для выполнения практических работ по курсу «Химическая технология топлив и углеродных материалов», а также для расчетов курсовых и выпускных квалификационных работ. Пособие содержит расчеты реакторов установок каталитической изомеризации легких парафиновых углеводородов, сернокислотного алкилирования изобутана бутиленами, производства оксигенетов на примере синтеза метил-трет-бутилового эфира. Представлен краткий теоретический материал по данным процессам, варианты технологического оформления реакторных блоков процессов, даны примеры расчетов реакторов технологических процессов.
Составители: Евдокимова Н.Г. , доц., канд. техн. наук
Грызина Е.В., ассистент
Хасанов Р.Г. , доц., канд. техн. наук
Александрова К.В., доц., канд. техн. наук
Рецензенты: Муртазин Ф.Р., доц., канд. техн. наук
Баширов Р. Ф., начальник отдела
технологического планирования
департамента перспективного развития и
инвестиций ОАО «Салаватнефтеоргсинтез»,
канд. техн. наук
© Уфимский государственный нефтяной технический университет, 2011
ВВЕДЕНИЕ
Необходимость улучшения качества автомобильных бензинов в России связана с ростом потребления высокооктановых бензинов и повышением экологических требований к ним. Вступление России в ВТО определяет необходимость введения соответствующих (европейских) стандартов на качество автомобильных топлив, модернизации НПЗ и использования конкурентоспособных катализаторов и технологий переработки нефтяных фракций.
Согласно принятому Правительством Российской Федерации Техническому регламенту «О требованиях к автомобильному и авиационному бензину, дизельному и судовому топливу, топливу для реактивных двигателей и топочному мазуту» от 27 февраля 2008 года к товарным бензинам ужесточаются требования по содержанию серы, бензолу, ароматическим и олефиновым углеводородам.
В России основными компонентами высокооктановых товарных автобензинов являются бензины каталитического риформинга и каталитического крекинга. Снижение норм по содержанию общей суммы ароматических углеводородов (нормы Евро-3, а также Евро-4 и Евро-5) объясняется как экологическими требованиями (в частности, из-за образования сажи и бензопирена), так и стремлением уменьшить нагарообразование в двигателях автомобилей.
Бензины каталитического крекинга характеризуются высокой массовой долей серы, октановыми числами 90 - 93 по исследовательскому методу. Они содержат 20- 25% масс. непредельных, 35 - 55% масс. парафино-нафтеновых и 25 - 40% масс. ароматических углеводородов. В их составе практически отсутствуют диеновые углеводороды, поэтому они обладают относительно высокой химической стабильностью (ИПО 800 – 900 мин). Бензины риформинга содержат 60 - 70% масс. ароматических углеводородов и имеют утяжеленный фракционный состав, в том числе 2 - 7% масс. бензола, поэтому для получения экологически чистых товарных бензинов необходимо изменение их компонентного состава.
В состав бензинов, выпускаемых в Российской Федерации, входит наибольшее количество бензинов каталитического риформинга – 52,8% масс., доля бензинов каталитического крекинга составляет всего 9,6% масс., доли изомеризата, алкилата и оксигенатов значительно ниже, чем в странах Западной Европы и США, и составляют 1,5, 0,3 и 0,2% масс. соответственно. При компаундировании бензинов в России используется 25,2% масс. прямогонных бензинов и 4,9% масс. бензинов термических процессов. Кроме того, в состав бензинов входит 5,7% масс. бутанов. Однако для разбавления реформатов до содержания бензола 1 % масс. на НПЗ России нет достаточного количества неароматических высокооктановых компонентов. Требования к компонентному составу бензинов дают возможность НПЗ для развития таких процессов, как изомеризация парафиновых углеводородов, алкилирование изобутана олефинами, производство оксигенатов.
Исходные данные
Исходными данными для расчета являются производительность реактора по исходному сырью, состав сырья, а также принимаемые на основе промышленных и лабораторных данных: температура реакции, мольное отношение изопарафин:олефин, объемное отношение катализатор: углеводороды в реакционной системе, число секций в реакторе и снижение концентрации катализатора в каждой секции.
Задачей расчета реактора является определение выходов алкилата и тепловых нагрузок каждой секции, давления в системе, размеров реактора и мешалки, мощности электродвигателя. В таблице 1.1 представлены варианты исходных данных для расчета реактора алкилирования.
Таблица 1.1 – Варианты заданий для расчета реактора алкилирования
| Вариант | Производительность, тыс.т/год | Число рабочих дней | Соотношение изобутан:олефины | Объемное соотношение кислоты и углеводородов |
| 1 | 300 | 340 | 6:1 | 1,1:1 |
| 2 | 270 | 330 | 8:1 | 1,5:1 |
| 3 | 60 | 335 | 7:1 | 2:1 |
| 4 | 100 | 350 | 9:1 | 1,8:1 |
| 5 | 150 | 340 | 8:1 | 1,7:1 |
| 6 | 80 | 330 | 7:1 | 1,2:1 |
| 7 | 110 | 335 | 9:1 | 1,3:1 |
| 8 | 120 | 342 | 6:1 | 1,6:1 |
| 9 | 250 | 345 | 10:1 | 1,9:1 |
| 10 | 180 | 340 | 8:1 | 1,8:1 |
| 11 | 200 | 350 | 7:1 | 1:1 |
| 12 | 150 | 330 | 9:1 | 1,1:1 |
| 13 | 220 | 335 | 6:1 | 1,5:1 |
| 14 | 240 | 340 | 10:1 | 2:1 |
| 15 | 300 | 350 | 8:1 | 1,8:1 |
| 16 | 280 | 335 | 6:1 | 1,6:1 |
| 17 | 100 | 338 | 10:1 | 1,1:1 |
| 18 | 150 | 340 | 9:1 | 1,3:1 |
| 19 | 250 | 350 | 7:1 | 1,8:1 |
| 20 | 200 | 345 | 6:1 | 1:1 |
| 21 | 140 | 337 | 8:1 | 1,5:1 |
| 22 | 300 | 335 | 6:1 | 1,4:1 |
| 23 | 150 | 350 | 9:1 | 2:1 |
| 24 | 270 | 340 | 10:1 | 1,5:1 |
| 25 | 120 | 345 | 8:1 | 1,9:1 |
| 26 | 250 | 350 | 9:1 | 1,6:1 |
| 27 | 200 | 330 | 6:1 | 1,5:1 |
| 28 | 300 | 335 | 7:1 | 1,2:1 |
| 29 | 150 | 345 | 10:1 | 1,3:1 |
| 30 | 220 | 350 | 9:1 | 1,7:1 |
Принимаем производительность реактора П = 300000 т/г = 36764,7 кг/ч сырья, состав которого приводится в таблице 1.2.
Таблица 1.2 – Состав сырья
| Показатели | Компоненты | Сумма | |||||
| С3Н6 | С3Н8 | С4Н8 | i-С4Н10 | н-С4Н10 | С5Н12 | ||
| Молекулярная масса Количество: кг/ч масс. доля | 42 220,59 0,6 | 44 588,24 1,6 | 56 10294,12 28 | 58 13529,41 36,8 | 58 11691,17 31,8 | 72 441,18 1,2 | - 36764,7 100 |
Для подавления реакций полимеризации олефинов создают в реакторе избыток (мольный) изобутана, составляющий 6-10:1 на олефины [2]. Чрезмерное повышение этого соотношения увеличивает капитальные и эксплуатационные затраты, поэтому поддерживать его выше 10:1 нерентабельно.
Примем отношение изобутан:олефин равным 9:1. Тогда количество изобутана, которое необходимо подать в реактор
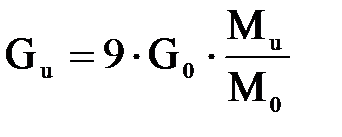 , (1.1)
, (1.1)
где Go — количество олефина (бутилена) в исходном сырье, кг/ч; Ми, Мо — молекулярная масса соответственно изобутана и олефина.
Получим
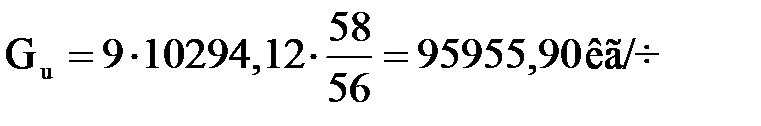 .
.
Состав сырья, подаваемого в реактор, с учетом избыточного изобутана приведен в таблице 1.3.
Таблица 1.3 – Состав сырья с учетом избыточного изобутана
| Показатели | Компоненты | Сумма | |||||
| С3Н6 | С3Н8 | С4Н8 | i-С4Н10 | н-С4Н10 | С5Н12 | ||
| Количество: кг/ч масс. доля | 220,59 0,185 | 588,24 0,494 | 10294,12 8,637 | 95955,90 80,51 | 11691,17 9,81 | 441,18 0,37 | 119191,2 100 |
Оптимальное объемное соотношение кислоты и углеводородов в реакционной зоне составляет от 1:1 до 2:1. Произведение соотношения кислота:углеводороды на время пребывания углеводородов в реакторе определяет истинную продолжительность реакции [4].
На основе промышленных данных [5] примем для первой секции реактора отношение объемов подаваемых в нее кислоты и углеводородов α= 1,2. Как будет показано в расчете, это отношение от секции к секции будет увеличиваться.
В процессе алкилирования применяется 97%-ная серная кислота, которая отрабатывается до 90%-ной концентрации, считая на моногидрат — H2SО4. В таблице 1.4 приведено принятое в расчете снижение концентрации кислоты по секциям реактора.
Таблица 1.4 – Снижение концентрации кислоты по секциям реактора
| Секции | Снижение концентрации кислоты, % H2SО4 | Средняя концентрация, % H2SО4 |
| 1 2 3 4 5 | 97 – 96 = 1 96 – 94,5 = 1,5 94,5 – 93 = 1,5 93 – 91,5 = 1,5 91,5 – 90 = 1,5 | 96,5 95,25 93,75 92,25 90,75 |
Алкилирование осуществляется при низкой температуре. Пределы температуры сернокислотного алкилирования от 273 до 283 К [6]. Примем температуру реакции Т = 278 К. Будем считать, что углеводороды и кислота загружаются в реактор также при температуре Т = 278 К.
В дальнейшем при расчете всех секций реактора будем полагать, что:
- пропилен, пропан, н-бутан и пентан, находящиеся в сырье, в реакцию не вступают, поэтому их количества в процессе остаются неизменными;
- вся масса олефинов вступает в реакцию алкилиропания, образуя соответствующее количество алкилата.
Расчет первой секции
Материальный баланс. Согласно схеме работы реактора (рисунок 1.1), во все пять секций исходное сырье поступает параллельными и равными потоками. Поэтому в первую секцию подается всего изобутана:
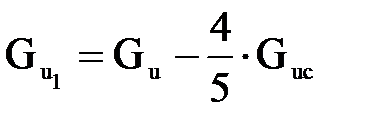 , (1.2)
, (1.2)
где Gис=13529,41 кг/ч - масса изобутана в исходном сырье (таблица 1.2);
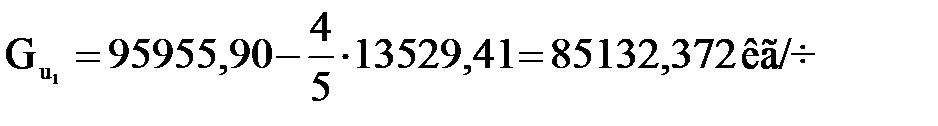 .
.
Количество поступающего в первую секцию циркулирующего изобутана
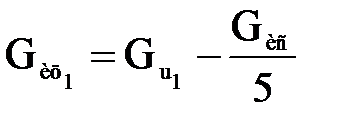 , (1.3)
, (1.3)
или
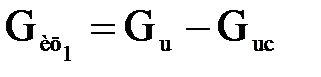 ;
;  (1.4)
(1.4)
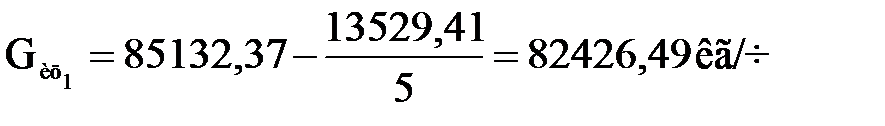 ;
;
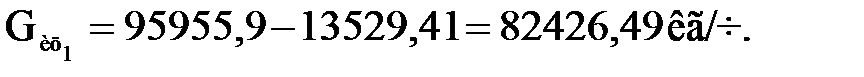
Состав загрузки первой секции реактора представлен в таблице 1.5.
Таблица 1.5 – Состав загрузки первой секции
| Компонент загрузки | Плотность при 278 К, кг/м3 | Мi | Количество | ||
| кг/ч | м3/ч | кмоль/ч | |||
| С3Н6 С3Н8 С4Н8 i-С4Н10(свежий) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Сумма Катализатор Всего | 627,3 597,9 642 575,3 575,3 595 641 - 1820 - | 42 44 56 58 58 58 72 - - - | 44,118 117,648 2058,82 2705,88 82426,29 2338,23 88,236 89779,22 339656,04 429435,26 | 0,0703 0,1968 3,2069 4,7034 143,2753 3,9298 0,1377 155,5202 186,6242 342,1444 | 1,05 2,67 36,76 46,65 1421,14 40,31 1,23 1550 - - |
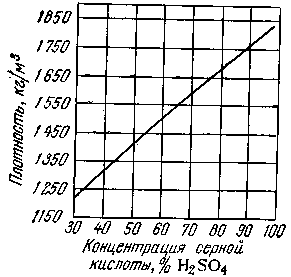
Так как плотность серной кислоты зависит от концентрации, то в дальнейшем при определении ее объема следует пользоваться графиком (рисунок 1.2) [7] и таблицей 1.3.
|
|
Рисунок 1.2 – График для определения плотности кислоты
Определим состав углеводородной массы, выходящей из первой секции. Согласно уравнению основной реакции алкилирования
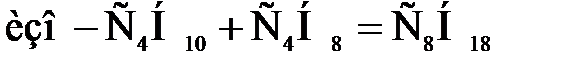 ,
,
в нее вступает 36,76 кмоль/ч олефина и такое же число кмоль/ч свежего изобутана (таблица 1.5), поэтому выход алкилата составит
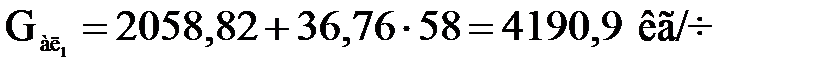 .
.
При этом количество свежего изобутана, не вошедшего в реакцию (отработанного)
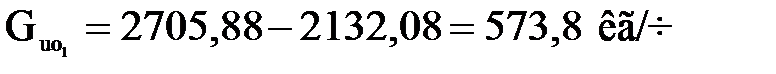
или
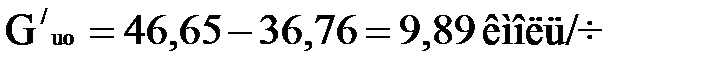 .
.
В таблице 1.6 приведен состав углеводородов, покидающих первую секцию.
Таблица 1.6 – Состав углеводородов, покидающих первую секцию
| Компоненты | Мi | Количество | Состав, мол. % | ||
| кг/ч | м3/ч | кмоль/ч | |||
| С3Н6 С3Н8 i-С4Н10(отработанный) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Алкилат | 42 44 58 58 58 72 114 | 44,118 117,648 573,8 82426,29 2338,23 88,236 4190,9 | 0,0703 0,1968 0,9974 143,2753 3,9298 0,1377 5,8614 | 1,05 2,67 9,89 1421,14 40,31 1,23 36,76 | 0,07 0,18 0,65 93,93 2,66 0,08 2,43 |
| Сумма | - | 89779,22 | 154,4687 | 1513,05 | 100 |
Тепловая нагрузка первой секции. Все внешние и внутренние материальные потоки реактора, по ранее принятому условию, имеют температуру Т = 278 К, поэтому тепловую нагрузку секции, без ущерба для точности расчета, принимаем равной теплу, которое выделяется в процессе алкилирования. Тепло основной реакции алкилирования по литературным данным [3] составляет 75—85% тепловой нагрузки секции. Приняв, что тепло основной реакции алкилирования составляет 80% тепловой нагрузки секции q1, получим
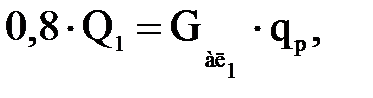 (1.5)
(1.5)
или
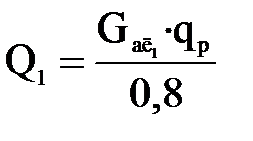 , (1.6)
, (1.6)
где Gал1 = 4190,9 кг/ч — количество алкилата, получаемого в первой секции (таблица 1.6);
qp = 1050 кДж/кг алкилата — теплота основной реакции алкилирования [3];
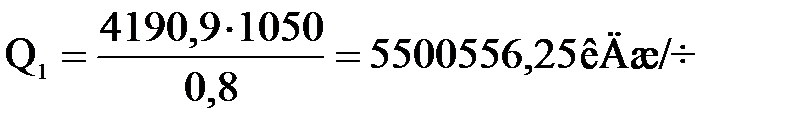 .
.
Давление в первой секции. Давление при температуре реакции Т = 278 К рассчитаем по уравнению изотермы жидкой фазы [9]:
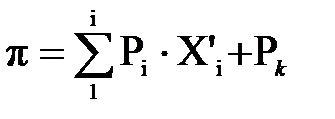 , (1.7)
, (1.7)
где Pi — давление насыщенных паров чистых углеводородов при Т = 278 К, определяется по диаграмме Кокса или таблицам [8]; х/i—мольные доли углеводородных компонентов (таблица 1.6); Рк — давление насыщенного пара серной кислоты (при Т = 278 К принимается равным нулю, так как температура ее кипения при нормальном давлении значительно выше 573 К).
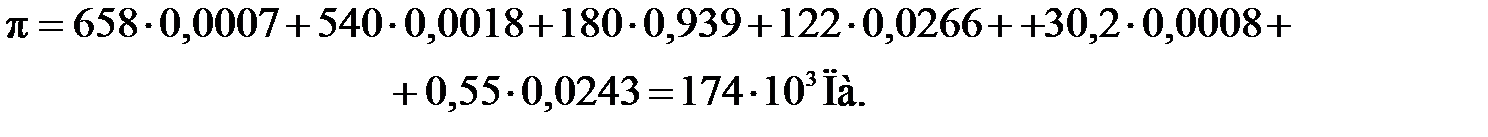
Во всех остальных секциях принимается такое же давление.
Количество углеводородов, испаряющихся в первой секции. Пары, уходящие из секции, находятся в равновесии с испаряющейся жидкостью. Их состав может быть определен по каждому компоненту из уравнения равновесия фаз, в котором все величины правой части известны [3]:
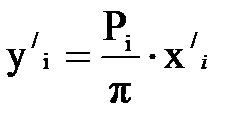 ; (1.8)
; (1.8)
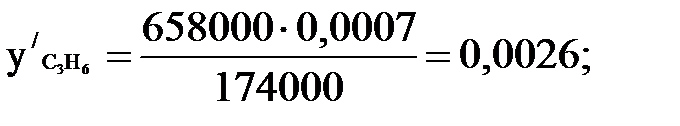
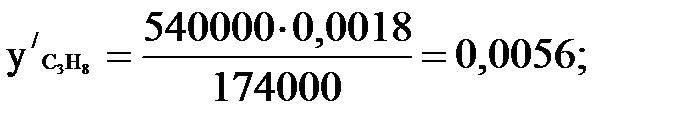
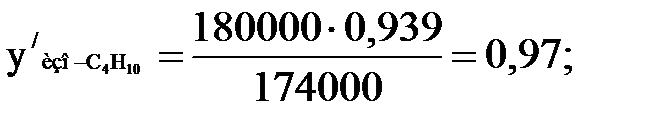
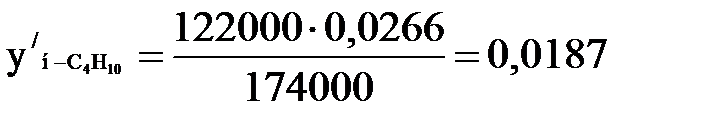 ;
;
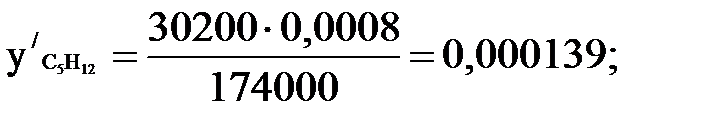
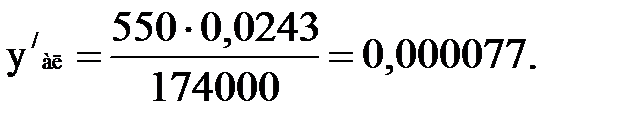
Проводим проверку:
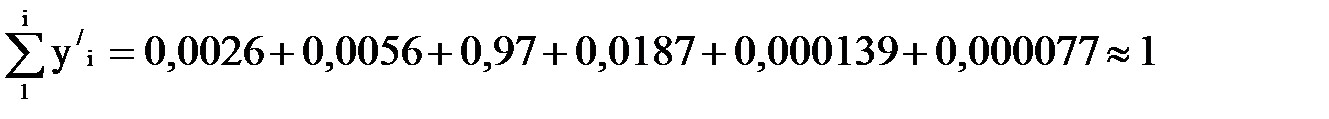
По найденным концентрациям компонентов в парах и теплотам испарения чистых компонентов при Т = 278 К [9] находим по правилу аддитивности теплоту испарения r/m смеси паров. Весь расчет сведен в таблицу 1.7.
Таблица 1.7 – Расчет теплоты испарения
| Компоненты | y/i, мольные доли | r /i, кДж/моль | r /I · y/i, кДж/кмоль |
| С3Н6 С3Н8 i-С4Н10 н-С4Н10 С5Н12 Алкилат (С8Н18) | 0,0026 0,0056 0,97 0,0187 0,000139 0,000077 | 15600 16200 20400 22000 27400 42300 | 40,5 90,7 19788 391,6 3,8 3,3 |
| Сумма | ≈1 | - | r/m=20318 |
Зная теплоту испарения смеси r/m и тепловую нагрузку секции Q1, определим количество паров углеводородов, образующихся в первой секции:
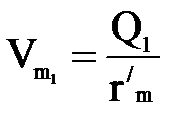 ; (1.9)
; (1.9)
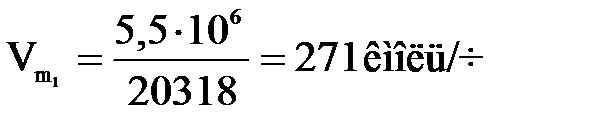 .
.
Количества каждого компонента в парах найдем по формуле
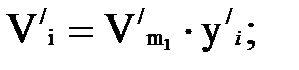 (1.10)
(1.10)
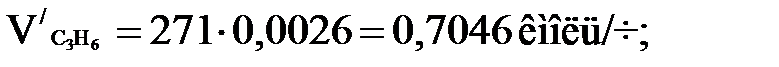
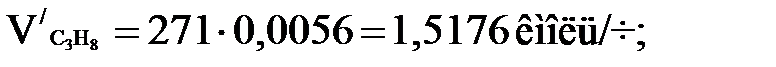
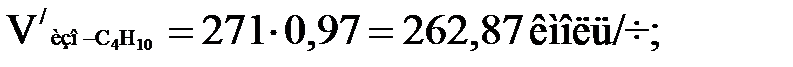
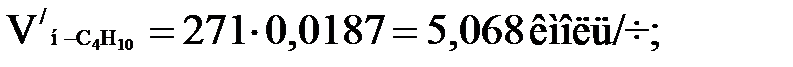
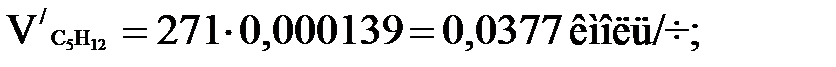
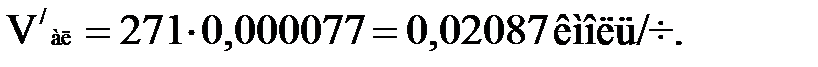
Проводим проверку:
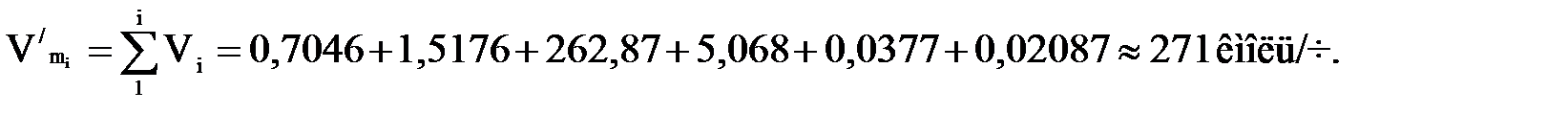
Анализируя сделанные расчеты, нетрудно сделать вывод, что практически весь теплосъем в первой секции осуществляется за счет испарения изобутана. Поэтому без большой ошибки количество испаряющегося изобутана можно определить из приближенного уравнения теплового баланса испарения
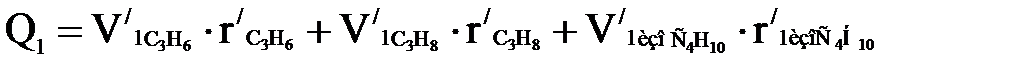 , (1.11)
, (1.11)
в котором количества паров пропилена и пропана считают равными количествам этих углеводородов в сырье. Таким образом
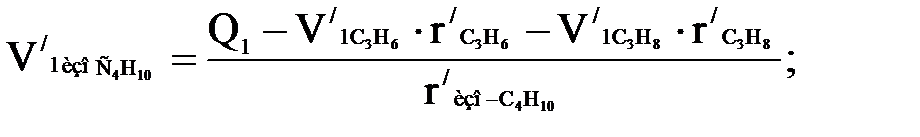 (1.12)
(1.12)

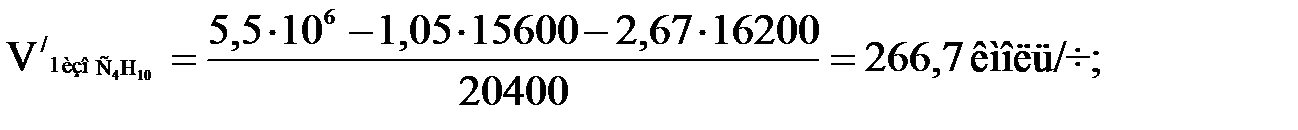
или
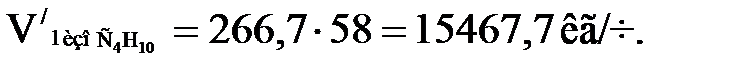
Этот результат очень близок к полученному выше.
Объем кислоты и углеводородов в первой секции. Из практики эксплуатации установок алкилирования известно [7], что объемная скорость находится в пределах 0,1—0,6 ч -1. Примем объемную скорость w = 0,5 ч -1. Тогда объем кислоты в секции:
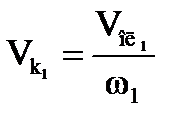 , (1.13)
, (1.13)
где Voл1-—3,2 м3/ч — количество олефина, подаваемого в секцию (таблица 1.5).
Получим
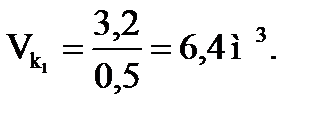
Зная, что отношение объема кислоты к объему углеводородов в первой секции α 1 = 1,2, найдем объем углеводородов в секции:
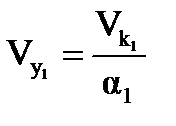 ; (1.14)
; (1.14)
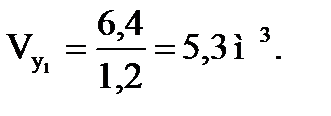
Суммарный объем кислоты и углеводородов в секции:
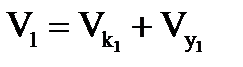 ; (1.15)
; (1.15)
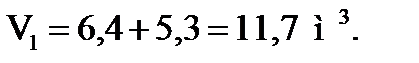
Найдем продолжительность пребывания смеси углеводородов и кислоты (время контакта) в первой секции:
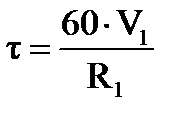 , (1.16)
, (1.16)
где R1 = 342,14 м3/ч — объем смеси, поступающей в первую секцию (таблица 1.4).
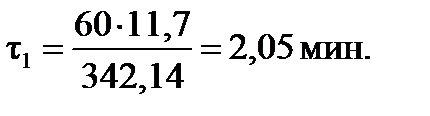
Размеры первой секции. В реакционных аппаратах емкостного типа, если жидкая смесь реагирующих веществ не вспенивается, степень заполнения равна φ = 0,7 - 0,85 [8]. Примем φ = 0,7. Тогда полный объем первой секции:
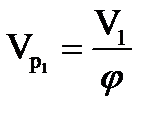 ; (1.17)
; (1.17)
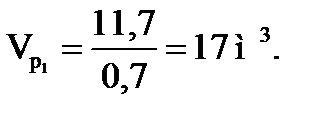
Принимая длину секции L = 2 м , найдем диаметр аппарата
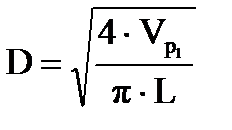 ; (1.18)
; (1.18)
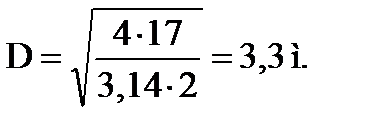
Принимаем D = 3,4 м.
Как указано выше, все пять реакционных секций аппарата будут иметь одинаковые размеры: D = 3,4 м, L = 2 м.
Расчет второй секции
Материальный баланс. При определении загрузки второй и всех остальных секций в целях некоторого упрощения расчета будем полагать, что вся пропан-пропиленовая фракция в любой секции испаряется полностью, а н-бутан, пентан и алкилат не испаряются. В соответствии со схемой работы реактора, количество сырья, подаваемого во вторую секцию, будет включать:
- пятую часть исходного (олефинового) сырья (таблица 1.1);
- не вошедший в реакцию (отработанный) изобутан свежего сырья первой секции (таблица 1.6);
- рециркулирующий изобутан с учетом его частичного испарения в первой секции ;
- н-бутан и пентан из первой секции (таблица 1.6);
- алкилат, полученный в первой секции (таблица 1.6);
- серную кислоту из первой секции (таблица 1.5).
Количество рециркулирующего изобутана, поступающего во вторую секцию (таблица 1.6):
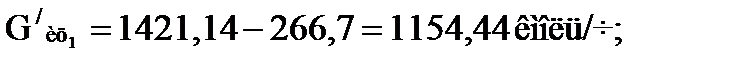

В таблице 1.8 приведены массовые и объемные количества компонентов загрузки второй секции с учетом изменения плотности серной кислоты и ее концентрации (таблица 1.3, рисунок 1.2).
Таблица 1.8 – Массовые и объемные количества компонентов загрузки второй секции
| Компонент загрузки | Количество | |
| кг/ч | м3/ч | |
| С3Н6+С3Н8 С4Н8 i-С4Н10(свежий) i-С4Н10(отраб.) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Алкилат Катализатор | 161,766 2058,82 2705,88 573,8 66957,52 2338,23+2338,23 88,236+88,236 4190,9 339656,044 | 0,2672 3,2069 4,7034 0,9974 116,3871 7,86 0,2753 5,8614 187,605 |
| Сумма | 421157,662 | 327,1637 |
Из таблицы 1.8 следует, что отношение объемов катализатора и углеводородов во второй секции равно
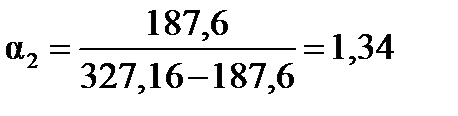 .
.
По сравнению с первой секцией это отношение повысилось за счет некоторого сокращения объема углеводородов и снижения плотности кислоты.
Количество алкилата, образующегося во второй секции, будет таким же, как в первой:
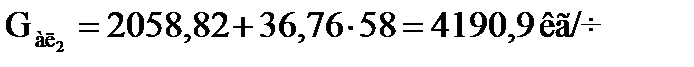 .
.
Количество свежего изобутана, не вошедшего в реакцию (отработанного), равно
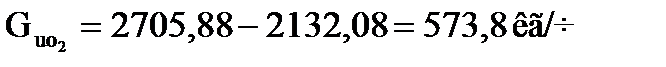 .
.
В таблице 1.9 приведен состав углеводородов, покидающих вторую секцию.
Таблица 1.9 – Состав углеводородов, покидающих вторую секцию
| Компоненты | Количество | ||
| кг/ч | м3/ч | кмоль/ч | |
| С3Н6+С3Н8 i-С4Н10(отработанный) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Алкилат | 161,766 573,8+573,8 66957,52 2338,23+2338,23 88,236+88,236 4190,9+4190,9 | 0,2672 1,9948 116,3871 7,8596 0,2753 11,7218 | 3,73 19,79 1154,44 80,63 2,45 73,59 |
| Сумма | 81501,618 | 138,5058 | 1334,63 |
Тепловая нагрузка второй секции. Вычисляется так же, как и для первой секции:
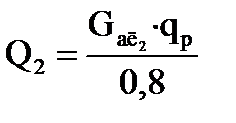 , (1.19)
, (1.19)
где Q ал .2= 4190,9 кг/ч — количество алкилата, полученного во второй секции (таблица 1.8).
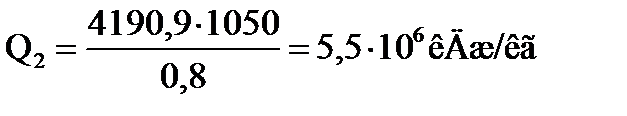 .
.
Количество углеводородов, испаряющихся во второй секции. При допущении, которое сделано при тепловом расчете первой секции, найдем количество изобутана, испаренного во второй секции:
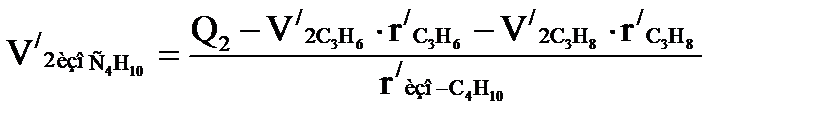 ; (1.20)
; (1.20)
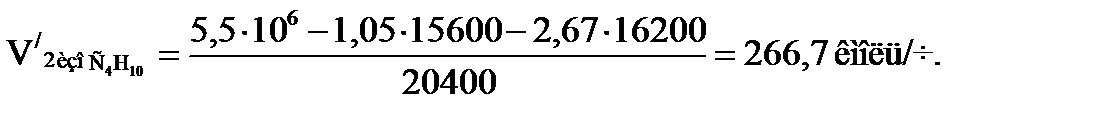
или
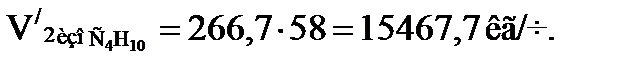
Время пребывания смеси углеводородов и кислоты во второй секции. Полный объем второй секции такой же, как и первой: VP 2 = VP 1 = 17 м3. При степени заполнения φ = 0,7 объем смеси углеводородов и кислоты будет равен
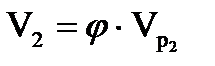 ; (1.21)
; (1.21)
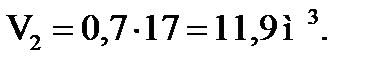
Время пребывания смеси (продолжительность контакта) во второй секции:
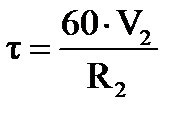 , (1.22)
, (1.22)
где R2 = 327,16 м3/ч — объем смеси, поступающей во вторую секцию (таблица 1.7);
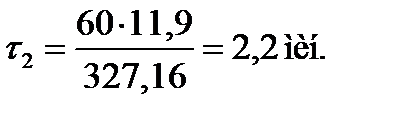
Объемная скорость подачи олефинов. Объем кислоты во второй секции:
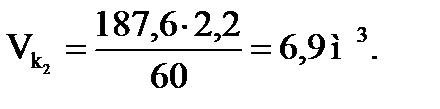
Объем углеводородов:
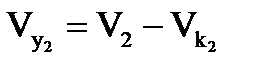 ; (1.23)
; (1.23)
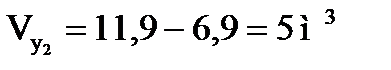 .
.
Объемная скорость подачи олефинов:
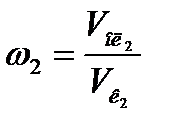 ; (1.24)
; (1.24)
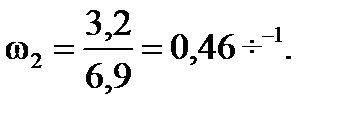
Расчет третьей секции
Все определения ведутся по аналогии с расчетом второй секции. Массовые и объемные количества компонентов загрузки даны в таблице 1.10.
Таблица 1.10 – Массовые и объемные количества компонентов загрузки третьей секции
| Компонент загрузки | Количество | |
| кг/ч | м3/ч | |
| С3Н6+С3Н8 С4Н8 i-С4Н10(свежий) i-С4Н10(отраб.) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Алкилат Катализатор | 161,766 2058,82 2705,88 573,8+573,8 51488,9 2338,23·3=7014,69 88,236·3=264,708 4190,9·2=8381,8 339656,044 | 0,2672 3,2069 4,7034 1,9948 89,5 11,79 0,413 11,7218 191,28 |
| Сумма | 412880,208 | 314,88 |
Отношение объемов катализатора и углеводородов в третьей секции равно
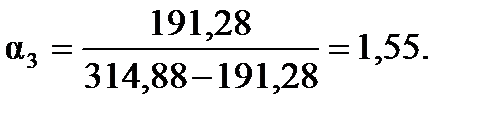
Количество алкилата, образующегося в третьей секции:
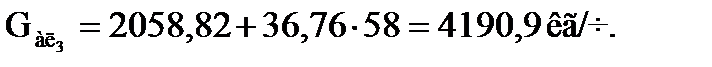
Количество свежего изобутана, не вошедшего в реакцию (отработанного), равно
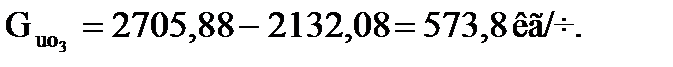
Тепловая нагрузка секции:
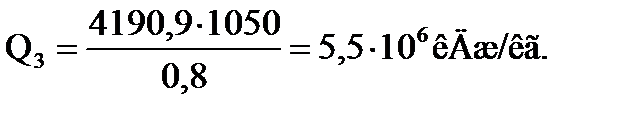
Количество углеводородов, испаряющихся в третьей секции:
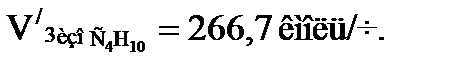
или
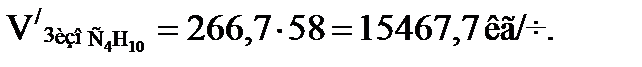
Время пребывания смеси углеводородов и кислоты:
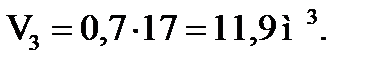
Время пребывания смеси (продолжительность контакта):
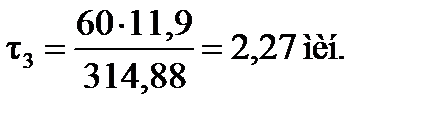
Объемная скорость подачи олефинов:
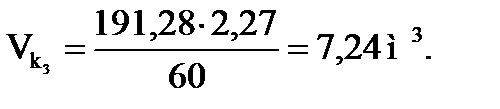
Объем углеводородов:
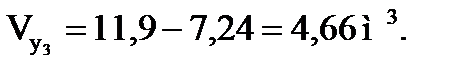
Объемная скорость подачи олефинов:
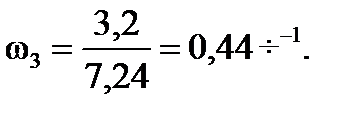
Расчет четвертой секции
Массовые и объемные количества компонентов загрузки даны в таблице 1.11.
Таблица 1.11 – Массовые и объемные количества компонентов загрузки четвертой секции
| Компонент загрузки | Количество | |
| кг/ч | м3/ч | |
| С3Н6+С3Н8 С4Н8 i-С4Н10(свежий) i-С4Н10(отраб.) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Алкилат Катализатор | 161,766 2058,82 2705,88 573,8·3=1721,4 36021,2 2338,23·4=9352,92 88,236·4=352,944 4190,9·3=12572,7 339656,044 | 0,2672 3,21 4,7034 2,9922 62,613 15,719 0,5506 17,583 192,5098 |
| Сумма | 404603,674 | 300,1482 |
Отношение объемов катализатора и углеводородов в четвертой секции равно
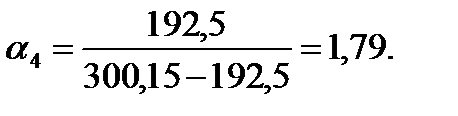
Количество алкилата, образующегося в четвертой секции:
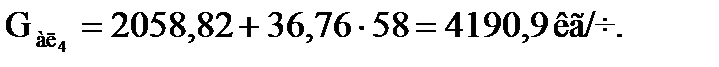
Количество свежего изобутана, не вошедшего в реакцию (отработанного), равно
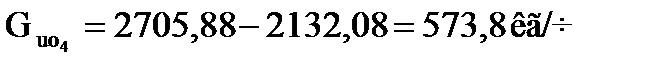 .
.
Тепловая нагрузка секции:
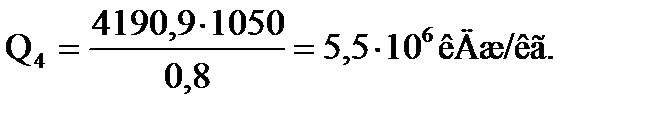
Количество углеводородов, испаряющихся в четвертой секции:
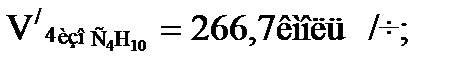
или
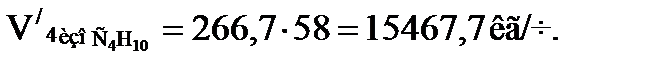
Время пребывания смеси углеводородов и кислоты:
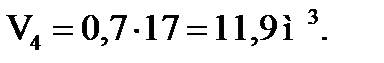
Время пребывания смеси (продолжительность контакта):
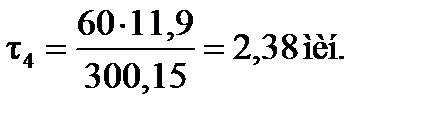
Объемная скорость подачи олефинов:
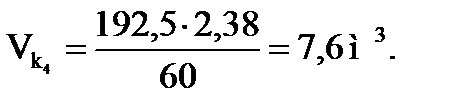
Объем углеводородов:
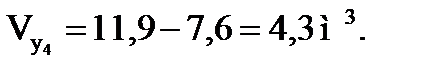
Объемная скорость подачи олефинов:
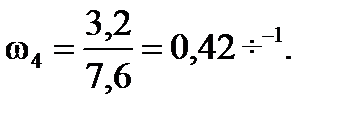
Расчет пятой секции
Массовые и объемные количества компонентов загрузки даны в таблице 1.12.
Отношение объемов катализатора и углеводородов в пятой секции равно
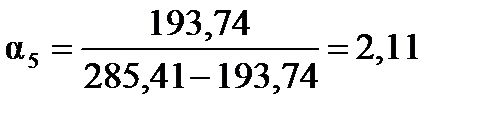 .
.
Количество алкилата, образующегося в пятой секции:
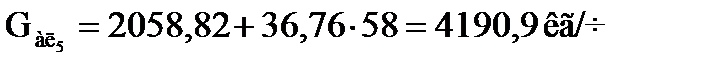 .
.
Таблица 1.12 – Массовые и объемные количества компонентов загрузки пятой секции
| Компонент загрузки | Количество | |
| кг/ч | м3/ч | |
| С3Н6+С3Н8 С4Н8 i-С4Н10(свежий) i-С4Н10(отработанный) i-С4Н10(рециркулят) н-С4Н10 С5Н12 Алкилат Катализатор | 161,766 2058,82 2705,88 573,8·4=2295,2 20553,5 2338,23·5=11691,15 88,236·5=441,18 4190,9·4=16763,6 339656,044 | 0,2672 3,21 4,7034 3,9896 35,7266 19,6489 0,6883 23,44 193,736 |
| Сумма | 396327,14 | 285,41 |
Количество свежего изобутана, не вошедшего в реакцию (отработанного), равно
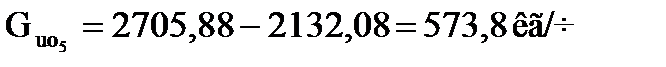
Тепловая нагрузка секции
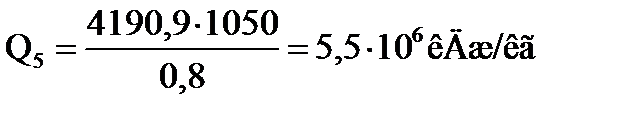
Количество углеводородов, испаряющихся в пятой секции
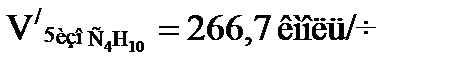
или
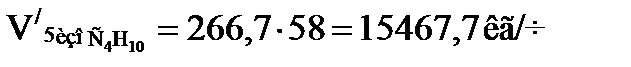
Время пребывания смеси углеводородов и кислоты
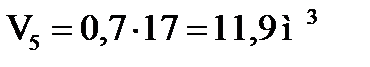
Время пребывания смеси (продолжительность контакта)
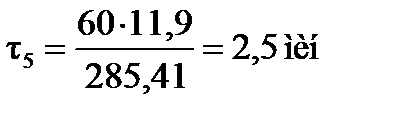
Объемная скорость подачи олефинов
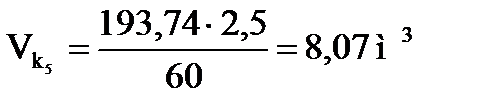
Объем углеводородов
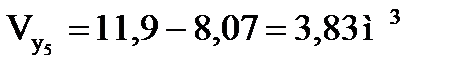
Объемная скорость подачи олефинов
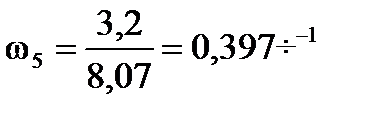
Объем реактора
Найдем общую длину цилиндрической части реактора
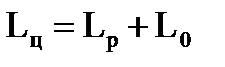 , (1.27)
, (1.27)
где 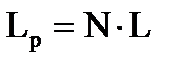 - длина реакционной зоны.
- длина реакционной зоны.
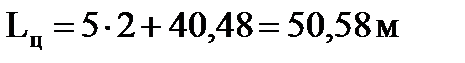
Объем цилиндрической части реактора (практически равный его объему) будет равен
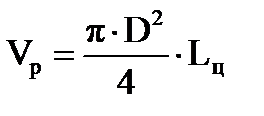 ; (1.28)
; (1.28)
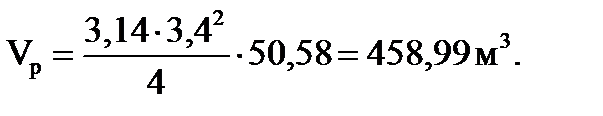
Исходные данные
В таблице 2.1 представлены варианты исходных данных для расчета реактора изомеризации.
Таблица 2.1 – Варианты заданий для расчета реактора изомеризации
| Вариант | Производитель-ность установки, тыс.т/год | Время работы установки, дни | Массовый расход ВСГ, % масс. на сырье | Температура процесса, оС | Давление, МПа |
| 1 | 100 | 330 | 0,1 | 450 | 3,0 |
| 2 | 70 | 350 | 0,2 | 350 | 3,5 |
| 3 | 80 | 340 | 0,15 | 400 | 4,0 |
| 4 | 120 | 300 | 0,3 | 430 | 4,5 |
| 5 | 150 | 320 | 0,25 | 360 | 5,0 |
| 6 | 140 | 340 | 0,1 | 370 | 3,8 |
| 7 | 80 | 330 | 0,2 | 430 | 4,3 |
| 8 | 110 | 350 | 0,15 | 420 | 5,2 |
| 9 | 200 | 360 | 0,3 | 480 | 3,9 |
| 10 | 160 | 320 | 0,25 | 380 | 4,6 |
| 11 | 180 | 330 | 0,1 | 400 | 4,8 |
| 12 | 200 | 350 | 0,2 | 350 | 5,0 |
| 13 | 220 | 340 | 0,15 | 450 | 4,0 |
| 14 | 150 | 300 | 0,3 | 350 | 3,7 |
| 15 | 100 | 320 | 0,25 | 400 | 3,0 |
| 16 | 210 | 340 | 0,1 | 430 | 3,5 |
| 17 | 150 | 330 | 0,2 | 360 | 4,0 |
| 18 | 180 | 350 | 0,15 | 370 | 4,5 |
| 19 | 250 | 360 | 0,3 | 430 | 5,0 |
| 20 | 240 | 320 | 0,25 | 420 | 3,8 |
| 21 | 140 | 330 | 0,1 | 480 | 4,3 |
| 22 | 150 | 350 | 0,2 | 380 | 5,2 |
| 23 | 230 | 340 | 0,15 | 400 | 3,9 |
| 24 | 160 | 300 | 0,3 | 350 | 4,6 |
| 25 | 70 | 320 | 0,25 | 450 | 4,8 |
| 26 | 80 | 340 | 0,1 | 350 | 5,0 |
| 27 | 90 | 330 | 0,2 | 400 | 4,0 |
| 28 | 110 | 350 | 0,15 | 430 | 3,7 |
| 29 | 100 | 360 | 0,3 | 360 | 5,2 |
| 30 | 200 | 320 | 0,25 | 370 | 5,3 |
По данным об имеющимся сырье принимаем производительность установки 100 тыс. тонн в год. Сырьём является фракция нк-62оС каталитического риформинга (таблица 2.2). Число рабочих дней установки принимаем 300 дней в году.
Таблица 2.2 – Состав сырья блока изомеризации
| Сырьё | % масс. | кг/ч | т/сут | тыс. т/г |
| пропан | 0,904 | 125,556 | 3,013 | 0,904 |
| i-бутан | 6,024 | 836,667 | 20,08 | 6,024 |
| н-бутан | 14,971 | 2079,306 | 49,903 | 14,971 |
| i-пентан | 37,425 | 5197,917 | 124,75 | 37,425 |
| н-пентан | 25,265 | 3509,028 | 84,217 | 25,265 |
| 2,2-ДМБ | 1,497 | 207,917 | 4,99 | 1,497 |
| ц-пентан | 4,104 | 570 | 13,68 | 4,104 |
| i-гексаны | 5,083 | 705,972 | 16,943 | 5,083 |
| н-гексан | 1,762 | 244,722 | 5,873 | 1,762 |
| ц-гексан | 0,091 | 12,639 | 0,303 | 0,091 |
| бензол | 1,491 | 207,08333 | 4,97 | 1,491 |
| толуол | 0,992 | 137,778 | 3,3067 | 0,992 |
| С7+ | 0,391 | 54,306 | 1,3033 | 0,391 |
| Всего | 100 | 13888,889 | 333,333 | 100 |
2.2 Расчёт реактора изомеризации
По данным с существующих установок с использованием катализатора СИ-2 принимаем степень конверсии н-парафинов:
- н-пентана – 98,4%,
- н-гексана – 98,7%.
Также принимаем выход побочных продуктов в % масс. на продукт:
- углеводороды ниже С5 – 2,2%,
- углеводороды выше С6 – 1,3%,
- потери 0,004%.
Тепловой баланс реактора
Основная задача расчета теплового баланса заключается в нахождении температуры сырья на входе в реактор. Так как процесс изомеризации происходит с выделением тепла от 6 до 8 кДж/моль, то для поддержания температуры реакции необходимо найти количество тепла, выделавшегося в процессе реакций изомеризации.
Примем конечную температуру продуктов изомеризации 130оС, теплоту реакции изомеризации 7 кДж/моль.
Принимая, что в процессе изомеризации подвергаются только пентаны и гексаны, с учетом количества молей углеводородов (таблица 2.3) общее количество тепла, выделяющееся при изомеризации пентанов и гексанов составит
Qреак=(Gm(C5)·k(C5)+Gm(C6)·k(C6))·qэф, (2.3)
где Gm – количество углеводорода, поступающего с сырьём, моль/ч; qэф – тепловой эффект реакции (7 кДж/моль).
Qреак= 48736,5·0,984·7/1000+811,544·0,987·7/1000=335,697+ 5,607= =341,304 МДж/ч.
По известным конечной температуре процесса и составу продукта, рассчитаем теплосодержание продукта на выходе из реактора. Теплосодержание жидкой фазы углеводородов определим по уравнению
qпр=(1,689·t2+0,0017·(t22))·((0,9943·r204+0,00915)0,5)-1, (2.4)
где t2 – конечная температура процесса (130 оС); r204 – средняя плотность компонентов сырья.
Плотность смеси рассчитаем исходя из массовых долей компонентов (таблица 2.4)
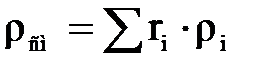 , (2.5)
, (2.5)
где ri – мольная доля i- компонента.
Тогда
qпр=305,709 кДж/кг.
Теплосодержание ВСГ при температуре t2 определим по формуле
qВСГ=10,976·t2 + 492,68, (2.6)
qВСГ=1919,63 кДж/кг.
Общее теплосодержание смеси на выходе из реактора
Qпр= qВСГ·GВСГ+ qпр·Gпр, (2.7)
где GВСГ – расход ВСГ на выходе из реактора, кг/ч; Gпр – расход смеси углеводородов без ВСГ и потерь на выходе из реактора, кг/ч.
Qпр= 1919,63·7,492+(3885,134-0,15-7,492)· 305,709=1199,767 МДж/ч.
Зная тепловой эффект реакции, а также энтальпию продуктов на выходе из реактора можно определить теплосодержание сырьевой смеси (Q0c) поступающей в реактор по формуле
Q0c= Qпр - Qреак, (2.8)
Q0c=1199,767 - 341,304=858,463 МДж/ч.
Методом подбора температуры на входе сырья в реактор и рассчитывая значение энтальпии смеси, необходимо добиться, чтобы значение рассчитанной энтальпии было равно ранее полученному, исходя из теплового баланса (Q0c).
Пусть температура сырья на входе в реактор составит t0=93,7оС. Рассчитаем, зная компонентный состав сырья (таблица 2.3), его теплосодержание при t0 по формуле (2.4). Среднюю плотность углеводородов сырья рассчитаем исходя из их массовых долей (таблица 2.4).
Теплосодержание углеводородной смеси на входе в реактор составит
qсыр=(1,689·93,7+0,0017·(93,72))·((0,9943·0,6235+0,00915)0,5)-1=218,342 кДж/кг.
Таблица 2.5 – Расчёт плотности углеводородов в сырье
| Состав | Массовые доли | кг/ч | Плотность относительная |
| i-пентан | 0,016 | 62,03806 | 0,659 |
| н-пентан | 0,905 | 3509,028 | 0,62 |
| i-гексан | 0,061 | 236,5201 | 0,656 |
| н-гексан | 0,018 | 69,79282 | 0,659 |
| Сырье |
| 3877,379 | 0,6235 |
Теплосодержание ВСГ находим по (2.6)
qВСГ=10,976·93,7 + 492,68=1521,183 кДж/кг.
Общее теплосодержание углеводородов с ВСГ с учётом массового расхода рассчитаем по (2.7)
Q¢ºс=218,342·3877,379+1521,183·7,755= 858,389 МДж/ч.
Для определения правильности выбранной температуры определим расхождение теплосодержания сырья реактора, рассчитанного по тепловому балансу (Qºс), и теплосодержания сырья, рассчитанного по принятой температуре t0 на входе в реактор (Q¢ºс).
DQ=100% · (Qºс - Q¢ºс )/Qºс (2.9)
DQ=(858,463-858,389)·100/858,463»0,01%.
Таким образом, температура t0 принята с достаточной точностью и может использоваться для дальнейших расчётов.
Исходные данные
Принятые исходные данные для расчета реактора представлены в таблице 3.1, состав сырья (бутен-изобутиленовой фракции) - в таблице 3.2, варианты заданий для расчета реактора синтеза МТБЭ - в таблице 3.3.
Таблица 3.1 – Исходные данные для расчета реактора
| Параметр | Единица измерения | Значение |
| Температура процесса, t | °С | 70 |
| Давление процесса, Р | МПа | 0,75 |
| Количество дней работы установки | - | 330 |
| Производительность по МТБЭ, GМТБЭ | т/год | 50000 |
| Производительность по МТБЭ, GМТБЭ | кг/ч | 6313,1 |
| Конверсия изобутилена, ХИБ | доля масс. | 0,95 |
| Доля изобутилена на образование изооктилена, ХИБИО | доля масс. | 0,005 |
| Доля изобутилена на образование третбутанола, ХИБТБ | доля масс. | 0,005 |
| Соотношение метанол : изобутилен (мольное), К | - | 4 |
| Селективность процесса по изобутилену (на МТБЭ), S | - | 0,99 |
Таблица 3.2 – Состав БИФ (бутен-изобутеновой фракции)
| Компонент | % масс. |
| ∑C3 | 0,5 |
| Изобутан | 2 |
| Н-бутан | 12 |
| Бутен-1 + бутен-2 | 37 |
| Изобутилен | 48,4 |
| ∑C5 | 0,1 |
| Итого | 100 |
Тепловой баланс реактора
Суть теплового баланса реактора заключается в определении количества несбалансированного тепла, образующегося в ходе процесса и в расчете количества водяного конденсата, необходимого для снятия избытка тепла процесса синтеза МТБЭ. Количество вносимого в реактор или уносимого из реактора тепла определится по формуле

где Gi – расход i-го компонента, кг/с; Сpi – теплоемкость i-го компонента, кДж/(кг∙град); ti – температура, °С.
Для углеводородных компонентов сырья и продуктов реакции теплоемкость определим по формуле
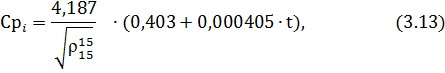
где 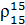 – относительная плотность нефтепродукта.
– относительная плотность нефтепродукта.
Значение 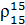 определим по формуле
определим по формуле
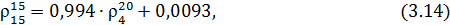
где 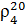 - относительная плотность нефтепродукта при 20 °С. Является справочной величиной.
- относительная плотность нефтепродукта при 20 °С. Является справочной величиной.
Значения плотностей углеводородных компонентов сырья представлены в таблице 3.5.
Таблица 3.5 – Плотности углеводородных компонентов сырья
| Компонент | Плотность, ρ420 | Плотность, ρ1515 |
| ∑C3 | 0,5100 | 0,5162 |
| Изобутан | 0,5573 | 0,5633 |
| Н-бутан | 0,5789 | 0,5847 |
| Бутен-1 + бутен-2 | 0,5945 | 0,6002 |
| Изобутилен | 0,595 | 0,6007 |
| ∑C5 | 0,6262 | 0,6317 |
| Диизобутилен | 0,7149 | 0,7199 |
Значения теплоемкости метанола, третбутанола и МТБЭ являются справочной величиной.
Потери тепла в реакторе принимаются равными 1 % от входящего тепла.
Реакция синтеза МТБЭ протекает с выделением тепла. Тепловой эффект реакции определяется по формуле

где НПРОД и НС – теплоты образования продуктов реакции и исходного сырья соответственно, кДж/моль.
Ввиду малой доли побочных реакций в ходе процесса их влиянием на тепловой эффект пренебрегаем. Теплоты образования метанола, изобутилена и МТБЭ приведены в таблице 3.6.
Таблица 3.6 – Теплоты образования компонентов
| Компонент | МТБЭ | Метанол | Изобутилен |
| Теплота образования, кДж/моль | -291 | -201 | -16,92 |
Таким образом, согласно реакции, по которой протекает процесс, тепловой эффект реакции составит
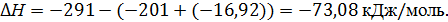
Мольное количество образовавшегося МТБЭ составит
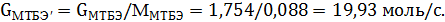
Таким образом, количество тепла, выделившееся в ходе синтеза МТБЭ составит
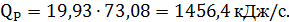
Тепловой баланс реактора представлен в таблице 3.7.
Из таблицы 3.7 видно, что разность входящего и уходящего тепла равняется
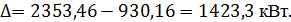
Количество воды, необходимой для снятия избытка тепла процесса, вычисляется по формуле:

где Срв – теплоемкость воды, принимается равной 4,187 кДж/(кг∙К); tН и tК – начальная и конечная температура соответственно охлаждающей воды, °С; принимаем соответственно 20 и 40 °С.
Подставляя значения, получим
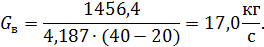
Таблица 3.7– Тепловой баланс реактора
| Компонент | Расход, кг/с | Температура, °С | Теплоемкость, кДж/(кг∙град) | Количество тепла, кДж/с |
| Приход |
|
|
|
|
| ∑C3 | 0,012 | 70,00 | 2,514 | 2,16 |
| Изобутан | 0,049 | 70,00 | 2,406 | 8,26 |
| Н-бутан | 0,294 | 70,00 | 2,362 | 48,64 |
| Бутен-1 + бутен-2 | 0,907 | 70,00 | 2,331 | 148,02 |
| Изобутилен | 1,187 | 70,00 | 2,330 | 193,54 |
| ∑C5 | 0,002 | 70,00 | 2,272 | 0,39 |
| Свежий метанол | 0,638 | 70,00 | 2,610 | 116,51 |
| Циркулирующий метанол | 2,074 | 70,00 | 2,610 | 379,00 |
| Вода | 0,002 | 70,00 | 4,187 | 0,53 |
| Тепло реакции | - | - | - | 1456,41 |
| Итого | 5,166 | 2353,46 | ||
| Расход | ||||
| МТБЭ | 1,754 | 70,00 | 2,511 | 308,20 |
| Непрореагировавший метанол | 2,074 | 70,00 | 2,610 | 379,00 |
| Непрореагировавший изобутилен | 0,059 | 70,00 | 2,330 | 9,68 |
| ∑C3 | 0,012 | 70,00 | 2,514 | 2,16 |
| Изобутан | 0,049 | 70,00 | 2,406 | 8,26 |
| Н-бутан | 0,294 | 70,00 | 2,362 | 48,64 |
| Бутен-1 + бутен-2 | 0,907 | 70,00 | 2,331 | 148,02 |
| ∑C5 | 0,002 | 70,00 | 2,272 | 0,39 |
| Изооктилен | 0,006 | 70,00 | 2,129 | 0,84 |
| Третбутанол | 0,007 | 70,00 | 2,771 | 1,44 |
| Потери | - | - | - | 23,53 |
| Итого | 5,166 | 930,16 |
Список литературы
1 Танатаров М.А., Ахметшина М.Н., Фасхутдинов Р.А. и др. Технологические расчеты установок переработки нефти: учеб. пособие для вузов. – М.: Химия, 1987. – 352 с.
3 Сарданашвили А. Г., Львова А. И. Примеры и задачи по технологии переработки нефти и газа.-2-е изд., - М.: Химия, 1980. – 256с.
5 Кузнецов А.А., Кагерманов С.М. и др. Расчеты процессов и аппаратов нефтеперерабатывающей промышленности. – Л.: Химия, 1974. – 343 с.
6 Дубовкин Н.Ф. Справочник по теплофизическим свойствам углеводородных топлив и их продуктов сгорания. – М.-Л.: Госэнергоиздат, 1962. – 288 с.
7 Флореа О., Смигельский О. Расчеты по процессам и аппаратам химической технологии. – М.: Химия, 1971. – 448 с.
8 Батунер Л.М. Процессы и аппараты органического синтеза и биохимической технологии. - Л., Химия, 1966. – 520с.
9 Варгафтик Н.Б. Справочник по теплофизическим свойствам газов и жидкостей. - М.: Физматгиз, 1963. – 708с.
10 Козлов Б.И. Процессы алкилирования, изомеризации и полимеризации в нефтепереработке. – М.: Химия, 1990. – 65 с.
11 Ахметов С.А. Технология глубокой переработки нефти и газа. –Уфа: Гилем, 2002. – 672 с.
12 Мириманян А.А., Вихман А.Г., Мкртпычев А.Л. Нефтепереработка и нефтехимия. – 2006. - №4. - С. 22-31.
13 Интернет-ресурс www.chemistry.ssu.samara.ru
14 Кузора И.Е., Томин В.П., Микишев В.А. и др. Технологии производства компонентов современных автомобильных бензинов // Химия и технология топлив и масел. – 2008. - №2. - С. 33.
15 Стыценко В.Д., Лавриненко А.А., Надра В.А. и др. Перспективы улучшения экологических и эксплуатационных свойств моторных топлив // Химия и технология топлив и масел. – 2008. - №5. - С. 52.
16 Ахметов С.А., Ишмияров М.Х., Кауфман А.А. Технология переработки нефти, газа и твердых горючих ископаемых: учеб. пособие. – СПб.: Недра, 2009. – 832 с.
17 Капустин В.М., Кукес С.Г., Бертолусини Р.Г. Нефтеперерабатывающая промышленность США и бывшего СССР. – М.: Химия, 1995. – 304 с.
18 Интернет-ресурс http://www.bmcompany.ru/ru/products/bioethanol/field_ of_application401.html. Высоко-кислородные добавки (оксигенаты) к топливу.
Содержание
|
| ||||
| Введение | 1 | |||
| 1 | Расчет процесса алкилирования изобутана олефинами | 2 | ||
| 2 | Расчет процесса изомеризации углеводородов | 18 | ||
| 3 | Расчет процесса синтеза метил-трет-бутилового эфира (МТБЭ) | 27 | ||
Редактор М.Е. Галина
Подписано в печать 01.-8.11. Бумага офсетная. Формат 60х84 1/16.
Гарнитура «Таймс». Печать трафаретная. Усл. печ. л. 2,4. Уч.-изд. л. 2,2.
Тираж 60. Заказ .
Издательство Уфимского государственного нефтяного технического университета
Адрес издательства:
450062, Республика Башкортостан, г. Уфа, ул. Космонавтов, 1
Филиал УГНТУ в г. Салавате
Кафедра химико-технологических процессов
Дата: 2019-02-25, просмотров: 812.