| Элемент | Полуреакция | Е0, В |
| Ag | Ag+ + 1ē = Ag | +0,80 |
| AgCl + 1ē = Ag + Cl- | + 0,22 | |
| Ag2+ + 1ē = Ag+ | + 1,98 | |
| Ag2О + Н2О + 2ē = 2Ag + 2ОН- | + 0,34 | |
| 2AgО + Н2О + 2ē = Ag2О + 2ОН- | + 0,607 | |
| Ag2S + 2ē = 2Ag + S2- | – 0,691 | |
| Ag2S + 2Н+ + 2ē = 2Ag + Н2S | – 0,0366 | |
| AgI + 1ē = Ag + I- | – 0,15 | |
| Al | AlO 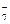 + 2H2O + 3 ē = Al + 4OH- + 2H2O + 3 ē = Al + 4OH-
| – 2,35 |
| Al(OH)3 + 3ē = Al + 4OH- | – 2,328 | |
| As | H3AsO4 + 2H+ + 2ē = HAsO2 + 2H2O | + 0,56 |
AsO 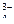 + 2H2O + 2ē = AsO + 2H2O + 2ē = AsO 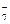 + 4OH- + 4OH-
| – 0,71 | |
2AsO 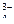 + 3SO42- + 40H+ + 28ē = As2S3 + 20 H2O + 3SO42- + 40H+ + 28ē = As2S3 + 20 H2O
| – 0,60 | |
| Be | Be2O 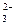 + 3H2O + 4ē = 2Be + 6OH- + 3H2O + 4ē = 2Be + 6OH-
| – 2,63 |
| Bi | NaBiO3 + 6H+ + 2ē = Bi3+ + 3H2O + Na+ | +1,81 |
| Br | BrO3- + 3H2O + 6ē = Br-+ 6OH- | +0,61 |
| Br2 + 2ē = 2Br- | +1,09 | |
| HBrO + H+ + 2ē = Br- + H2O | +1,34 | |
| Cl | Cl2 + 2ē = 2Cl- | +1,36 |
| ClO3- + 6H+ + 6ē = Cl- + 3H2O | +1,46 | |
| ClO- + H2O + 2ē = Cl- + 2OH- | +0,92 | |
| 2ClO- + 2H2O + 2ē = Cl2 + 4OH- | +1,56 | |
ClO 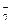 + 2H2O + 4ē = Cl- + 4OH- + 2H2O + 4ē = Cl- + 4OH-
| +0,76 | |
ClO 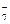 + H2O + 2ē = ClO- + 2OH- + H2O + 2ē = ClO- + 2OH-
| +0,66 | |
ClO 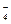 + 8H+ + 8ē = Cl- + 4H2O + 8H+ + 8ē = Cl- + 4H2O
| +1,389 | |
ClO 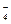 + H2O + 2ē = ClO + H2O + 2ē = ClO 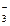 + 2OH- + 2OH-
| +0,36 | |
| HClO2 + 2H+ + 2ē = HClO + H2O | + 1,645 | |
| F | 2F- + 2ē = F20 | +2,65 |
| Cr | Cr2O72- + 14H+ + 6ē = 2Cr3+ + 7H2O | +1,33 |
CrO 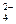 +2H2O + 3ē = CrO2- + 4OH- +2H2O + 3ē = CrO2- + 4OH-
| - 0,21 | |
CrO 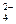 + 4H2O + 3ē = Cr3+ + 8OH- + 4H2O + 3ē = Cr3+ + 8OH-
| +1,45 | |
CrO 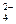 + 8H+ + 3ē = Cr3+ + 4H2O + 8H+ + 3ē = Cr3+ + 4H2O
| +1,47 | |
| Cr(OH)3 + 3ē = Cr + 3OH- | – 1,48 | |
| CrO3 + 6H+ + 3ē = Cr3+ + 3H2O | – 0,11 | |
CrO 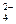 + 4H2O + 3ē = Cr(OH)3 + 5OH- + 4H2O + 3ē = Cr(OH)3 + 5OH-
| – 0,13 | |
| H | 2H2O + 2ē = H2 + 2OH- | – 0,83 |
| H2O2 + 2H+ + 2ē = 2H2O | +1,776 | |
| I | 2IO3- + 12H+ + 10ē = I2 + 6H2O | +1,195 |
| 2IO- + 4H+ + 2ē = I2 + 2H2O | +1,10 | |
| HIO + H+ + 2ē = I- + H2O | +0,987 | |
| IO- + H2O + 2ē = I- + 2OH- | +0,485 | |
IO 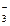 + 6H+ + 6ē = I- + 3H2O + 6H+ + 6ē = I- + 3H2O
| +1,085 | |
IO 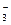 + 2H2O+ 4ē = IO- + 4OH- + 2H2O+ 4ē = IO- + 4OH-
| +0,15 | |
IO 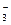 + 3H2O+ 6ē = IO- + 6OH- + 3H2O+ 6ē = IO- + 6OH-
| +0,26 | |
| I2 + 2ē = 2I- | +0,54 | |
| 2HIO + 2H+ + 2ē = I2 + 2H2O | +1,439 | |
| Fe | Fe(OH)3 + 1ē = Fe(OH)2 + OH- | – 0,56 |
| Fe2O3 + 4H+ + 2ē = 2FeOH+ + H2O | +0,16 | |
| Fe3+ + 1ē = Fe2+ | +0,77 | |
| Mn | MnO2 + 4H+ + 2ē = Mn2+ + 2H2O | +1,24 |
MnO 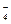 + 8H+ + 5ē = Mn2+ + 4H2O + 8H+ + 5ē = Mn2+ + 4H2O
| +1,53 | |
MnO 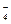 + 1ē = MnO42- + 1ē = MnO42-
| +0,56 | |
| MnO2 + 4OH- + 2ē = Mn2+ + 2H2O | +1,15 | |
MnO 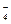 + 2H2O + 2ē = MnO2 + 4OH- + 2H2O + 2ē = MnO2 + 4OH-
| +0,60 | |
MnO 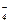 + 4H+ + 3ē = MnO2 + 2H2O + 4H+ + 3ē = MnO2 + 2H2O
| +1,679 | |
MnO 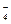 + 2H2O + 3 ē = MnO2 + 4OH- + 2H2O + 3 ē = MnO2 + 4OH-
| +0,595 | |
| Mn(OH)2 + 2ē = Mn + 2OH- | – 1,56 | |
| Mn(OH)3 + 1ē = Mn(OH)2 + OH- | +0,15 | |
| Mn2O3 + 6H+ + 2ē = 2Mn2+ + 3H2O | +1,485 | |
| N | NO 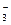 + 2H+ + 1ē = NO2 + H2O + 2H+ + 1ē = NO2 + H2O
| +0,77 |
| N2 + 2H2O + 6H+ + 6ē = 2NH4OH | 0,092 | |
| 3N2 + 2H+ + 2ē = 2HN3 | – 3,09 | |
N2H 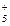 + 3H+ + 2ē = 2NH + 3H+ + 2ē = 2NH 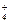
| +1,275 | |
| N2O + 2H+ + 2ē = N2 + H2O | +1,766 | |
N2O4 + 2ē = 2NO 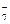
| +0,867 | |
| N2O4 + 2H+ + 2ē = 2HNO2 | +1,065 | |
| N2O4 + 4H+ + 4ē = 2NO + 2H2O | +1,035 | |
| 2NO + 2H+ + 2ē = N2O + H2O | +1,591 | |
| 2NO + H2O + 2ē = N2O + 2OH- | +0,76 | |
| HNO2 + H+ + 1ē = NO + H2O | +0,983 | |
NO 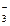 + 3H+ + 2ē = HNO2 + H2O + 3H+ + 2ē = HNO2 + H2O
| +0,94 | |
NO 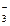 + 2H+ + 2ē = NO2- + H2O + 2H+ + 2ē = NO2- + H2O
| +0,84 | |
NO 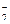 + H2O + ē = NO + 2OH- + H2O + ē = NO + 2OH-
| – 0,46 | |
NO 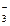 + 4H+ + 3ē = NO + 2H2O + 4H+ + 3ē = NO + 2H2O
| +0,96 | |
2NO 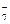 + 2H2O + 4ē = N2O + 2H2O + 4ē = N2O 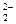 + 4OH- + 4OH-
| – 0,18 | |
2NO 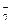 + 3H2O + 4ē = N2O + 6OH- + 3H2O + 4ē = N2O + 6OH-
| +0,15 | |
2NO 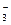 + 2H2O + 2ē = N2O4 + 4OH- + 2H2O + 2ē = N2O4 + 4OH-
| – 0,85 | |
2NO 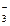 + 4H+ + 2ē = N2O4 + 2H2O + 4H+ + 2ē = N2O4 + 2H2O
| +0,803 | |
NO 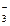 + H2O + 2ē = NO + H2O + 2ē = NO 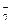 + 2OH- + 2OH-
| +0,01 | |
| О
| O2 + 2H+ + 4ē = 4OH- | +0,40 |
| O2 + 2H+ + 2ē = H2O2 | +0,69 | |
| O2 + 4H+ + 4ē = 2H2O | +1,229 | |
| O2 + 2H2O + 2ē = H2O2 + 2OH- | – 0,146 | |
| O3 + 2H+ + 2ē = H2O + O2 | +2,076 | |
| O2 + 2H2O + 4ē = 4OH- | +0,40 | |
| O3 + 2H2O + 2ē = O2 + 2OH- | +1,24 | |
| P | H3PO4 + 5H+ + 5ē = P + 4H2O | -0,41 |
| H3PO4 + 2H+ + 2ē = H3PO3 + H2O | -0,28 | |
| Pb | [Pb(OH)4]2- + 2ē = Pb + 4OH- | -0,52 |
| PbO2 + 4H+ + 2ē = Pb2+ + 2H2O | +1,46 | |
| PbO2 + 2ē = PbO22- | +1,70 | |
| Pb4+ + 4ē = Pb | +0,77 | |
| S | S + 2ē = S2- | -0,48 |
| S + H2О + 2ē = HS- + ОН- | - 0,478 | |
| SO42- + 10H+ + 8ē = H2S + 4H2O | +0,30 | |
| S + 2H+ + 2ē = H2S | +0,142 | |
| SO2 + 4H+ + 4ē = S + 2H2O | +0,45 | |
| SO42-+ 4H+ + 2ē = SO2 + 2H2O | +0,16 | |
| SO42- + 8H+ + 6ē = S + 4H2O | +0,35 | |
| SO42- + 8H+ + Cu2+ + 8ē = CuS + 4H2O | +0,42 | |
| SO42- + 2H+ + 2ē = SO32- + H2O | -0,10 | |
| Se | SeO42- + 2H+ + 2ē = SeO32- + H2O | +1,15 |
Варианты контрольных работ
| № варианта | Номера заданий относящихся к данной работе | |||||||||||||
| 1 | 301 | 331 | 361 | 391 | 421 | 451 | 481 | 511 | 541 | 571 | 601 | 631 | 661 | 691 |
| 2 | 302 | 332 | 362 | 392 | 422 | 452 | 482 | 512 | 542 | 572 | 602 | 632 | 662 | 692 |
| 3 | 303 | 333 | 363 | 393 | 423 | 453 | 483 | 513 | 543 | 573 | 603 | 633 | 663 | 693 |
| 4 | 304 | 334 | 364 | 394 | 424 | 454 | 484 | 514 | 544 | 574 | 604 | 634 | 664 | 694 |
| 5 | 305 | 335 | 365 | 395 | 425 | 455 | 485 | 515 | 545 | 575 | 605 | 635 | 665 | 695 |
| 6 | 306 | 336 | 366 | 396 | 426 | 456 | 486 | 516 | 546 | 576 | 606 | 636 | 666 | 696 |
| 7 | 307 | 337 | 367 | 397 | 427 | 457 | 487 | 517 | 547 | 577 | 607 | 637 | 667 | 697 |
| 8 | 308 | 338 | 368 | 398 | 428 | 458 | 488 | 518 | 548 | 578 | 608 | 638 | 668 | 698 |
| 9 | 309 | 339 | 369 | 399 | 429 | 459 | 489 | 519 | 549 | 579 | 609 | 639 | 669 | 699 |
| 10 | 310 | 340 | 370 | 400 | 430 | 460 | 490 | 520 | 550 | 580 | 610 | 640 | 670 | 700 |
| 11 | 311 | 341 | 371 | 401 | 431 | 461 | 491 | 521 | 551 | 581 | 611 | 641 | 671 | 701 |
| 12 | 312 | 342 | 372 | 402 | 432 | 462 | 492 | 522 | 552 | 582 | 612 | 642 | 672 | 702 |
| 13 | 313 | 343 | 373 | 403 | 433 | 463 | 493 | 523 | 553 | 583 | 613 | 643 | 673 | 703 |
| 14 | 314 | 344 | 374 | 404 | 434 | 464 | 494 | 524 | 554 | 584 | 614 | 644 | 674 | 704 |
| 15 | 315 | 345 | 375 | 405 | 435 | 465 | 495 | 525 | 555 | 585 | 615 | 645 | 675 | 705 |
| 16 | 316 | 346 | 376 | 406 | 436 | 466 | 496 | 526 | 556 | 586 | 616 | 646 | 676 | 706 |
| 17 | 317 | 347 | 377 | 407 | 437 | 467 | 497 | 527 | 557 | 587 | 617 | 647 | 677 | 707 |
| 18 | 318 | 348 | 378 | 408 | 438 | 468 | 498 | 528 | 558 | 588 | 618 | 648 | 678 | 708 |
| 19 | 319 | 349 | 379 | 409 | 439 | 469 | 499 | 529 | 559 | 589 | 619 | 649 | 679 | 709 |
| 20 | 320 | 350 | 380 | 410 | 440 | 470 | 500 | 530 | 560 | 590 | 620 | 650 | 680 | 710 |
| 21 | 321 | 351 | 381 | 411 | 441 | 471 | 501 | 531 | 561 | 591 | 621 | 651 | 681 | 711 |
| 22 | 322 | 352 | 382 | 412 | 442 | 472 | 502 | 532 | 562 | 592 | 622 | 652 | 682 | 712 |
| 23 | 323 | 353 | 383 | 413 | 443 | 473 | 503 | 533 | 563 | 593 | 623 | 653 | 683 | 713 |
| 24 | 324 | 354 | 384 | 414 | 444 | 474 | 504 | 534 | 564 | 594 | 624 | 654 | 684 | 714 |
| 25 | 325 | 355 | 385 | 415 | 445 | 475 | 505 | 535 | 565 | 595 | 625 | 655 | 685 | 715 |
| 26 | 326 | 356 | 386 | 416 | 446 | 476 | 506 | 536 | 566 | 596 | 626 | 656 | 686 | 716 |
| 27 | 327 | 357 | 387 | 417 | 447 | 477 | 507 | 537 | 567 | 597 | 627 | 657 | 687 | 717 |
| 28 | 328 | 358 | 388 | 418 | 448 | 478 | 508 | 538 | 568 | 598 | 628 | 658 | 688 | 718 |
| 29 | 329 | 359 | 389 | 419 | 449 | 479 | 509 | 539 | 569 | 599 | 629 | 659 | 689 | 719 |
| 30 | 330 | 360 | 390 | 420 | 450 | 480 | 510 | 540 | 570 | 600 | 630 | 660 | 690 | 720 |
| 31 | 327 | 359 | 361 | 394 | 425 | 461 | 507 | 538 | 554 | 572 | 623 | 650 | 681 | 692 |
| 32 | 301 | 358 | 362 | 395 | 424 | 462 | 506 | 518 | 555 | 574 | 625 | 640 | 672 | 698 |
| 33 | 329 | 340 | 369 | 396 | 423 | 463 | 505 | 519 | 556 | 576 | 627 | 631 | 663 | 699 |
| 34 | 328 | 359 | 380 | 397 | 422 | 473 | 504 | 520 | 548 | 578 | 629 | 641 | 687 | 710 |
| 35 | 327 | 358 | 389 | 420 | 421 | 472 | 483 | 528 | 543 | 580 | 619 | 651 | 689 | 711 |
| 36 | 326 | 357 | 388 | 419 | 450 | 471 | 482 | 519 | 547 | 582 | 617 | 632 | 690 | 712 |
| 37 | 325 | 356 | 387 | 418 | 449 | 460 | 481 | 520 | 549 | 584 | 615 | 642 | 663 | 713 |
| 38 | 324 | 355 | 386 | 417 | 448 | 479 | 500 | 521 | 550 | 586 | 614 | 652 | 665 | 714 |
| 39 | 323 | 354 | 385 | 416 | 447 | 478 | 509 | 522 | 553 | 588 | 613 | 633 | 667 | 715 |
| 40 | 322 | 353 | 384 | 415 | 446 | 477 | 508 | 523 | 555 | 590 | 601 | 644 | 669 | 716 |
| 41 | 321 | 352 | 383 | 414 | 445 | 476 | 507 | 524 | 557 | 592 | 602 | 655 | 662 | 717 |
| 42 | 320 | 351 | 382 | 413 | 444 | 475 | 506 | 525 | 559 | 594 | 603 | 636 | 661 | 718 |
| 43 | 319 | 350 | 381 | 412 | 443 | 474 | 505 | 526 | 560 | 596 | 604 | 646 | 662 | 719 |
| 44 | 318 | 349 | 380 | 411 | 442 | 473 | 504 | 527 | 562 | 598 | 605 | 656 | 663 | 720 |
| 45 | 317 | 348 | 379 | 410 | 441 | 472 | 503 | 528 | 564 | 600 | 606 | 631 | 664 | 695 |
| 46 | 316 | 347 | 378 | 409 | 440 | 471 | 487 | 529 | 541 | 571 | 607 | 632 | 665 | 697 |
| 47 | 315 | 346 | 376 | 408 | 439 | 470 | 488 | 518 | 542 | 573 | 608 | 633 | 666 | 694 |
| 48 | 314 | 345 | 375 | 407 | 438 | 469 | 489 | 530 | 543 | 575 | 609 | 634 | 667 | 692 |
| 49 | 313 | 344 | 374 | 406 | 437 | 468 | 490 | 531 | 544 | 577 | 610 | 635 | 668 | 701 |
| 50 | 312 | 343 | 373 | 405 | 436 | 467 | 491 | 532 | 545 | 579 | 611 | 636 | 669 | 702 |
| 51 | 311 | 342 | 372 | 404 | 435 | 466 | 492 | 533 | 546 | 600 | 612 | 637 | 670 | 703 |
| 52 | 310 | 341 | 371 | 403 | 434 | 465 | 493 | 534 | 547 | 581 | 613 | 638 | 671 | 704 |
| 53 | 309 | 340 | 370 | 402 | 433 | 464 | 494 | 535 | 548 | 583 | 614 | 639 | 672 | 705 |
| 54 | 308 | 339 | 369 | 401 | 432 | 463 | 495 | 536 | 549 | 585 | 615 | 640 | 673 | 706 |
| 55 | 307 | 338 | 368 | 400 | 431 | 462 | 496 | 537 | 550 | 587 | 616 | 641 | 674 | 707 |
| 56 | 306 | 337 | 367 | 399 | 430 | 461 | 497 | 538 | 551 | 589 | 617 | 642 | 675 | 708 |
| 57 | 305 | 336 | 366 | 398 | 429 | 460 | 498 | 539 | 552 | 591 | 618 | 643 | 676 | 709 |
| 58 | 304 | 335 | 365 | 397 | 428 | 459 | 499 | 540 | 553 | 593 | 619 | 644 | 677 | 690 |
| 59 | 303 | 334 | 364 | 396 | 427 | 458 | 500 | 511 | 554 | 595 | 620 | 645 | 678 | 691 |
| 60 | 302 | 333 | 363 | 395 | 426 | 457 | 501 | 512 | 555 | 597 | 621 | 646 | 679 | 692 |
| 61 | 301 | 332 | 393 | 394 | 425 | 456 | 502 | 513 | 556 | 599 | 622 | 647 | 680 | 693 |
| 62 | 303 | 331 | 392 | 394 | 435 | 460 | 503 | 514 | 557 | 571 | 623 | 648 | 681 | 694 |
| 63 | 306 | 334 | 391 | 395 | 434 | 461 | 504 | 515 | 558 | 572 | 624 | 649 | 682 | 695 |
| 64 | 309 | 335 | 381 | 396 | 423 | 462 | 505 | 516 | 559 | 573 | 625 | 650 | 683 | 696 |
| 65 | 308 | 336 | 371 | 397 | 422 | 463 | 506 | 517 | 560 | 574 | 626 | 651 | 684 | 697 |
| 66 | 304 | 337 | 372 | 398 | 421 | 464 | 507 | 518 | 561 | 575 | 627 | 652 | 685 | 698 |
| 67 | 305 | 338 | 382 | 399 | 450 | 465 | 508 | 519 | 562 | 576 | 628 | 653 | 686 | 699 |
| 68 | 316 | 339 | 390 | 400 | 449 | 466 | 509 | 521 | 563 | 577 | 629 | 654 | 687 | 700 |
| 69 | 310 | 340 | 366 | 401 | 448 | 467 | 510 | 522 | 564 | 578 | 630 | 655 | 688 | 691 |
| 70 | 315 | 341 | 368 | 402 | 447 | 468 | 501 | 523 | 565 | 600 | 601 | 656 | 689 | 692 |
| 71 | 311 | 342 | 369 | 403 | 446 | 469 | 491 | 524 | 566 | 599 | 602 | 657 | 690 | 693 |
| 72 | 314 | 343 | 371 | 404 | 445 | 470 | 493 | 525 | 567 | 598 | 603 | 658 | 681 | 694 |
| 73 | 312 | 344 | 374 | 405 | 444 | 471 | 495 | 526 | 568 | 597 | 604 | 659 | 672 | 695 |
| 74 | 313 | 345 | 375 | 406 | 443 | 472 | 486 | 527 | 569 | 596 | 605 | 660 | 663 | 696 |
| 75 | 325 | 346 | 376 | 407 | 442 | 473 | 506 | 528 | 570 | 595 | 606 | 631 | 661 | 697 |
| 76 | 324 | 347 | 378 | 408 | 441 | 474 | 507 | 529 | 541 | 594 | 607 | 637 | 668 | 698 |
| 77 | 323 | 348 | 382 | 409 | 440 | 475 | 488 | 530 | 558 | 593 | 608 | 638 | 669 | 699 |
| 78 | 322 | 349 | 383 | 410 | 439 | 476 | 489 | 531 | 559 | 592 | 609 | 639 | 670 | 700 |
| 79 | 321 | 350 | 384 | 411 | 438 | 477 | 490 | 532 | 560 | 591 | 610 | 640 | 671 | 701 |
| 80 | 320 | 351 | 385 | 412 | 437 | 478 | 491 | 533 | 561 | 590 | 611 | 641 | 672 | 702 |
| 81 | 319 | 352 | 387 | 413 | 436 | 479 | 492 | 534 | 562 | 589 | 612 | 642 | 673 | 703 |
| 82 | 318 | 353 | 389 | 414 | 435 | 480 | 493 | 535 | 563 | 588 | 613 | 643 | 674 | 704 |
| 83 | 317 | 354 | 381 | 415 | 434 | 463 | 494 | 536 | 564 | 587 | 614 | 644 | 675 | 705 |
| 84 | 316 | 355 | 383 | 416 | 433 | 472 | 495 | 537 | 565 | 586 | 615 | 645 | 676 | 706 |
| 85 | 315 | 356 | 385 | 417 | 432 | 466 | 496 | 538 | 566 | 585 | 616 | 646 | 677 | 707 |
| 86 | 314 | 357 | 377 | 418 | 431 | 474 | 497 | 539 | 567 | 584 | 617 | 647 | 678 | 708 |
| 87 | 313 | 358 | 379 | 419 | 430 | 475 | 498 | 540 | 568 | 583 | 618 | 648 | 679 | 709 |
| 88 | 312 | 359 | 370 | 420 | 429 | 456 | 499 | 511 | 569 | 582 | 619 | 649 | 680 | 710 |
| 89 | 311 | 360 | 368 | 421 | 428 | 459 | 500 | 512 | 570 | 581 | 620 | 650 | 681 | 711 |
| 90 | 310 | 336 | 366 | 422 | 427 | 457 | 501 | 513 | 542 | 580 | 621 | 651 | 682 | 712 |
| 91 | 331 | 345 | 364 | 423 | 426 | 458 | 502 | 514 | 543 | 579 | 622 | 652 | 683 | 713 |
| 92 | 328 | 332 | 382 | 424 | 425 | 459 | 503 | 515 | 544 | 578 | 623 | 653 | 684 | 714 |
| 93 | 326 | 334 | 390 | 423 | 427 | 460 | 504 | 516 | 545 | 577 | 624 | 654 | 685 | 715 |
| 94 | 325 | 338 | 378 | 422 | 423 | 461 | 505 | 517 | 547 | 576 | 625 | 655 | 686 | 716 |
| 95 | 324 | 340 | 386 | 421 | 436 | 462 | 506 | 518 | 549 | 575 | 626 | 656 | 687 | 717 |
| 96 | 329 | 342 | 384 | 394 | 448 | 463 | 507 | 519 | 550 | 574 | 627 | 657 | 688 | 718 |
| 97 | 327 | 344 | 372 | 400 | 449 | 464 | 508 | 520 | 551 | 573 | 628 | 658 | 689 | 719 |
| 98 | 330 | 346 | 390 | 409 | 450 | 465 | 509 | 521 | 552 | 572 | 629 | 659 | 662 | 720 |
| 99 | 324 | 348 | 365 | 410 | 441 | 466 | 510 | 522 | 553 | 571 | 630 | 660 | 690 | 691 |
Список литературы
1. Глинка Н.Л. Задачи и упражнения по общей химии: Учеб. пособие. – М.: Интеграл-Пресс, 2001.
2. Задачи и упражнения по общей химии: Учеб. пособие / Под ред. Н.В. Коровина. – М.: Высш. шк., 2003.
3. Задачи по общей и неорганической химии: Учеб. пособие для студ. высш. учеб. заведений / Под ред. Р.А. Лидина. – М.: ВЛАДОС, 2004.
4. Задачник по общей химии для металлургов / Под ред. Б.Г. Коршунова. – М.: Высш. шк., 1977.
5. Литвинова Т.Н. Сборник задач по общей химии: Учеб. пособие. – М., 2007.
6. Михилев Л.А., Пасет Н.Ф., Федотова М.И. Задачи и упражнения по неорганической химии: Учеб. пособие. – СПб.: Химия, 1995.
7. Морачевский А.Г., Патров Б.В., Сладков И.Б. Сборник примеров и задач по физической химии. – Л.: ЛПИ им. М.И. Калинина, 1974.
8. Романцева Л.М., Лещинская З.И., Суханова В.А. Сборник задач и упражнений по общей химии: Учеб. пособие. – М.: Высш. шк., 1991.
9. Сборник задач и упражнений по общей химии: Учеб. пособие / С.А. Пузаков, В.А. Попоков, А.А. Филиппова. – М.: Высш. шк., 2004.
10. Котенко Г.А., Ульянова О.В. Программа и контрольные задания по дисциплине «Поверхностные явления и дисперсные системы» для студентов заочной формы обучения: Учеб.-метод. пособие. – Череповец: ЧГУ, 2005.
11. Калько О.А., Кузнецова Ю.С., Кунина Н.В. Неорганическая химия. Сборник задач, часть 2: Учеб.-метод. пособие. – Череповец: ЧГУ, 2010.
12. Калько О.А., Кузнецова Ю.С., Ульянова О.В. Химия: Растворы. Дисперсные системы: Учеб. пособие. — Череповец: ФГБОУ ВПО ЧГУ, 2014.
13. Краткий справочник физико-химических величин / Под ред. А.А. Равделя и А.М. Пономаревой – СПб.: «Иван Федоров», 2008.
Оглавление
Введение .......................................................................................... 3
Способы выражения состава растворов ....................................... 3
Коллигативные свойства растворов неэлектролитов ..................... 6
Коллигативные свойства растворов электролитов ...................... 10
Свойства растворов слабых и сильных электролитов .................. 13
Ионное произведение воды. рН растворов ................................... 16
Произведение растворимости ........................................................ 19
Гидролиз солей ............................................................................... 22
Дисперсные системы ....................................................................... 25
Окислительно-восстановительные реакции ................................... 28
Гальванические элементы ............................................................... 32
Электролиз ...................................................................................... 36
Коррозия металлов ........................................................................ 39
Жесткость воды ............................................................................... 43
Элементы органической химии ...................................................... 46
Приложения .................................................................................... 50
Список литературы ........................................................................ 62
Дата: 2019-02-25, просмотров: 454.