Основу рестриктивных расстройств (от лат. restrictio – ограничение) дыхания составляет изменение вязкоэластических свойств легочной ткани.
К рестриктивным нарушениям дыхания относят гиповентиляционные расстройства, возникающие вследствие ограничения расправления лег ких из-за повреждения белков их интерстиция под действием ферментов (эластаза, коллагеназа и др.). В состав интерстиция входят коллаген (60-70 %), эластин (25-30 %), гликозаминогликаны (1 %), фибронектин (0,5 %). Фиб риллярные белки обеспечивают стабильность каркаса легких, его эластичность и растяжимость, создают оптимальные условия для выполнения основной газообменной функции. Структурные измене ния белков интерстиция проявляются снижением растяжимости ле гочной паренхимы и повышением эластического сопротивления легочной ткани. Так, при развитии эмфиземы нарушается равновесие между синтезом и распадом эластина, так как имеющийся избыток протеаз не уравновешивается ингибиторами протеолитических ферментов. При этом на ибольшее значение имеет дефицит -1-антитрипсина.
Сопротивление, которое приходится преодолевать дыхатель ным мышцам во время вдоха, может быть эластическим и неэлас тическим.
Эластическая тяга легких направлена на сокращение объема легких. То есть, это величина, обратная растяжимости. Примерно 2/3 эластической тяги легких зависит от поверхностного натяжения стенок альвеол. Эластическая тяга легких численно равна транспульмональному давлению. На вдохе увеличивается транспульмональное давление и объем легких. В зависимости от фазы дыхания имеются колебания внутриплеврального давления: в конце спокойного выдоха оно составляет 2-5 см вод. ст., в конце спокойного вдоха - 4-8 см вод. ст., на высоте максимального вдоха - 20 см вод. ст.
Растяжимость легких (податливость легких, легочный комплеанс) - величина, характеризующая изменения объема легких на единицу транспульмонального давления. Растяжимость - величина, обратно пропорциональная эластичности. Основным фактором, оп ределяющим предел максимального вдоха, является растяжимость. По мере углубления вдоха растяжимость легких прогрессивно уменьшается, а эластическое сопротивление становится наиболь шим. Поэтому главным фактором, определяющим предел макси мального выдоха, является эластическое сопротивление легких.
Выделяют две группы факторов, приводящих к ограничительным на рушениям вентиляции легких: 1) внелегочные и 2) внутрилегочные.
Рестриктивные расстройства дыхания внелегочного происхождения могут быть следствием сдавления туловища, вызванного воздействиями ме ханического характера (сдавление одеждой или предметами производс твенного оснащения, тяжелыми предметами, землей, песком и т.п., особенно, при различных катастрофах), либо возникают вследствие ограничения экскурсий грудной клетки при пневмо-, гидро- и гемотораксе и других патологи ческих процессах, ведущих к компрессии легочной ткани и нарушению расправления альвеол при вдохе.
Пневмоторакс возникает из-за попадания воздуха в плевральную полость и бывает первичным или спонтанным, (например, при кистах бронхов, сообщающихся с плевральной полостью) и вторичным (опухоли, туберкулез и др.), травматического и искусственного происхождения, а по механизму - открытым, закрытым и клапанным.
К рестриктивным наруше ниям дыхания относятся также поверхностные, учащенные дыхательные движения, возникающие в связи с чрезмерным окостенением реберных хрящей и малой подвижностью связочно-суставного аппарата грудной клетки.
Знание меxанизмов обpазования плевpальной жидкоcти объясняет целый pяд клинических cиндpомов. Так, у больныx c легочной гипеpтензией и пpизнаками пpавожелудочковой недоcтаточноcти также как и у больных c xpоничеcким легочным cеpдцем в cтадии пpавожелудочковой недоcтаточноcти, cкопления жидкоcти в плевpальной полоcти не пpоиcxодит. Cкопление тpанccудата в плевpальной полоcти возникает при диcфункции левого желудочка с pазвитием клиничеcкиx пpизнаков заcтойной cеpдечной недоcтаточноcти. Возникновение этого клиничеcкого феномена cвязывают c повышением давления в легочныx капилляpаx, что и пpиводит к пpопитыванию тpанccудата чеpез повеpxноcть виcцеpальной плевpы в ее полоcть. Удаление тpанccудата поcpедcтвом тоpакоцентеза cнижает объем циpкулиpующей кpови и давление в легочныx капилляpаx, поэтому в cовpеменные теpапевтичеcкие pекомендации эта пpоцедуpа включена как обязательная пpи ведении больныx c заcтойной cеpдечной недоcтаточноcтью.
Патофизиологичеcкие закономеpноcти возникновения тpанccудата пpи заcтойной cеpдечной недоcтаточноcти обуcловлены большим объемом кpови в cиcтеме малого кpуга кpовообpащения. При этом возникает эффект объем-давление-тpанccудат.
В оcнове этих закономеpноcтей pазвития экccудативного плевpита лежит возpаcтающий поток белков ферментов, фоpменныx элементов и электролитов кpови в плевральную полость.
Поверхность плевральных листков микроворсинок концентpиpует большое количеcтво гликопpотеинов и гиалуpоновой киcлоты и окpужена фоcфолипидами, т.е. по cвоей моpфологичеcкой xаpактеpиcтике напоминает альвеоляpный cуpфактант. Эти особенности объяcняют легкоcть cкольжения повеpxноcтей пеpиетального и виcцеpального лиcтков плевpы. Мезотелиальные клетки активно участвуют в воспалительном процессе. Мигpация нейтpофилов в плевpальную полоcть оcущеcтвляетcя под дейcтвием некотоpыx цитокинов, к котоpым, в чаcтноcти, отноcитcя интеpлейкин-8. Выcокая концентpация данного цитокина наблюдаетcя у больныx c эмпиемой плевpы. Меcтом cинтеза этого цитокина являютcя вовлеченные в воcпалительный пpоцеcc мезотелиальные клетки и иx воpcинки. Интеpлейкин-8 оказалcя чувcтвительным теcтом в пpоведении xимиотеpапии и оценке ее эффективноcти у больныx c мезотелиомой. Его рассматривают как биомаpкеp в диффеpенциальной диагноcтике воcпалительныx и канцеpогенныx плевpитов. В экcпеpиментальныx уcловияx были иcпользованы антитела пpотив интеpлейкина-8, что пpивело к ингибиpующему эффекту на пpоцеcc мигpации нейтpофилов в плевpальную полоcть. В физиологичеcкиx уcловияx ингибиpующим эффектом на дейcтвие xемоаттpактанта обладает интеpлейкин-10.
Рестриктивные расстройства дыхания легочного происхождения возникают в результате : 1) изменения вязкоэластических свойств, в том числе потери эластических волокон, легочной ткани; 2) повреждения сурфактанта или снижения его активности.
Нарушения вязкоэластических свойств легочной ткани отмечается при: - различных видах повреждений паренхимы легких; - диффузном фиброзировании легких различного происхождения (первичная эмфизема легких, пневмосклероз, пневмофиброз, альвеолиты); - очаговых изменениях в легких (опухоли, ателектазы); - отеке легких различного генеза (воспалительный, застойный). Растяжимость легких резко (более 50 %) уменьшается при уве личении кровенаполнения легких, интерстициальном отеке, в том числе воспа лительного характера. Так, в далеко зашедших случаях эмфиземы легких (из-за снижения растяжимости их даже при максимальном вдохе) не удается достичь предела функциональной растяжимости лег ких. В силу снижения эластической тяги легких происходит формирование бочкообразной грудной клетки.
Уменьшение растяжимости легочной ткани является типичным проявлением фиброза легких.
Потеря эластических свойств легочной ткани происходит при разрушении эластических волокон под влиянием длительного действия многих патогенных факторов (токсины микробов, ксенобиотики, табачный дым, нарушения пита ния, пожилой и старческий возраст), активирующих протеолитические ферменты.
Растяжимость и эластичность легких зависят также от тонуса альвеол и терминальных бронхиол.
Преимущественно по рестриктивному типу развиваются:
острая диффузная пневмония (крупозная пневмония),
пневмоторакс,
гидроторакс,
гемоторакс,
ателектаз.
60. Пневмоторакс. Этиология, клиника, лечение.
Пневмоторакс (греч. pnéuma —воздух,thorax — грудная клетка) – скопление газа в плевральной полости, ведущее к спадению ткани легкого, смещению средостения в здоровую сторону, сдавлению кровеносных сосудов средостения, опущению купола диафрагмы, что, в конечном итоге вызывает расстройство функции дыхания и кровообращения.
Этиология
В основе механизма развития пневмоторакса лежат две группы причин:
1. Механические повреждения грудной клетки или легких:
закрытые травмы грудной клетки, сопровождающиеся повреждением легкого отломками ребер; открытые травмы грудной клетки (проникающие ранения);
ятрогенные повреждения (как осложнение лечебных или диагностических манипуляций - повреждение легкого при постановке подключичного катетера, межреберной блокаде нерва, пункции плевральной полости); искусственно вызванный пневмоторакс -искусственный пневмоторакс
накладывается с целью лечения туберкулеза легких, с целью диагностики — при проведении торакоскопии.
2. Заболевания легких и органов грудной полости:
неспецифического характера – вследствие разрыва воздушных кист при буллезной болезни (эмфиземе) легких, прорываабсцесса легкого в полость плевры (пиопневмоторакс), спонтанногоразрыва пищевода; специфического характера - пневмоторакс вследствие разрыва каверн, прорыва казеозных очагов при туберкулезе.
Клиника пневмоторакса
Выраженность симптомов пневмоторакса зависит от причины заболевания и степени сдавления легкого.
Пациент с открытым пневмотораксом принимает вынужденное положение, лежа на поврежденной стороне и плотно зажимая рану. Воздух засасывается в рану с шумом, из раны выделяется пенистая кровь с примесью воздуха, экскурсия грудной клетки асимметрична (пораженная сторона отстает при дыхании).
Развитие спонтанного пневмоторакса обычно острое: после приступа кашля, физического усилия либо без всяких видимых причин. При типичном начале пневмоторакса появляется пронзительная колющая боль на стороне пораженного легкого, иррадиирующая в руку, шею, за грудину. Боль усиливается при кашле, дыхании, малейшем движении. Нередко боль вызывает у пациента панический страх смерти. Болевой синдром при пневмотораксе сопровождается одышкой, степень выраженности которой зависит от объема спадения легкого (от учащенного дыхания до выраженной дыхательной недостаточности). Появляется бледность или цианоз лица, иногда - сухой кашель.
Спустя несколько часов интенсивность боли и одышки ослабевают: боль беспокоит в момент глубокого вдоха, одышка проявляется при физическом усилии. Возможно развитие подкожной или медиастинальной эмфиземы – выход воздуха в подкожную клетчатку лица, шеи, грудной клетки или средостения, сопровождающийся вздутием и характерным хрустом при пальпации.
Аускультативно на стороне пневмоторакса дыхание ослаблено или не выслушивается. Примерно в четверти случаев спонтанный пневмоторакс имеет атипичное начало и развиваться исподволь. Боль и одышка незначительные, по мере адаптации пациента к новым условиям дыхания становятся практически незаметными. Атипичная форма течения характерна для ограниченного пневмоторакса, при незначительном количестве воздуха в полости плевры.
10. Диффузионные формы дыхательной недостаточности. Причины, проявления.
Дыхательная недостаточность - это состояние, при котором не обеспечивается поддержание нормального газового состава крови, либо последнее достигается за счет напряжения компенсаторных механизмов внешнего дыхания, что ведёт к снижению функциональных резервов организма.
Диффузионная недостаточность дыхания встречается при:
1) утолщении альвеолярно-капиллярной мембраны (отечность);
2) уменьшении площади альвеолярной мембраны;
3) уменьшении времени контакта крови с альвеолярным воздухом;
4) увеличении слоя жидкости на поверхности альвеол, интерстициальной жидкости между альвеолярным эпителием и стенкой капилляров (при левожелудочковой недостаточности, при токсическом отеке легких).
Диффузия нарушается также при заболеваниях, ведущих к уплотнению, огрубению коллагена и развитию соединительной ткани в интерстиции легкого (ряд хронических и подострых заболеваний легких, например, бериллиоз, интерстициальный фиброз Хамера-Ричи, продуктивный гипертрофический альвеолит).
Уменьшение числа капилляров, оплетающих альвеолы (эмфизема легких), или их воспалительное повреждение (волчаночный васкулит) отражается на скорости и полноте диффузии. Диффузия недостаточна при значительном ускорении кровотока по легочным капиллярам.
В норме время прохождения крови по капиллярам альвеол, т.е. время контакта крови с газом, составляет 2/3с. Для полной диффузии газов достаточно 0,2-0,25 с. При большем ускорении кровотока газы не успевают диффундировать даже при нормальном составе альвеолярного газа и нормальном состоянии альвеокапиллярной мембраны.
Для диффузионной недостаточности характерно наличие гипоксемии, ибо нарушается диффузия кислорода. Гиперкапнии не наблюдается, поскольку углекислый газ диффундирует в 25 раз быстрее кислорода. Напряжение углекислоты в крови может оказаться даже сниженным вследствие компенсаторного увеличения вентиляции при гипоксемии.
Дыхание кислородом, повышая парциальное давление последнего в альвеолярном газе и увеличивая градиент давления, позволяет преодолеть эффект снижения диффузии и добиться полного насыщения крови кислородом, т.е. устранить гипоксемию.
11) Нарушения легочного кровотока (перфузионные формы недостаточности), их причины, последствия. Соотношение вентиляции и перфузии в норме и при патологии.
Нарушение диффузии газов через альвеолярно-капиллярный барьер.
Причины: увеличение толщины мембраны за счет: возрастания количества жидкости в альвеолах, отека межмембранного пространства, утолщения клеток эндотелия и эпителия; увеличение плотности мембраны вследствие: кальцификации, возрастания вязкости геля интерстиция, увеличение количества коллагеновых и эастических волокон.
Нарушение вентиляционно – перфузионных отношений:
В норме соотношение между величинами вентиляции и перфузии сопряжены в лёгких: кровоток реализуется в тех участках лёгкого, в которых осуществляется вентиляция, происходит газообмен между воздухом альвеол и кровью, протекающей по межальвеолярным капиллярам.
Нарушение сопряжения вентиляции и перфузии лёгких приводит к развитию дыхательной недостаточности.
Основные причины дисбаланса вентиляции и перфузии:
1.Обтурация ветвей лёгочной артерии
2.Сдавление сосудов лёгочной артерии
3.Спазм мышц стенок ветвей лёгочной артерии
4. Шунтирование крови (минуя альвеолы)
5.Расстройства биомеханики дыхания (обструкция биомеханики дыхания, дыхательных путей, нарушение растяжимости легких).
6. Нарушение механизмов регуляции внешнего дыхания.
Причины нарушения лёгочного кровотока:
гипертензия и гипотензия в малом круге кровообращения;
расстройства кровообращения в системе бронхиальных артерий.
Нарушения соотношения вентиляции и перфузии
Эффективность внешнего дыхания во многом зависит от соотношения альвеолярной вентиляции и перфузии, как на уровне лёгких в целом, так и их отдельных участков: долей, сегментов, субсегментов, групп альвеол. Поддержание нормального газового состава крови затруднено при недостаточной перфузии хорошо вентилируемых альвеол или, наоборот, избыточной перфузии плохо вентилируемых альвеол. Адекватность минутного объёма вентиляции минутному объёму кровотока характеризует показатель вентиляционно-перфузионных отношений, в норме он равен 0,8–1,0. Только в этом случае газообмен через альвеолокапиллярные мембраны достаточен.
Даже в физиологических условиях возможно несоответствие между вентиляцией и перфузией отдельных участков лёгких. Систолическое давление в лёгочной артерии составляет 15–25 мм рт.ст., а диастолическое — 5–10 мм рт.ст. (в среднем, 9–15 мм рт.ст.). Давление в лёгочных капиллярах равно 7–8 мм рт.ст. (пульсовые колебания 3–5 мм рт.ст.). Столь низкие значения гидростатического давления в малом круге означают существенную зависимость лёгочного кровотока от положения тела. Поскольку у взрослого человека верхушки лёгких расположены на 15 см выше основания лёгочной артерии, то гидростатическое давление в верхних долях лёгких примерно равно артериальному, т.е. при вертикальном положении тела снабжение капилляров этих долей кровью недостаточно. В основании лёгких ситуация противоположная. Поэтому даже у здорового человека в верхушках лёгких избыточна вентиляция, а в основании лёгких — избыточна перфузия, что снижает эффективность внешнего дыхания. При горизонтальном положении тела происходит сочетание избыточной вентиляции передних отделов лёгких с избыточной перфузией их задних участков.
Кроме гравитационных сил, неравномерности вентиляционно-перфузионных отношений способствуют анатомическая и биофизическая гетерогенность отдельных участков лёгких, локальные различия тонуса бронхов и сосудов, а также градиент транспульмонального давления. Адекватность альвеолярной вентиляции и перфузии в различных участках лёгочной ткани поддерживают соответствующие ауторегуляторные механизмы. Например, недостаточная вентиляция, приводящая к снижению парциального напряжения кислорода в альвеолах, вызывает локальный спазм лёгочных артериол (рефлекс Эйлера–Лилиестрандта). Этот эффект бывает усилен локальным ацидозом, вызывающим ангиоспазм. Гиповентиляция обычно протекает с гиперкапнией, частично восстанавливающей вентиляцию альвеол благодаря бронходилатации. Всё это способствует поддержанию нормальных вентиляционно-перфузионных отношений. Кроме того, гиперкапния, гипоксемия и ионы Н+ также стимулируют дыхательный центр, облегчая альвеолярную вентиляцию. Столь же биологически целесообразна гуморальная регуляция тонуса бронхов и сосудов. В частности, гистамин, одновременно вызывая сужение лёгочных сосудов и бронхоспазм, существенно не меняет вентиляционно-перфузионных отношений.
Нарушение вентиляционно-перфузионных отношений бывает при длительном дыхании чистым кислородом, искусственной вентиляции лёгких, курении, альвеолитах, ателектазах, бронхиальной астме, локальных нарушениях перфузии при микротромбозах, капиллярном сладже и стазе, тромбоэмболии лёгочной артерии, внутрилёгочном шунтировании крови и др. Во всех этих случаях увеличен объём функционального мёртвого пространства и, следовательно, количество плохо оксигенированной крови, оттекающей от лёгких. Кроме того, при гипоксемической форме дыхательной недостаточности (сочетании гипоксемии и нормокапнии) альвеолярная вентиляция обычно избыточна относительно транскапиллярного тока крови.
38. Паренхиматозная желтуха. Этиология, патогенез, проявления, последствия.
Различают инфекционные и неинфекционные причины возникновения печё ночных желтух.
• Инфекционные причины. К ним относят вирусы, бактерии, плазмодии.
• Неинфекционные причины печёночных желтух: органические и неоргани ческие гепатотоксические вещества (например, четырёххлористый углерод, этанол, парацетамол и др.), гепатотропные AT, цитотоксические лимфоциты и макрофаги, новообразования.
Характер и выраженность нарушений функций печени зависят от степени аль терации и массы повреждённых гепатоцитов. В значительной части случаев повреждение, начинаясь с изменения структуры клеточных мембран и/или подавления активности ферментов, нарастает и может завершиться деструкци ей печёночных клеток. В любом случае при повреждении паренхимы печени происходят расстройства желчеобразования и желчевыведения.
Стадии желтухи.
Первая стадия (преджелтушная):
- Повреждение и снижение активности ферментов, разрушающих уроби-линоген. Проявления: уробилиногенемия и уробилиногенурия.
- Альтерация мембран гепатоцитов, повышение их проницаемости и вы ход в интерстиций и кровь компонентов цитоплазмы. Проявления: фер-ментемия (в крови повышается активность трансаминаз АЛТ и ACT, a также других ферментов, характерных для печени) и гиперкалиемия (выз вана повреждением большого числа гепатоцитов).
- Снижение активности глюкуронилтрансферазы. Проявления: уменьше ние образования прямого билирубина и как следствие — содержания стеркобилиногена в крови, моче и экскрементах.
Вторая стадия (желтушная):
Для желтушной стадии характерно дальнейшее усугубление альтерации гепатоцитов и их ферментов. Это приводит к нарушению работы «би-лирубинового конвейера» (цитоплазматический белок гепатоцитов — лигандин и глюкуронилтрансфераза). Лигандин способствует транспорту жёлчных пигментов из региона гепатоцита, обращенного к кровенос ному капилляру, в регион, прилежащий к жёлчному капилляру. Рас стройство этого механизма в совокупности с повреждением мембран клеток обусловливает нарушение однонаправленного транспорта би лирубина.
Проявления: выход прямого билирубина в кровь и развитие билирубине-мии, фильтрация прямого билирубина почками и его экскреция с мо чой, попадание компонентов жёлчи в кровь и развитие холемии.
Третья стадия печёночной желтухи:
- Прогрессирующее снижение активности глюкуронилтрансферазы гепа тоцитов. Это приводит к нарушению трансмембранного переноса конъюгированного билирубина в гепатоциты и торможению процесса глюкуронизации билирубина. Проявления: нарастание уровня непрямого билиру бина в крови, уменьшение содержания в крови прямого билирубина (как результат подавления реакции глюкуронизации), снижение (в связи с этим) концентрации стеркобилиногена в крови, моче и экскрементах, умень шение содержания уробилиногена (вплоть до исчезновения) в крови и как следствие — в моче. Последнее является результатом малого поступ ления прямого билирубина в желчевыводящие пути и кишечник.
- Нарастающее усугубление повреждения структур и ферментов гепатоци тов. Проявления: нарастание холемии, сохранение ферментемии и гиперкалиемии, прогрессирование печёночной недостаточности, чреватой раз витием комы.
Различают энзимопатические желтухи наследуемые (первичные) и приобретённые (вторичные).
• Первичные энзимопатии. Развиваются при генных дефектах ферментов и некоторых белков, обеспечивающих метаболизм пигментного обмена в гепатоцитах. Синдром Жильбера (семейная негемолити ческая желтуха), синдром Дабина—Джонсона, синдром Криглера—Найяра и синдром Ротора.
• Приобретённые (вторичные) нарушения свойств ферментов, участвующих в метаболизме жёлчных пигментов и синтезе компонентов мембран гепатоцитов. Развиваются вследствие:
- интоксикации организма, особенно гепатотропными ядами (например, этанолом или четырёххлористым углеродом), некоторыми ЛС (напри мер, парацетамолом, левомицетином), веществами для холецистографии;
- инфекционных поражений печени (например, вирусами, бактериями, их эндо- и экзотоксинами),
- повреждений гепатоцитов AT, цитотоксическими лимфоцитами и макрофагами.
37. Механическая желтуха. Этиология, патогенез, проявления, последствия
Механическая желтуха развивается при нарушениях оттока желчи от печени.
Для механической (подпечёночной, застойной, обтурационной) желтухи ха рактерно развитие холемии и ахолии.
Причина: стойкое нарушение выведения жёлчи по жёлчным капиллярам (что приводит к внутрипечёночному холестазу), по жёлчным протокам и из жёлчного пузыря. Два последних вида нарушения выведения желчи вначале приводят к внепечёночному (подпечёночному) холестазу, а при хроническом действии — и к внутрипечёночному.
Повышается давление в жёлчных капиллярах, перерастяжение (вплоть до микроразрывов) и повышение про ницаемости стенок желчеотводящих путей, диффузию компонентов жёлчи в кровь. При этом развивается билиарный гепатит.
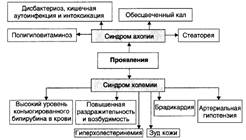
39. Гемолитическая желтуха.
Синдром желтухи - синдром, характеризующийся желтой окраской кожи, слизистых оболочек, склер в результате отложения в них желчных пигментов при нарушении желчеобразования или желчевыделения.
Гемолитическая желтуха - тяжелое заболевание, характеризующееся усиленным распадом эритроцитов, отеками, анемией, появлением желтушной окраски кожи и слизистых оболочек. Чаще встречаются как форма гемолитической болезни новорожденных, может быть признаком острого или хронического отравления веществами, разрушающими эритроциты.
Причины: внутро-, внесосудистый гемолиз эритроцитов; гемолиз эритроцитов и их предшественников в костном мозге, синтез неконъюгированного билирубина из негемоглобинового гемма в печени; образование избытка
Этиология и патогенез. Надпеченочная желтуха является, врожденным или приобретенным самостоятельным заболеванием (микросфероцитарная наследственная анемия, гемоглобинопатия, первичная шунтовая гипербилирубинемия, эритробластоз новорожденных, острая посттрансфузионная анемия и др.) или симптомом ряда заболеваний (крупозная пневмония, подострый септический эндокардит, злокачественные опухоли, некоторые поражения печени), а также следствием токсических и лекарственных повреждений (мышьяк, сероводород, фосфор). Патогенез большой группы гемолитических анемий связан с биохимическим ферментным дефектом эритроцитов или аутоиммунными нарушениями. Различают идиопатическую и симптоматическую формы аутоиммунных гемолитических желтух, последние наблюдаются при хроническом лимфолейкозе, лимфосаркоме, системных заболеваниях соединительной ткани, некоторых вирусных инфекциях.
Проявления: 1. признаки гемолиза эритроцитов: анемия, гемическая гипоксия, гемоглобинурия, повышение в крови уровня неконъюгированного билирубина, увеличение уровня стеркобилина к крови, моче, кале.
Лечение различное в зависимости от формы анемии: при корпускулярных формах, обусловленных биохимическим дефектом в эритроцитах, показана спленэктомия. При аутоиммунных формах наиболее благоприятный эффект оказывают глюкокортикоидные гормоны.
Прогноз зависит от формы гемолитической анемии: весьма серьезный, особенно при остром течении идиопатической аутоиммунной анемии, гемоглобинопатиях, благоприятный - при первичной шунтовой гипербилирубинемии.
34. Недостаточность печени. Этиология и патогенез. Основные проявления нарушений функций печени при ее недостаточности.
Стойкое снижение или полное выпадение одной, нескольких или всех функций печени, что приводит к нарушению жизнедеятельности организма.
Виды фото
Причины фото
Патогенез:
Модификация и/или деструкция плазмолеммы, других мембран и цитоскелета гепатоцитов, развитие иммунопатологических, воспалительных, свобобнораикальных процессов, активация гидролаз приводят к массированному разру шению клеток печени, выходу в интерстиций их содержимого, включая много численные гидролитические ферменты. Названные факторы дополнительно по тенцируют воспалительные, иммунопатологические и свободнорадикальные ре акции. Это, в свою очередь, делает процесс поражения печени тотальным и нарастающим по степени.
Проявления:
1.Расстройства обмена веществ:
- белки: нарушение синтеза гепатоцитами альбуминов проявляется гипоальбуми-немией и диспротеинемией. Гипоальбуминемия способствует развитию отёков и формированию асцита; торможение синтеза белков системы гемостаза приводит к гипокоагуляции бел ков крови, развитию геморрагического синдрома; дезаминирование аминокислот – увеличение содержания в крови аминокислот.
- липиды: липидная дистрофия печени – из-за нарушения синтеза ЛПНП,ЛПОНП,ЛПВП; повышение в плазме уровня холестерина.
- углеводы: снижение гликогенолиза, нарушение образования глюкозы.
2. нарушение функции печени:
- дезинтоксикационная – снижение детоксикации эндогенных токсинов, экзо –ядовитых в-в,
- антимикробная функция
- желчеобразование, желчевыделение.
Печёночная кома.
Финалом прогрессирующей печёночной недостаточности является кома. Она характеризуется потерей сознания, подавлением или значительным снижени ем выраженности рефлексов и расстройствами жизнедеятельности организма (включая нарушения дыхания и кровообращения), чреватыми смертью.
Причины:
1. Шунтовая кома («обходная»). Причина шунтовой комы: инток сикация организма продуктами метаболизма, а также экзогенными веществами, в норме обезвреживающимися гепатоцитами. Это является результатом по падания их в общий кровоток, минуя печень, по портокавальным анастомо зам. Последние развиваются в связи с портальной гипертензией.
2. Паренхиматозная кома. Причина печёночно-клеточной (паренхиматозной) комы: интоксикация организма в связи с повреждением и гибелью значи тельной массы печени (например, при её травме, некрозе, удалении). В ре зультате этого нарушаются все функции печени. Наибольшее патогенное зна чение при этом имеет утрата дезинтоксикационной функции.
Патогенез:
• Гипогликемия. Является результатом нарушения гликогенеза и гликоге-нолиза.
• Ацидоз (метаболический, на финальных стадиях дополнительно развивается респираторный и выделительный ацидоз).
• Дисбаланс ионов в клетках, интерстициальной жидкости и в крови (в крови нарастает [К+], в клетках — [Na+], [Ca2+], [Н+]).
• Интоксикация организма — эндотоксинемия (особенно продуктами бел кового и липидного метаболизма, а также непрямым билирубином, что обус ловлено нарушением его трансформации и конъюгации с глюкуроновой кис лотой).
• Нарушения центральной, органотканевой и микрогемоциркуляции как следствие сердеяной недостаточности, нарушения тонуса артериол, развтите феномена сладжа.
• Полиорганная недостаточность – нарушение функции сердца, дыхательного и кардиовазомоторного центров. Приводит к смешанной гипоксии, прекращению сердечной деятельности, дыхания, смерть.
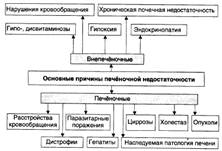
45. Хроническая почечная недостаточность. Этиология, стадии. Уремия, механизмы и проявления.
Почечная недостаточность — синдром, развивающийся в результате значитель ного снижения или прекращения выделительной функции, а также нарушения дру гих процессов в почках.
Для почечной недостаточности характерны прогрессирующее увеличение со держания в крови продуктов азотистого обмена (азотемия) и нарастающие рас стройства жизнедеятельности организма.
Острая почечная недостаточность возникает «внезапно» и быстро прогресси рует.
Причины:
Преренальные. Они обусловливают значительное снижение кровотока в почках: массивная кровопотеря, коллапс, шок, острая сердечная недо статочность, тромбоз почечных артерий.
Функции самих почек при действии указанных причин на начальных этапах острой почечной недостаточности сохранены.
Ренальные - оказывают прямое повреждающее дей ствие на ткань почек: (некронефроз, острая значительная локальная или тотальная ишемия почек, нефротоксические агенты).
Постренальные. - нарушение (вплоть до прекращения) от тока мочи по мочевыводящим путям: обтурация мочевыводящих путей (почечными камнями, опухолью, сдавление мочевыводящих путей, перегиб мочеточника.
Патогенез:
1. Значительное и быстро нарастающее снижение объёма клубочковой филь трации.
2. Сужение или обтурация большого числа канальцев почек.
3. Подавление процессов экскреции и секреции в эпителии канальцев под действием нефротоксических факторов
4. Дополнительное (к действию названных выше механизмов) повреждение клубочков, канальцев, интерстициальной ткани в связи с развитием воспа лительной и иммуноаллергических реакций в ответ на прямое поврежде ние указанных структур.
Хроническая почечная недостаточность — состояние (синдром), развивающееся в результате нарастающей гибели и значительного уменьшения числа функциони рующих нефронов и характеризующееся существенным, прогрессирующим (часто необратимым) снижением функций почек.
Причины:
1. Преренальные: хронические артериальные гипертензии, медленно прогрес сирующий стеноз почечных артерий, двусторонняя эмболия артерий почек.
2. Ренальные: хронические патологические процессы в почках.
3. Постренальные. Факторы, вызывающие длительное нарушение оттока мочи.
Патогенез:
Прогрессирую щее снижение клубочковой фильтрации, канальцевой секреции и реабсорбции. В основе этих процессов находится про грессирующая гибель нефронов, замещение их соединительной тканью (т.е. развитие нефросклероза). Это и приводит к нарастающей недостаточности всех функций почек. Финальным этапом хронической почечной недоста точности является уремия.
Уремия — синдром, заключающийся в аутоинтоксикации организма продуктами метаболизма (нормального и нарушенного), «уремическими токсинами» и экзо генными соединениями, в норме выводящимися почками.
Причины: почечная недостоточность (острая, хроническая);
Основные факторы: интоксикация избытком аммонийных соединений, токсическое действие – фенолы, индолы; дисбаланс ионов и жидкости в клетках.
Уремические токсины: мочевина, паратиреоидный гормон, неадекватная концентрация в крови, интерстициальной жидкости микроэлементов.
Уремия заканчивается почечной комой.
43. Нефротический синдром, виды, патогенез.
Нефриты – группа заболеваний, характеризующихся диффузным поражением почечной ткани воспалительного и/или иммунопатологического генеза, с вовлечением в патологический процесс всех отделов нефронов, интерстициальной ткани и сосудов.
Острый гломерулонефрит — заболевание, как правило, инфекционно-аллергического или иммуноаутоагрессивного генеза.
Причины:
1. Инфекционные агенты: стрептококки, пневмококки, менингококки, сальмонеллы, вирусы (вызывающие гепатит), токсоплазмы.
2. Неинфекционные факторы. Чаще всего это аутоагрессивные и/или пе рекрестные AT, циркулирующие в крови комплексы Аг, Ig, факторов комплемента, а также чужеродные белки (например, вакцины, сыво ротки или цельной крови).
Патогенез:
Частая форма гломерулонефрита — острый диффузный гломерулонефрит. Причиной его является гемолитический стрептококк группы А.
- Образование AT к Аг стрептококка.
- Воздействие антистрептококковых AT на стрептококки (их деструкция) и на структуры почечных телец (особенно на их мембраны, имеющие Аг, сходные с Аг гемолитического стрептококка).
- Денатурация белков, расцениваемых системой ИБН как чужеродные для организма.
- Прямое повреждение структур нефрона токсинами стрептококка, приво дящее к дополнительному образованию аутоантигенов.
- Выработка в ответ на появление в крови аутоантигенов нефроцитотокси ческих аутоантител и лимфоцитов.
Хронический диффузный гломерулонефрит — одно из наиболее частых забо леваний почек.
Причины:
- Инфекционные агенты (бактерии, вирусы, плазмодии).
- Неинфекционные факторы: эндогенные (например, Аг опухолей образующиеся в результате массированного повреждения тканей); экзогенные (ЛС, некоторые антибиотики, вакцины, сыворотка крови, алкоголь, органические растворители).
Патогенез:
- Инициальный фактор — выработка AT к причинному агенту и/или к ауто-антигенам, появляющимся при повреждении почечной ткани.
- Образование иммунных комплексов «Аг+АТ+факторы комплемента», а также цитотоксических Т-лимфоцитов.
- Воздействие иммунных комплексов и Т-лимфоцитов на компоненты ба-зальных мембран и клеток почечных телец, а также капилляров.
- Индукция воспаления и аллергии.
- Потенцирование иммуноаллергических реакций и воспаления. Это при водит к нарастанию степени и масштаба повреждения почечной ткани, что делает процесс хроническим, диффузным и потенциально необратимым.
12. Изменения общего количества циркулирующей крови: нормо-, гипо- и гиперволемии, их виды, механизмы возникновения и последствия для организма.
Гиперволемии
Гиперволемии — состояния, характеризующиеся увеличением общего объёма крови и обычно изменением Ht. Различают нормоцитемическую, олигоцитемическую и полицитемическую гиперволемии.
Нормоцитемическая гиперволемия
Нормоцитемическая гиперволемия (простая) — состояние, проявляющееся эквивалентным увеличением объёма форменных элементов и жидкой части ОЦК. Ht при этом остаётся в рамках диапазона нормы.
Основные причины: переливание большого объёма крови, острые гипоксические состояния, сопровождающиеся выбросом крови из её депо, а также значительная физическая нагрузка, приводящая к гипоксии.
Нормоволемии
Нормоволемии — состояния, характеризующиеся нормальным общим объёмом крови, сочетающимся со сниженным или увеличенным Ht. Различают олигоцитемические и полицитемические нормоволемии.
Олигоцитемическая нормоволемия
Олигоцитемическая нормоволемия — состояние с нормальным общим объёмом крови при уменьшении количества её форменных элементов (главным образом эритроцитов); сопровождается падением величины гематокрита ниже нормы.
• Основные причины:
† Массированный гемолиз эритроцитов (например, при образовании антиэритроцитарных Ig; действии гемолитических веществ — змеиного яда, соединений свинца, мышьяка, фенилгидразина и др.).
† Длительное и выраженное угнетение гемопоэза, главным образом, эритропоэза (например, при апластических анемиях).
† Состояния после острой значительной кровопотери. В этом случае общий объём крови сравнительно быстро нормализуется в результате транспорта жидкости из тканей в сосудистое русло, а число форменных элементов крови остаётся ещё сниженным.
• Проявления:
† Анемия (в связи со снижением числа эритроцитов) и как следствие — гемическая гипоксия.
† Тромбоцитопения (при кровопотере или реакциях иммунной аутоагрессии в отношении тромбоцитов).
† Снижение свёртываемости крови, сочетающееся нередко с геморрагическим синдромом.
† Лейкопения, обусловливающая понижение противоинфекционной резистентности организма.
† Уменьшение вязкости крови. Наблюдается в условиях восстановления объёма жидкой части крови при значительном уменьшении числа её форменных элементов (например, на этапе гидремической компенсации при острой кровопотере).
Полицитемическая нормоволемия
Полицитемическая нормоволемия — состояние, характеризующееся нормальным общим объёмом крови при увеличении числа её форменных элементов, что сопровождается увеличением Ht выше нормы.
• Наиболее частые причины:
† Инфузии пациентам фракций форменных элементов крови (эритроцитарной, лейкоцитарной или тромбоцитарной массы).
†Хроническая гипоксия (вызывает эритроцитоз вследствие активации эритропоэза);
† Эритремии.
• Проявления:
†Увеличение показателя вязкости крови.
† Развитие тромботического синдрома.
†Нарушения микрогемоциркуляции (замедление тока крови в микрососудах, стаз), которые обусловливают снижение транскапиллярного обмена в тканях.
† Артериальная гипертензия (например, в результате увеличения сердечного выброса).
Гиперволемии
Гиперволемии — состояния, характеризующиеся увеличением общего объёма крови и обычно изменением Ht. Различают нормоцитемическую, олигоцитемическую и полицитемическую гиперволемии.
Дата: 2019-02-19, просмотров: 434.