Металлы представляют собой кристаллические тела с закономерным расположением атомов в узлах пространственной решетки. Решетки состоят из ряда кристаллических плоскостей, расположенных друг от друга на расстоянии нескольких нанометров (1 нм = 10-9 м). Для железа эти расстояния 28,4 нм (α=Fe) и 36,3 нм (γ=Fe). Большинство металлов имеет пространственное строение решетки в виде простых геометрических фигур, обладающих плотнейшей упаковкой – это кубические объемно- и гранецентрированные и гексагональные решетки (рисунок 4.1).
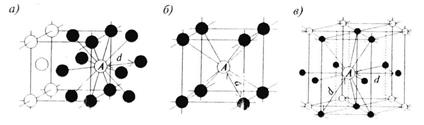
а) кубической гранецентрированной (К12); б) объемно-центрированной (К8);
в) гексагональной (К12)
Рисунок 7.1 – Координационные числа (плотность упаковки) кристаллических решеток:
Плотность упаковки характеризуется координационным числом, представляющим собой число соседних атомов, находящихся на равном и наименьшем расстоянии от данного атома. Чем больше число, тем плотнее упаковка. Для объемно-центрированной кубической упаковки оно равно 8 (К8); гранецентрированной – 12 (К12); гексагональной – тоже 12 (К12). В кубической объемно-центрированной решетке кристаллизуются К, Na, Li, α-Fe, Mo, W, V, Cr, Ba, и др.; кубической гранецентрированной – Ni, Ag, Au, Pt, Cu, γ-Fe; в гексагональной – Mg, Cd, Ru, Be, α-Ti, α-Zn и др.
Расстояние между центрами ближайших атомов в решетке называется периодом решетки. Период решетки для большинства металлов находится в пределах 0,1-0,7 нм.
Отдельные участки кристаллической решетки прочно связаны между собой в комплексы – зерна. Взаимное расположение зерен отдельных элементов и сплавов определяют структуру металлов и их свойства.
Атомы металлов характеризуются малым количеством электронов (1…2) на наружной оболочке, легко отдают их, что подтверждается высокой электропроводностью.
Многие металлы в зависимости от температуры претерпевают структурные изменения кристаллической решетки.
Железо, олово, титан и другие металлы обладают свойствами аллотропии, т. е. способностью одного и того же элемента при различной температуре иметь разную кристаллическую структуру. Аллотропические превращения сопровождаются выделением или поглощением теплоты. Железо имеет четыре аллотропические формы: α-Fe, β-Fe, γ-Fe, δ-Fe. Практическое значение имеют α-Fe и γ-Fe, так как β-Fe и δ-Fe отличаются от α-Fe только величиной межатомного расстояния, а для β-Fe характерно отсутствие магнитных свойств.
Температура, при которой, происходит переход металла из одного аллотропического вида в другой, называется критической. Величины этих температур видны на диаграмме охлаждения и нагревания чистого железа (рис. 7.2) в виде участков, свидетельствующих о том, что фазовые превращения происходят с выделением теплоты при нагревании. До точки Кюри ( 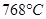 ) железо магнитно, выше – немагнитно.
) железо магнитно, выше – немагнитно.
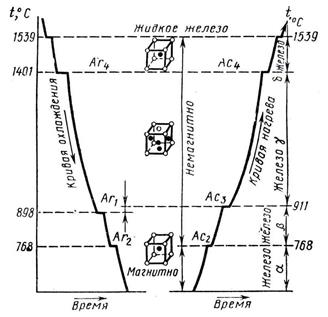
Рисунок 7.2 – Кривые охлаждения и нагревания железа
Все металлы находятся в твердом состоянии до определенной температуры. При нагреве металла амплитуда колебания атомов достигает некоторой критической величины, при которой происходят разрушение кристаллической решетки и переход металлов из твердого в жидкое состояние. Процесс кристаллизации заключается в росте кристаллов путем отложения новых кристаллических групп вокруг возникших зародышей. Рост кристаллических образований происходит в определенных направлениях. Вначале образуются главные оси кристалла путем роста в трех взаимно перпендикулярных направлениях, а затем от каждой из этих осей образуются новые и возникает не полностью завершенный кристалл, называемый дендритом. В дальнейшем все промежутки между осями дендрита заполняются упорядоченно расположенными атомами.
В условиях несвободной кристаллизации образующиеся кристаллы получают неправильные очертания и форму и называются кристаллитами, или зернами. Величина зерен оказывает существенное влияние на механические свойства металлов: чем мельче зерна, тем прочнее металл.
Технические металлы и сплавы представляют собой поликристаллические тела, состоящие из большого числа различно ориентированных кристаллических зерен (поперечные размеры зерен 0,001-0,1 мм). Поэтому в целом металлы принято считать условно изотропными телами.
Однако при одинаковой ориентации кристаллитов такой мнимой изотропности наблюдаться не будет. Кристаллическая решетка реальных металлов и сплавов далека от идеального строения.
В реальных кристаллах всегда содержатся дефекты, которые подразделяют на точечные, линейные, поверхностные и объемные. Размеры точечного дефекта близки к межатомному расстоянию. У линейных дефектов длина на несколько порядков больше ширины; у поверхностных дефектов мала толщина, а ширина и длина больше ее на несколько порядков. Объемные дефекты (поры, трещины) имеют значительные размеры во всех трех направлениях.
Дефекты сохраняют подвижность, способны перемещаться в кристаллической решетке и при сближении взаимодействуют между собой. В большинстве случаев подвижность дефектов контролируется диффузией. Передвижение дислокаций под действием напряжений не связано с массопереносом, дислокации подвижны и при низких температурах, когда диффузия уже не играет никакой роли.
К самым простым точечным дефектам относятся вакансии, межузельные атомы основного вещества, чужеродные атомы внедрения (рисунок 7.3).
Вакансией называется пустой узел кристаллической решетки, а межузельным атомом – атом, перемещенный из узла в позицию между узлами.
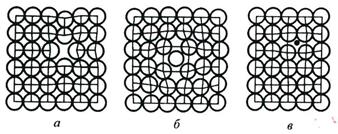
а – вакансии; б – межузельный атом; в – примесный атом внедрения
Рисунок 7.3 – Точечные дефекты в кристаллической решетке
Вакансии и межузельные атомы появляются в кристаллах при любой температуре выше абсолютного нуля из-за тепловых колебаний атомов. Каждой температуре соответствует равновесная концентрация вакансий, а также межузельных атомов. Например, в меди при 20-25 °С содержится 10-13 % (ат.) вакансий, а вблизи точки плавления – уже 0,01 % (ат.) (одна вакансия приходится на 104 атомов).
Пересыщение точечными дефектами достигается при резком охлаждении после высокотемпературного нагрева, при пластическом деформировании и при облучении нейтронами. В последнем случае концентрация вакансий и межузельных атомов одинакова: выбитые из узлов решетки атомы становятся межузельными атомами, а освободившиеся узлы становятся вакансиями.
С течением времени избыток вакансий сверх равновесной концентрации уничтожается на свободных поверхностях кристалла, порах, границах зерен и других дефектах решетки. Места, где исчезают вакансии, называются стоками вакансий. Вакансии являются самой важной разновидностью точечных дефектов; они ускоряют все процессы, связанные с перемещениями атомов (диффузия, спекание порошков и т.д.).
Все виды точечных дефектов искажают кристаллическую решетку и, в определенной мере, влияют на физические свойства, преимущественно на электропроводность, магнитные свойства. На механические свойства металлов точечные дефекты практически не влияют.
Важнейшие виды линейных несовершенств – краевые и винтовые дислокации (рисунок 7.4). Краевая дислокация в сечении представляет собой край «лишней» полуплоскости в решетке (см. рисунок 7.4.а). Вокруг дислокаций решетка упруго искажена.
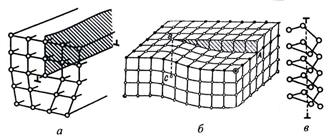
Рисунок 7.4 – Схемы краевой (а) и винтовой (б) дислокаций, вектора Бюргенса (в)
Мерой искажения служит так называемый вектор Бюргенса (рисунок 7.4.в).
Краевые, или линейные, дислокации характеризуются появлением в кристалле добавочной незавершенной атомной плоскости (электроплоскости). Дислокация называется положительной (рисунок 7.4а), если экстраплоскость лежит в верхней части кристалла, и отрицательной, если она расположена в нижней части кристалла.
Винтовая дислокация (рисунок 7.4.б) появляется, если в кристалле сделать надрез и сдвинуть вниз одну часть кристалла относительно другой на одно межатомное расстояние (на рисунке 7.4.б плоскость сдвига заштрихована). Как видно из рисунка, смещение уменьшается от точки А к точке В, что вызывает изгиб атомных плоскостей. Несовершенная область вокруг линии ВС называется винтовой дислокацией, так как после появления такого несовершенства атомные плоскости кристалла закручиваются подобно винтовой лестнице.
К поверхностным дефектам относят большеугольные и малоугольные границы, дефекты упаковки, границы двойников.
Поликристаллический сплав содержит большое число мелких зерен, границы между которыми представляют переходный слой шириной 1-5 нм. В нем нарушена правильность расположения атомов, имеющая скопления дислокаций, повышена концентрация примесей. Если соответствующие кристаллографические направления в соседних зернах образуют углы в десятки градусов, то такие границы называют большеугольными. Если же такой угол невелик (не более 5°), то такие границы называют малоугольными.
Дефект упаковки – это часть атомной плоскости, ограниченной дислокациями, в пределах которой нарушен нормальный порядок чередования атомных слоев.
Поверхностные дефекты влияют на механические и физические свойства металлов. Чем мельче зерно, тем выше предел текучести, вязкость и меньше опасность хрупкого разрушения.
Диффузия протекает значительно быстрее вдоль границ зерен, чем сквозь кристаллы, особенно при нагреве. Взаимодействие между дефектами, перемещение их в кристаллах отражается на свойствах материалов.
К объемным дефектам в кристаллах относят микротрещины в них, поры и различные включения.
Дислокации играют главную роль в процессах пластической деформации металлов, они в значительной мере определяют их реальную прочность.
Дефекты кристаллического строения возникают уже в процессе кристаллизации металла. Взаимодействие дефектов между собой приводит к образованию новых несовершенств, и, как следствие, к изменению таких свойств металлов как прочность и пластичность. При этом с возрастанием плотности дислокаций реальная прочность металла может проходить через минимум, так как дислокации из параллельных друг другу могут переходить в расположенные в разных плоскостях и направлениях. Последние дислокации, мешая друг другу перемещаться, будут увеличивать прочность металла, и снижать его пластичность (явление наклепа). На этом основано упрочнение металлов путем термической обработки, сопровождающееся измельчением зерна и изменением кристаллической решетки.
Дата: 2019-02-02, просмотров: 914.